凹凸棒石/CoFe2O4 磁性复合材料制备及对亚甲基蓝吸附性能
2015-04-14杨远盛李正军王诗生盛广宏
杨远盛,李正军,王诗生,盛广宏
(1.安徽省环境科学研究院,安徽 合肥 230061;2.安徽工业大学 能源与环境学院,安徽 马鞍山 243032 )
染料废水主要来源于纺织、印染、染料制造业,具有高色度、高浓度、成分复杂等特征,且部分染料及合成产物含有“三致”成分,因此,对染料废水的处理已成为环保科技工作者研究的焦点[1-3]。目前,处理染料废水的方法有电化学法[4]、吸附法[5-6]、化学氧化法[7]、生物处理法[8]等。其中吸附法凭借其操作性强、治理费用低、设计运行容易等优点,被认为最具应用前景的治理方法[9],而吸附材料是吸附处理染料废水的关键。目前用于处理染料废水的吸附材料有活性炭、树脂、粘土矿物、各种工农业废弃物等[10]。其中粘土矿物吸附剂是近年来国内外十分关注的廉价吸附材料[11-12]。
凹凸棒石作为一种链层状结构含水富镁硅酸盐的矿物,具有贯穿整个结构大小为0. 38 nm ×0.63 nm的孔道,具有较大的比表面积及良好的吸附性能,已被广泛应用于水处理领域[13]。近10 余年来,国内外学者对凹凸棒石作为天然廉价吸附剂进行了深入的研究[14-16]。然而由于凹凸棒石晶体细小,表面带有结构电荷,在水悬浮体系中表现出优异的胶体性能和胶体稳定性,导致吸附饱和后的凹凸棒石从水中分离较为困难[17]。为了解决这个问题,将凹凸棒石与纳米磁性材料复合,从而获得一种具有吸附性能和磁性能的复合材料。Liu 等[18-19]通过共沉淀法制备凹凸棒石/Fe3O4磁性复合材料。但是,考虑磁性复合材料再生问题,当采用加热方式再生时,纳米级Fe3O4可能被氧化成Fe2O3而失去磁性,影响吸附材料的重复使用[20]。近年来具有抗氧化性的CoFe2O4作为磁分离材料已在废水处理领域中有所应用[21]。从当前的研究来看,还未见将CoFe2O4与凹凸棒石结合制备磁性复合材料。
本文采用低温回流法制备凹凸棒石/CoFe2O4磁性复合材料,通过序批式吸附实验,研究了pH值、投加量对吸附的影响以及吸附热力学和动力学,且初步探讨了其吸附机理。
1 实验部分
1.1 材料与仪器
FeCl3·6H2O、Co(NO3)2·6H2O、亚甲基蓝(MB)、HCl、NaOH 均为分析纯;凹凸棒石。
Bruker D8 Advance 型X 射线衍射仪;TENSOR27 型傅里叶变换红外光谱仪;JMS-64900LV 型扫描电镜;振动样品磁强计;SHZ-B 型水浴恒温振荡箱;722S 型可见光光度计;PHS-3E 型精密pH 计;FA1004N 型电子天平。
1.2 AT/CoFe2O4 磁性复合材料(MAT)的制备
采用低温回流法制备MAT,具体过程如下:称取5.41 g FeCl3·6H2O 和2.91 g Co(NO3)2·6H2O溶于蒸馏水中,在室温下强烈搅拌5 min,逐滴加入氢氧化钠溶液至pH >11,后将凹凸棒石2.35 g 加入混合液中,继续强烈搅拌30 min,将混合液置于电热套内保持100 ℃回流2 h。冷却后的混合液进行磁分离,用稀盐酸调pH 至中性,再用蒸馏水洗涤数次,60 ℃条件下烘干后研磨备用。
1.3 序批式吸附实验
精密称取MAT 0. 050 g,置于25 mL 浓度为100 mg/L的MB 溶液中,分别用稀HCl 和NaOH 溶液调节pH 值在3 ~9 范围内,置于恒温振荡器中,在温度293 K、转速150 r/min 条件下,振荡至吸附平衡,磁分离,测定上清液的吸光度并计算MB 溶液的平衡浓度和去除率。
式中 V——MB 溶液的体积,L;
m——MAT 的质量,g;
C0——MB 溶液的初始浓度,mg/L;
Ce——吸附平衡浓度,mg/L。
式中 W——去除率,%;
C0——MB 溶液的初始浓度,mg/L;
Ce——吸附平衡浓度,mg/L。
2 结果与讨论
2.1 催化剂表征
2.1. 1 FTIR 分析 图1 为凹凸棒石、CoFe2O4、MAT 的红外图谱。
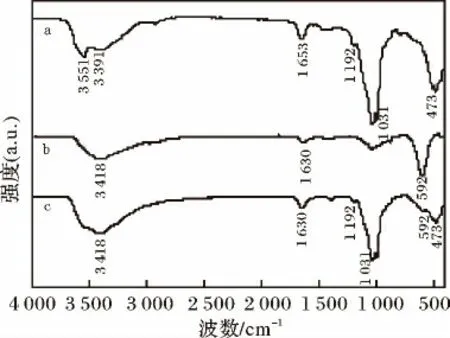
图1 凹凸棒石(a)、CoFe2O4(b)和MAT(c)红外光谱图Fig.1 IR spectra of attapulgite(a),CoFe2O4(b)and MAT(c)
由图1(a)可知,3 551 cm-1和3 393 cm-1为凹凸棒石中Mg—OH 的伸缩振动;1 653 cm-1为凹凸棒石中吸附水的弯曲振动;1 192 cm-1为凹凸棒石中(Mg,Al)—O 的伸缩振动;1 031 cm-1为AT 中Si—O 桥非内—Si 的非对称伸缩振动;473 cm-1为凹凸棒石中Si—O—Si 的弯曲振动[16]。
由图1(b)可知,592 cm-1为CoFe2O4纳米粒子八 面 体 位 的 特 征 伸 缩 振 动[22],1 630 cm-1为CoFe2O4纳米粒子中吸附水分子的H—O—H 的弯曲振动;而3 418 cm-1为CoFe2O4纳米粒子表面吸附的水分子的O—H 的伸缩振动[23]。
由图1(c)可知,凹凸棒石在1 192,1 031,473 cm-1处对应的特征峰值在MAT 中并未改变,只是相应的强度有所减弱,说明MAT 依然保持了凹凸棒石的主要特征,合成过程中凹凸棒石的性质并未发生改变。同时,CoFe2O4在590,1 630,3 418 cm-1处对应的特征峰值也并未改变,说明磁性粒子CoFe2O4以简单的物理沉积负载于凹凸棒石表面。2.1.2 磁滞回线分析 图2 为凹凸棒石、MAT 和CoFe2O4的磁滞回线。
由图2 可知,凹凸棒石、MAT 和合成CoFe2O4的饱和比磁化强度分别为0.19,14.00,60.57 emu/g。MAT 磁性较强,易于磁分离,磁化过程中,MAT 磁化强度随外加磁场强度增大而增大,最终趋于饱和;当外加磁场强度逐渐降低至0 时,MAT 磁化强度也趋近于0;反向施加磁场,MAT 磁化强度反向趋于饱和,MAT 的磁滞回线接近重合的S 型曲线,故可以认为MAT 具有良好的超顺磁性,这与磁性沸石磁滞回线[24]和磁性坡缕石磁滞回线[18]相似。MAT 磁性相对于CoFe2O4有所减弱,主要是加入了等质量磁性很弱的凹凸棒石。

图2 凹凸棒石(a)、MAT(b)和CoFe2O4(c)磁滞回线Fig.2 Hysteresis loops of attapulgite(a),MAT(b)and CoFe2O4(c)
2.1. 3 SEM 分析 图3 为凹凸棒石与MAT 的SEM 照片。

图3 凹凸棒石(a)和MAT(b)的SEM 照片Fig.3 SEM micrographs of attapulgite(a)and MAT(b)
由图3(a)可知,凹凸棒石出现团聚形态和不规则的块状形状;由图3(b)可知,凹凸棒石表面覆盖铁酸钴,呈现出不同的表面形貌,揭示了铁酸钴可以轻微改变凹凸棒石外表面结构,这与凹凸棒石的比表面积和微孔体积改变相符。
2.1.4 比表面积分析 凹凸棒石、MAT 和铁酸钴的比表面积、微孔面积、外表面积和微孔体积测试结果见表1。

表1 凹凸棒石、MAT 和铁酸钴的比表面积、微孔面积、外表面积和微孔体积Table 1 BET surface area,microporous area,external surface area and microporous volumeof attapulgite,MAT and CoFe2O4
由表1 可知,相比较凹凸棒石,MAT 的比表面积略有增大,主要原因是铁酸钴覆盖在凹凸棒石表面,并且铁酸钴的外表面积较大,使得MAT 的比表面积略有增大。但MAT 的微孔体积减小较大,主要是铁酸钴进入凹凸棒石的孔道,占据了一定的体积,并且铁酸钴的微孔体积为0。通过比较,MAT 具有较大的比表面积和微孔体积,具有一定的吸附效果。2.1.5 XRD 分析 图4 为凹凸棒石和MAT 的XRD 图。

图4 凹凸棒石(a)和MAT(b)的XRD 图Fig.4 XRD patterns of attapulgite and MAT
由图4(a)可知,凹凸棒石成分还有一定量的石英。其主要的衍射峰在2θ 为8.32,13.62,16.28,19.82,20.74,27.38,35.10°。由图4(b)可知,MAT中的凹凸棒石主要的衍射峰没有发生改变,只是衍射峰的强度有所降低,其中在2θ 为18. 3,30. 1,35.4,43.1,53.5,57.1,62.6°出现了CoFe2O4的衍射峰。CoFe2O4的衍射峰[22]没有改变,表明凹凸棒石以简单的物理沉积方式负载CoFe2O4,与MAT 的红外光谱图相符。
2.2 MAT 投加量的影响
MAT 投加量对其吸附MB 影响见图5,未调pH。
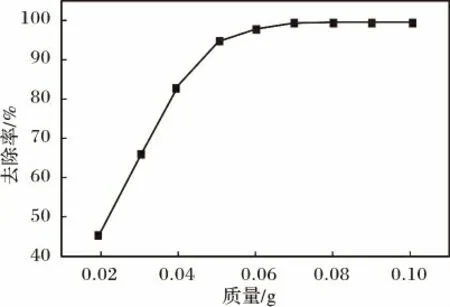
图5 MAT 投加量对吸附MB 的影响Fig.5 Influence of MAT dosage on MB adsorption
由图5 可知,去除率随着MAT 投加量的增加而增大,投加量为0.050 g 时,去除率达到95%;投加量大于0.050 g,去除率基本保持不变。所以,对于25 mL 浓度为100 mg/L 的MB 溶液,最佳投加量为0.050 g。
2.3 pH 的影响
pH 值对MAT 吸附MB 影响见图6。
由图6 可知,在研究pH 范围内,MAT 对MB 的吸附量随着pH 值的增大而逐渐增大,在pH <5,吸附量随pH 升高上升明显;pH >5,吸附量随pH 升高变化不明显。可能原因:在较低pH 值时,MAT 表面带正电荷,与溶液中MB 阳离子存在一定的静电斥力作用;随着pH 的升高,MAT 表面电荷发生变化,表面负电荷也逐渐增多,与溶液中MB 阳离子存在一定的静电引力作用,有助于对MB 吸附量的增加,与艾伦弘等[25]报道结果一致。
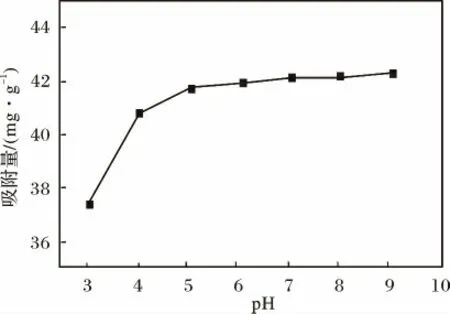
图6 pH 对吸附MB 的影响Fig.6 Influence of pH on MB adsorption
2.4 吸附热力学
2.4.1 吸附等温线 测定不同初始浓度达到平衡时的吸附量,精密称取10 份MAT 0. 050 g,置于25 mL浓度为100 mg/L 的MB 溶液中,未调节pH,将溶液置于恒温振荡器中,在温度293 K、转速150 r/min条件下,按照设定的时间间隔取样,磁分离,测定上清液的吸光度并计算MB 溶液的平衡浓度。以吸附量qt(mg/g)对平衡浓度Ce(mg/L)作图,得到吸附等温线见图7。
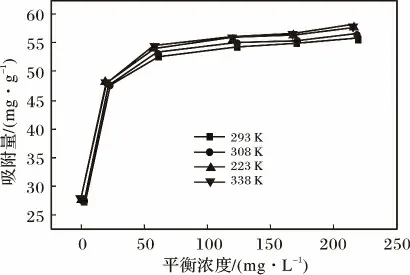
图7 MB 在MAT 上的吸附等温线Fig.7 Adsorption isotherms of MB onto MAT
利用Langmuir 和Freundlich 等温式对吸附等温线进行拟合,结果见表2。
Langmuir 吸附等温方程一个重要的特点定义了无量纲的分离因子RL,公式如下:

其中RL表示吸附过程的性质,0 <RL<1,为优惠吸附;RL>1,为非优惠吸附;RL=1,为可逆吸附;RL=0,为非可逆吸附[15]。
式中 qe——平衡吸附量,mg/g;
Ce——平衡浓度,mg/L;
qm——单层饱和吸附量,mg/g;
b——吸附平衡常数,L/mg;
k——常数,与温度、吸附剂种类、采用的计量单位有关。
由表2 可知,Langmuir 等温方程能很好地描述MAT 对MB 的吸附(R2均大于0.99)。Langmuir 等温方程的qm和b 的值均随着温度的升高而增大,这表明吸附过程是吸热,温度升高,有利于吸附。其中在实验研究的浓度范围内,Langmuir 等温方程特征分离系数为:0 <RL<1,说明MAT 对MB 的吸附为优惠吸附。
2.4.2 热力学参数 应用Gibbs 方程可以计算温度对平衡吸附的影响:

式中 b——吸附平衡常数,L/mg;
b’——Langmuir 常数,L/mg;
R——气体常数,8.314 J/(mol·K);
T——绝对温度,K;
ΔG——吸附自由能变,kJ/mol;
ΔH——吸附焓变,kJ/mol;
ΔS——吸附熵变,J/(mol·K)。
由于吸附等温线符合Langmuir 等温方程,所以按式(3)由ln b 和1 000/T 作图的斜率计算出吸附焓变ΔH,再分别按式(1)、(2)计算出吸附自由能变ΔG、吸附熵变ΔS,结果见表3。
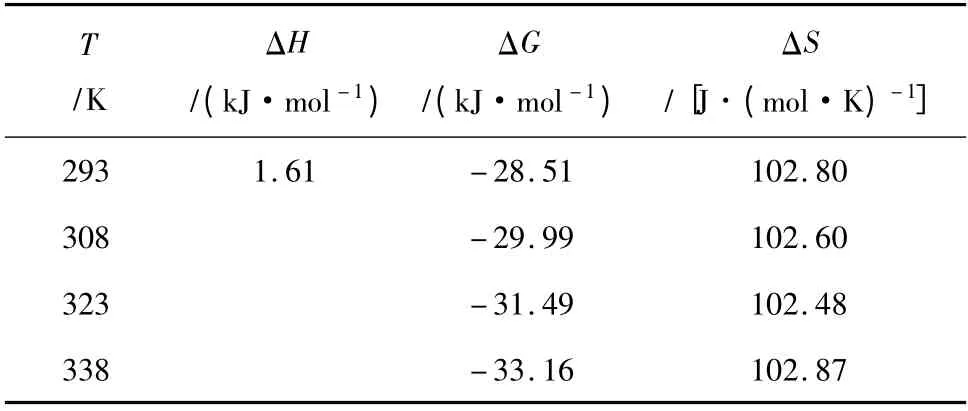
表3 热力学参数Table 3 Results of thermodynamic parameters
由表3 可知,MAT 对MB 吸附焓变ΔH 为1.61 kJ/mol,说明吸附过程是一个吸热过程,升高温度,有利于吸附。可能原因MAT 对MB 的吸附过程是先解吸水分子,再吸附MB 阳离子基团的过程,其中解吸是吸热过程,而吸附是放热过程,由于水的摩尔体积比MB 的摩尔体积小很多,所以吸附单位摩尔体积MB 阳离子需要解吸较多的水分子,这样解吸过程吸收的热量大于吸附过程放出的热量,最终导致吸附全过程为吸热过程[26]。
吸附自由能变ΔG 是吸附推动力和吸附优惠性的体现。一般来说,物理吸附的自由能变小于化学吸附,前者在-20 ~0 kJ/mol 内,而后者在-400 ~-80 kJ/mol 内[15]。本实验吸附自由能变ΔG 在-33.16 ~-28.51 kJ/mol,表明MAT 对MB 阳离子的吸附并不是单一的物理或化学吸附,而是物理和化学吸附并存的吸附过程。ΔG <0,说明该吸附过程在常温下是一个自发过程。温度升高,ΔG 的绝对值增大,其自发程度增强,说明升高温度,有利于吸附。
对于液相吸附,在固体表面上溶质和溶剂同时被吸附,吸附过程总熵变是溶质的吸附(伴随熵减少即自由度减少)与溶剂的解吸(导致熵增加即自由度增加)两者的总合,它取决于溶质和溶剂与固体表面作用的强弱及它们的分子体积的大小[15]。本实验吸附熵变ΔS 均大于0,说明MAT 对MB 的吸附是吸附焓变和熵变共同推动的结果,由于吸附过程中解吸的水分子比吸附的MB 分子多,即溶剂的解吸对体系熵变的贡献大,因而该吸附过程是一个熵增过程。
2.5 吸附动力学
精密称取10 份MAT 0.050 g,置于25 mL 浓度为100 mg/L 的MB 溶液中,未调节pH,将溶液置于恒温振荡器中,在温度293 K,转速150 r/min 条件下,按照设定的时间间隔取样,磁分离,测定上清液的吸光度并计算MB 溶液的平衡浓度,以确定MAT吸附溶液中MB 吸附速率,结果见图8。
为了研究MAT 对MB 的吸附动力学的定量描述,揭示吸附量随时间的变化情况,选用准一级动力学模型和准二级动力学模型对实验数据进行模拟。
准一级动力学模型:

准二级动力学模型:

式中 qe、qt——平衡时和t 时刻的吸附量,mg/g;
t ——吸附时间,min;
k1——准一级方程的吸附速率常数,min-1;
k2——准二级方程的吸附速率常数,g/(mg·min)。
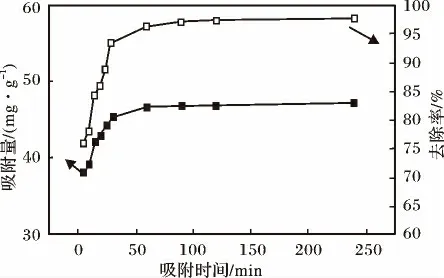
图8 MAT 对MB 的吸附动力学Fig.8 Adsorption kinetic curves of MB onto MAT
由图8 可知,在吸附实验的初期阶段,MAT 对MB 的吸附速率很大,吸附量和去除率上升明显,在25 min 时,吸附量达到45 mg/g,去除率达到95%,基本达到吸附平衡;t >25 min 时,吸附曲线基本趋于平坦。分析其原因:在反应初期,溶液中的MB 浓度较高,MB 浓度梯度大,扩散速率快,同时,MB 阳离子(带正电)与MAT 表面活性位点(带负电)之间存在静电引力作为吸附的推动力,故吸附速率较大;反应后期,随着吸附的进行,溶液中的MB 浓度降低,浓度梯度减小,扩散速率减慢。据报道,MB 阳离子 在 水 溶 液 中 的 大 小1. 70 nm × 0. 76 nm ×0.325 nm,而在AM 晶体结构中平行于c 轴方向排列的内孔通道为0.38 nm ×0.63 nm,而MAT 的内孔道比凹凸棒石的内孔道还要小,故MB 阳离子根本不能进入微孔,只能在外表面吸附,吸附很快达到平衡,所以MAT 对MB 的吸附属于外表面吸附。
按照上述2 种模型进行拟合,通过曲线的斜率和截距可以得到动力学参数,见表4。

表4 MAT 对MB 吸附动力学参数Table 4 Kinetic parameters of MB absorption by MAT
由表4 可知,准二级动力学模型能很好的描述MAT 对溶液中MB 的吸附动力学过程(R2达到0.999)。同时,由准二级动力学模型计算的平衡吸附量qe与实验中得到的平衡吸附量qee值基本相等;而由准一级动力学模型计算的qe与实验中得到的qee值相差较大,主要原因是准一级模型作用前需要知道qe值,但实际吸附过程中,真正达到平衡所需时间很长,不可能准确测得其平衡吸附量。
3 结论
(1)通过低温回流法制备的磁性吸附材料MAT能有效解决凹凸棒石不易与水分离的问题,且对MB 有良好的吸附能力,可作为一种高效、廉价、环保的吸附剂来去除废水中的有害物质。
(2)磁性CoFe2O4以简单的物理沉积负载于凹凸棒石表面,MAT 饱和比磁化强度为14 emu/g,具有良好的超顺磁性,其比表面积175.85 m2/g,略大于凹凸棒石。
(3)pH 在3 ~9 内,MAT 的吸附量随pH 值的增大而增大;对于25 mL 浓度为100 mg/L的MB 溶液,MAT 的最佳投加量为0.050 g。
(4)MAT 对MB 的吸附热力学符合Langmuir 吸附等温方程,是一个吸热、自发、熵增的吸附过程,其动力学符合准二级动力学方程,属于外表面吸附。
[1] Annadurai G,Juang R S,Leed J. Use of cellulose-based wastes for adsorption of dyes from aqueous solution[J].Journal of Hazadous Materials,2002,92(3):263-274.
[2] 薛方亮,张雁秋. 染料废水处理技术最新研究进展[J].水科学与工程技术,2007(2):26-29.
[3] 陈文华,李刚,许方程,等. 染料废水污染现状及处理方法研究进展[J].浙江农业科学,2014(2):264-269.
[4] Kariyajjanavar P,Jogttappa N,Nayaka Y A. Studies on degradation of reactive textile dyes solution by electrochemical method[J]. Journal of Hazardous Materials,2011,190(1/2/3):952-961.
[5] Guo J,Chen S,Liu L,et al. Adsorption of dye from wastewater using chitosan-CTAB modified bentonites[J].Colloid Interface Science,2012,382(1):61-66.
[6] Zhu H Y,Fu Y Q,Jiang R,et al. Adsorption removal of Congo red onto magnetic cellulose/Fe3O4/activated carbon composite:Equilibrium,kinetic and thermodynamic studies[J]. Chemical Engineering Journal,2011,173:494-502.
[7] Xu H,Li M,Miao J,et al. Fenton reagent oxidation and decolorizing reaction kinetics of reactive red SBE[J].Energy Procedia,2012,16:58-64.
[8] Mustafa I,Delia T S. Biological treatment of acid dyeing wastewater using a sequential anaerobic/aerobic reactor system[J]. Enzyme and Microbial Technology,2006,38(7):887-892.
[9] Gao C,Huang T,Peng D P.The research progress of adsorption method for dyeing wastewater treatment[J]. Energy Environmental Protection,2014,28(1):30-34.
[10]陆朝阳,沈莉莉,张全兴,等. 吸附法处理染料废水的工艺[J].工业水处理,2004,24(3):12-16.
[11] Sarma G K,Gupta S S,Bhattacharyya K G. Methylene blue adsorption on natural and modified clays[J].Separation Science Technology,2011,46(10):1602-1614.
[12]何玉凤,王燕,张振花,等. 膨润土基共聚复合物的制备及对亚甲基蓝的脱色性能[J]. 环境化学,2013,32(8):1554-1558.
[13]陈天虎,徐晓春,岳书仓.苏皖凹凸棒石粘土纳米矿物学及地球化学[M].北京:科学出版社,2004:1-316.
[14]彭书传,王诗生,陈天虎,等. 凹凸棒石吸附水溶性染料的热力学研究[J].硅酸盐学报,2005,33(8):1012-1017.
[15]Chen L,Xuan G. Thermodynamic study of Th(IV)sorption on attapulgite[J]. Applied Radiation and Isotopes,2008,67(1):1-6.
[16]Falayi T,Ntuli F.Removal of heavy metals and neutralisation of acid mine drainage with un-activated attapulgite[J]. Journal of Industrial and Engineering Chemistry,2014,20(4):1285-1292.
[17]庆承松,宋浩,陈天虎,等. 凹凸棒石/γ-Fe2O3/C 纳米材料的制备与表征[J]. 硅酸盐学报,2009,37(4):548-553.
[18]Liu Y S,Liu P,Su Z X,et al.Attapulgite-Fe3O4magnetic nanoparticles via co-precipitation technique[J]. Applied Surface Science,2008,255(5):2020-2025.
[19]王维清,冯启明,赵晓东.Fe3O4/坡缕石磁性复合材料的制备及其表征[J].非金属矿,2010,33(1):21-23.
[20] Peng X J,Luan Z K,Zhang H M. Montmorillonite-Cu(II)/Fe(III)oxides magnetic material as adsorbent for removal of humic acid and its thermal regeneration[J].Chemosphere,2006,63(2):300-306.
[21]Wang L X,Li J C,Wang Y Q,et al.Adsorption capability for Congo red on nanocrystalline MFe2O4(M = Mn,Fe,Co,Ni)spinel ferrites[J]. Chemical Engineering Journal,2012,181/182:72-79.
[22] Yavuz O,Ram M K,Aldissi M,et al. Synthesis and the physical properties of MnZn ferrite and NiMnZn ferritepolyaniline nanocomposite particles[J].Journal of Materials Chemistry,2005,15(7):810-817.
[23]艾伦弘,蒋静.铁酸钴纳米晶体的低温合成、谱学表征及磁性[J].应用化学,2010,27(1):78-81.
[24]Cao J L,Liu X W,Fu R,et al. Magnetic P zeolites:synthesis,characterization and the behavior in potassium extraction from seawater[J]. Separation and Purification Technology,2008,63(1):92-100.
[25]艾伦红,蒋静,唐娟.活性炭/CoFe2O4复合物的制备及其对亚甲基蓝的吸附性能[J]. 应用化学,2010,27(6):710-715.
[26] Ghosh D,Bhattacharyya K G. Adsorption of methylene blue on kaolinite[J]. Applied Clay Science,2002,20(6):295-300.
