SBSE-TDU-GC/MS法同步测定饮用水源水中16种多溴联苯化合物
2015-04-12董黎静戴玄吏滕加泉章霖之余益军薛银刚
董黎静,戴玄吏,滕加泉,章霖之,余益军,薛银刚*
(1.常州市环境监测中心,江苏 常州 213014;2.江苏新锐环境监测有限公司,江苏 张家港 215600)
SBSE-TDU-GC/MS法同步测定饮用水源水中16种多溴联苯化合物
董黎静1,戴玄吏2,滕加泉1,章霖之1,余益军1,薛银刚1*
(1.常州市环境监测中心,江苏 常州 213014;2.江苏新锐环境监测有限公司,江苏 张家港 215600)
通过对萃取和解吸条件进行优化,实现搅拌棒吸收萃取(SBSE)-热脱附-气相色谱/质谱联用以同时测定饮用水源水中16种多溴联苯单体。此法在2~50 ng/L范围内线性良好,取10 mL水样,搅拌棒吸收萃取1 h后,16种多溴联苯单体的检出限为0.5~1.1 ng/L。对实际水样进行2个质量浓度的加标回收,平均回收率为89.2%~102%。
多溴联苯;SBSE搅拌棒吸收萃取;气相色谱/质谱法;饮用水源水
多溴联苯(polybrominated biphenyls,简称PBBs)常被用作为溴代阻燃剂,用于家具、建材和电子等产品中[1]。PBBs具有潜在的免疫毒性、神经毒性、致癌性、生殖毒性和内分泌干扰等毒性,逐渐被停止生产使用[2]。国内外学者对 PBBs的研究主要集中于空气、土壤、污水处理厂污泥、湖泊沉积物和鱼肉等生物样品[3-7]。
我国的电子垃圾拆解区,研究人员已经从空气、土壤、食品中检测到了PBBs的存在,对周边居民存在潜在的危害[8]。目前水体沉积物和生物体内的PBBs检出水平达到了ng/g,海水中多溴联苯的检出限达到ng/L[9]。
环境样品中PBBs的含量相对较低,且PBBs具有亲脂性,较难溶于水,选择提取效率与灵敏度高、选择性好的前处理方法十分必要。常用的前处理技术包括液液萃取[10]、固相萃取[11]、固相微萃取[12]等。液液萃取需消耗大量有机溶剂,且效率低;固相萃取技术需要大体积上样量和浓缩步骤。固相微萃取(SPME)不需要有机溶剂,仅依靠附有固相微萃取涂层的纤维头就能完成提取、分离、浓缩的全过程。
在SPME 基础上,Baltussen等提出了一种新的样品预处理技术——搅拌棒吸附萃取(SBSE),它由10 mm涂有聚二甲氧基硅氧烷(PMDS)的搅拌棒构成。在水中搅拌时,搅拌棒能将待测有机组分萃取并富集到PMDS萃取相,再通过热解吸(TDU)或溶解解吸的方法进行色谱质谱分析[13]。SBSE萃取相体积是SPME的50~250倍,且萃取回收率更好,已用于多环芳烃[14-15]、多氯联苯[16-17]、烷基酚[18]等有机化合物的富集。
1 材料与方法
1.1 仪器与试剂
仪器:气相色谱-质谱联用仪(7890/5975C,美国Aglient公司);热脱附管老化器(TC2,德国Gerstel公司);具备CIS进样口和TDU脱附系统多功能全自动样品前处理平台(MPS,德国Gerstel公司);SBSE固相萃取搅拌棒(规格20 mm×1 mm,25 μL PDMS,德国Gerstel);IKA磁力搅拌器(RT-10,德国);色谱柱HP-5MS(30 m×0.32 mm,膜厚0.25 μm,美国Aglient公司)。试剂:去离子水,PBB混标(PBB-Mix5,10 mg/L,德国Dr.Ehrenstorfer公司)。
1.2 仪器条件
热脱附条件(TDU):不分流模式进样,从100 ℃开始以400 ℃/min的速率升至300 ℃,保持10 min,传输线温度280 ℃;冷进样口从-5 ℃开始以12 ℃/min升至100 ℃,保持15 min。
气相色谱条件:进样口温度:200 ℃; 载气:氦气; 进样方式:不分流进样;柱恒流(恒流模式):1 mL/min;升温程序:从100 ℃开始,保持2 min,以5 ℃/min的速率升至290 ℃,保持5 min。
质谱条件:离子源:电子轰击(EI)源;离子源温度:230 ℃; 离子化能:70 eV;接口温度:280 ℃,四级杆温度150 ℃;溶剂延迟:3.5 min。全扫描(Scan)范围:35~450 u; 在选择离子扫描模式(SIM)下优化SBSE萃取条件,绘制校准曲线,分析实际样品。16种PBBs单体的定量、定性离子及保留时间见表1,其总离子流图见图1。

表1 16种PBBs单体的定量、定性离子及保留时间

图1 16种PBBs单体的总离子流图
1.3 样品处理和分析
1.3.1 SBSE搅拌棒老化
SBSE搅拌棒在初次使用前需要进行条件标准化,将1个搅拌棒放在一根空的热脱附样品管中,插入老化器,通入氮气在300 ℃加热4 h,氮气流量为1 mL/min。为了减少脱附后残留物的影响,实验过程中SBSE搅拌棒每次使用5~6次后需再老化1次,条件与上面相同。
1.3.2 条件影响试验
影响SBSE萃取条件的因素包括:水样体积、基体改进剂、萃取平衡时间。在水样体积影响试验中,采用不同体积的空白加标样品,在其他相同试验条件下,考察样品体积变化对萃取效果的影响。试验水样分别含有体积分数为0,5%和10%的甲醇,考察基体改进剂对萃取响应峰面积的影响。通过在相同水样体积和加标浓度的条件下,改变SBSE的萃取平衡时间,选择最佳的样品萃取时间。
1.3.3 解吸试验
为了减少有机试剂的使用,解吸实验将测定完毕后的SBSE搅拌棒再次通过热脱附过程来解吸SBSE上残留的PBBs化合物。根据SBSE残留PBBs峰面积的变化,确定热脱附解吸次数,并计算解析效率。
1.3.4 样品分析
移取水样10 mL在小烧杯中,加体积分数为10%的甲醇作为基体改进剂,放入搅拌棒,以1 200 r/min搅拌1 h。萃取后,取出搅拌棒,用少量蒸馏水洗涤棒表面,然后用擦镜纸吸去表面水分,采用全扫描方式/SIM方式进行GC/MS测定。
2 结果与讨论
2.1 萃取条件的优化
2.1.1 样品体积的选择
分别采用10,25,50 mL空白加标样品(加标量为50 ng),SBSE相同转速下萃取1 h后热脱附解吸分析样品,考察峰面积变化。以PBB3、PBB7、PBB30、PBB49、PBB101和PBB153为例,结果见图2。

图2 不同体积水样SBSE萃取响应值丰度
由图2可见,随着水样体积增加,在相同加标量的情况下,各组分响应值下降,即随着样品体积的增加萃取效率呈下降趋势,因此该试验选择的样品体积为10 mL。
2.1.2 SBSE萃取时间的选择
考察了10 mL空白加标水样(50 ng/L)中PBBs化合物在不同萃取时间(0.5~4 h)的响应峰面积的变化趋势。以PBB3、PBB7、PBB30、PBB49、PBB101和PBB153为例,结果见图3。

图3 萃取时间对响应丰度的影响
由图3可见,萃取时间从0.5 h增加到1 h时,PBB3、PBB7和PBB30响应值增幅较大,而PBB49、PBB101、PBB153各组分响应值增幅较小;随着萃取时间的延长,各组分响应值的增加缓慢,趋于平衡。为提高萃取效率,选择1 h为最佳萃取时间。
2.1.3 SBSE基体改进剂的影响
PBBs化合物是疏水性物质,易被容器壁吸附,为了消除器壁的影响,提高萃取效率,分别在10 mL 空白加标水样(50 ng/L)中加入体积分数为0,5%,10%的甲醇后在相同转速下萃取1 h,以PBB3、PBB7、PBB30、PBB49、PBB101和PBB153为例,结果见图4。

图4 甲醇对萃取响应丰度的影响
由图4可见,加入甲醇能明显提高萃取效率。6种PBBs化合物随水样中甲醇体积分数增加,各物质响应峰面积均有增加。考虑到提高PBBs分析灵敏度,试验选择添加10%甲醇。
2.1.4 SBSE解吸残留实验
将测定完毕后的SBSE搅拌棒再次通过热脱附过程来解吸SBSE上残留的PBBs化合物。为了掌握解吸是否完全,将测定完毕后的SBSE搅拌棒通过热脱附过程连续解吸3次,单次解吸的响应峰面积与3次峰面积之和的比值定义为解吸率。以PBB3、PBB7、PBB30、PBB49、PBB101和PPBB153为例,6种PBBs的3次热脱附解吸率见图5。
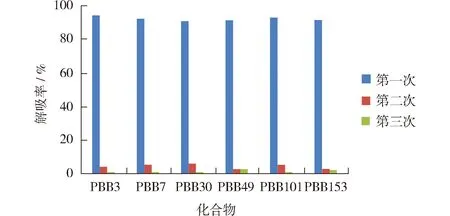
图5 6种PBBs化合物的解吸率
由图5可见,第一次热脱附的解吸率都在90%以上,考虑到实验效率,在实际分析时解吸1次即可。
2.2 方法能效评价
取10 mL试验用水于小烧杯中,加入体积分数为10%的基体改进剂甲醇,用微量注射器分别移取一定体积的标准样品注入水中,配制含有16种PBBs目标化合物,5个校准系列质量浓度分别为2,5,10,20和50 ng/L。放入搅拌棒,以1 200 r/min搅拌1 h,萃取完成后,取出搅拌棒,用少量蒸馏水洗涤棒表面,然后用擦镜纸吸去表面水分,参照仪器参考条件1.2,采用SIM方式进行GC/MS测定。从低浓度到高浓度依次进样分析,记录标准系列目标物和对应内标的保留时间、定量离子的响应值,绘制标准曲线,相关系数见表2。
采用该方法分别萃取7个空白加标平行样(加标量为2 ng/L),做精密度实验,并计算7次平行测定的标准偏差,按照式(1)计算方法检出限,方法测定下限为4倍检出限。
MDL=t(n-1,0.99)×S
(1)
式中:MDL——检出限;n——样品的平行测定次数;t——自由度为n-1,置信度为99%时的t分布(单侧)(n=7时,t=3.143);S—n次平行测定的标准偏差。

表2 16种PBBs的相关系数、精密度、检出限与测定下限实验结果
2.3 实际样品测定和加标回收实验
用该方法测定常州魏村水厂的饮用水源水样品,并做2个质量浓度水平的加标回收实验(10和50 ng/L),每个浓度水平做7次平行实验。其中,实际水样中16种PBBs均未检出,加标实验结果见表3。

表3 加标回收实验结果
[1] 刘国瑞,李丽,孙素芳,等.多溴联苯的污染来源、分析方法和环境污染特征[J].化学进展,2014,26(8):1434-1444.
[2] 董亮,张秀蓝,史双昕,等.新型持久性有机污染物分析方法研究进展[J].中国科学:化学,2013,43(3):336-350.
[3] WANG M S,CHEN S J,HUANG K L,et al.Determination of levels of persistent organic pollutants (PCDD/Fs,PBDD/Fs,PBDEs,PCBs,and PBBs) in atmosphere near a municipal solid waste incinerator[J].Chemosphere,2010,80(10):1220-1226.
[4] ZHANG W H,WU Y X,SIMONNOT M O .Soil Contamination due to E-Waste Disposal and Recycling Activities:A Review with Special Focus on China[J].Pedosphere,2012,22(4):434-455.
[5] CLARKE B,PORTER N,SYMONS R,et al.Polybrominated diphenyl ethers and polybrominate d biphenyls in Australian sewage sludge[J].Chemosphere,2008,73(6):980-989.
[6] MALAVIA J,SANTOS F J,GALCERAN M T.Simultaneous pressurized liquid extraction and clean-up for the analysis of polybrominated biphenyls by gas chromatography-tandem mass spectrometry[J].Talanta,2011,84(4):1155-1162.
[7] JOANNA G,ADAM G,RYSZARD C.PBB levels in fish from the Baltic and North seas and in selected food products from Poland[J].Chemosphere,2010,78(10):1272-1278.
[8] SONG Q B,LI J H.A systematic review of the human body burden of e-waste exposure in China[J] .Environment International,2014,68:82-93.
[9] 陈良壁,曾景斌,马春华.多壁碳纳米管固相微萃取纤维制备及其在海水中多溴联苯测定中的应用[J].中国科学 B辑:化学,2009,39(12):1652-1657.
[10] 何松洁,李明圆,金军,等.凝胶渗透色谱柱去脂-气相色谱-质谱法测定人血清中新型卤系阻燃剂[J].分析化学研究报告,2012,40:1054-1062.
[11] PEPICH B V,PRAKASH B,DOMINO M M,et al.Development of U.S.EPA Method 527 for the analysis of selected prestides and flame retardants in the UCMR Survery[J].Environmental Science & Technology,2005,39(13):4996-5004.
[12] POLO M,GOMEZ-NOYA G,QUINTANA J B,et al.Development of a solid-phase microextraction gas chromatography/tandem mass spectrometry method for polybrominated diphenyl ethers and polybrominated biphenyls in water samples[J].Analytical Chemistry,2004,76(4):1054-1062.
[13] 曾凡刚.SBSE-TDU-GC快速测定茶叶中7种拟除虫菊酯类农药残留[J].农药,2010,49(4):277-279.
[14] 徐媛,刘文民,赵景红,等.固相萃取搅拌棒萃取-气相色谱分析海水中的多环芳烃[J].分析化学,2005,33(10):1401-1404.
[15] 杨蕾,王宝兴,候英,等.应用搅拌棒吸附萃取-热脱附-气相色谱/质谱法快速测定滇池水系中的16种多环芳烃[J].色谱,2007,25(5):745-752.
[16] 顾海东,秦宏兵,尹燕敏,等.SBSE-GC/MS法测定水源水中7种多氯联苯单体[J].环境监测管理与技术,2010,22(2):44-47.
[17] 曹小吉,王丽萍,江南,等.搅拌棒吸附萃取-气相色谱-质谱法测定化妆水中多氯联苯[J].理化检验:化学分册,2012,48(6):705-708.
[18] 秦宏兵,顾海东,张晓赟.搅拌棒吸附萃取-热脱附-气相色谱-质谱法测定水中3种烷基酚[J].理化检验:化学分册,2014,50(5):602-605.
Simultaneous Determination of 16 PBBs in Drinking Source Water by Stir Bar Sorptive Extraction-Thermal Desorption-Gas Chromatography/Mass Spectrometry
DONG Li-jing1,DAI Xuan-li2,TENG Jia-quan1,ZHANG Lin-zhi1,YU Yi-jun1,XUE Yin-gang1*
(1.ChangzhouEnvironmentalMonitoringCenter,Changzhou,Jiangsu213001,China;2.JiangsuXinruiEnvironmentalMonitoringCo.Ltd.,Lianyungang,Jiangsu215600,China)
A total of 16 polybrominated biphenyls (PBBs) in drinking source water were determined by GC/MS with stir bar sorptive extraction (SBSE) and thermal desorption technique.By optimizing the process of extraction and desorption,the results showed good linearity ranging from 2 to 50 ng/L.With the sampling volume of 10 mL and SBSE of 1 h,the detection limits of 16 PBBs were between 0.5 and 1.1 ng/L.The recovery test was carried out by standard addition of two concentrations into actual water samples,and the average recovery rates were in the range of 89.2%~102%.
Polybrominated biphenyls; Stir bar sorptive extraction; GC/MS; Drinking source water
2015-05-04;
2015-07-05
江苏省环境监测科研基金资助项目(1302)
董黎静(1980—),女,工程师,博士,研究方向为环境中有机物的检测分析。
*通讯作者:薛银刚 E-mail:yzxyg@126.com
X832;O657.6;O657.7
B
1674-6732(2015)05-0037-05
