瑞舒伐他汀钙口腔崩解片的制备及溶出度测定方法
2015-04-07张瑞杰王静侯娟
张瑞杰 王静 侯娟
作者单位: 066000河北省秦皇岛市妇幼保健院(张瑞杰) ;河北医科大学药学院(王静) ;河北医科大学第四医院(侯娟)
瑞舒伐他汀钙口腔崩解片的制备及溶出度测定方法
张瑞杰王静侯娟
作者单位: 066000河北省秦皇岛市妇幼保健院(张瑞杰) ;河北医科大学药学院(王静) ;河北医科大学第四医院(侯娟)
【摘要】目的确定瑞舒伐他汀钙口腔崩解片制备的工艺参数,建立体外溶出度测定方法。方法分别考察了不同原料药粒度、制粒筛目数、颗粒含水量和硬度对口崩片质量的影响;采用《中国药典》2010年版中规定的篮法测定溶出度,紫外分光光度法测定溶液吸光度,并对溶出度测定方法进行验证。结果确定了瑞舒伐他汀钙口腔崩解片制备的工艺参数;溶出度测定方法的准确度高,精密度好,辅料不干扰测定。结论该制剂制备工艺简单、合理;溶出度测定方法准确可靠。
【关键词】瑞舒伐他汀钙;口腔崩解片;工艺参数;溶出度
项目来源:河北省医学科学研究重点课题计划(编号: 20110124)
瑞舒伐他汀钙是新一代HMG-COA还原酶抑制剂,较其他同类药物显示出更好的调脂效果,并能逆转动脉粥样硬化的进程,促使斑块消退,减少心血管事件发生率和死亡率,被医药界誉为“超级他汀”。目前在国内上市的瑞舒伐他汀钙有片剂和胶囊剂,为满足患者需求,本课题组研制了瑞舒伐他汀钙口腔崩解片并对其处方组成进行了优化[1],本文对瑞舒伐他汀钙口崩片制备工艺研究过程报告如下。
1 仪器与试药
1.1仪器T6新世纪-紫外可见分光光度计(北京普析通用仪器有限责任公司),ZRS-8G溶出试验仪(天津大学无线电厂),电子天平(上海浦春计量有限公司),DP30A单冲压片机(北京国药龙立科技有限公司) ; YD-1片剂硬度仪(天津鑫州科技有限公司),DHG-9053A型电热恒温鼓风干燥箱(上海一恒科技有限公司)。
1.2试药瑞舒伐他汀钙对照品(中国药品生物制品检定所,批号: 101028-201001),瑞舒伐他汀钙原料药(南京正大天晴制药有限公司,批号: 20111013,纯度98.0%),瑞舒伐他汀钙口腔崩解片(自制,批号: 20120528、20120529、20120530),交联聚维酮(北京风礼商贸有限责任公司),乳糖(天津市化学试剂一厂),甘露醇(北京索莱宝科技有限公司),阿斯巴甜(广州市芬美源生物科技有限公司),甜菊糖(杭州普修生物科技有限公司),薄荷脑,香橙香精(上海华宝孔雀香精香料有限公司),硬脂酸镁(天津市永昌盛化工有限公司)。
2 方法与结果
2.1口腔崩解片制备工艺参数的确定依照处方称取主药及辅料,混合均匀后加粘合剂制软材,过筛制得湿颗粒,干燥得干颗粒,整粒,Φ 6 mm浅凹冲压片,整个过程避光操作。
2.1.1原料药的处理:瑞舒伐他汀钙原料过80目120目筛,与辅料混合均匀后制粒、干燥、整粒、加入外加辅料混合后压片,测定瑞舒伐他汀钙口崩片15 mi溶出量[2]。不同粒度的瑞舒伐他汀钙所制得口崩片其15 min的溶出量无明显差别,且均大于85%;因此瑞舒伐他汀钙原料粒径大小对制备过程及片剂的溶出行为无影响。故选择80目筛对瑞舒伐他汀钙原料进行处理。见表1。

表1 原料药粒度对产品质量影响的测定结果
2.1.2制粒筛目数的选择:选用过80目筛的瑞舒伐他汀钙,与辅料混合均匀,制软材,分别用20目、30目及40目筛网制粒,40℃干燥,再用20目、30目及40目筛网整粒,将颗粒与外加的辅料混匀后压片,以总混物料的混合均匀度及重量差异为指标,选择制粒筛目数[3]。使用20目筛所制颗粒较大,与外加辅料混合易分层,片剂混合均匀度较差(RSD大于3.0% ),重量差异较大(超出了±7.5%的限度),40目筛制粒时物料不易通过筛网。综合考虑颗粒的流动性及制粒时的难易程度,确定以30目筛制粒。见表2。
2.1.3颗粒水分的选择:颗粒中含有适量的水分能增加颗粒的塑性形变,减少弹性,有利于压片,硬度亦较好。依据文献,以片子的外观、硬度、脆碎度为指标,考察颗粒水分对瑞舒伐他汀钙口崩片质量的影响[4]颗粒水分为5%时,有粘冲现象;而颗粒水分为0.5%时,颗粒的静电作用明显,片剂硬度较小,脆碎度较大不利于包衣。本结果显示,只有颗粒水分在1% 3%,片剂的外观良好,硬度和脆碎度能够满足包衣要求。因此,干燥过程中控制颗粒水分1.0%~3.0%。见表3。

表2 混合均匀度及重量差异测定结果
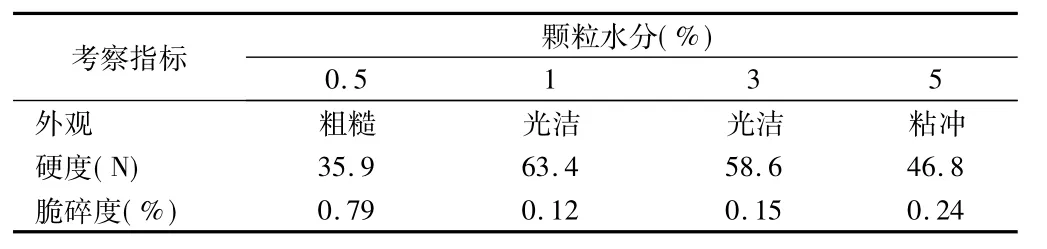
表3 颗粒水分考察结果
2.1.4片剂硬度的选择:压片时,调解压力调节器,得到平均硬度分别为30 N、60 N及100 N的片子,以崩解时限、脆碎度及15分钟溶出量为指标[5],对片子硬度进行选择。片子平均硬度为30 N时,崩解时限短,脆碎度大于1%;片子平均硬度为60 N时,脆碎度较小,但崩解时限长,15 min的溶出量降低;片子平均硬度为40 N,片剂崩解时限较短,脆碎度小于1%,15 min的溶出量大于85%。因此,硬度控制在35~45 N。见表4。
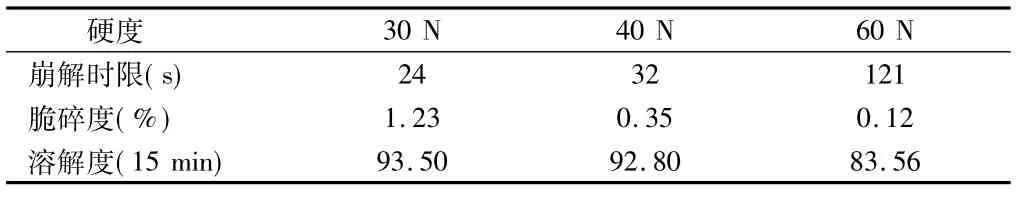
表4 硬度选择
2.1.5验证试验:依照确定的工艺参数制备3批样品,对其进行全面质量检查。3批样品各项指标均符合质量要求。由此可知确定的工艺参数合理可行。见表5。
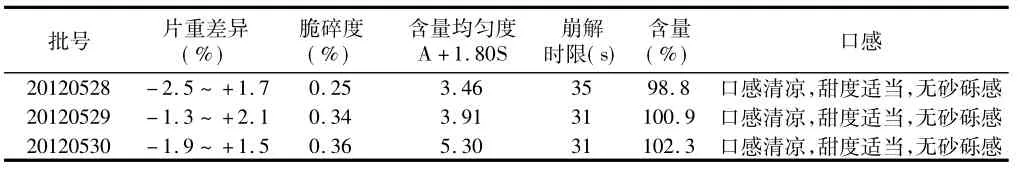
表5 验证试验结果
2.2瑞舒伐他汀钙口腔崩解片溶出度测定方法的方法学验证
2.2.1紫外吸收特性:精密称取150 mg瑞舒伐他汀钙原料药,置50 ml量瓶中,超声15 min溶解后,加水稀释至刻度,摇匀。精密量取稀释液1 ml置250 ml量瓶中,以水定容至刻度。于200~400 nm范围内进行紫外扫描,扫描结果显示在241 nm处有最大吸收,确定241 nm为测定波长[6]。见图1。
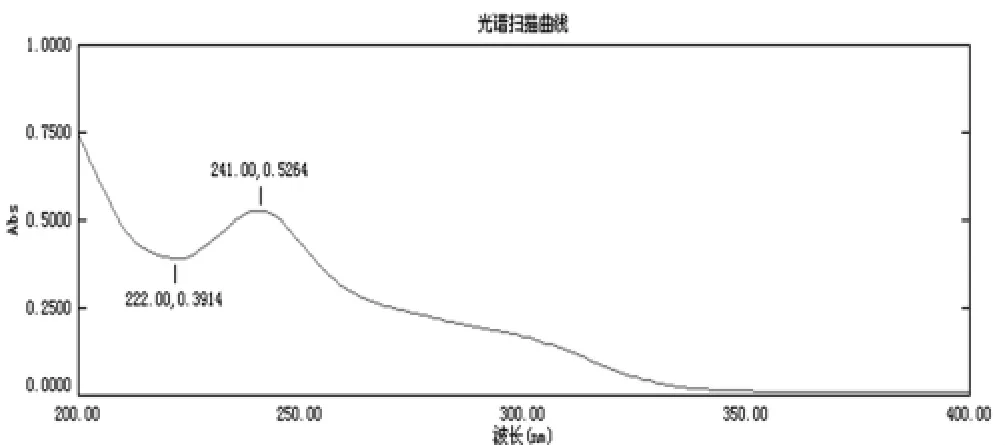
图1 光谱扫描曲线
2.2.2辅料干扰试验:取不含主药的空白辅料适量置于100 ml量瓶中,加水至刻度,超声溶解,经0.45 μm微孔滤膜过滤,取续滤液5 ml,置于50 ml容量瓶中加水至刻度,摇匀,即得空白辅料溶液,于20~400 nm范围内进行光谱扫描,结果显示,空白辅料对主药的测定无影响。见图2。
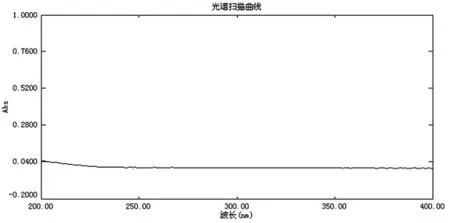
图2 空白辅料光谱扫描曲线
2.2.3标准曲线的制定:称取瑞舒伐他汀钙对照品10 mg,精密称定,置100 ml量瓶中,加水适量,超声15 min溶解后加水稀释至刻度,摇匀。分别量取0.5 ml、1.0 ml、1.5 ml、2.0 ml、2.5 ml、3.0 ml至25 m量瓶中,用水定容至刻度。采用紫外分光光度法,于241 nm处测定吸光度。以浓度(C)为横坐标,吸光度(A)为纵坐标绘制标准曲线,得回归方程A=0.038 -0.002,r=0.9998。结果表明瑞舒伐他汀钙浓度在2.22~13.32 μg/ml范围内与吸光度线性关系良好2.2.4回收率试验:分别精密称取瑞舒伐他汀钙约6 mg、10 mg、13 mg,加入相应处方量辅料,置于100 m量瓶中,加入适量水,超声15 min,用水定容至刻度,精密量取1 ml置10 ml量瓶中,用水定容至刻度,过滤滤液在241 nm处测定吸光度,重复测定3次。结果显示,高、中、低三个浓度样品的回收率分别为102.4% 102.1%,101.9%,平均RSD为0.25% (n=3),符合要求。
2.2.5精密度试验:将2.2.4项配制的高、中、低3个浓度样品在1 d内重复测定3次并连续测定3 d,3个浓度样品的日内RSD分别0.49%、0.56%、0.44% (n=3),日间RSD分别为0.42%、0.29%、1.07% (n=3),精密度良好。
2.2.6溶液稳定性考察:称取10 mg瑞舒伐他汀钙置于100 ml量瓶中,加水适量,超声溶解,用水定容至刻度。再量取稀释液5 ml至50 ml量瓶中,加水定容至刻度。分别在0 h、1 h、2 h、3 h、4 h、8 h时测定吸光度。分避光与不避光的2组进行实验,避光组6个时间点吸光度值的RSD为0.45% (n=6),不避光组6个时间点吸光度值的RSD为0.34% (n=6)。结果表明瑞舒伐他汀钙溶液在避光与不避光环境中8 h内稳定性良好。
2.2.7溶出度测定结果:依照《中国药典》2010年版二部附录第一法(篮法)[7],以1 000 ml水为溶出介质,转速为100 r/min,溶出温度为37℃。检测方法为紫外分光光度法,检测波长为241 nm。3批样品在5 min时均已溶出完全,释药迅速,符合规定。见表6。
表6 三批口崩片的溶出度测定结果 n=6,%±s

表6 三批口崩片的溶出度测定结果 n=6,%±s
批号5min 10 min 15 min 20 min 25 min 30 min 20120528 97.6±0.74 108.8±0.48 108.4±0.74 108.4±0.74 108.4±0.74 108.2±0.74 20120529 98.3±0.29 100.3±0.58 100.3±0.58 100.4±1.05 100.2±0.29 100.3±0.50 20120530 97.9±0.77 108.2±0.29 109.3±0.77 109.2±0.58 109.2±0.58 109.3±0.50
3 讨论
瑞舒伐他汀钙是近年来研发的一种新型他汀类调脂药,其可选择性抑制肝脏中的3-羟基3-甲基戊二酰辅酶A(HMG—COA)还原酶,干扰胆固醇的合成,较其他同类药物显示出更好的调脂效果。同时,其安全性和耐受性良好,不良事件发生率低。该药于2009年列入我国“医保”目录。基于瑞舒伐他汀钙良好的疗效和安全性,加之该药上市剂型少(只有普通片剂和胶囊),为满足患者需求,本研究选择瑞舒伐他汀钙为模型药物,研制其口腔崩解片。该药不需要水或只需少量水即可顺利吞下,具有吸收快、起效快、肝脏首关效应小、生物利用度高、对胃肠道刺激小、服用方便等优点,特别适合老人及吞咽困难的患者。本研究考察了制备瑞舒伐他汀钙口崩片的工艺参数,所确定制备工艺简单可行,产品质量稳定可控。本文还建立了瑞舒伐他汀钙口崩片溶出度测定方法并进行了方法学考察,结果表明,该溶出度测定方法准确,可靠,能够对瑞舒伐他汀钙口腔崩解片的质量进行有效的体外控制。
参考文献
1侯娟,王静.瑞舒伐他汀钙口腔崩解片的制备工艺优化.中国药房2013,24: 4270-4272.
2汪涛,丁立秀.瑞舒伐他汀钙原料药中有关物质的测定.现代药物与临床,2014,29: 603-606.
3孙俊.瑞舒伐他汀钙片的含量及溶出度测定.中国药业,2010,19 30-31.
4鲁迪.高效液相色谱法测定瑞舒伐他汀钙片的含量.中国处方药2014,12: 34-35.
5张得胜,庄波阳,王凌.高效液相色谱法测定瑞舒伐他汀钙片有关物质.海峡药学,2013,25: 29-32.
6魏碧凤.HPLC测定瑞舒伐他汀钙片的含量及溶出度.海峡药学2012,24: 88-90.
7中华人民共和国国家药典委员会.中国药典.第二部.北京:化学工业出版社,2010.附录85-87.
·护理研究·
(收稿日期:2014-10-18
doi:10.3969/j.issn.1002-7386.2015.09.048
【文章编号】1002-7386(2015) 09-1411-03
【文献标识码】A
【中图分类号】R 917
