经皮经肝穿刺胆囊外引流术治疗重症急性胆囊炎
2015-03-24孙青龙董重谋付雪峰
孙青龙 董重谋 黄 锐 薛 辉 付雪峰
黑龙江省牡丹江林业中心医院放射介入科,黑龙江牡丹江 157000
急性胆囊炎是普外科常见的急腹症之一,临床上常需急诊行开腹或腹腔镜下胆囊切除术治疗,但对于老年合并严重基础疾病的患者,急诊手术和麻醉风险明显加大,特别是伴发严重疾患或胆囊极度肿大、周围组织渗出水肿明显患者,其并发症和死亡率明显增加。近年来,随着介入诊疗技术的快速发展,经皮经肝穿刺胆囊外引流术作为急性重症性胆囊炎患者姑息性治疗越来越被临床医师和患者接受,为评价该技术的可行性和有效性,本研究回顾性分析3年来我科室通过该技术治疗的42例患者的临床相关资料,现报道如下。
1 资料与方法
1.1 临床资料
本组患者42例,男24例,女18例;平均年龄72岁。术前均有典型胆囊炎临床症状及体征,均经实验室及彩超、CT或MRCP检查证实胆囊肿大、胆囊结石,胆囊壁增厚及腔内积气,胆囊窝周围渗出,组织粘连等相关影像(图1 ~ 4)。其中高龄合并严重基础疾病31例,胆囊肿大明显周围渗出组织粘连明显11例。术前均经院里相关科室会诊后,认为均不能急诊行胆囊切除术。
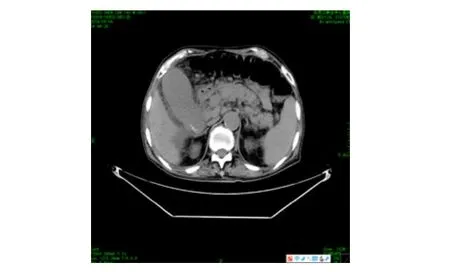
图1 胆囊增大,壁周围渗出,见多发结石
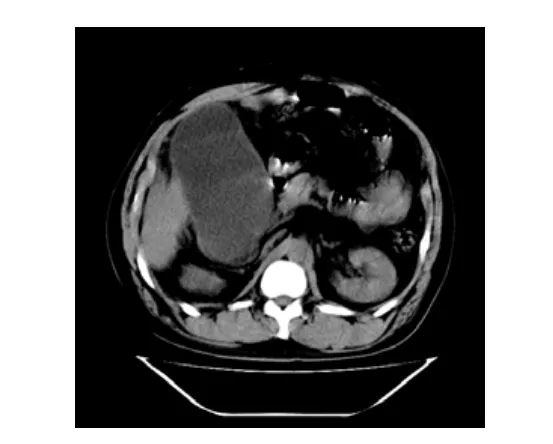
图2 胆囊明显肿大,壁变薄
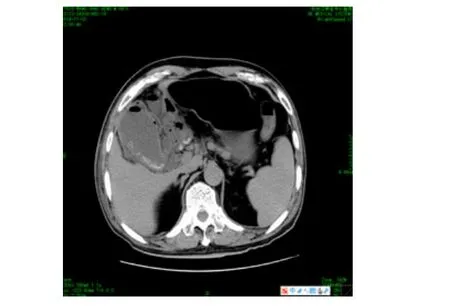
图3 胆囊内多发结石,腔增大可见胆囊底积气,周围渗出明显
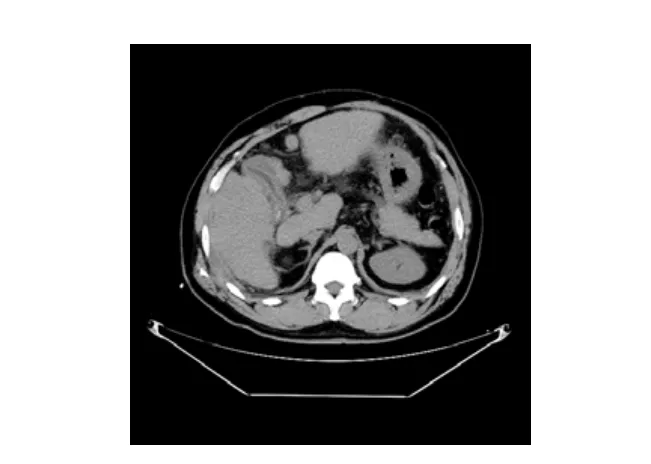
图4 PTGBD术撤除外引流观后见胆囊壁仍明显增厚
1.2 方法
患者术前均经CT定位,选择胆囊与肝脏接触面积最大层面确定体表穿刺点,根据CT测量穿刺的距离和角度,穿刺路径经过肝脏,从胆囊与肝脏紧密接触处穿刺进入胆囊。定位后患者平躺DSA检查床上,常规心电监护、吸氧。穿刺点局麻后,切开2mm小口,用18G穿刺针根据术前CT定位导向进针,穿刺成功后,抽出10mL胆汁,做菌培养,经穿刺针鞘管推注部分造影剂,明确胆囊的形态及位置,引入超滑导丝,在胆囊腔内成袢,置入外引流管,造影证实引流管位于胆囊内(图5~8)。体表蝶形固定翼固定外引流管,接引流袋引流胆汁。术后继续抗炎、保肝、补液等对症治疗,并根据胆汁药敏结果调整抗菌药物和冲洗外引流管。
2 结果
41例患者CT定位DSA引导下胆囊穿刺成功,1例因胆囊床固定较少漂浮腹腔内穿刺失败,急诊外科手术,术后DIC死亡。40例患者术后24 ~ 72h临床症状、体征明显缓解(表1);9例非结石性胆囊炎患者术后1个月拔管康复;31例患者结石性胆囊炎患者1 ~ 2个月后行胆囊切除术。1例患者胆囊穿刺置管成功后,引流不畅,行外科胆囊切除术,术后病理回报胆囊坏疽(图9~10)。

图5 见穿刺针进入胆囊内造影见结石充盈缺损影
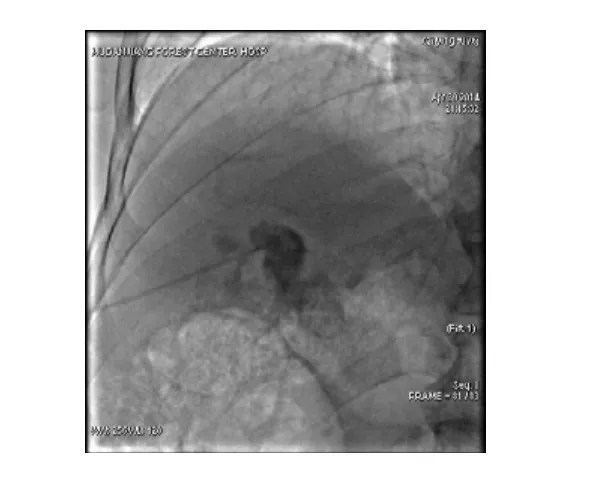
图6 经穿刺针外鞘推注造影剂见快速弥散在增大的胆囊腔内
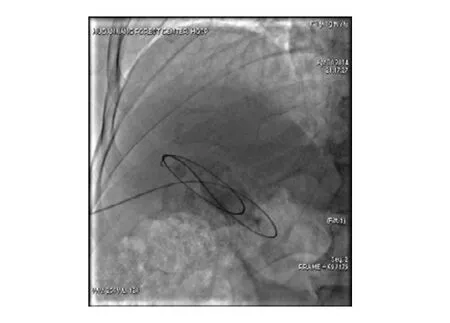
图7 经鞘管引入导丝于胆囊腔内成袢

图8 经导丝引入外引流流管造影证实位于胆囊腔内
41例患者胆汁细菌培养肺炎克雷伯杆菌11例、日沟维肠杆菌2例、大肠埃希菌3例、表皮葡萄球菌2例、路邓葡萄球菌1例、弗氏枸橼酸杆菌4例、屎肠球菌2例、阴沟肠杆菌2例、14例胆汁细菌培养48h无细菌生长。其中大部分胆汁细菌药敏证实革兰氏阴性细菌感染,对氨基糖苷类抗生素(庆大霉素)及喹诺酮类抗生素(氧氟沙星)敏感、第三代头孢菌素类抗生素(头孢哌酮)敏感。

图9 同一患者术前胆囊肿大,渗出明显,术后1周胆囊明显缩小,渗出减少
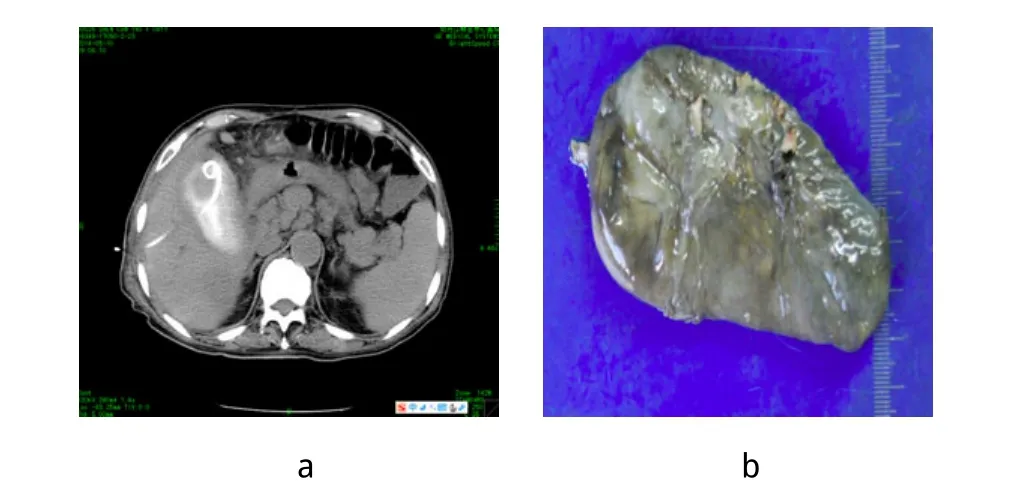
图10 另一患者PTGBD术后1d胆囊炎症状体征加重,外科切除后见胆囊完全坏疽

表1 PTGBD治疗前后疗效观察
3 讨论
急性胆囊炎是常见的外科急腹症,按照其发病学及临床表现特点可分为急性结石性胆囊炎和非结石性胆囊炎,急性结石性胆囊炎是最常见的一种类型,约占人总数的90%~95%,其发生与解释嵌顿造成胆囊出口梗阻有关,临床上表现为急性胆囊炎的典型特征。目前主要治疗方法是开腹或腹腔镜下胆囊切除术。但对于老年患者合并严重基础疾病,如高血压、肺心病、糖尿病、心脏病等的重症患者,外科手术及麻醉风险明显增加,经皮经肝穿刺胆囊外引流术作为一种急性期的姑息性治疗方法能明显改善患者临床症状及体征,降低急性期并发症及病死率,从而使患者获得外科择期手术的机会,对于部分非结石急性胆囊炎患者能够达到治愈目的[1]。
关于经皮套管针胆囊穿刺减压术记录最早可追溯到1743年,于19世纪末应用于临床[2]。通过直接经皮穿刺实施的诊断性胆囊造影,最早完成于1922年,但很快被口服胆囊造影所取代[3]。在发明抗生素及应用局部成像技术前,经皮胆囊穿刺外引流术由于具有感染胆汁外漏致使重度或致命性腹膜炎的高风险,通常仅被用于急诊造影或外科手术前的减压治疗。最初大家担心胆囊穿刺或置管可能导致患者死亡率增加,但是,自1979年以来,越来越多的报道证实了超声引导下使用适当的穿刺针和引流管经皮胆囊穿刺外引流术的安全性[4-5]。现在的经皮经肝胆囊穿刺外引流术技术已经相当规范,并且被广泛应用于临床诊断和治疗中。
急性胆囊炎可能是一些危重患者,特别是大手术或创伤后多系统功能障碍患者未被发现的致命并发症。右上腹疼痛、发热、白细胞增多以及可触及的 可能很难被发现或者难以同其他器官系统并发症相鉴别。其他检查,如超声或肝胆CT,对于危重患者和卧床患者用来诊断急性胆囊炎并不可靠。这些患者通常因病情太重而不能承受胆囊切除术。相比之下,经皮经肝穿刺胆囊外引流术治疗这些复杂病例的安全方法。与外科手术相比,经皮方法的优点包括:安全性高,仅需要局麻及少量镇静或不需要镇静,即使急性胆囊炎诊断错误,也只有较小的风险。最初认为急性胆囊炎的诊断需要依靠胆汁查到细菌、存在浓汁及等待细菌培养阳性。然而随着经验的增长McGahan和Lindfors指出胆汁检验的敏感度低于50%,最可能的原因是有效的抗生素使胆汁无菌,或者是在感染过程中胆囊炎不是主要的因素。同样,胆囊内胆汁抽吸物阴性的结果也不能排除急性胆囊炎的诊断。今天,通过持续胆囊引流患者的观察,如果48h后退热、白细胞计数恢复正常及临床症状明显缓解,即使是胆汁无感染证据,通常也可以诊断急性胆囊炎。如果临床症状无明显改善,应该立即行胆管造影来证实胆囊管是否通畅。胆管狭窄也能引起败血症,并且可以通过扩张和经胆囊管的超选择引流来治疗。胆囊重度积脓很快就可以致命,但如果早期诊断,并迅速充分的经皮引流,生存率仍很高。所有通过导管技术治疗或诊断的胆囊炎患者,如果发展到右上腹疼痛加重或出现腹膜炎体征,表明胆囊发生坏疽或穿孔,应该考虑立即行胆囊切除术[7]。
拟行经皮经肝穿刺胆囊外引流术治疗重症急性胆囊炎的患者应进行详细的术前病史采集和体格检查;检查基础的血清胆红素,淀粉酶,脂肪酶,碱性磷酸酶,血常规,正常或可纠正后的凝血功能。因为病态胆囊内的胆汁通常是感染性的,诊断性造影检查或介入操作前1~4h应给予广谱抗生素,并持续12h。当存在胆囊炎或者胆管炎时,抗生素应用时间可以更长一些。如果可能的话,术前应重复腹部超声或CT检查仪以帮助确定穿刺胆囊的路径。为控制疼痛,该手术通常在静脉镇静局麻下进行。如果胆囊体积增大或张力高并突出于肝下缘,可于超声实时监测下,用导管鞘针或套管针直接经肝或于肝下穿刺胆囊。目前,市售的各种带鞘穿刺针,可放在带有许多侧孔的可锁袢的引流管内[8]。这样在提供较好引流的同时,大大降低了引流管移位的几率,进而减少了胆汁性腹膜炎的发生。尽管理论上一步法可以防止胆汁溢出到腹腔内,并在紧急情况下可用于床边操作,但是,此法并不能保证绝对安全,尤其在胆囊不增大或胆囊壁慢性增厚的情况下[9]。因胆囊可能被推移位,内陷或穿孔和进一步压缩。在穿刺困难时使用大直径套管针穿刺胆囊的无效操作可能会导致肝脏撕裂或附近肠管的穿孔,对慢性胆结石且胆囊不大的患者,首先通过同轴的22G或17G的带鞘针置入一个可以移去的固定装置更安全,这样可以使纤维化的胆囊固定,防止在胆囊穿刺引流置管术过程中路径丢失或阻止胆囊壁的内陷[10]。引流管放置后,每天监测引流量,用生理盐水定期冲洗以维持导管通畅。胆汁引流量随着患者病情的稳定和胆总管功能的恢复,将逐渐减少。定期随访导管,以防止移位和脱落。因为经肝穿刺途径行胆囊穿刺引流术窦道的形成需要2~6周,尤其是老年人和慢性消耗性患者,过早拔出引流管会引起胆囊漏或腹膜炎,由于这个原因,术者在拔管前应使用导丝及对比剂定期复查引流道。
经皮经肝穿刺胆囊外引流术治疗重症急性胆囊炎术的并发症主要有出血、胆瘘、导管移位和邻近器官损伤。并发症发生率5%~10%。技术成功率95%~100%,有效率在70%~85%。病情明显改善常在72h后。30d的死亡率为10%~20%。胆汁漏出所致症状性腹膜炎是经皮经肝穿刺肝胆管引流和胆囊外引流术的严重并发症。一些进行经皮胆管操作的患者,可能形成大量的胆汁性腹水,而没有立即表现出腹膜炎的改变,而另一些患者,小量胆汁漏出就可能引起严重的胆汁性腹膜炎。很明显,细菌感染在此并发症中起最主要的作用。这一点已经在试验中得到证实,向大鼠腹腔内注入胆汁并未产生有害的影响。然而,当接种胆汁中混有大肠埃希菌时,所致的发病率明显高于单纯注射胆汁所致的发病率[11]。通过使用直径小的穿刺针和导管,以及在胆囊注入无菌盐水稀释造影剂后立即将其内胆汁抽出的方法,可以减少感染胆汁的漏出。在行经胆囊介入操作前,应给予广谱抗生素预防感染。除胆汁性腹膜炎外,胆汁漏出也可以发生在数天或数周之后。如果拔出引流管时不注意,或引流管错放至腹膜腔,或引流管拔出过早,可能并发胆汁漏。应该记住,老年和身体虚弱的患者胆囊外引流术窦道形成需要4~6周,免疫缺陷的患者,可能需要2~3个月甚至更长时间。其他并发症还包括胆道出血、严重的迷走神经反应、气胸、腹腔内出血和败血症。尽管应用性能良好的穿刺针和导管进行单纯的诊断性胆囊造瘘术后并发症少。但是,大样本的回顾性研究证实需要外科手术、输血或血管加压治疗的主要并发症发生率达5.6%~8.7%[12]。这些并发症的发生通常是因为病变累及胆囊壁,使用了较粗的套管针和引流管或存在严重的并发症或多系统功能衰竭。因操作引起的出血、胆囊穿孔和败血症的发病率低于2%,并且如前所述常与患者并发症的治疗情况相关。
经皮经肝穿刺胆囊外引流术是进行细菌学诊断和对比研究的一种安全方法,当作为介入操作的入路时,患者能较好耐受。对合并多种危险因素的急重症患者,即试用姑息性治疗,也可以作为最终治疗手段[13]。
[1] 张秋学,杨东山,张磊.胆囊穿刺引流治疗老年急性坏疽性胆囊炎40例[J].中国现代普通外科进展,2012,15:329-330.
[2] Glenn F,Grafe WR Jr. Historical events in bioliary tract surgery[J].Arch Surg,1966,93:848-855.
[3] Burckhardt H,Muller W. Versuche über die punktion der Gallenblseundihre Rntgendarstellung[J].Dtsch Z Chir,1921,162:168-171.
[4] Elyaderani M,Gabriele O.Percutaneous chelecystostomy and cholangiography in patients with obstructive jaundice[J].Radiology,1979,130:601-602.
[5] Shaver RW,Hawkins IF Jr,Soong J. Percutaneous cholecystostpmy[J].AJR Am J Roentgenol,1982,138:1133-1136.
[6] Bryne MF,Suhocki P,Mitchell RM,et al. Percutaneous cholecystostomy in patients with actue cholecystitis:experience of 45 patients at a US referral center[J].J AM Coll Surg,2003,197:206-211.
[7] 董寅,繆金透.老年急性胆囊坏疽穿孔24例临床分析[J].肝胆外科杂志,2004,12(5):363-364.
[8] McGahan JP.A new catheter design for percutaneous cholecystostomy[J].Radiology,1988,166:49-52.
[9] Sosna J,Copell L,Kane RA,et al. Ultrasound-guided percutaneous cholecystostomy:update on technique and clinical applications[J].Surg Technol Int,2003,11:135-139.
[10] Cope C.Percutaneous subhepatic cholecystostomy with removable anchor[J].AJR Am J Roentgenol,1988,151:1129-1132.
[11] Andersson R,Tranberg KG,Bengmark S. Roles of bile and bacteria in biliary peritonitis[J].Br J Surg,1990,77:36-39.
[12] Teplick SK,Brandon JC,Wolferth CC,et al. Percutaneous interventional gallbladder procedures:personal experience and literature review[J].Gastrointest Radiol,1990,15:133-136.
[13] 李恒华.超声引导下经皮胆囊穿刺引流术对老年急性胆囊炎的疗效分析[J].中国医药科学,2014,4(7):195-197.
