铒掺杂二氧化钛制备及其光催化性能研究
2015-03-23沈常宇
魏 健,沈常宇,代 凯
(1.中国计量学院 光学与电子科技学院,浙江 杭州 310018;2.淮北师范大学 物理与电子信息学院,安徽 淮北 235000)
铒掺杂二氧化钛制备及其光催化性能研究
魏 健1,2,沈常宇1,代 凯2
(1.中国计量学院 光学与电子科技学院,浙江 杭州 310018;2.淮北师范大学 物理与电子信息学院,安徽 淮北 235000)
通过水热合成法制备了二氧化钛和稀土饵离子掺杂二氧化钛光催化剂,并通过X射线衍射仪、紫外-可见分光光度计等测试手段对产物结构和性能进行了表征,研究了不同二氧化钛质量浓度、饵离子掺杂浓度对次甲基蓝(MB)光催化性能的影响.结果表明,所制备的二氧化钛的晶型为锐钛矿型;饵离子掺杂的二氧化钛对比纯二氧化钛的光催化性能有显著提高.当二氧化钛质量浓度为3 g/L时,对MB的降解效果最好;通过研究饵离子掺杂对MB光催化动力学模型,表明饵离子掺杂有较高的一级反应速率Kapp,且饵离子最佳掺杂量为5%.
二氧化钛;铒掺杂;光催化;次甲基蓝
印染企业在企业生产过程中将产生大量的工业废水,如果将含有染料的工业废水不加处理直接排放入河水湖泊中,将造成严重的染料污染.此类染料废水具有以下几个特点:染料废水浓度高、成分复杂、毒性大、污染物的种类比较多、易溶解、降解困难等[1].TiO2光催化降解废水中污染物是一种新型的有关环境治理技术,可以应用于染料废水、有机废水、农药废水、表面活性剂以及含油废水等的降解,具有广阔的前景[2].

本文采用水热合成法制备了纯TiO2以及饵掺杂TiO2光催化剂,通过对次甲基蓝(MB)的降解实验,结合XRD、UV-Vis表征分析结果,讨论了TiO2的浓度、稀土Er3+掺杂量对MB光催化性能的影响,Er3+掺杂对MB光催化动力学采用一级动力学模型来描述[11],对比上述文献,本实验结果有较高的一级反应速率Kapp,光催化时间较短.
1 实验部分
1.1 光催化剂的制备
按化学通式Ti1-xErxO2(x的取值范围为0≤x≤0.1)称取反应试剂Er(NO3)3·5H2O、Ti(SO4)2并加入200 mL去离子水,在磁力搅拌器上进行搅拌,边搅拌边加入20 mL氨水,搅拌30 min,待试剂完全溶解并混合均匀后用离心机进行离心,取出沉淀物,把沉淀物转移到锥形瓶中并加入200 mL去离子水和10 mL过氧化氢后进行回流,回流4 h后将溶液放入反应釜中,在180 ℃条件下加热15 h.从反应釜中取得样品进行离心,然后蒸发后得到Er3+掺杂的TiO2样品.纯TiO2制备方法同上,只是制备过程中不用添加Er(NO3)3·5H2O即可.
1.2 样品的表征
Er3+掺杂的TiO2样品的X射线衍射谱采用德国布鲁克DX-2000型X射线衍射(XRD)仪测定,管电压为40 kV,管电流40 mA,扫描范围2θ=10°~80°,扫描步长为0.08°;MB的紫外-可见吸收光谱采用日本岛津公司生产的UV3600型紫外-可见分光光度计(UV-vis)测定.
1.3 光催化性能研究
样品的光催化性能以光催化降解MB来评价.光源为250 W主波长365 nm的汞灯,光催化剂的加入量为2 g/L,加入200 mL质量浓度为8 mg/L的MB溶液,调节pH后,在室温条件下用磁力搅拌器搅拌,每隔10 min取10 mL反应液,离心分离后取上层清液,用分光光度计(UV-vis)测定MB最大吸收波长为663 nm的吸光度值的变化可求得降解率η

(1)
其中:C0—样品的溶液初始浓度,C—样品的光催化一段时间的溶液浓度.
2 结果与分析
2.1 催化剂的表征
图1为纯TiO2和Er3+掺杂TiO2的XRD图谱,其中(a)、(b)、(c)、(d)、(e)分别代表TiO2、Ti0.97Er0.03O2、Ti0.95Er0.05O2、Ti0.93Er0.07O2、Ti0.90Er0.10O2.从图中可以看出,衍射峰曲线表明样品晶型以锐钛矿型为主,在衍射角2θ为25.3°处出现了很强的晶面衍射峰.衍射角在25.3°、37.8°、48.20°、53.9°、62.55°,分别对应TiO2锐钛矿型的(101)、(004)、(200)、(105)、(204)面衍射峰.图中显示制备的样品结晶度较高,晶粒中基本没有出现其它的杂质峰,说明样品的纯度较高.从晶面衍射峰图谱可以看出,随着Er3+掺杂浓度的不断增加,衍射角在25.3°对应的(101)衍射峰强度减弱,从离子半径角度来分析,由于Er3+半径比Ti4+大,Er3+不易取代Ti4+从而进入TiO2晶格内部,而是以间隙取代的形式占据TiO2晶格的间隙位置,并且有一部分以稀土氧化物形式均匀分布在TiO2晶粒中,所以Er3+掺杂TiO2会使晶粒变小导致衍射峰强度逐渐减弱.

图1 不同Er3+掺杂TiO2的XRD图谱Figure 1 XRD spectra of TiO2 with different Er3+ contents
2.2 MB溶液的光催化降解机理和性能研究
图2为MB的化学结构和光催化反应路径,在光催化降解过程中MB中的色胺组含有N-脱烷基起着重要的作用[12],MB溶液的颜色逐渐减弱是由于部分甲基团分解和蓝移,最后MB溶液降解成H2O,CO2和其他无机分子[13].

图2 MB的化学结构和光催化反应路径Figure 2 Chemical structure of MB and the photocatalytic reaction pathway

TiO2+hv→e-+h+,
(2)

(3)
h++OH-→·OH,
(4)

(5)
图3为MB溶液的吸光度A随时间变化曲线,纯TiO2光催化剂质量浓度为3 g/L加入到200 mL质量浓度为8 mg/L MB溶液,在光源为250 W主波长365 nm的汞灯照射120 min的条件下,在本实验中,有四个最大吸收峰分别在245 nm,292 nm,612 nm和663 nm.我们选择研究发射带为663 nm处的MB溶液浓度随时间变化,光谱带在663 nm发生蓝移,如图4蓝移51 nm从663 nm到612 nm,最终随着光催化降解消失,光谱带在292 nm也发生蓝移,从292 nm到285 nm,这与已有报道类似[15].

图3 近紫外光下MB溶液的光谱随时间变化曲线Figure 3 Temporal spectral changes of MB in aqueous TiO2 suspensions under UV illumination

图4 光谱带在663 nm处发生蓝移量Figure 4 Wavelength blue-shifts of the 663 nm Spectra band
2.3 TiO2质量浓度对MB光催化性能影响
如图5,在光源为250 W主波长365 nm的汞灯照射80 min的条件下,TiO2光催化剂质量浓度为1 g/L、2 g/L、3 g/L、4 g/L,加入到200 mL质量浓度为8 mg/L MB溶液,当纯TiO2质量浓度为3 g/L时,MB的光催化降解率最大.当继续增加TiO2的用量,MB的光催化降解率不能继续增加,反而下降,最佳降解质量浓度为3 g/L.这是因为光催化剂增加,使催化表面积增加,提高光的利用率增加空穴和电子对,来提高光催化降解率.当光催化剂质量浓度达到一定时,可能形成聚集体,非辐射过程增加使光催化降解率降低.
在上述条件下,又增加了2组对照试验,一组是只在汞灯照射下,另一组只添加纯TiO2(3 g/L)没有光照,80 min之后MB的光催化效率很低,基本无降解.说明MB只有同时在光照和添加催化剂的情况下才能有效地降解.

图5 紫外光照射下MB的光催化降解 Figure 5 Photocatalytic degradation of MB under UV illumination
2.4 Er3+掺杂量对MB光催化的影响
利用紫外-可见分光光度计(UV-vis)对样品光降解性能进行表征.如图6不同Er3+掺杂TiO2降解MB光催化效率,其光催化性能得到一定程度的提高,主要有以下几个原因:
1)Er3+掺杂对TiO2晶格结构的影响.因为Er3+的半径大于Ti4+的半径,只有少量的Er3+进入晶格内部,取代了Ti4+.没有进入晶格内部的Er3+以间隙取代的形式占据TiO2晶格的间隙位置,形成Ti—O—Er的键合.从光催化效率方面分析,Er3+进入晶格内部,取代了Ti4+,或是Er3+以间隙取代的形式都会使电荷不平衡,最终影响光催化效率[16].
2)Er3+掺杂对TiO2晶粒尺寸的影响.Er3+掺杂会使TiO2的晶粒尺寸减小,由于晶粒尺寸减小会导致晶粒内部的内应力增加,从而改变TiO2的能带结构,使能级与能级之间的间距变窄,最终影响光催化效率[17].
由图6,当催化时间为80 min时,TiO2,Ti0.97Er0.03O2,Ti0.95Er0.05O2,Ti0.93Er0.07O2,Ti0.90Er0.10O2对应的C/C0值依次为0.22,0.18,0.06,0.13,0.3,则Er3+的掺杂量为5%时光催化效率最高,此时的降解率为94%.Er3+掺杂量继续增加,光催化性能反而降低.主要是因为掺入过量的Er3+,Er3+会附着在TiO2的表面,会成为光生电子和空穴对的复合中心,增加了电子和空穴的复合几率,使光催化性能下降.

图6 不同Er3+掺杂TiO2降解MB随时间变化曲线图Figure 6 Photocatalytic degradation of MB with different Er3+ contents
2.5 Er3+掺杂对MB光催化动力学研究
Er3+掺杂TiO2对MB溶液光催化降解过程,如图7符合Langmuir-Hinshelwood速率方程[18]
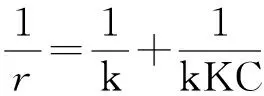
(6)
其中:C—MB溶液光催化t时的质量浓度值;k—速率常数;K—吸附平衡常数.
对速率方程(6)积分得到
lnC/C0=-Kappt.
(7)
其中:C0—MB溶液的初始质量浓度,Kapp—一级反应速率,t—反应时间.

图7 不同Er3+掺杂TiO2的降解动力学Figure 7 Degradation kinetics of different Er-doped TiO2
Er3+掺杂对MB光催化动力学采用一级动力学模型来描述,如表1实验结果饵离子掺杂有较高的一级反应速率Kapp,且饵离子最佳掺杂量为5%.
表1 MB降解动力学常数和相关系数
Table 1 Degradation kinetics constants and correlation coefficient of MB

光催化剂 一级反应速率/min-1相关系数TiO20.01830.9957Ti0.97Er0.03O20.02080.9990Ti0.95Er0.05O20.03330.9983Ti0.93Er0.07O20.02420.9966Ti0.9Er0.1O20.01440.9870
2.6 MB的降解效率比较
染料或有机化合物的降解效率高度依赖于实验条件,如光照射源、反应时间、染料类型,以及使用的光催化剂[20].在这项研究中,我们比较了本研究与先前研究报告利用太阳光、高压钠灯、碘钨灯、UV-LED灯作为光源对染料溶液进行光催化降解,比较这些结果列于表2中.Er3+掺杂TiO2的具有较高的光催化性能主要是因为Er-TiO2具有较为丰富的氧空位和表面缺陷,为俘获电子和对污染物的吸附提供了很好的条件,加速了光生电子-空穴对的复合.另一方面汞灯源是一个很好的近紫外光源用于光催化降解染料.从上述比较的结果,Er3+掺杂TiO2是一个有效的光催化剂用于降解MB溶液.本文获得Er3+掺杂TiO2的光催化时间为80 min时,降解率达到94%.

表2 本文与已有文献报道的降解率与降解时间对比
3 结 语
通过水热合成法制备了TiO2和Er3+掺杂TiO2光催化剂,XRD图谱表明所制备的二氧化钛样品结晶度较高,而且纯度较高.通过制备Er3+掺杂TiO2对MB光催化性能的研究,Er3+的掺杂明显提高了TiO2的光催化活性,有较高的一级反应速率Kapp,最佳掺杂量为5%.其光催化时间为80 min时,降解率达到94%,光催化效果优异,具有较好的光催化处理染料废水的前景.
[1] YAN Chunxiang, WANG Chongqing, YAO Jianfeng, et al. Adsorption of methylene blue on mesoporous carbons prepared using acid-and alkaline-treated zeolite X as the template[J]. Colloids and Surfaces A: Physicochemical and Engineering Aspects,2009,333(1):115-119.
[2] VOORTHUIZEN V E, ZWIJNENBURG A, MEER W, et al. Biological black water treatment combined with membrane separation[J]. Water Research,2008,42(16):4334-4340.
[3] AN Taicheng, LIU Jikai, LI Guiying, et al. Structural and photocatalytic degradation characteristics of hydrothermally treated mesoporous TiO2[J]. Applied Catalysis A: General,2008,350(2):237-243.
[4] FENG Huajun, ZHANG Minhong, YU Liya, Hydrothermal synthesis and photocatalytic performance of metal-ions doped TiO2[J]. Applied Catalysis A: General,2012,413:238-244.
[5] LIU Tongxu, LI Xiangzhong, LI Fangbai. Enhanced photocatalytic activity of Ce3+-TiO2hydrosols in aqueous and gaseous phases[J]. Chemical Engineering Journal,2010,157(2):475-82.
[6] LI Fang, LI Xia, NI Kai. Photocatalytic degradation of an odorous pollutant: 2-mercaptobenzothiazole in aqueous suspension using Nd3+-TiO2 catalysts[J]. Industrial & Engineering Chemistry Research,2006,45(1):1-7.
[7] UMAR K, HAQUE M M, MUNEER M, et al. Mo, Mn and La doped TiO2: synthesis, characterization and photocatalytic activity for the decolourization of three different chromophoric dyes[J]. Journal of Alloys and Compounds,2013,578:431-438.
[8] ANTIC Z KRSMANOVIC R M, NIKOIC M G, et al. Multisite luminescence of rare earth doped TiO2anatase nanoparticles[J]. Materials Chemistry and Physics,2012,135(2):1064-1069.
[9] CACCIOTTI I, BIANCO A, PZEEOTTI G, et al. Synthesis, thermal behaviourand luminescence properties of rare earth-doped titania nanofibers[J]. Chemical Engineering Journal,2011,166(2):751-764.
[10] KIBOMBO H, WEBER A, WU C, et al. Effectively dispersedeuropium oxide dopants in TiO2aerogel supports for enhanced photocatalytic pollutant degradation[J]. Journal Photochemistry and Photobiology A: Chemistry,2013,269:49-58.
[11] 徐小勇,施卫国,胡学冰,等.氮掺杂二氧化钛光催化降解亚甲基蓝的动力学研究[J].硅酸盐通报,2009,28(2):332-335. XU Xiaoyong, SHI Weiguo, HU Xuebing, et al. Research on photocatalysis degradation kinetics of N-doped TiO2to methylene blue[J]. Bulletin of the Chinese Ceramic Society,2009,28(2):332-335.
[12] ZHAO Wei, CHEN Chuncheng, LI Xiangzhong, et al. Photodegradation of sulforhodamine-B dye in platinized titania dispersions under visible light irradiation: influence of platinum as a functional co-catalyst[J]. The Journal of Physical Chemistry B,2002,106(19):5022-5028.
[13] ZHANG Tianyang, HORIKOSHI S, HIDAKA H, et al. Photocatalyzed N-demethylation and degradation of methylene blue in titania dispersions exposed to concentrated sunlight[J]. Solar Energy Materials and Solar Cells,2002,73(3):287-303.
[14] LIANG Cunhua, LI Fangbai, LIU Chengshuai, et al. The enhancement of adsorption and photocatalytic activity of rare earth ions doped TiO2for the degradation of Orange I[J]. Dyes and Pigments,2008,76(2):477-84.
[15] ZHANG Tianyong, OYAMA T, AOSHIMA A, et al. Photooxidative N-demethylation of methylene blue in aqueous TiO2dispersions under UV irradiation[J]. Journal of Photochemistry and Photobiology A: Chemistry,2001,140(2):163-172.
[16] ZHANG Yuhong, ZHANG Huaxiang, XU Yongyi, et al. Significant effect of lanthanide doping on the texture and properties of nanocrystalline mesoporous TiO2[J]. Journal of Solid State Chemistry,2004,177(10):3490-3498.
[17] ELBAHY Z M, ISMAIL A A, MOHAMED R M. Enhancement of titania by doping rare earth for photodegradation of organic dye (Direct Blue)[J]. Journal of Hazardous Materials,2009,166(1):138-143.
[18] DAI Kai, LU Luhua, DAWSON G. Development of UV-LED/TiO2device and their application for photocatalytic degradation of methylene blue[J]. Journal of Materials Engineering and Performance,2013,22(4):1035-1040.
[19] NATARAJAN T S, NATARAJAN K, BAJAJ H C, et al. Enhanced photocatalytic activity of bismuth-doped TiO2nanotubes under direct sunlight irradiation for degradation of Rhodamine B dye[J]. Journal of Nanoparticle Research,2013,15(5):1-18.
[20] NATARAJAN K, NATARAJAN T S, BAJAJ H C, et al. Photocatalytic reactor based on UV-LED/TiO2coated quartz tube for degradation of dyes[J]. Chemical Engineering Journal,2011,178:40-49.
Preparation and photocatalytic performance of Er-doped TiO2
WEI Jian1,2, SHEN Changyu1, DAI Kai2
(1. College of Optical and Electronic Technology, China Jiliang University, Hangzhou 310018, China; 2. School of Physics and Electronic Information, Huaibei Normal University, Anhui Huaibei 235000, China)
The photocatalysts of TiO2and rare earth Er-doped TiO2were prepared by the hydrothermal synthesis method. The structure and the performance of the products were analyzed by using the X-ray diffraction (XRD) and ultraviolet-visible spectroscopy. We found that the crystal structure of TiO2was anatase, but the photocatalytic ability of Er-doped TiO2to methylene blue(MB) was improved significantly compared to the pure TiO2. The catalytic kinetics models of the catalysts to MB show that there is the highest reaction rateKappwith the concentration of TiO2at 3 g/L, while the optimal dosage of Er-doped is 5%.
TiO2; Er-doped; photocatalysis; methylene blue

1004-1540(2015)01-0080-07
10.3969/j.issn.1004-1540.2015.01.015
2014-07-18 《中国计量学院学报》网址:zgjl.cbpt.cnki.net
国家自然科学基金资助项目(No.61405185).

O643.3
A
