卡培他滨维持治疗对联合化疗有效的复发转移三阴乳腺癌的临床观察*
2015-03-18罗海涛邹静荷古伟光胡建新贺志仁吕淑新
罗海涛,邹静荷,古伟光,胡建新,贺志仁,徐 敏,吕淑新
(南方医科大学附属南海医院/佛山市南海区人民医院肿瘤科二区,广东佛山528200)
乳腺癌是女性中较为常见的恶性肿瘤,有20%~30%的乳腺癌确诊时已经有转移,复发转移是影响预后的主要因素[1]。其治疗的目的是为了延长患者生存时间,减轻症状,提高生命质量。其中激素受体雌激素受体(ER)、孕激素受体(PR)及人类表皮生长因子受体2(HER2)阴性的三阴性乳腺癌(TNBC)患者约占乳腺癌的15%,其发病年龄较小,病理分级高,复发转移发生时间早,预后较差[2-3],所以需对体力状况良好但病情进展迅速的患者给予联合方案化疗以控制肿瘤。延长一线化疗时间可改善转移性乳腺癌患者总生存期(OS)和无病生存期(DFS)[4]。因此,为了延续巩固一线化疗的疗效,推迟肿瘤进展时间并延长生存时间,选择其中一种药物进行维持治疗,有重要的临床应用意义。本研究开展卡培他滨维持治疗对联合化疗有效的复发转移三阴乳腺癌取得一定的疗效,现将临床研究结果报道如下。
1 资料与方法
1.1 一般资料 选择浸润性乳腺癌激素受体ER、PR及HER2均为阴性,病灶为不可切除的局部晚期或已经转移的女性患者46例,分成治疗组(n=23)和对照组(n=23)。治疗组平均年龄64岁(32~69岁),(T4N0~2M0)ⅢB期9例,(任何TN3M0)ⅢC期8例,(任何T任何NM1)Ⅳ期6例;对照组平均年龄65岁(31~68岁),ⅢB期8例,ⅢC期10例,Ⅳ期5例。两组的年龄、临床分期具有可比性(P>0.05)。纳入标准:(1)年龄18~70岁;(2)东部肿瘤协作组(ECOG)身体状况评分(PS)0~1分[5];(3)经过病理和免疫组织化学明确诊断的浸润性乳腺癌,激素受体ER、PR及HER2阴性,病灶为不可切除的局部晚期或已经转移的患者,ⅢB~Ⅳ期;(4)至少有1个可测量的病灶;(5)无主要器官的功能障碍;(6)预计生存期有3个月以上;(7)能理解本治疗方案并签署知情同意书者;(8)进行血清及尿妊娠实验检查,排除怀孕可能。排除标准:不可控制的心脏疾病;不完全或完全肠梗阻;孕妇或哺乳期妇女。
1.2 方法
1.2.1 治疗方法 治疗组:所有三阴乳腺癌患者接受多西他赛(75mg/m2)联合顺铂(80mg/m2)方案化疗,3周为1个疗程,在准备第3个疗程前复查进行评价疗效,化疗6个疗程后4周复查进行疗效评价,获得完成缓解(CR)、部分缓解(PR)及稳定(SD)的患者进入卡培他滨单药维持治疗阶段,卡培他滨维持治疗剂量每次1 000mg/m2,2次/天,连用21d,停7d为1个疗程,直至病情进展(PD)或者不良反应不可耐受、死亡。对照组:单纯接受多西他赛(75mg/m2)联合顺铂(80mg/m2)方案化疗,3周为1个疗程,化疗6个疗程后进行疗效评价,疗效评价方法与治疗组相同,获得CR、PR及SD的患者进行观察。两组患者同时进行双膦酸盐每3~5周1次的治疗。
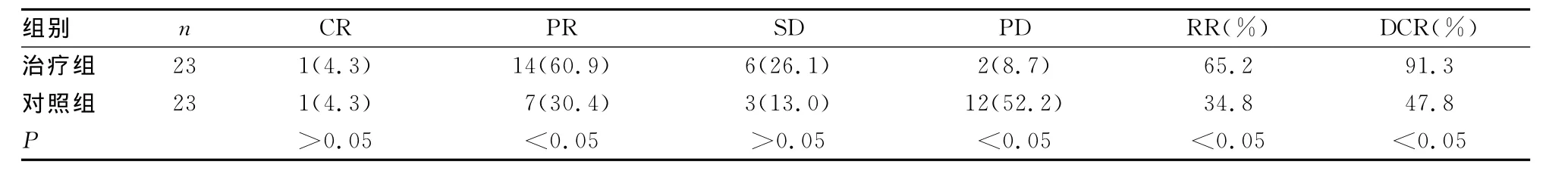
表1 两组患者近期疗效[n(%)]

表2 两组患者毒性反应比较(n)
1.2.2 疗效和不良反应 评价标准参照《WHO关于实体瘤疗效评价标准》。CR:所有可见病灶均完全消失,疗效维持4周以上;PR:各病灶最大双径乘积总和(或)单径总和缩小50%以上,并在至少4周后复测确认;SD:各病灶最大双径乘积总和或单径总和增大小于25%或缩小不足25%,无新病灶出现,并在至少4周后复测确认;PD:至少其中1个病灶的双径乘积或单径增大25%以上,或出现新病灶,或不能判断(NE)未能明确判断者。疗效计算:临床有效率(RR)=(CR+PR)/总例数×100%,疾病控制率(DCR)=(CR+PR+SD)/总例数×100%[5]。毒性反应根据美国国立癌症研究所常见不良反应标准(2.0版)评价,依照世界卫生组织标准分为0~Ⅳ级[6]。
1.2.3 随访时间 疗效确认后1个月开始,每1个月定期随访复查一次,包括B超、CT、磁共振成像(MRI)及发射型计算机断层扫描仪(ECT)项目,随访至PD或患者死亡。
1.3 统计学处理 采用SPSS18.0软件包进行统计学分析,计数资料用率表示,组间采用χ2检验,检验水准α=0.05,以P<0.05为差异有统计学意义。
2 结 果
2.1 近期疗效 治疗组的PR、PD、RR及DCR率明显优于对照组,差异有统计学意义(P<0.05),见表1。
2.2 不良反应 主要急性毒性反应有骨髓抑制、胃肠道反应、肝功能损害及手足综合征等,治疗组较对照组毒性反应稍大,骨髓抑制较为明显,但差异无统计学意义(P>0.05),见表2。只有治疗组出现手足综合征的毒性反应,与对照组比较差异有统计学意义(P<0.05)。手足综合征的评价标准根据HFS的毒性分级标准进行评估,分为3级[7],其中Ⅰ度47.8%(11/23),Ⅱ度30.4%(7/23),Ⅲ度8.7%(2/23),有3例患者没有出现手足综合征。所有毒性反应经处理后均能顺利完成治疗。
3 讨 论
乳腺癌是目前妇女比较常见恶性肿瘤,其中约11.2%~16.3%乳腺癌患者属于ER、PR和HER2均为阴性的三阴性乳腺癌(TNBC)。此类型常伴随乳腺癌易感基因1(BRCA1)突变,是一类侵袭性强,容易出现复发转移,治疗方法有限,预后较差的乳腺癌[8]。因缺乏内分泌治疗及针对HER2的分子靶向治疗的适应证,其治疗手段相对于其他乳腺癌受到限制,一般选择联合方案化疗。为了改善患者生命质量、延长生存时间及减少不良反应,选择和优化化疗方案是治疗的关键,这时需要为患者选择最佳治疗措施,采用有效、低毒的化疗药物维持治疗是近年来的研究热点。
晚期乳腺癌目前是难以治愈的,化疗停止后疾病比较容易发生进展,所以维持治疗方案显得尤其重要,可以明显延长乳腺癌患者的疾病进展时间[9]。对于三阴性的乳腺癌患者,选择一种有效、低毒、方便、能够维持给药的治疗方法,显得更加重要[10]。维持治疗模式主要巩固一线治疗的疗效,延缓疾病进展,最终延长OS,还可以减少化疗药物毒性的积累,进一步提高患者生命质量。卡培他滨是一种口服氟尿嘧啶制剂,该药具备有效、方便、低毒等特点,口服后迅速吸收,生物利用度高,吸收后迅速转化为5-氟尿嘧啶,具有较高的靶向性,并且优先进入肿瘤组织中,因没有了胃肠外给药的屏障问题,对乳腺癌具有较好的临床疗效[11]。对于老年且体质较弱患者,卡培他滨按标准剂量使用比较容易出现严重的胃肠道反应及手足综合征等不良反应,而持续使用低浓度的化疗药物每次1 000mg/m2,不引起严重的消化道反应和手足综合征。卡培他滨安全性高,骨髓抑制发生率较低,是一个适合长时间维持治疗的高效低毒药物。卡培他滨在复发转移性乳腺癌的治疗应用逐渐增多,丛雪等[12]报道卡培他滨联合顺铂治疗晚期三阴性乳腺癌疗效好,毒性反应可以耐受。廖瑜倩等[13],Kotsori等[14]观察长春瑞滨联合卡培他滨治疗复发转移性三阴乳腺癌近期疗效好,不良反应轻,可作为晚期三阴性乳腺癌患者一线和二、三线治疗的选择。
多个研究中心的研究结果显示,卡培他滨单药治疗晚期乳腺癌的有效率为20%~40%,治疗中不需要预防和辅助用药,安全性好,患者有较好的生命质量[15]。目前晚期乳腺癌患者大多是不可治愈的,需要采用全程管理治疗模式,根据患者的依从性,充分权衡治疗的利弊,进行维持治疗,从而改善生命质量及延长生存时间。2007年美国临床肿瘤学会(ASCO)年会上报告的一项回顾性分析显示,对于复发转移性乳腺癌患者,卡培他滨联合化疗治疗有效或SD者后续卡培他滨单药维持治疗,32.2%患者临床获益,81%患者保持原有疗效,中位肿瘤进展时间为4个月[16]。卡培他滨维持治疗转移行乳腺癌,显著延长患者生存时间,改善生命质量[16]。
本研究对进行6个疗程联合方案化疗有效的复发转移三阴乳腺癌进行口服卡培他滨维持治疗,取得了较好的疗效,且不良反应较低。治疗组其RR及DCR分别为65.2%和91.3%,高于单纯行联合方案化疗的对照组(34.8%和47.8%),治疗组疾病进展率为8.7%明显较对照组低(52.2%),两组间差异有统计学意义(P<0.05)。毒性反应方面,两组出现骨髓抑制、胃肠道反应及肝功能异常多为Ⅰ、Ⅱ、Ⅲ度,经处理后患者均能耐受治疗,中途无需停药,治疗组的毒性反应较对照组增加,但差异无统计学意义(P>0.05)。使用卡培他滨维持治疗的患者出现手足综合征,以Ⅰ、Ⅱ度为主,但在经过对症治疗后手足综合征的毒性反应明显减轻,可继续进行治疗。除手足综合征外,治疗组与对照组的不良反应对比较为相似,维持治疗不失为是一种有前景的治疗模式。
本研究显示卡培他滨疗效确切,有效率明显提高,而且毒性反应较轻,显著改善患者生命质量。但目前病例数较少,观察时间短,生存率、复发率及远期生存质量有待进一步观察。
[1]Steger GG,Bartsch R.Trends and novel approaches in neoadjuvant treatment of breast cancer[J].Breast Care(Basel),2011,6(6):427-433.
[2]陈茂山,袁杰,成宏,等.p53在乳腺癌中的表达及其临床意义[J].重庆医学,2014,43(9):1069-1071.
[3]邱献华,王公平.三阴性乳腺癌110例临床分析[J].重庆医学,2012,41(27):2827-2828,2831.
[4]Zapf I,Tizedes G,Pavlovics G,et al.Primary systemic therapy in breast cancer patients(2007-2010)[J].Magy Seb,2011,64(5):223-228.
[5]周际昌.实用肿瘤内科学[M].北京:人民卫生出版社,1998:45-48.
[6]孙燕,石远凯.临床肿瘤内科手册[M].北京:人民卫生出版社,2007:147-149.
[7]李玺,姜华,郭卫平,等.卡培他滨引起的手足综合征发病特点与治疗观察[J/CD].中华临床医师杂志:电子版,2011,5(6):1781-1783.
[8]智英辉,尼杰,田秀芳,等.雄激素受体在三阴性乳腺癌的表达及其预后意义[J].重庆医学,2012,41(27):2812-2815.
[9]Morgan GJ,Gregory WM,Davies FE,et al.The role of maintenance thalidomide therapy in multiple myeloma:MRC Myeloma IX results and meta-analysis[J].Blood,2012,119(1):7-15.
[10]Blum JL,Barrios CH,Feldman N,et al.Pooled analysis of individual patient data from capecitabine monotherapy clinical trials in locally advanced or metastatic breast cancer[J].Breast Cancer Res Treat,2012,136(3):777-788.
[11]Pino MS,Milella M,Gelibter A,et al.Capecitabine and celecoxib as second-line treatment of advanced pancreatic and biliary tract cancers[J].Oncology,2009,76(4):254-261.
[12]丛雪,王亚帝,哈敏文,等.卡培他滨联合顺铂治疗晚期三阴性乳腺癌的疗效观察[J].中国药房,2012,23(24):2226-2228.
[13]廖瑜倩,樊英,万以叶,等.长春瑞滨联合卡培他滨治疗晚期三阴性乳腺癌的疗效及生存观察[J].中国肿瘤临床与康复,2012,19(2):150-152.
[14]Kotsori AA,Dolly S,Sheri A,et al.Is capecitabine efficacious in triple negative metastatic breast cancer?[J].Oncology,2010,79(5/6):331-336.
[15]Huang H,Jiang Z,Wang T,et al.Single-agent capecitabine maintenance therapy after response to capecitabinebased combination chemotherapy in patients with metastatic breast cancer[J].Anticancer Drugs,2012,23(7):718-723.
[16]Kamal AH,Camacho F,Anderson R,et al.Similar survival with single-agent capecitabine or taxane in first-line therapy for metastatic breast cancer[J].Breast Cancer Res Treat,2012,134(1):371-378.
