听力学教学中新生儿耳聋基因筛查咨询要点*
2015-03-17刘海红周怡郝津生倪鑫
刘海红周怡郝津生倪鑫
·听力学教育·
听力学教学中新生儿耳聋基因筛查咨询要点*
刘海红1周怡1郝津生1倪鑫1
流行病学研究提示50%~70%的听力障碍与遗传因素相关[1~5],即为遗传性聋(表1),其中,综合征型聋(syndromic hearing impairment,SHI)约占30%,非综合征型聋(non-syndromic hearing impairment,NSHI)约占70%。新生儿耳聋基因筛查可以预知与遗传相关的高危听障新生儿和迟发性听力损失,弥补现有新生儿听力筛查方法的不足[6,7],有效提高遗传性聋患儿的检出率,进一步推进听力障碍早期发现、早期诊断、早期干预的有序实施。对于具有某些可能致聋敏感因素的新生儿,可以通过针对性咨询做好听力保健和听力损失的预防,将可避免的听力损失降到最低。本文旨在通过对首都医科大学附属北京儿童医院开展的新生儿耳聋基因筛查结果咨询工作的分析,将耳聋基因筛查咨询要点应用于听力学教学实践中,以利促进婴幼儿听力保健工作的有效开展。

表1 新生儿和儿童时期致聋因素构成比[15](%)
1 咨询对象及耳聋基因筛查简介
咨询工作对象为北京市2012年4月至2014年7月期间出生并由耳聋基因筛查显示携带耳聋基因的1 718例新生儿家长。新生儿在出生后3~5天内采集足跟末梢血2个直径10 mm足跟血血斑(或2~3 ml脐带血),血液样本采集使用EDTA或枸橼酸钠抗凝,血斑中提取的DNA采用博奥生物有限公司的九项遗传性聋基因检测试剂盒(微阵列基因芯片法)检测4个耳聋相关基因的9个位点:GJB2(35 del G,176 del 16,235 del C,299 del AT)、SLC26A4(IVS7-2 A>G,2168 A>G)、线粒体DNA 12S r RNA(1555 A>G,1494 C>T)、GJB3(538 C>T)。经专业遗传学培训并考核通过的听力学技术人员将耳聋基因筛查结果通过短信发放给新生儿家长,并针对耳聋基因筛查结果采用电话咨询和门诊就诊咨询方式对新生儿家长进行指导,咨询内容涉及突变基因、位点、听力保健、日常注意事项等。
2 耳聋基因突变位点分布
2012年4月至2014年7月期间出生并由首都医科大学附属北京儿童医院完成耳聋基因筛查的新生儿共42 231例,筛查显示携带耳聋基因的新生儿1 718例,总携带率为4.07%(1 718/42 231)。其中GJB2基因杂合突变(携带者)925例(携带率为2.19%,925/42 231),SLC26A4基因杂合突变581例(携带率为1.38%,581/42 231),线粒体12S r RNA基因均质或异质突变106例(携带率为0.25%,106/42 231),GJB3基因杂合突变106例(携带率为0.25%,106/42 231);1 718例新生儿耳聋基因位点突变分布见表2。
在1 718例耳聋基因突变携带者中,GJB2突变率达2.19%,占全部突变位点总数的53.84%(925/1 718,说明GJB2不仅在新生儿中具有较高的突变率,该基因也是耳聋相关基因中突变率最高的基因;其中,GJB2 235 delC基因突变688人,占总筛查人
数的1.63%(688/42 231),成为该基因突变率最高的位点;其后依次为GJB2 299 del AT(198人,0.47%);GJB2 176 del16(37人,0.09%)和GJB2 35 delG位点(2人,0.00)。SLC26A4基因为另一突变率较高的基因,突变率为1.38%,占全部突变的33.82%(581/1 718);其中,SLC26A4 2168 A>G基因突变88人(突变率0.21%),SLC26A4 IVS7 -2 A>G基因突变493人(突变率1.17%,493/42 231)。线粒体12S r RNA基因突变率为0.25%,占全部突变的6.17%(106/1 718),其中,以线粒体12S r RNA 1555 A>G基因突变位点较多见,该基因位点突变的检出对有效指导临床安全用药十分重要。
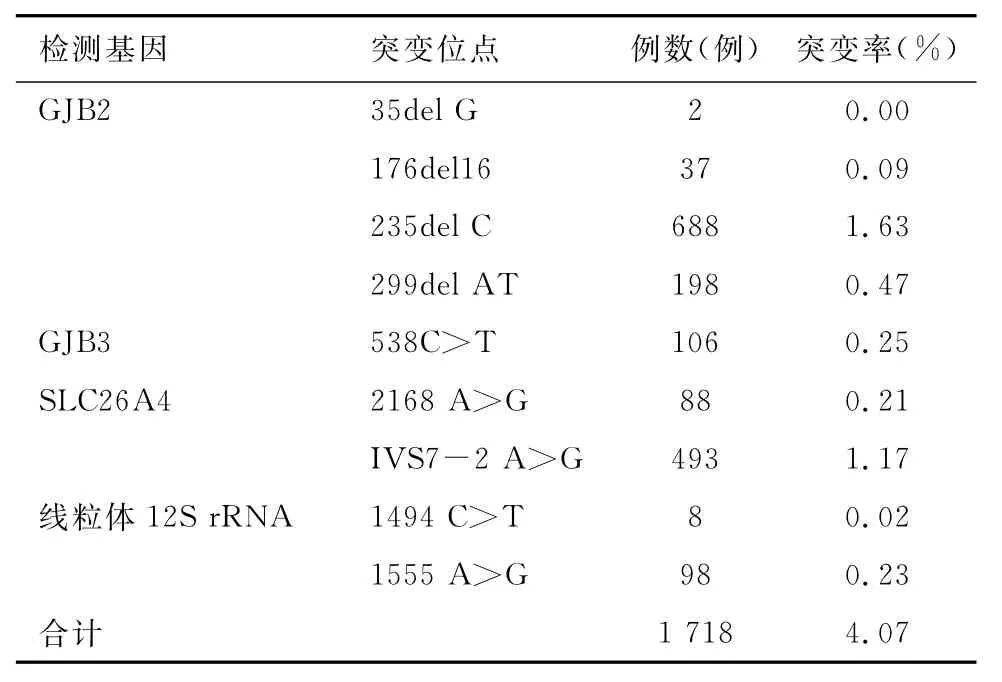
表2 1 718例新生儿检出的耳聋基因突变位点分布
3 耳聋基因筛查结果咨询要点
针对耳聋基因筛查结果异常新生儿,咨询人员采用电话咨询和门诊就诊咨询两种方式对家长进行指导,其中,对于复合杂合和纯和突变者,咨询中建议家长到耳科及听力门诊行进一步耳部及听觉相关检查以确诊其听功能;对于耳聋基因突变携带者,随访过程中给与家长针对性指导。
家长得知新生儿为耳聋基因突变携带者往往会恐慌,咨询中应向其解释隐性遗传的特点,使其了解如果耳聋基因筛查结果显示其为一个基因位点杂合突变者,则为基因突变携带者,新生儿并不一定会表现出听力障碍;同时又应该让其理解耳聋基因携带者潜在的致聋风险性,即有将该基因遗传给后代的可能性,如果夫妻双方均为某一特定隐性耳聋基因杂合突变携带者,则婚配后生育听障儿童的概率为25%,咨询中应提醒有再生育计划的家长行耳聋基因产前筛查。咨询过程中应将具有高度遗传专业性质的耳聋基因筛查结果向家长深入浅出的讲解清楚,既要让家长引起重视,又不能引起家长过度恐慌,咨询人员应为家长提供必要的耳和听力保健常识,如:有效避免噪声暴露导致的听力下降、注意用药安全等,后者对于携带线粒体12S r RNA基因突变者尤为重要。针对不同基因突变涉及的咨询要点见表3。

表3 耳聋基因芯片筛查结果咨询要点
4 咨询人员应掌握的基本背景知识和咨询注意事项
GJB2基因突变是引起遗传性聋的常见致聋基因,该基因表现为隐性遗传,其235 del C突变类型在听力正常人群中的携带率为1%~2%[3,4,8]。GJB2基因突变相关性聋在听力损失的发病年龄、程度、听力曲线特征等报道不一,具有明显的多态性特点。在我国人群中,常见GJB2基因突变类型主要有235 del C、299 del AT和176 del 16[9],GJB2基因的纯合突变和杂合突变导致的听力损失程度有差别,有研究表明35delG的纯合突变导致的听力损失较杂合突变更严重[10]。该基因突变者往往表现为双侧听力损失,也偶有单侧受累的报告;在发病年龄方面也存在明显差异,部分表现为出生时即耳聋,也有部分在婴幼儿和/或儿童时期发病。咨询中不容忽视的一点为,常规的新生儿听力筛查并不能将所有的GJB2纯和或复合杂合突变患儿筛查出来,越来越多的报道显示GJB2基因突变者具有迟发性听力损失的特点,如Orzan等[11]研究显示,约有50%的极重度聋患儿在3月龄时具有正常听觉行为,20%在6月龄时具有正常听觉行为,其迟发性听力损失的特点在咨询过程中应格外提醒家长予以关注。
SLC26A4基因突变是导致感音神经性聋的另
一重要遗传学病因,该基因突变与大前庭水管综合征(large vestibular aqueduct syndrome,LVAS)密切相关,LVAS表现为前庭水管扩大合并感音神经性或混合性聋,由Valvassori等于1978年首先描述并命名。在感音神经性聋中LVAS所占比例很高,可达1%~12%[12];以往研究提示LVAS为典型的常染色体隐性遗传,SLC26A4基因突变是其明确的致病因素,SLC26A4基因检测是诊断大前庭水管综合征的重要方法之一。LVAS的典型临床表现为进行性、波动性听力下降,发病形式可突然或隐匿,可以从出生到青春期任何时期发病,其发病或病情加重往往与头部外伤、感冒等因素相关;耳聋基因筛查可有效实现LVAS的早期发现,通过遗传咨询可使患儿家长充分了解LVAS患者听力下降的潜在高危因素,并通过针对性指导使其更好的协助患儿保护残余听力。LVAS患儿的确诊年龄较发病年龄明显延迟,即确诊年龄滞后于发病年龄;因家长往往对患儿病情不了解,在日常生活中对避免LVAS患者听力受损的注意事项知晓度不够,导致患儿出现进行性波动性听力下降;对于此类患者的咨询中建议以书面形式将LVAS的遗传倾向、临床表现、注意事项以及助听器干预须知发放给家长,以便最大限度保护患儿听力,防止或延缓其听力下降的发生。
线粒体DNA 12S r RNA基因为母系遗传,该基因的1494C>T、1555 A>G突变通过改变线粒体DNA的空间结构形成新的与氨基糖苷类抗生素(Am An)作用的结合位点,从而导致对氨基糖苷类药物敏感而致聋。在耳毒性药物相关的听力损失者中12Sr RNA基因1555G突变占较高比例,我国学者2006年开展的研究显示,门诊的听力障碍患者中检测发现由于12S r RNA 1555G突变致聋的比例为5%,聋哑学校中聋哑患者该基因突变比例则高达12%[13]。对于此类基因突变患儿的咨询中建议将常用的具有耳毒性的药物以书面形式发放给家长并予以指导,避免用药不慎导致婴幼儿听力下降。此外,由于该基因母系遗传的特点,咨询过程中除对新生儿用药给予合理指导外,还应就其家族中其他母系家庭其他成员的安全用药给予指导,避免家庭成员出现耳毒性药物导致的听力下降。
咨询中还应请家长关注婴幼儿或儿童随年龄增长听力损失易感因素的变化,如表1所示,新生儿和儿童时期致聋因素有所区别,如随年龄增长,SLC26A4、GJB2、线粒体DNA 1555 12S r RNA基因突变以及迟发性听力损失发病比例升高,即使通过听力筛查,家长也应在更长的时间内对儿童进行密切观察和检测,并注意不同年龄时期听力损失的易感因素,最大限度的保护好儿童听功能。
基因突变是儿童遗传性聋常见的致病因素之一,其基因突变方式、位点复杂多样,并具有种族特异性,临床表型具有明显多态性特征,规范开展耳聋基因筛查咨询工作对于听力保健、产前诊断等具有重要意义,是听力学学生应掌握的基本知识。
1 江凌晓,凌月仙,蔡桂君,等.遗传性耳聋基因芯片检测的临床应用研究[J].分子诊断与治疗杂志,2011,3:170.
2 张艳,卞颖华,许鹏飞,等.应用耳聋基因芯片技术检测非综合征型耳聋基因突变[J].生物技术通讯,2010,21:22.
3 王冰,徐洁,姚红兵,等.重庆市非综合征型耳聋患儿GJB2基因突变分析[J].重庆医学,2009,38:1028.
4 欧阳治国,吴皓.GJB2基因突变及其听力损失特点[J].听力学及言语疾病杂志,2008,16:72.
5 王秋菊,赵亚丽,兰兰,等.新生儿聋病基因筛查实施方案与策略研究[J].中华耳鼻咽喉头颈外科杂志,2007,42:809.
6 Green GE,Smith RJ,Bent JP,et al.Genetic testing to identify deaf newborns[J].JAMA,2000,284:1245.
7 Norris VW,Arnos KS,Hanks WD,et al.Does universal newborn hearing screening identify all children with GJB2(Connexin 26)deafness?Penetrance of GJB2 deafness[J].Ear Hear,2006,27:732.
8 Huculak C,Bruyere H,Nelson TN,et al.V37I connexin 26 allele in patients with sensorineural hearing loss:evidence of its pathogenicity[J].Am J Med Genet A,2006,140:2394.
9 Dai P,Yu F,Han B,et al.GJB2 mutation spectrum in 2063 Chinese patients with nonsyndromic hearing impairment[J].J Transl Med,2009,7:26.
10 Cryns K,Orzan E,Murgia A,et al.A genotype-phenotype correlation for GJB2(connexin26)deafness[J].J Med Genet,2004,41:147.
11 Orzan E,Murgia A.Connexin 26 deafness is not always congenital[J].Int J Pediatr Otorhinolaryngol,2007,71:501.
12 Valvassori GE,Clemis JD.The large vestibular aqueduct syndrome[J].Laryngoscope,1978,88:723.
13 郭玉芬,徐百成,韩东一,等.中国西北地区线粒体DNA1 2Sr RNAA1 555G和GJB2基因突变[J].中国耳鼻咽喉头颈外科,2006,13:666.
(2014-09-01收稿)
(本文编辑 雷培香)
10.3969/j.issn.1006-7299.2015.04.017
时间:2015-4-28 10:25
R764.43
A
1006-7299(2015)04-0400-03
* 国家自然科学基金(83100838),北京市自然科学基金(7144212)、北京市科技新星计划(xx2014B059)、首都医科大学基础临床合作研究重点项目(13JL06)资助
1 首都医科大学附属北京儿童医院耳鼻咽喉头颈外科(北京100045)
倪鑫(Email:nixin@bch.com.cn)
网络出版地址:http://www.cnki.net/kcms/detail/42.1391.R.20150428.1025.001.html
