丙型肝炎病原学不同检测方法的临床应用价值对比分析*
2015-03-15龙宏洋叶玉芬朱学强
龙宏洋,叶玉芬,朱学强,王 涵
(广东省珠海市香洲区人民医院检验科 519070)
·论 著·
丙型肝炎病原学不同检测方法的临床应用价值对比分析*
龙宏洋,叶玉芬,朱学强,王 涵
(广东省珠海市香洲区人民医院检验科 519070)
目的 探讨抗体、抗原及核酸检测在丙型肝炎诊断中的应用价值。方法 收集2012年1月到2013年12月珠海市香洲区人民医院筛查抗-HCV抗体阳性标本48份。用3种抗体试剂、2种抗原试剂及HCV-RNA复核检测结果。结果 复核阳性丽珠37份,科华36份,新创36份,莱博21份,康润18份,HCV-RNA 28份。3种抗体试剂复核均阴性的10份标本中检出HCV-RNA阳性1份,莱博抗原阳性3份,康润抗原阳性1份。3种抗体灵敏度均为96.4%,阳性预测值为72.9%~75.0%;2种抗原试剂灵敏度分别为40.0%和83.3%,阳性预测值分别为57.0%和83.3%。结论 丙型肝炎病毒抗体检测具有较高的诊断灵敏度,但诊断特异性较低,对抗-HCV抗体阳性标本采用抗体加抗原模式进行复核对丙型肝炎诊断具有重要的价值,对有疑问的标本再用HCV-RNA进行确证,可预防误诊、漏诊。
丙型肝炎病毒; 丙型肝炎病毒抗体; 丙型肝炎病毒抗原; 丙型肝炎病毒核酸
丙型肝炎是由丙型肝炎病毒(HCV)感染引起的一种严重威胁人类健康的疾病,据世界卫生组织统计,全球HCV感染者超过1.7亿,每年全球新发感染者约350万人[1]。全国流行病学调查资料显示,我国一般人群HCV抗体(抗-HCV)阳性率约为3.2%,中国约有4 000万人感染HCV,约占全球总感染人数的1/4,居世界之首。在HCV感染者中,约80%的急性丙型肝炎患者无明显症状,且在发病初期常被隐匿,这些感染者常发展成严重的肝硬化,甚至肝癌。此外,目前尚无HCV的预防疫苗,一旦感染HCV,仅有20%的患者能自发清除病毒,而潜伏的丙型肝炎患者不仅自身健康风险巨大,同时也是威胁社会公共卫生的隐患。控制HCV传播,需依赖实验室及时、准确的诊断,并尽早地进行有效的治疗。目前临床用于HCV的检测方法主要有抗-HCV抗体检测、HCV核心抗原检测及核酸检测。本研究通过采用不同的检测方法对48份临床抗-HCV抗体阳性标本进行检测,探讨不同病原学检测方法在HCV感染诊断中的应用价值。现将研究结果报道如下。
1 资料与方法
1.1 标本来源 收集2012年1月至2013年12月本院手术前、输血前患者、产检孕妇和门诊疑似HCV感染患者抗-HCV抗体筛查阳性标本48份。所有标本用原批次抗体试剂双孔复核阳性,收集双份血清,其中一份以专用管收集用于HCV-RNA检测,另一份于-20 ℃保存用于抗-HCV抗体、HCV核心抗原检测。
1.2 仪器与试剂 所用仪器有美国Bio-Tek公司生产的ELX-800酶标仪、ELX-50洗板机,美国ABI公司生产的7500荧光定量聚合酶链反应(PCR)仪。实时荧光定量PCR检测试剂由湖南圣湘生物科技有限公司提供。常规酶联免疫吸附试验(ELISA) 抗-HCV抗体筛查试剂为珠海丽珠试剂股份有限公司生产的抗-HCV检测试剂盒(简称丽珠)。复核抗-HCV抗体的试剂有3种:丽珠试剂(批号201310512),上海科华生物工程股份有限公司生产的抗-HCV抗体检测试剂盒(简称科华,批号201308011),英科新创(厦门)科技有限公司生产的HCV-Ab检测试剂盒(简称新创,批号2013085808);检测HCV核心抗原的试剂有2种:山东莱博生物科技有限公司生产的HCV核心抗原检测试剂盒(简称莱博,批号201308003),湖南康润药业有限公司生产的HCV核心抗原检测试剂盒(简称康润,批号20130902)。所有试剂均在有效期内使用,仪器设备定期进行维护、校准。
1.3 检测方法 3种抗-HCV抗体检测方法均为间接ELISA,2种HCV核心抗原检测方法均为双抗体夹心法,由同一人在相同条件下严格按照试剂说明书进行操作,检测HCV核心抗原、抗体。核酸检测采用实时荧光定量PCR检测技术,由广州金域医学检验中心有限公司完成,HCV-RNA水平小于500 拷贝为阴性,≥500 拷贝为阳性。
1.4 统计学处理 采用SPSS17.0统计学软件进行数据处理与统计学分析,计数资料以例数与百分率表示,组间比较采用χ2检验;以α=0.05为检验水准,P<0.05为差异有统计学意义。
2 结 果
2.1 48份抗-HCV抗体初筛阳性标本各种试剂复核结果 所有试剂复核结果与抗体初筛结果比较差异均有统计学意义(P<0.05);3种抗体检测试剂的复核结果比较差异无统计学意义(P>0.05);2种抗原检测试剂的复核结果比较差异无统计学意义(P>0.05);抗体检测的阳性率高于HCV-RNA,但只有丽珠试剂与HCV-RNA检测阳性率比较差异有统计学意义(P<0.05);抗原检测的阳性率低于HCV-RNA,但只有康润试剂与HCV-RNA检测阳性率比较差异有统计学意义(P<0.05)。见表1。
2.2 3种抗体试剂复核全部阴性的10份标本抗原及HCV-RNA检测结果 10份抗体复核阴性的标本检出HCV-RNA阳性1份,莱博抗原阳性3份,康润抗原阳性1份,比较差异均无统计学意义(P>0.05)。见表2。
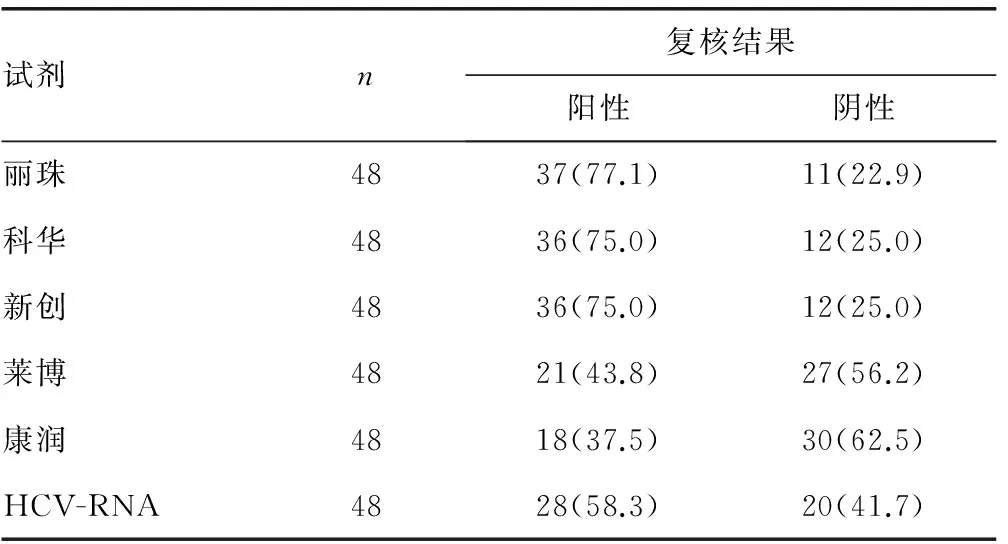
表1 48份抗-HCV抗体阳性标本各种试剂复核结果[n(%)]
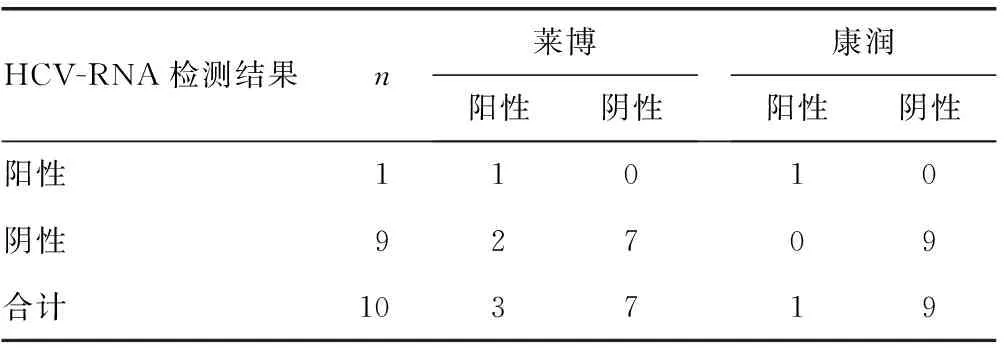
表2 3种抗体试剂复核全阴性标本抗原及 HCV-RNA检测结果
2.3 抗体、抗原试剂检测结果与HCV-RNA结果比较 3种抗体的诊断灵敏度、特异性、阳性预测值、阴性预测值比较差异均无统计学差异(P>0.05);而抗原试剂中,康润的灵敏度、特异性、阳性预测值、阴性预测值均高于莱博,差异有统计学意义(P<0.05)。抗体的诊断灵敏度及阴性预测值均高于抗原,差异有统计学意义(P<0.05);而康润抗原检测的阳性预测值高于抗体,差异有统计学意义(P<0.05)。见表3。

表3 抗体、抗原试剂检测结果与HCV-RNA结果的比较
3 讨 论
丙型肝炎是我国常见的传染病,由HCV感染引起,主要经输血传播,对人类健康危害极大。目前大部分医院已经开展了HCV检测项目,常规用于术前、输血前及孕前产前检查等。现阶段HCV的检测方法主要有3种,即抗体、核酸及抗原检测。抗-HCV抗体检测是最早确立的实验室诊断方法,被广泛用于HCV感染的临床诊断、健康人群体检和血液筛查[2]。HCV核心抗原几乎与HCV-RNA同时出现,是HCV感染的早期标志,目前市售的HCV核心抗原检测试剂盒多采用双抗体夹心ELISA法来检测血清总核心抗原或游离核心抗原。本研究结果显示,48份抗体初筛阳性标本的抗体、抗原及HCV-RNA的复核结果比较差异有统计学意义(P<0.05),且复核阳性率由大到小依次为抗体、HCV-RNA、核心抗原,与龙润乡等[3]研究结果相似。分析原因可能有:(1)抗-HCV抗体筛查存在较大的假阳性率,美国疾病预防控制中心(CDC)研究报道,在抗-HCV抗体阳性率小于10%的人群中,假阳性率平均为35%[4]。值得注意的是有5份标本3种抗体试剂检测均为强阳性[样本吸光度(OD)值/临界值比值(S/CO值)大于9]而HCV-RNA复核为阴性,可能与抗体试剂盒的假阳性有关。(2)核心抗原因其水平较低,对检测试剂和检测人员的要求高,或由于标本中的抗-HCV抗体与用于核心抗原检测的单克隆抗体竞争结合抗原而造成假阴性[5]。
本研究所选48份标本均为抗-HCV抗体阳性标本,理论上用抗体试剂复查时应显示全阳性,但仍有10份(22.9%)标本3种抗体试剂检测全阴性。这与王迅等[6]研究结果相似,45.53%的标本抗体复核阴性。与文献[6]自动化初筛大量标本不同,本研究初筛与复核都为小批量、手工操作,由于初筛与复核有1种相同试剂,排除该因素,10份标本的初筛S/CO都小于3.8。作者认为可能是抗-HCV抗体降解所致,降解的发生可能与标本保存时间过长、保存温度过高及反复冻融有关,也可能与手工操作存在的差异有关。在该10份抗-HCV抗体复核阴性标本中有1份标本的2种抗原试剂复核阳性,HCV-RNA复核阳性,结合该患者临床出现黄疸、肝功能异常等症状,判断此患者处于感染早期,抗体效价较低,单纯用抗体试剂复核则有漏检的可能。本研究还发现,假定HCV-RNA检测为真阳性,3种抗体的灵敏度都为96.4%,阳性预测值为72.9%~75.0%,三者的灵敏度、特异性、阳性预测值、阴性预测值比较差异均无统计学意义(P>0.05)。抗原检测中,康润的灵敏度、特异性、阳性预测值、阴性预测值均优于莱博(P<0.05)。此外,抗体的诊断灵敏度及阴性预测值均高于抗原(P<0.05),而抗原检测的阳性预测值高于抗体(P<0.05)。然而,张健等[7]研究表明抗体与抗原试剂的检测结果无明显差异。
近年来关于丙型肝炎抗体检测试剂的研究较多。因检测抗-HCV抗体试剂盒的各生产厂家使用的HCV基因重组抗原种类、抗原区段及各区段的比例不同,所以不同厂家的试剂的灵敏度和特异性存在一定的差异,抗-HCV抗体的检测结果不尽相同[8-9]。本研究显示,3种抗体试剂的阳性检出率比较差异无统计学意义(P>0.05);但假阳性率高达32.1%(9/28),阳性预测值低;同时漏检了1份阳性标本,假阴性率为3.6%(1/28)。2种抗原检测试剂检出率比较差异无统计学意义(P>0.05),但灵敏度、特异性等比较差异有统计学的意义,说明抗原试剂的质量在各厂家之间也存在差异。由此可见,仅用一种试剂判断HCV感染需谨慎,HCV筛查阳性标本同样需要进行确证。HCV的确证试验一般有重组免疫印迹试验(RIBA)和HCV-RNA检测。RIBA是具有高特异性的抗-HCV抗体的确证试验,但因试剂价格昂贵其在实际检测中的应用受到了限制。而HCV-RNA检测实验操作复杂,容易交叉污染形成假阳性,且仪器、试剂同样昂贵,仍然难以在基层实验室推广。我国CDC在HCV临床诊断的相关规范中要求抗-HCV抗体阳性的标本需要采用原有试剂双孔或原有试剂加另一种不同实验原理或厂家的试剂进行复核试验。国内已有研究对各种不同复核模式进行了探讨[10-11]。
综上所述,采用抗体双孔或抗体加抗体的复核模式容易造成误诊或漏诊。而抗原试剂有较高的阳性预测值,采用抗体加抗原的复核模式,对HCV的诊断具有重要的价值。对有疑问的标本再用HCV-RNA或RIBA进行确证,可预防误诊及漏诊。
[1]Lauer GM,Walker BD.HePatitis C virus infection[J].N Engl J Med,2001,345(1):41-52.
[2]张瑞,李金明.丙型肝炎病毒感染临床检测程序的建立及结果报告与解释[J].中华检验医学杂志,2010,33(10):990-992.
[3]龙润乡,杨蓉,白慧珠,等.HCV抗体阳性样品核酸及核心抗原检测分析[J].医学研究杂志,2010,39(12):41-43.
[4]Alter MJ,Kuhnert WL,Finelli L,et al.Guidelines for laboratory testing and result reporting of antibody to hepatitis C virus.Centers for Disease Control and Prevention[J].MMWR Recomm Rep,2003,52(RR-3):1-13.
[5]谭晓霞,纪勇平,骆昊翠.丙型肝炎病毒核心抗原检测的临床应用价值[J].检验医学,2010,25(2):134-136.
[6]王迅,刘宇宁,贾尧,等.丙型肝炎病毒抗体筛查阳性结果确证方案的探讨[J].中国输血杂志,2008,21(4):255-258.
[7]张健,刘宜仲,杨珊,等.HCV核心抗原检测在血液筛查中的初步研究[J].现代检验医学杂志,2012,27(2):110-111.
[8]孟庆玲,鲁健,邱丰,等.丙型肝炎IgG抗体ELISA诊断试剂比对分析[J].中华实验和临床病毒学杂志,2013,27(3):221-223.
[9]傅立强,桑列勇,蒋国瑾.ELISA试剂检测抗HCV反应性结果分析[J].检验医学,2012,27(7):588-591.
[10]鲜玉萍,杨红英.丙型肝炎核心抗原检测的临床意义[J].检验医学与临床,2012,9(18):2320-2321.
[11]金一鸣,方志红,曹谊.血液筛查中丙型肝炎病毒检测方法的应用评价[J].检验医学与临床,2013,10(5):552-553.
Comparative analysis on clinical application values of different methods for detecting hepatitis C pathogens*
LONGHong-xiang,YEYu-fen,ZHUXue-qiang,WANGHan
(DepartmentofClinicalLaboratory,XiangzhouDistrictPeople′sHospital,Zhuhai,Guangdong519070,China)
Objective To investigate the application value of antibody,antigen and nucleic acid detections in the diagnosis of hepatitis C.Methods 48 anti-HCV positive specimens in our hospital from Jan. 2012 to Dec. 2013 were collected.The detection results were re-detected by HCV-RNA,3 kinds of antibody reagent and 2 kinds of antigen reagent.Results The positive result of re-detection was in 37 specimens by Lizhu,in 36 specimens by Kehua,in 36 specimens by Xinchuang,in 21 specimens by Laibo,in 18 specimens by Kangrun,in 28 specimens of HCV-RNA.Among 10 specimens of negative result re-detected by 3 kinds of antibody reagent,1 specimen of HCV-RNA positive,3 specimens of Laibo antigen positive and 1 specimen of Kangrun positive were detected out.The sensitivities of 3 kinds of antibody all were 96.4%,the positive predictive value was 72.9%-75.0%;the sensitivity of 2 kinds of antigen reagent was 40.0% and 83.3% respectively,and the positive predictive value was 57.0% and 83.3% respectively.Conclusion The HCV antibody detection could have the higher diagnostic sensitivity,but its specificity may be lower.Re-detecting the anti-HCV positive samples by using antibody plus antigen model could be of great value to the diagnosis of hepatitis C.Using HCV-RNA for confirming the questionable specimens could be prevent misdiagnosis and missed diagnosis.
hepatitis C virus; hepatitis C virus antibody; hepatitis C virus antigen; hepatitis C virus antigen RNA
广东省珠海市科技计划项目(2012D0401990008)。
龙宏洋,男,本科,主管检验师,主要从事临床检验方面研究。
10.3969/j.issn.1672-9455.2015.05.008
A
1672-9455(2015)05-0597-03
2014-11-10
2014-12-28)
