用于AMS测量的14C样品制备方法
2015-03-10杨旭冉庞义俊
杨旭冉,庞义俊,何 明,窦 亮,姜 山
(1.中国原子能科学研究院,北京 102413;2.广西师范大学,广西 桂林 541004)
用于AMS测量的14C样品制备方法
杨旭冉1,庞义俊2,何 明1,窦 亮1,姜 山1
(1.中国原子能科学研究院,北京 102413;2.广西师范大学,广西 桂林 541004)
为了开展基于加速器质谱(accelerator mass spectrometry,AMS)的14C测量和14C样品制备系统的研究,深入分析样品制备原理和样品制备过程,设计并优化样品制备系统,建立14C的样品制备方法及一套集成的14C样品制备系统。利用AMS测量技术对制备的样品进行了测量和分析,结果显示,建立的样品制备方法所制备的样品已满足AMS测量的要求。
加速器质谱(AMS);14C;样品制备方法;样品制备系统
14C是碳的长寿命放射性核素,其半衰期为5 730年[1],在环境研究中,分析14C在环境中的成因、本底浓度及最终去向是研究的热点。14C既是宇宙成因核素,又是人工放射性核素。宇宙射线在进入大气层的过程中,引起了与氮和氧的核反应而生成了14C[2]。
14C的应用范围非常广泛,在考古研究中,利用14C可以进行5万年以内的年龄测量[3];在环境研究中可以进行大气雾霾来源解析等工作[4];在生物医学研究中可以进行药物的药理学等研究。此外,14C在海洋科学、核环境监测、碳循环[5-6]等领域都有着广泛的应用。在加速器质谱技术发明以前,14C主要利用液体闪烁进行测量[7],此方法需要的样品量多,测量灵敏度低。目前,加速器质谱(AMS)是测量14C灵敏度最高的分析技术[8],监测自然界中丰度偏低的长寿命核素,如10Be,14C,36Cl,41Ca,129I等[9],通过测量该放射性核素与其稳定同位素的比值进行年代和示踪研究[10],具有样品用量少、测量时间短等优点。而利用加速器质谱进行14C的测量[11],需要将待测样品制备成石墨形式才能满足AMS测量的需要[12]。因此,本工作拟建立用于AMS测量的样品制备流程,为开展基于14C的研究工作奠定基础。
1 AMS-14C样品制备
1.1 样品制备原理
对于AMS用14C石墨单质的样品制备,需要解决的关键问题有:(1) 样品制备过程中尽量降低“现代”碳的干扰;(2) 最终14C样品以碳单质形式存在;(3)在测量过程中可以引出可供探测的束流[13-14]。
目前,加速器质谱14C石墨单质样品制样原理基本相同,均为将样品中含碳物质通过充分燃烧转化为14CO2,然后通过还原反应,将14C还原成14C石墨单质[15]。根据过程中还原剂的不同,可分为两类。(1) 氢法。氢气和Fe作为还原剂参与反应,即为将氢气按比例加入到纯化后的14CO2中(铁粉作为催化剂也放置于收集纯化后14CO2的反应管内),等两种气体按比例混合均匀后,密封并加热,从而使14CO2转化为石墨单质。(2) 锌法。Zn作为还原剂参与反应[16],即为将纯化后的14CO2转移到装有指定规格及比例的锌粉反应管内,密封后再进行加热、还原反应,此过程中没有引入其他气体。
通过对两种方法进行比较可见,氢法反应速度快,但由于后引入氢气,氢气的纯净度直接会影响样品精度,从转化率角度看,氢法的转化率需要通过理论计算得出;而锌法反应时间较长,同时由于未引入额外气体,可以监控反应过程中气体含量的变化过程,转化率可直接通过压力变化测量(即理论反应完全后系统内没有残余气体)。通过对两种方法的深入研究,在锌法的基础上选择加入TiH进行反应,在不单独引入氢气的情况下,可以降低气体原因可能产生的干扰并且可观测其转化率。
1.2 样品制备过程
1.2.1 原始样品处理 原始样品需要经过物理选择、化学预处理、充分燃烧三个步骤,从而将原始样品中的含碳化合物提取并转化成CO2。
物理选择则是通过物理手段(碾碎、剪切等)处理原始样品,以木头为例,将木头用干净的镊子等破开,尽量取木心未暴露在空气中的木头样品。(通过对最终石墨样品量的控制,结合样品本身含碳组分的含量来计算原始样品质量)化学预处理则是通过酸洗(浸泡于1.2 mol/L的HCl中,加热至80 ℃并保持6 h,纯水洗净)、碱洗(浸泡于0.5 mol/L的NaOH中,加热至80 ℃并保持2 h,更换NaOH重复操作直至液体基本无色)、酸洗(浸泡于1.2 mol/L的HCl中,加热至80 ℃并保持2 h,纯水洗净至pH7,80 ℃下烘干)达到去除原始样品内的碳酸盐(土壤样品中则以富非酸和腐殖酸为主)等可能会存在的现代碳的干扰。
充分燃烧过程是指将通过化学预处理后的样品,在真空状态下进行充分有效的燃烧(在高温下,足量CuO用来保证其充分燃烧),从而将其内部碳完全转化成CO2。将处理后的样品与CuO(700~800 mg)放置于反应管(内径为8 mm的石英管)内,然后加入银丝,排除燃烧后SO2的干扰,将燃烧管接入到真空系统中(如图1),抽真空至1.0×10-5mbar,将其在真空条件下用玻璃焊枪密封并截断,截断后的燃烧管转移至马弗炉中,500 ℃预热30 min, 850 ℃燃烧2 h。
燃烧过程中所发生的化学反应如下。
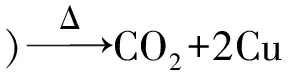
1.2.2 样品还原过程 当原始样品转化为CO2以后,通过一套二氧化碳纯化系统,将纯化后的CO2转移至反应管A内,进入还原阶段,即将收集并纯化后的CO2还原为石墨单质。
从二氧化碳纯化系统(如图1)中可以清楚看到,整个系统可分为三个部分,中间为真空动力部分;右侧为样品抽真空部分(上文提到的燃烧前的真空操作);左侧为CO2纯化部分。本研究设计中,将整个14C样品制备系统有机的整合到了一起,具有以下优点:(1) 可以高效的利用真空系统为抽真空及CO2纯化连个部分服务;(2) 加强了流水线作业的能力;(3) 防止了交叉污染;(4) 整个系统可分开单独拆卸,方便清理及调整。

图1 样品制备系统Fig.1 The sample preparation system
二氧化碳纯化系统,即为将燃烧反应后的气体通过该系统,将可能存在的水蒸气等杂质通过系统进行去除,最终将纯净的CO2转移至反应管A。纯化过程中,燃烧后的气体依次通过液氮-酒精和纯液氮两个冷陷(将两种液体装入到恒温罐中,再将恒温罐套在U型管外),通过不同气体的凝固点不同进行分离、提纯。液氮-酒精为液氮和酒精的混合液体,即将液氮缓慢加入到酒精中,同时伴随不间断搅拌使酒精不会冷凝,最终使温度稳定在-78 ℃左右,其目的将水蒸气等冷凝点在-78 ℃以上的杂质气体凝固;纯液氮,即为零下196 ℃的液氮,其目的将CO2锁定。在CO2随着管道转移到测量区域时,用液氮恒温罐将CO2冷冻住,关闭测量区域两侧阀门,撤掉液氮恒温罐可明显观察到测量区域的玻璃管内,在液氮所及高度平面上有一层白色物质,该物质即为冷冻后的CO2;使该区域恢复至室温,白色消失,G2读数还是上升,通过记录G2冷冻前和冷冻后的数据及测量区域体积,可计算得到理论CO2的体积从而推出最终碳的质量。通过纯化后的CO2进入到反应管A中,需要对其进行还原。用玻璃焊枪在真空下封断反应管A,截断后的反应管A转移至马弗炉中并加热, 650 ℃下反应6 h从而使CO2转化为石墨单质。
样品还原过程中所发生的化学反应如下。
在此环节中,锌和氢化钛作为还原剂放置在直径为10 mm的反应管A中,铁粉作为催化剂放置在直径为6 mm的反应管B中,反应管B置于A内。CO2的还原反应将在铁粉表面发生,最终样品以石墨单质形式附着于铁粉表面,同时为后期加速器质谱的检测提高引出束流能力。
2 结果与分析
在建立了14C样品制备装置和方法基础上,为了检验此系统的性能,对三种样品进行了制备,分别是14C标准样品(OX1,N.I.S.T Oxalic Acid I(C2H2O4),现代碳标准样品,由1955年的甜菜根制备得来)、空白样品(购买的商业空白)和现代木头样品(生长的柳树树枝)。在制备完成后利用中国原子能科学研究院新建立的单级14C专用AMS测量装置上对样品进行了初步测定,测定结果列于表1。

表1 AMS测量结果Table 1 The AMS measurements results
从三个样品的引出束流可以看出,每个样品12C-的引出束流均大于10 μA,此束流已能满足AMS实验测量对样品的要求; 标准样品测量结果为1.2×10-12,此数据与标准比值1.293 3×10-12相差8%,在可容许范围内;空白样品测量的结果为7.4×10-14,此数据比预期的高,主要是由于中国原子能科学研究院新建立的单级14C专用AMS测量装置还处于研发阶段,仪器的测量灵敏度不够高;现代木头样品含量为1.5×10-12,此结果与预期值符合。从束流的测量结果说明成功建立了用于AMS测量的14C样品制备装置和制备流程,从标准样品和空白样品的初步测量结果可见,样品制备稳定,有效避免了交叉污染,满足AMS测样需要。
3 结论
综上所述,该14C样品制备系统可以安全使用,具有相应的稳定性和可靠性,可制备出供AMS测量的合格14C样品。其中,引入了氢化钛使得还原过程避免了氢法再次引入气体的干扰,同时解决了锌法时间长、效率低的问题,完成了样品制备系统过程的优化,从应用角度上看,如PM2.5可通过过滤膜收集,然后通过该系统制备成专用样品,对其进行源解析等,诸多应用均建立在样品制备的基础上。该系统为开展在环境研究、生物医学、核设施监测等领域的研究提供了有力支撑。
致谢:本工作得到国家自然科学基金(11375272)的支持。
[1] Knie K, Faestermann T, Korschinek G, et al. High-sensitivity AMSfor heavy nuclides at the Munich Tandem accelerator[J]. Nucl Instr Meth B,2000, 172: 717-720.
[2] Klevinskas G, Juodis L, Plukis A,et al. Determination of 129I activity in the RBMK-1500 main circulation circuit[J]. NuclEng Des, 2008, 238: 1 518-1 524.
[3] IAEA. Management of waste containing tritium and carbon-14[R]. Vienna: International Atomic Energy Agency, 2004.
[4] Dias C M, Santos R V, Stenstrom K, et al.14C content in vegetation in the vicinities of Brazilian nuclear power reactors[J]. Journal of Environ mental Radioactivity, 2008, 99: 1 095-1 101.
[5] 王钟堂,龚传德,向元益,等. 秦山核电基地外围环境中树轮14C水平分析[J]. 辐射防护,2012,32(5):283-288.
Wang Zhongtang, Gong Chuande, Xiang Yuanyi, et al. Levels of14C in the tree rings in the vicinity of Qinshan nuclear power plant[J]. Radiation Protection, 2012, 32(5): 283-288(in Chinese).
[6] Ragnar H, Göran S. Accelerator mass spectrometry[J]. Mass Spectrom Rev, 2008, 27: 398-427
[7] Shen H T, Jiang S, He Ming, et al. AMS measurements of fission products at CIAE[J]. Nucl Instr Meth B, 2013, 294(1): 136-142.
[8] Paul M, Hollos G, Kaufman A, et al. Measurementof 129I concentrations in the environment after the Chernobyl reactor accident[J]. Nucl Instr Meth B, 1987, 29: 341-345.
[9] Fink D, Middleton R, Klein J, et al.41Ca: Measurement by accelerator mass spectrometry and applications[J]. Nucl Instr Meth B, 1990, 47: 79-96.
[10]Knie K, Faestermann T, Korschinek G, et al. High-sensitivity AMS for heavy nuclides at the Munich Tandem accelerator[J]. Nucl Instr Meth B, 2000, 172: 717-720.
[11]董克君,何明,姜山. 一门十分活跃的核分析技术-加速器质谱(AMS)最新进展[J]. 物理,2006,35(6):508-513.
Dong Kejun, He Ming, Jiang Shan, A activity nuclear analysis technology-the last development of accelerator mass spectrometry[J]. Physics, 2006, 35(6): 508-513(in Chinese).
[12]He M, Jiang S, Nagashima Y, et al. Measurement of the cross-section of 14N (16O, α)26Al with AMS[J]. Nucl Instr Meth B, 2005, 240(3): 612-616.
[13]Turteltaub K W, Felton J S, Gledhill B L, et al. Accelerator mass spectrometry in biomedical dosimetry: relationship between low-level exposure and covalent binding of heterocyclic amine carcinogens to DNA[J]. Proc Natl Acad Sci USA, 1990, 87(14): 8 288-8 292
[14]周卫建,张洁. 超灵敏小型回旋加速器质谱计14C测年的样品制备和制样系统[J]. 核技术,2001,24(增):236-243.
Zhou Weijian, Zhang Jie. The sample preparation at AMS14C dating[J]. Nuclear techniques, 2001, 24(S): 236-243(in Chinese).
[15]Suter M, Balzer R, Bonani G, et al. Precision measurements of14C in AMS-some results and prospects[J]. Nucl Instr Meth B, 1984, 5: 117-122.
[16]Shima T, Okazaki F, Kikuchi T, et al. Measurement of the13C (n, γ)14C cross section at stellar energies[J]. Nuclear Physics A, 1997, 621(1): 231-234.
Method of14C Sample Preparation for AMS Measurement
YANG Xu-ran1, PANG Yi-jun2, HE Ming1, DOU Liang1, JIANG Shan1
(1.ChinaInstituteofAtomicEnergy,Beijing102413,China;2.GuangxiNormalUniversity,Guilin541004,China)
In order to carry out the application research of14C by accelerator mass spectrometry (AMS), the principle of sample preparation were systematically studied and more attention was paid to improve the preparation process efficiently. The set of integrated system of sample preparation was built up on the research. The experimental results showed that the sample preparation scheme was able to meet the demand of AMS measurement.
accelerator mass spectrometry (AMS);14C; method of sample preparation; sample preparation system
10.7538/tws.2015.28.02.0065
2015-03-10;
2015-04-08
国家自然科学基金(No11375272)
杨旭冉(1988—),男,河北保定人,博士研究生,粒子物理与原子核物理专业
姜 山,研究员,E-mail: jiangs@ciae.ac.cn
TL99
A
1000-7512(2015)02-0065-04
