脑深部电刺激丘脑底核背外侧治疗帕金森病患者效果观察
2015-03-07陈宝友李强刘爱彬
陈宝友,李强,刘爱彬
脑深部电刺激丘脑底核背外侧治疗帕金森病患者效果观察
陈宝友,李强,刘爱彬
目的 观察丘脑底核背外侧部电刺激方法治疗帕金森病的效果以及安全性。方法 帕金森病患者15例进行丘脑底核背外侧部电刺激,并根据治疗后疗效和不良反应情况分析与评判治疗的有效性和安全性。结果 与手术前比较,患者UPDRSIII评分和UPDRSII评分,治疗后均有显著改善(P<0.05,P<0.01);用药量、起效时间、药效持续时间等药效学指标都有显著提高(P<0.05);Schwab、Hoehn-yahr评分显示,与术前比较,手术后患者在“开”期和“关”期都有显著改善显著(P<0.05,P<0.01);与术前比较,术后运动功能评分均改善显著(P<0.05,P<0.01);治疗后有相关不良反应出现,如睁眼困难、短暂语言障碍等,通过调节刺激参数都得到了改善。结论 丘脑底核背外侧部电刺激治疗方法对帕金森病具有良好的治疗效果以及安全性。
丘脑底核;帕金森病;电刺激;临床效果
【DOI】 10.3969 /j.issn.1671-6450.2015.01.007
神经系统变性疾病——帕金森病一般多见于中老年人。20世纪60年代发现左旋多巴治疗帕金森病有良好疗效以后被广泛应用[1],但左旋多巴长期使用以后均无可避免地会出现疗效下降的问题,并且有超过30%的患者在6~9年以后可发生异动症[2,3]。锥体外系属于运动系统的重要部分,主要由基底神经节构成。端脑衍生的相关皮质下核团总称为基底神经节,其与运动有关的神经联系,与大脑皮质相关的神经环路直接通路和间接通路相关[3~5],见图1。研究发现丘脑底核背外侧部电刺激治疗方法能够利用微弱的电刺激直接作用到患者脑组织目标部位,主要是对脑内特定的神经核团进行高频电刺激,以改变相应核团兴奋性达到改善帕金森病症状[6],起到治疗效果并且具有良好的安全性,现予以探讨分析。

图1 神经环路直接通路和间接通路
1 资料与方法
1.1 临床资料 2010年4月—2012年8月我院神经科治疗帕金森病患者15例,排除标准:(1)有脑萎缩和精神障碍等;(2)患有其他系统性疾病,包括肝肾功能异常、糖尿病、甲状旁腺功能异常、胃肠功能异常等;(3)对左旋多巴类药物完全无效。男6例,女9例;年龄49~75(59.2±9.6)岁;病程4.0~8.5(6.3±3.6)年。随访时间为术后3~48(20.3±13.2)个月。其中帕金森综合征3例,原发性帕金森病12例。僵直、运动迟缓症状并伴随偶发震颤8例,入睡困难4例。
1.2 治疗方法 (1)丘脑底核背外侧部电刺激治疗方法[7]:首先予以头架进行固定,对患者脑部进行高场强核磁共振成像系统(荷兰飞利浦公司,3.0T)扫描,确定目标位置选取丘脑底核背外侧部为靶位,普鲁卡因静脉复合全麻后钻孔插入微电极(电压1.5~3.5 V,频率为130~180 Hz)至目标靶位,然后需预刺激以确保患者无不良反应。丘脑底核背外侧部微电极植入,双侧13例、单侧2例。(2)药物治疗方法[8]:对所有纳入研究的患者在手术前后服用抗帕金森药物情况(每天服用量)进行分析。抗帕金森药物主要包括左旋多巴、多巴胺受体激动剂等,服用方案依据各个药物说明书。最后根据文献报道的不同药物剂量换算公式进行统计:美多巴100 mg=美多巴缓释剂130 mg=左旋多巴83 mg+脱羟酶抑制剂或抑制剂=多巴胺受体激动剂1 mg。
1.3 观察指标 帕金森病评分采用统一帕金森评分量表(UPDRS)[9],共4个部分42个小项对患者精神情况和日常生活进行评估,4个部分分别为I精神/情绪/行为、II日常生活、III运动情况、IV并发症;治疗前后采用Hoehn-yahr评分量表[10]和Schwab评分量表[11]对患者病情程度和残障程度进行评估,并且针对患者出现的不良反应情况进行安全性的评判。
1.4 评价标准 术前及治疗后12个月对患者的治疗效果进行判断。每次分别在药物的“开” 或“关” 与刺激器的“开” 或“关” 4种组合状态下进行评估。药物“开”和“关” 状态分别表示12 h内有和无服用抗帕金森病药物,刺激器“开”和“关” 状态分别表示2 h内有和无脑深部电刺激。术前指标与术后指标进行对比分析,如果帕金森病患者的情况没有改善或不明显则无效,有明显好转则为治疗效果明显。

2 结 果
2.1UPDRS评分和药物效应 与术前比较,UPDRSIII评分治疗后未服药和服药时均有显著降低(P<0.05,P<0.01),其中手术后未服药时评分和手术前服药时评分相当(P>0.05);而手术治疗后UPDRSII评分显著提高(P<0.05);此外术后用药量、起效时间、药效持续时间都有显著改善(P<0.05)。见表1。
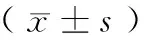
表1 帕金森病患者手术前后UPDRS评分和药效学比较
注:与术前比较,aP<0.05,bP<0.01
2.2 日常生活评分Schwab评分、Hoehn-yahr评分手术治疗前“关”期与“开”期比较,差异有统计学意义(P<0.05或<0.01);手术治疗后“关”期与“开”期比较,差异无统计学意义(P>0.05);但是与手术治疗前比较,在“开”期和“关”期都有显著性的改善(P<0.05),尤其对于“关”期,改善更为显著(P<0.01)。见表2。
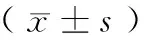
表2 帕金森病患者手术前后日常生活评分
注:与术前比较,aP<0.05,bP<0.01;与“开”期比较,cP<0.05,dP<0.01
2.3 运动功能评分 手术前运动功能评分在药物的 “关”期与“开”期比较,有显著性差异(P<0.05);手术治疗后,震颤、僵直、运动迟缓等运动功能评分,“关”期与“开”期比较,无显著性的差异(P>0.05);但是和治疗前比较,均有改善作用(P<0.05或<0.01)。见表3。
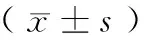
表3 帕金森病患者手术前后运动功能评分
注:术前与“开”期比较,aP<0.05;与术前比较,bP<0.05,cP<0.01
2.4 治疗效果与不良反应 术后随访治疗效果明显的患者14例、无效1例。患者的症状从第3个月开始逐渐好转,1年后患者的UPDRSIII评分平均改善率为67.8%,生活能力评分平均改善率为71.5%,患者原有帕金森病控制药物的用量平均减少68.3%。术中颅内出血1例(6.7%),无死亡病例。治疗后对患者的随访发现有短暂不良反应,主要有睁眼困难1例(6.7%),智力减退以及短暂语言障碍2例(13.3%),抑郁症状1例(6.7%),通过刺激参数调节以后都得到了改善。
3 讨 论
帕金森病早期使用药物进行治疗确实能够起到良好的作用,但是药物长期使用以后(一般在4年)就会逐渐出现药效减退的问题[12]。尤其是长期使用左旋多巴等一系列治疗帕金森病的药物以后有可能导致患者出现异动症更加剧了患者的痛苦。通过丘脑底核背外侧部电刺激治疗后确实能够对帕金森病起到良好的效果,并且实际治疗安全性良好[7,8]。只是由于植入微电极的参数必须要进行不断地调整才能够保证疗效的稳定。文献分析也证明丘脑底核背外侧部电刺激的安全性,虽然会导致少部分患者出现一定的不良反应,但是通过参数调节都能够起到良好的控制作用[13]。
丘脑底核背外侧部电刺激治疗手术后短期效果与药物的作用相近,但是丘脑底核背外侧部电刺激优势在长期开机治疗的情况下就逐渐体现,丘脑底核背外侧部电刺激治疗通过长时间证明,作用效果不断提高,而药物则会出现药效减退以及带来并发症的问题[14]。
本次研究发现,丘脑底核背外侧部电刺激治疗可以改善UPDRSIII评分和UPDRSII评分,未服药和服药时均有显著改善,特别对未服药时评分改善更为显著。相关研究证实,丘脑底核背外侧部电刺激治疗手术可以使脑部辅助运动区、前额皮质的背外侧区、扣带回前部血流增多,同时参与边缘系统信息处理的脑部分因为受到电刺激,进而对情感、认知和行为产生调节作用,显著地改善了UPDRSIII评分和UPDRSII评分。同时显著减少用药量,改善起效时间、药效持续时间,特别有利于减少药物,增加起效时间,与其他报道相似[13]。手术治疗后日常生活量表Schwab、Hoehn-yahr评分都有显著性的改善。震颤、僵直、运动迟缓等具体行为明显改善。丘脑底核背外侧部电刺激治疗有3个靶点,丘脑底核、丘脑腹内侧核、苍白球内侧部,其中对丘脑腹内侧核的点刺激可以有效控制震颤的症状,同时有文献报道,大脑桥脑脚核部位受到电刺激也是改善帕金森患者运动障碍症状的原因之一[14]。
丘脑底核背外侧部电刺激治疗过程中出现不良反应有意识错乱、智力减退、语言障碍、抑郁等。实际治疗过程中通过对电刺激参数的调节能够实现控制。丘脑底核背外侧部电刺激治疗过程中的相关不良反应也应该得到重视,并积极采取措施予以预防。
关于丘脑底核背外侧部电刺激与药物治疗之间的关系还有待进一步的研究。丘脑底核背外侧部电刺激虽然对帕金森病的治疗效果明显且安全性高,但相比药物疗效还存在一定不足,在丘脑底核背外侧部电刺激治疗的基础上结合药物治疗将是研究的重点。
总之,丘脑底核背外侧部电刺激相比药物能更好地对帕金森病患者进行治疗,尤其是帕金森病晚期治疗过程中更适宜采用丘脑底核背外侧部电刺激。
1 高歌,牛朝诗,傅先明.帕金森病丘脑底核深部脑刺激术后参数的调整[J].中国微侵袭神经外科杂志,2011,16(9):401-403.
2TripolitiEE,TzallasAT,TsipourasMG,etal.AutomaticdetectionoffreezingofgaiteventsinpatientswithParkinson'sdisease[J].ComputMethodsProgramsBiomed,2013,110(1):12-26.
3KollerWC,PahwaR,LyonsKE.SurgicaltreatmentofParkinson'sdisease[J].NeurSci,1999,167(1):1-10
4 王涛,乔洪文,刘雁勇,等.28烷醇对6-羟基多巴胺致帕金森病大鼠的行为学作用及其机制研究[J].中国康复理论与实践,2013,19(11):1001-1005.
5HeijnenBJ,SpeyerR,BaijensL,etal.Neuromuscularelectricalstimulationversustraditionaltherapyinpatientswithparkinson'sdiseaseandoropharyngealdysphagia:effectsonqualityofLife[J].Dysphagia,2012,27(3):336-345.
6RoemmichRT,FieldAM,ElrodJM,etal.InterlimbcoordinationisimpairedduringwalkinginpersonswithParkinson'sdisease[J].ClinicalBiomechanics,2013,28(1):93-97.
7 梁晋川,胡小吾,周晓平,等.帕金森病丘脑底核电刺激术后脑多巴胺转运体变化[J].中华神经外科杂志,2013,29(12):1200-1203.
8ChenYI,RenJQ,KaptchukTJ,etal.Restoringcerebraldopaminehomeostasisbyelectricalforepawstimulation:AnfMRIstudy[J].Synapse,2012,66(4):331-339.
9LeeKH,BlahaCD,HarrisBT,etal.Dopamineeffluxintheratstriatumevokedbyelectricalstimulationofthesubthalamicnucleus:potentialmechanismofactioninParkinson'sdisease[J].EurJNeurosci,2006,23(4):1005-1014.
10JimenezF,VelascoF,Carrillo-RuizJD,etal.ComparativeevaluationoftheeffectsofunilaterallesionversuselectricalstimulationoftheglobuspallidusinternusinadvancedParkinson'sdisease[J].StereotactFunctNeurosurg,2006,84(2/3):64-71.
11FuentesR,PeterssonP,SiesserWB,etal.SpinalcordstimulationrestoreslocomotioninanimalmodelsofParkinson'sdisease[J].Science,2009,323(5921):1578-1582.
12KangG,LowergMM.Interactionofoscillations,andtheirsuppressionviadeepbrainstimulation,inamodeloftheCortico-Basalganglianetwork[J].IEEETransNeuralSystRehabilEng,2013,21(2):244-253.
13VelascoF,JiménezF,PérezML,etal.ElectricalstimulationoftheprelemniscalradiationinthetreatmentofParkinson'sdisease:anoldtargetrevisedwithnewtechniques[J].Neurosurgery,2001,49(2):293-306.
14PanS,IplikciS,WarwickK,etal.Parkinson'sdiseasetremorclassification-Acomparisonbetweensupportvectormachinesandneuralnetworks[J].ExpertSystAppl,2012,39(12):10764-10771.
The clinical efficacy of deep brain stimulation of the lateral dorsal subthalamic nucleus for patients with Parkinson's disease
CHENBaoyou,LIQiang,LIUAibin.
DepartmentofNeurosurgery,theAffiliatedHospitalofLogisticsCollegeofChinesePeople'sArmedPoliceForce,Tianjin300162,China
Objective To observe the effect and safety of subthalamic nucleus lateral dorsal electrical stimulation for the treatment of Parkinson's disease.Methods Subthalamic nucleus lateral dorsal electrical stimulation was performed in 15 patients with Parkinson's disease, and according to the efficacy and safety of treatment, the efficacy and adverse reactions of treatment were analyzed and evaluated.Results Compared with before surgery, after treatment, patients' UPDRS III score and UPDRS II score were significantly improved (P<0.05,P<0.01);dosage,onsettime,durationofefficacywereimproved(P<0.05);Schwab,Hoehn-yahrscoresshowedthatcomparedwithpreoperative,postoperativepatientshasimprovedsignificantlyinthe"on"and"off"period(P<0.05,P<0.01);comparedwiththepreoperative,motorfunctionscoreswereimprovepostoperatively(P<0.05,P<0.01);aftertreatment,relatedadversereactions,suchasopeneyedifficultieswereoccurred,butthroughtheadjustmentofstimulation,theseparameterswereimproved.Conclusion The subthalamic nucleus lateral dorsal electrical stimulation treatment method has a good therapeutic effect and safety for treating of Parkinson's disease.
Subthalamic nucleus; Parkinson's disease; Electric stimulation;Clinical effect
300162 天津,武警后勤学院附属医院神经外一科
2014-10-17)
