续骨酒质量标准研究
2015-02-27胡翼安张丹雁冯小映陈庆奇
胡翼安, 张丹雁*, 冯小映, 陈庆奇
(1.广州中医药大学,广东广州 510006;2.广州市正骨医院,广东广州 510045;3.南方医科大学附属佛山市妇幼保健院,广东佛山 528000)
续骨酒质量标准研究
胡翼安1, 张丹雁1*, 冯小映2, 陈庆奇3
(1.广州中医药大学,广东广州 510006;2.广州市正骨医院,广东广州 510045;3.南方医科大学附属佛山市妇幼保健院,广东佛山 528000)
[目的]建立续骨酒的定量定性检测方法,为续骨酒质量控制提供理论依据。[方法]采用薄层色谱法(TLC)对续骨酒中的栀子、地黄定性鉴别;采用高效液相色谱法(HPLC)测定栀子苷的含量。[结果]TLC鉴别分离度好、专属性强;含量测定中栀子苷在0.151 1~2.518 0 mg范围内呈良好线性关系,线性回归方程为Y=925 558X- 11 386,r=0.999 9(n=7),平均回收率为99.4%,RSD%为1.4。[结论]该试验所建立的方法简便、准确、专属性强、精密度高、重复性好,可作为续骨酒的质量控制方法。
续骨酒;质量标准;地黄;栀子苷
续骨酒是广州市正骨医院的一个常用制剂。续骨酒主要由闹羊花、续断、栀子、姜黄、生地黄、独活等中药组成,具有活血化瘀、消肿止痛、驱风祛湿、舒筋通络的功效,对各种骨折肿痛、跌打损伤、风湿骨痛有确切的疗效。续骨酒是一安全、有效、使用方便的外用喷雾剂,很受患者欢迎,却至今缺乏一个全面、完善的质量标准。现行的续骨酒内控质量标准中只有2010年版中国药典中有关喷雾剂通则项下的检查,包括外观、总固体、乙醇量、装量、微生物限度等项目,这些检查项既不能保证制剂的质量,亦保障不了临床用药的有效性和安全性,因此很有必要对续骨酒中的药材和有效成分进行鉴别,并测定其有效成分的含量,以提高续骨酒的质量和临床用药的有效性。笔者采用薄层色谱法对栀子、地黄进行定性鉴别,用高效液相色谱法对续骨酒中栀子苷进行了含量测定,为续骨酒质量标准的制定提供一定的科学依据,也为续骨酒后期在临床上的发展应用奠定基础。
1 材料和方法
1.1 仪器岛津高效液相色谱仪(LC-10ATvp泵、SPD-10Avp紫外检测器、CTO-10ASvp柱温箱、CBM-20A控制器、SIL-20A自动进样器,LC solution化学工作站);KQ-300型超声波清洗器(功率300 W,频率40 kHz,东莞市科桥超声波设备有限公司);AUW220D型万分之一分析天平(日本SHIMADZU公司);Goodlook-1000型薄层色谱成像系统(上海科哲生化科技有限公司);薄层层析硅胶G板(德国MACHEREY-NAGEL公司,批号006153)。
1.2 试药栀子对照药材(批号120986-201309,中国药品生物制品检定所),地黄对照药材(批号121180-201005,中国药品生物制品检定所),栀子苷对照品(批号110749-201316,中国药品生物制品检定所);续骨酒(广州市正骨医院,批号20140101、20140201、20140301、20140401、20140501)和续骨酒栀子阴性溶液(广州市正骨医院);甲醇为色谱纯,其余为分析纯。
1.3 方法
1.3.1栀子的TLC鉴别 。取本品20 ml,蒸干,加乙醇2 ml使溶解,作为供试品溶液;取缺栀子的阴性对照样品20 ml,同法制成缺栀子阴性对照溶液;再取栀子对照药材1 g,加50%甲醇10 ml,超声40 min,滤过,取续滤液作为对照药材溶液;另取栀子苷对照品,加乙醇制成每1 ml含4 mg的溶液,作为对照品溶液。按照薄层色谱法[1]试验,吸取上述供试品溶液和阴性对照溶液各4 ml、对照药材溶液及对照品溶液各2 ml,分别点于同一硅胶G薄层板上,以乙酸乙酯-丙酮-氨水-甲醇-水(5∶5∶1∶0.5∶0.5)为展开剂[2],展开,取出,晾干。喷以10%硫酸乙醇溶液,105 ℃加热至斑点清晰。在日光下检视,供试品色谱中,在与对照药材色谱和对照品色谱相应的位置上,应分别显相同颜色的斑点,阴性对照应无干扰。
1.3.2地黄的TLC鉴别。取续骨酒原液作为供试品溶液。取地黄对照药材1 g,加80%甲醇50 ml,超声30 min,滤过,滤液蒸干,残渣加水5 ml使溶解,用水饱和正丁醇振摇提取4次,每次10 ml,合并正丁醇液,蒸干,残渣加甲醇2 ml使溶解,作为对照药材溶液。按照薄层色谱法试验[1],吸取供试品溶液和对照药材溶液各5 ml,分别点于同一硅胶G薄层板上,以正丁醇-冰醋酸-水-甲醇(6∶3∶3∶2)为展开剂[3],展开,取出,晾干。喷以10%硫酸乙醇溶液,105 ℃加热至斑点清晰。在日光下检视,供试品色谱中,在与对照药材色谱相应的位置上,应分别显相同颜色的斑点,应阴性对照无干扰。
1.3.3栀子苷的含量测定。
1.3.3.1色谱条件与系统适用性试验。色谱柱为迪马ODS色谱柱(250×4.6 mm,5 μm),流动相为甲醇-水(20∶80),流速1.0 ml/min;柱温30 ℃;检测波长237 nm。理论塔板数按栀子苷峰计算应不低于3 000。
1.3.3.2供试品溶液的制备。精密吸取续骨酒10 ml,置于25 ml容量瓶,加入甲醇溶解并稀释至刻度,摇匀,用0.45 mm孔径微孔滤膜滤过,取续滤液作为供试品溶液。
1.3.3.3对照品溶液的制备。取栀子苷对照品适量,精密称定,置于50 ml容量瓶中,加入甲醇溶解并稀释至刻度,摇匀,制成含251.8 mg/ml的对照品溶液;精密吸取上述对照品溶液5 ml,置于20 ml容量瓶,加入甲醇至刻度,摇匀,制得含62.94 mg/ml的栀子苷对照品溶液。
1.3.3.4阴性对照溶液的制备。按缺栀子的阴性对照样品,按“1.3.3.2”项下方法制备,即得缺栀子阴性对照溶液。
1.3.3.5测定方法。分别精密吸取供试品溶液及对照品溶液各10 μl,注入高效液相色谱仪,测定,即得。
1.3.3.6标准曲线的制备及线性考察。精密吸取栀子苷对照品溶液(251.8 mg/ml)各0.6、1.0、2.0、4.0、6.0、8.0、10.0 ml,分别注入高效液相色谱仪,按“1.3.3.1”色谱条件进行测定并绘制标准曲线。
1.3.3.7稳定性试验。将按“1.3.3.2”项制备的供试品溶液(批号20140101)于0、2、4、8、12、24 h分别进样10 μl,按“1.3.3.1”色谱条件测定。
1.3.3.8精密度试验。精密取栀子苷对照品溶液10 μl,采用高效液相色谱法,连续测定6次。
1.3.3.9重复性试验。取供试品溶液(批号20140101)按“1.3.3.5”项下方法,连续测定6次。
1.3.3.10加样回收试验。在已知含量的续骨酒加入一定量的栀子苷对照品溶液,按“1.3.3.5”项下方法测定,并计算回收率。

注:1、17为栀子对照药材;18为栀子苷对照品;19为缺栀子的阴性对照溶液;2~16为续骨酒样品(2~4批号20140101、5~7批号20140201、8~10批号20140301、11~13批号20140401、14~16批号20140501)。图1 栀子薄层鉴别
1.3.3.11样品测定。精密称取续骨酒样品,按“1.3.3.2”项下方法制备供试品溶液,分别精密吸取供试品溶液和对照品溶液各10 μl,采用高效液相色谱法测定。
2 结果与分析
2.1 栀子的TLC鉴别从图1可以看出,供试品色谱中,在与栀子对照药材色谱和栀子苷对照品色谱相应的位置上,分别显相同颜色的斑点,缺栀子阴性对照品色谱相应的位置上没有干扰。
2.2 地黄的TLC鉴别从图2可以看出,在与地黄对照药材色谱显相同颜色的斑点,缺地黄阴性对照品色谱相应的位置上没有干扰。
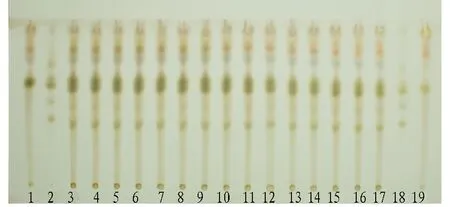
注:2、18为地黄对照药材;1、19为缺地黄的阴性对照液;2~16为续骨酒样品(3、4、5批号为20140101;6、7、8批号为20140201;9、10、11批号为20140301;12、13、14批号为20140401;15、16、17批号为20140501)。图2 生地黄薄层鉴别

注:a为续骨酒供试品;b为栀子苷对照品;c为缺栀子的阴性对照样品。图3 续骨酒栀子苷含量测定色谱图
2.3 栀子苷的含量测定
2.3.1色谱条件及系统适应性试验。在该色谱条件下检测,绘制供试品、栀子苷对照品和缺栀子阴性对照品色谱图(图3)。由图3可见,供试品和栀子苷对照品在相同的保留时间(32.5 min),缺栀子阴性对照品在相对应的保留时间没有影响。供试品所测定主峰附近无明显杂峰,经计算,样品主峰与其他组分峰的分离度>1.5。
2.3.2标准曲线的制备及线性考察。通过“1.3.3.1”色谱条件测定栀子苷对照品,以栀子苷进样量(X)为横坐标、峰面积(Y)为纵坐标进行线性回归,得出线性回归方程为Y=925 558X- 11 386(r=0.999 9),结果表明,栀子苷在0.151 1~2.518 0 mg范围内呈良好的线性关系。
2.3.3稳定性试验。按“1.3.3.7”项,分别于0、2、4、8、12、24 h测定续骨酒中的栀子苷。测得24 h内平均峰面积为662 523,RSD=2.1%(n=6),表明被测样品在24 h内稳定。
2.3.4精密度试验。按“1.3.3.8”项,连续测定6次,测得平均峰面积为590 545,RSD=1.1%,表明在此试验条件下精密度良好。
2.3.5重复性试验。按“1.3.3.9”项,连续测定6次。测得同一批号中,平均峰面积为660 066,栀子苷平均浓度为173.7 μg/ml,RSD=1.2%,结果显示重复性良好。
2.3.6加样回收试验。由表1可见,该试验方法中栀子苷的平均回收率达99.4%,RSD为1.4%,表明该方法准确、可靠,可用于续骨酒中栀子苷的含量测定。
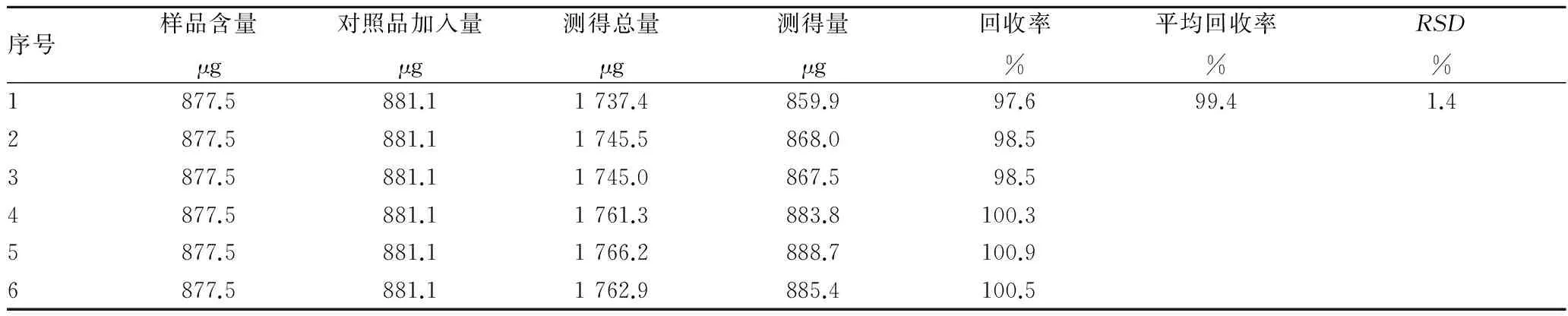
表1 续骨酒中栀子苷加样回收率试验
2.3.7样品测定。由表2可知,3批续骨酒中栀子苷含量为155.1~176.6 μg/ml,平均含量为163.6 μg/ml,RSD为0.20%~0.49%。
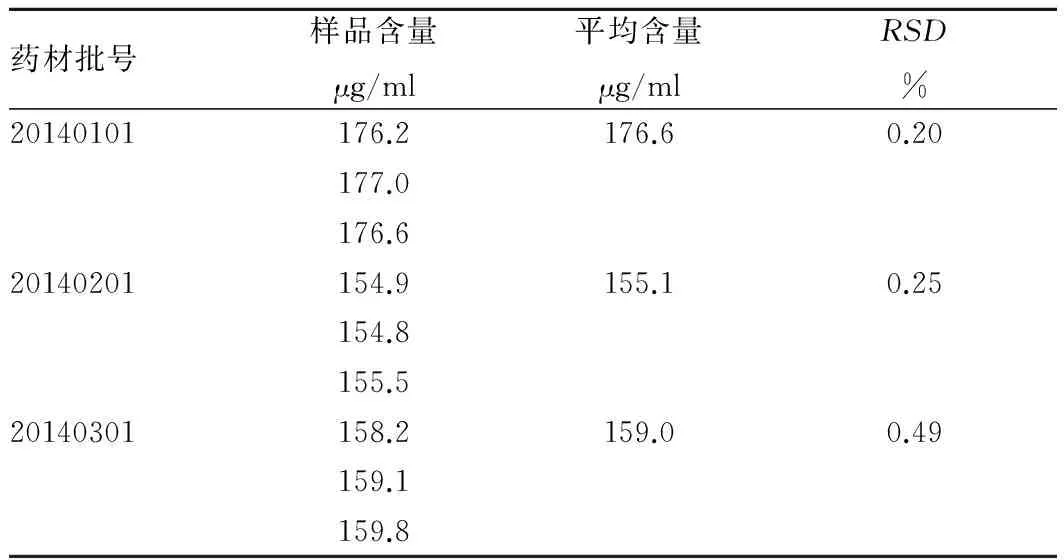
表2 3批续骨酒中栀子苷含量测定
3 小结与讨论
(1)栀子的薄层色谱鉴别中,按药典方法的展开系统分离效果较差,经查阅文献,改用乙酸乙酯-丙酮-氨水-甲
醇-水(5∶5∶1∶0.5∶0.5)为展开剂,结果显示斑点清晰、分离度好,可作为续骨酒的定性鉴别指标。
(2)地黄的薄层色谱鉴别中,按药典方法的展开系统分离效果较差,斑点模糊,经查阅文献,改用正丁醇-冰醋酸-水-甲醇(6∶3∶3∶2)为展开剂,结果显示斑点清晰、分离度好,可作为续骨酒的定性鉴别指标。
(3)该研究采用HPLC法测定了续骨酒中栀子苷的含量,样品分离度高,测定方法重复性良好、回收率高、专属性强,可作为该制剂质量控制的含量测定指标。
(4)该研究测得续骨酒中栀子苷的平均含量为163.6 μg/ml,考虑到药材来源、制剂生产等因素,暂规定本品每毫升中含栀子以栀子苷(C17H24O10)计,不得少于90 μg/ml。
[1] 国家药典委员会.中华人民共和国药典(一部)[S].北京:中国医药科技出版社, 2010:231, 附录34-35.
[2] 方道硕, 钟亚玲, 宋英.清热泻火胶囊的质量标准[J].中国药师, 2008, 11(4): 406- 408.
[3] 冯文涛, 谢颖, 张榕.凉血颗粒所用药材的薄层鉴别[J].华西药学杂志, 2008, 23(4): 502.
Quality Standard Research forXugujiu
HU Yi’an1, ZHANG Dan-yan1*, FENG Xiao-ying2et al
(1.Guangzhou University of Chinese Medicine, Guangzhou, Guangdong 510006; 2.Guangzhou Orthopedic Hospital, Guangzhou, Guangdong 510045)
[Objective] To establish qualitative and quantitative detection method forXugujiu, and provide a theoretical basis for the quality control.[Method] Gardeniae Fructus and Rehmanniae Radix were identified by TLC, the content of Jasminoidin was determined by HPLC.[Result] The spots in TLC was clear, the negative control was no interference.Content determination of Jasminoidin had good linear relationship between 0.151 1 to 2.518 mg, the linear regression equation wasY=925 558X- 11 386,r=0.999 9(n=7), the average recovery was 99.4%, RSD 1.4%.[Conclusion] The method is simple, accurate, specified, high precision and good repeatability.It can be used for quality control ofXugujiu.
Xugujiu; Quality standard; Rehmanniae Radix; Jasminoidin
佛山市卫生和计生局医学科研课题(408239275162)。
胡翼安(1987- ),男,广东广州人,硕士研究生,研究方向:医院制剂。*通讯作者,教授,博士生导师,从事中药鉴定研究。
2015-02-02
S 567
A
0517-6611(2015)08-047-03
