纳米氧化锆粉体的制备与表征
2015-02-23吴佳航,刘国军,张桂霞,刘素花,王妍,张鹏飞
吴 佳 航,刘 国 军,张 桂 霞,刘 素 花,王 妍,张 鹏 飞
(大连工业大学 纺织与材料工程学院,辽宁 大连 116034)
0 引 言
纳米粒子因其独特的微观结构,具有小尺寸效应、表面效应、量子尺寸效应和宏观隧道效应,因此有着独特的热、光、电、磁和催化等物理化学性质[1]。纳米氧化锆是一种熔点和沸点高,硬度和强度大,常温下为绝缘体,而高温下则具有导电性的无机非金属材料[2]。氧化锆因其特殊的性能,主要应用于高温陶瓷、耐火材料、釉料、压电元件、陶瓷电容器、气敏元件、固体电解质电池、光学玻璃、二氧化锆纤维及锆催化剂等[3-6]。氧化锆具有优异的耐热、耐腐蚀和可塑性,已成为新材料领域重要的基础原料[7]。有研究表明,100nm 的ZrO2在拉伸疲劳试验中晶粒出现300%的超塑性,由于晶粒粒径的减小,材料性能有了数量级的提高,烧结温度大大下降,作为添加剂它能使脆性材料增韧,韧性材料强度更强,陶瓷材料的脆性问题可望得到解决[8]。另外,由于氧化锆的化学稳定性好,其表面同时具有酸性和碱性,并同时拥有氧化性和还原性,近年来,ZrO2引起了催化领域学者的广泛兴趣[9]。
氧化锆粉体的制备方法有很多,包括化学气象沉淀法[10]、水热法[11]、溶胶-凝胶法[12]等,但这些方法在工业实施上有一定困难。化学沉淀法一般是指将沉淀剂加入到金属盐溶液中进行沉淀,然后再对沉淀物进行固液分离、洗涤、干燥以及加热分解等后处理,从而制得粉末产品[13],其合成工艺简单,制备条件易于控制,所得粉体纯度高、粒度小且分布均匀。
本实验以硝酸锆和氨水为原料,采用化学沉淀法制备纳米氧化锆粉体,在合成过程中,引入表面活性剂(吐温)作为晶粒生长抑制剂,防止发生团聚。考察粉体的合成条件并对其进行表征,以此粉体为基础,将其添加到丙烯酸酯乳液中,为后续的氧化锆/丙烯酸酯复合乳液各方面性能研究打下基础。
1 实 验
1.1 原 料
硝酸锆(Zr(NO3)4·5H2O),分析纯,天津市福晨化学试剂厂;氨水(NH3·H2O),分析纯,天津市凯信化学工业有限公司;乙醇,分析纯,天津市永大化学试剂有限公司。
1.2 制备方法
将一定量的硝酸锆和去离子水装于有恒压滴液漏斗、搅拌器、冷凝管的三口烧瓶中,并置于预设好温度的水浴锅中,搅拌直至溶解完全;然后加入一定量表面活性剂及分散剂;再配制一定浓度的氨水溶液,以每3秒1滴的速度向三口烧瓶中滴加氨水溶液;滴加完毕后保温陈化一段时间;最后冷却至室温,用乙醇和去离子水洗涤、抽滤至pH 为7左右,出料、烘干、煅烧,即得到要制备的氧化锆粉体。
1.3 粉体表征
采用称重法进行计算测定氧化锆产率。使用X 射线衍射仪(PC,JAPAN)分析样品的晶相结构,并用Scherrer公式[14]计算氧化锆晶粒尺寸及晶面间距。采用美国TA 公司的Q50型热重分析仪及WCR-20型热重分析仪分析干燥后的前驱物的TG、DTA 曲线,测定温度范围为20~700 ℃,升温速率为20 ℃/min。采用德国BRUKER 公司的TENSO27 型衰减全反射红外光谱仪进行测试。
2 结果与讨论
2.1 氧化锆前驱物粉体的热分析
图1为氧化锆前驱物在20~800℃的TG-DTA变化曲线图。从TG 曲线可以看出,在整个加热过程中,氧化锆前驱物总质量损失约为23%,100 ℃以下对应于结合水的消除过程和残余有机物(如乙醇)的挥发,100 ℃约到350 ℃对应前驱物中结构水的挥发和残留的沸点较高的有机物的燃烧分解(如表面活性剂)。另外,从图中DTA 曲线可以看出,在100℃附近出现吸热峰,这是因为前驱物中水分子和有机物的挥发吸收热量导致的。在450 ℃附近出现尖锐的放热峰,而且失重速率很快,这是因为氧化锆前驱物分解以及结晶水的挥发,在此过程中,前驱物转化为晶相,形成一定的晶型。随着温度的升高,约450 ℃后均处于吸热状态,说明800 ℃后可能会有晶型的转变。
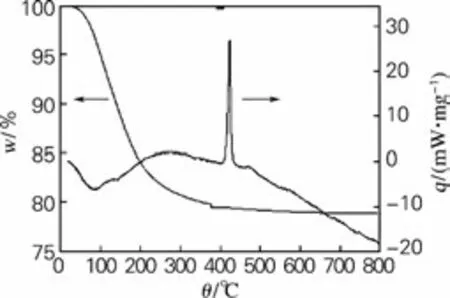
图1 氧化锆前驱物的TG-DTA 变化曲线Fig.1 TG-DTA curves of the zirconia precursor
2.2 氧化锆前驱物及煅烧后的红外分析
图2为氧化锆前驱物及经450℃煅烧后的红外光谱图,从图中可以看出,在3 420cm-1附近的吸收峰为水和羟基的伸缩振动峰,在1 384 和1 622cm-1为水和羟基的弯曲振动吸收峰,在507cm-1附近为Zr—O—Zr键的伸缩振动吸收峰,这说明前驱物经450 ℃煅烧后发生晶型转变,反应产物转变为氧化锆,这与“2.1”结果相符合。
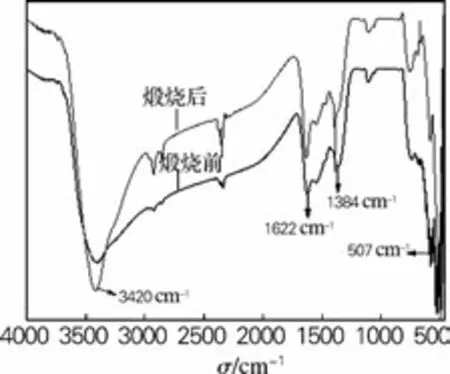
图2 氧化锆煅烧前后的红外光谱图Fig.2 The IR spectra of the zirconia before and after calcination
2.3 氧化锆前驱物及煅烧后的晶型分析
图3和图4分别为氧化锆前驱物和氧化锆粉体干燥后的XRD图。从图中可以看出前驱物为典型的非晶相物质,图中的衍射峰宽化并不尖锐,具有“馒头”状衍射峰,这是非晶物质所固有的特点。而将前驱物在450 ℃下煅烧后,就会发生晶化,由Scherrer公式计算出其晶粒尺寸为20.2nm。与JCPDS制定的标准卡对比,其曲线的峰值、峰位与单斜相和四方相氧化锆特征衍射峰相对应。无机粉体中含有单斜氧化锆(2θ=30.28°,35.18°),四方氧化锆(2θ=50.58°,60.12°),主要是以单斜为主,粉体的衍射峰呈现一定程度的弥散和宽化现象,造成这种现象的原因有两方面[15]:一方面是小尺寸晶粒的出现;另一方面是原子水平上的微应力影响。这种弥散和宽化现象说明所得粉体具有超细的结构,晶粒尺寸很小。

图3 前驱物粉体XRD图Fig.3 XRD patterns of the precursor powders

图4 氧化锆粉体XRD图Fig.4 XRD patterns of the zirconia powders
2.4 锆盐浓度对粉体的影响
表1 为 锆 盐 浓 度 分 别 为0.2,0.4,0.5 和0.7mol/L时对氧化锆产率和晶粒尺寸的影响。从表1可以看出,随着锆盐浓度增加,氧化锆的产率先增大后减小,晶粒尺寸总体随着锆盐浓度增大而增大,这是因为锆盐离子浓度增加,制备出来的氧化锆产生团聚的现象比较严重,影响氧化锆的产率,当锆盐浓度较小时,以晶核生成为主,因此粒子尺寸小,产率较低,而晶粒的尺寸主要由晶体成核的过程所控制,锆盐浓度增大,晶体成核速度较快,晶核数目增多,发生碰撞的概率增大,故容易产生尺寸较大的晶粒。

表1 锆盐浓度对氧化锆产率及晶粒尺寸的影响Tab.1 The influence of zirconium oxychloride concentration on zirconia yield and particle size
图5 为不同锆盐浓度条件下,450 ℃煅烧3h的氧化锆粉体的XRD 分析谱图。可以看出,不同锆盐浓度下的氧化锆粉体的晶型没有太大变化,但晶体的结构完整性有所不同,根据计算公式可得,在锆盐浓度分别为0.2,0.4,0.5 和0.7mol/L时,其晶面间距分别为29.293,29.482,29.255,29.218 nm。当锆盐浓度为0.4mol/L时,其晶面间距最接近标准卡片的数值(31.639nm),结晶完整性最好,但晶面间距仍存在差异,这可能是因为煅烧温度较低,结晶不够完整所导致的。

图5 不同锆盐浓度下氧化锆粉体的XRD图Fig.5 XRD patterns of the powders in different concentration of aqueous zirconium oxychloride solution
2.5 煅烧温度的粉体晶相的影响
图6是氧化锆前驱物分别在500,600,700,800 ℃下煅烧3h的XRD图。从图中可以看出,当煅烧温度为500 ℃时,同时具有四方相和单斜相的特征衍射峰,在30°附近有个尖锐的四方相衍射峰,随着煅烧温度的升高,此衍射峰逐渐变小。李云凯等[16]研究发现,当粒子尺寸较小时,四方相较易形成,反之,易于形成单斜相,因为当粒子的尺寸增大后,四方相的稳定性有所下降,从而倾向于转变为单斜相。当煅烧温度为800 ℃时,30°附近四方相衍射峰消失,这正是由于随着煅烧温度升高,氧化锆晶粒生长速度增大,晶粒尺寸变大,使得晶型由四方相逐渐转变为单斜相。
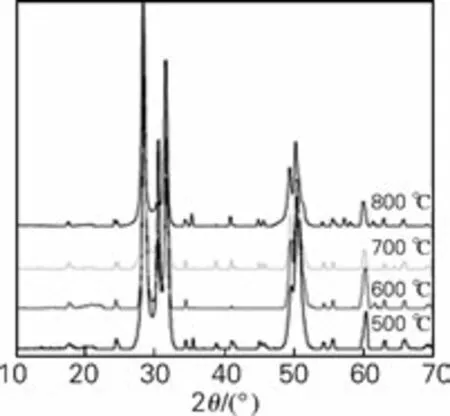
图6 不同煅烧温度下氧化锆粉体的XRD图Fig.6 XRD patterns of the powders at different calcinations temperatures
3 结 论
(1)采用化学沉淀法,以硝酸锆和氨水为原料制备氧化锆粉体,在450℃左右,氧化锆前驱物分解,由无定型转变为晶相,红外谱图上表现出Zr—O—Zr伸缩振动吸收峰。
(2)前驱物为典型的非晶相物质,具有“馒头”状衍射峰,这是非晶物质所固有的特点,将前驱物在450℃下煅烧后,就会发生晶化,煅烧后的氧化锆粒子中同时存在单斜相和四方相,主要以单斜相为主,晶粒尺寸为20.2nm。
(3)不同锆盐浓度下的氧化锆粉体的晶型没有太大变化,但晶体的结构完整性有所不同,当锆盐浓度为0.4mol/L时,粉体的产率高、晶粒尺寸小,结晶完整性最好。
(4)随着煅烧温度升高,氧化锆晶粒生长速度增大,晶粒尺寸变大,晶型由四方相逐渐转变为单斜相。
[1]邵旭,林龙,翟滨,等.纳米银嵌入的杂化材料[J].大连工业大学学报,2013,32(5):346-349.(SHAO Xu,LIN Long,ZHAI Bin,ZHAI Shang-ru,et al.Nanosilver embedded hybrid material[J].Journal Dalian Polytechnic University,2013,32(5):346-349.)
[2]郑文裕,陈潮汐,陈仲从.二氧化锆的性质、用途及其发展方向[J].无机盐工业,2000,32(1):18-20.
[3]毕诗文.氧化铝生产工艺[M].北京:化学工业出版社,2006:127-128.
[4]李小斌,刘桂华,彭志宏,等.高苛性比铝酸钠溶液中氧化铝的回收[J].中国有色金属学报,1999,9(2):403-406.
[5]NOWORYTA A.Mathematical model of the desiliconization of aluminate solutions[J].Hydrometallurgy,1981,7(1/2):107-115.
[6]NOWORYTA A.On the removal of silica from aluminate solutions:mechanism and kinetics of the process[J].Hydrometallurgy,1981,7(1/2):99-106.
[7]孙亚光,余丽秀.二氧化锆制备及发展趋势[J].化工新型材料,1999,28(4):27-30.
[8]王焕英,宋秀芹.化学沉淀法制备纳米氧化锆的研究[J].河北师范大学报,2001,26(5):488-491.
[9]杨广慧,张彦.纳米氧化锆的制备及应用[J].化工新型材料,1999,27(5):21-23.
[10]殷声.现代陶瓷及其应用[M].北京:北京科学技术出版社,1990:222-223.
[11]李汶军,施尔畏,郑燕青,等.水热盐溶液卸压法制备氧化物粉体[J].无机材料学报,1999,14(3):456-460.
[12]SANGEETA D,RAMAMURT H.Nanometersized ZrO2particles prepared by a sol-emulsion-gel method[J].American Ceramic Society,1990,73(9):2760-2763.
[13]温立哲,余忠民,黄慧民,等.纳米氧化锆的制备及其干燥技术[J].广东工业大学学报,2002,19(1):63-69.
[14]吴刚.材料结构表征及应用[M].北京:化学工业出版社,2002:277-278.
[15]LIMA R S,KUCUK A,BERNDT C C.Integrity of nanostructured partially stabilized zirconia after plasma spray processing[J].Materials Science and Engineering A,2001,313(4):75-82.
[16]李云凯,周张健.陶瓷及其复合材料[M].北京:北京理工大学出版社,2007:23-26.
