利斯的明中间体含量及ee值的RP-HPLC法测定*
2015-02-23李永红周方方付路平刘宏民
李永红,周方方, 付路平,刘宏民#
1)郑州大学新药研究开发中心 郑州 450001 2)郑州大学药学院 郑州 450001
利斯的明中间体含量及ee值的RP-HPLC法测定*
李永红1,2),周方方2), 付路平2),刘宏民1,2)#
1)郑州大学新药研究开发中心 郑州 4500012)郑州大学药学院 郑州 450001
关键词利斯的明;手性药物中间体;ee值
摘要目的:建立RP-HPLC法测定生物转化液中利斯的明中间体含量及ee值的方法。方法:以Lux 3u Cellulose-1为手性分离柱,以正己烷异丙醇(VV=92.57.5)为流动相,检测波长217 nm,进样量20 μL。结果:中间体能够完全分离,在测定中间体含量的同时能够测定样品的ee值。结论:该方法准确、灵敏、精密度良好,适合生物转化液中利斯的明中间体含量及ee值的测定。
AbstractAim: To establish a RP-HPLC method to determine the ee values and content of rivastigmine intermediates in bioconversion broth.Methods: The determination was performed on a Lux 3u Cellulose-1 column with a 92.57.5(VV) mixture of n-hexane and isopropanol alcohol as mobile phase, determination wavelength of 217 nm and injection volume of 20 μL.Results: The two intermediates were completely separated. The ee value could be determined as well as the determination of the content of the intermediates.Conclusion: The method is accurate and sensitive with high precision.It is suitable for the determination of the ee values and content of rivastigmine intermediates in bioconversion broth.
利斯的明可以选择性地在大脑区域内作用并有较长持续时间的活性,是氨基甲酸酯类乙酰胆碱酯酶抑制剂[1-2]。Enz等[3]通过HPLC-MS的方法测定了利斯的明的代谢产物在大鼠脑和血浆中的浓度。Pommier等[4]开创了采用GC-MS测定人体血浆样品中利斯的明浓度的方法。该研究建立了利用RP-HPLC测定生物转化液中利斯的明中间体含量及ee值的方法。该方法快速、简单,且不受杂质的影响,报道如下。
1材料与方法
1.1仪器型号与试剂HYG-Ⅱa 型自动摇瓶柜(上海欣蕊自动化设备有限公司),R-1005旋转蒸发仪(郑州长城科工贸有限公司),Waters 1525高效液相色谱仪,色谱柱为Lux 3u Cellulose-1柱(4.6 mm×250 mm,美国Phenomenex公司)。菌种来源:郑州大学药学院筛选并保藏的一株能产生立体选择性酯酶的菌种。正己烷为色谱纯(天津康科德科技有限公司),其他试剂为分析纯。
参考文献1.2样品的拆分原理及制备[5-8],作者筛选到一株能产生立体选择性酯酶的菌株,用脂肪酶Novozym453转化化合物2,以乙酸异丙烯酯为酰基供给体,得到中间体(R)-1和(S)-2。见图1。
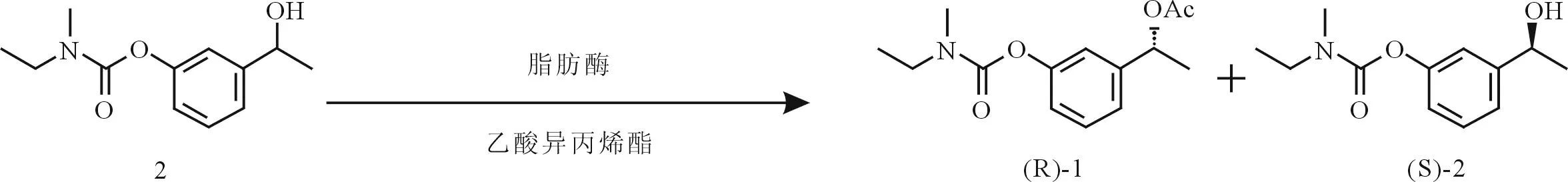
图1 化合物2的转化
具体制备步骤如下:将菌种转接到培养基,于28 ℃、220 r/min条件下培养48 h后加入底物,同等条件下转化12 h得到转化液。合并用相同体积的乙酸乙酯萃取转化液3次后的有机相;经无水Na2SO4干燥后,旋转蒸发仪蒸干,用相应的流动相溶解,0.45 μm微孔滤膜滤过后用于测定。
1.3色谱条件流动相为V正己烷V异丙醇=92.57.5,流速0.8 mL/min,检测波长为217 nm,柱温25 ℃,进样量20 μL。
1.4色谱峰的归属转化12 h后,分析转化底物和产物的HPLC图谱,并以此样品图谱与实验室保藏菌种转化产品的HPLC图谱对比,进行色谱峰的归属。
1.5方法学分析
1.5.1标准曲线的绘制[9-10]准确称量自制的化合物2[(R)-2为化合物2的R型异构体]和化合物1各1.0 g,加异丙醇溶解并定容至100 mL,配成2种化合物质量浓度均为10 g/L的混合标准样品。取适量上述混合样品,用流动相稀释为质量浓度分别为0.25、0.50、0.75、1.00、1.25和1.50 g/L的标准溶液,按1.3提供的条件测定并进行线性回归分析,求得标准曲线。
1.5.2 精密度实验按照1.3方法,取一份转化液进行测定,重复5次,记录其峰面积并计算RSD值。
1.5.3加标回收率在转化液中加入不同质量浓度的混合标准样品,按1.3方法测定,计算加标回收率。
1.5.4样品ee值的计算通过样品2个异构体的峰面积来计算ee值,ee=(R异构体峰-S异构体峰)/(S异构体峰+R异构体峰)×100%。
2结果
2.1化合物的分离效果用上述液相条件,在利斯的明中间体拆分过程中,化合物2和化合物1的分离效果比较理想。各个中间体名称、结构、色谱图和分离结果见图2。左:化合物2和化合物1混合物的HPLC图谱;中:消旋的化合物2转化12 h后转化为(S)-2、(R)-1的HPLC图谱;右:化合物2的HPLC图谱。
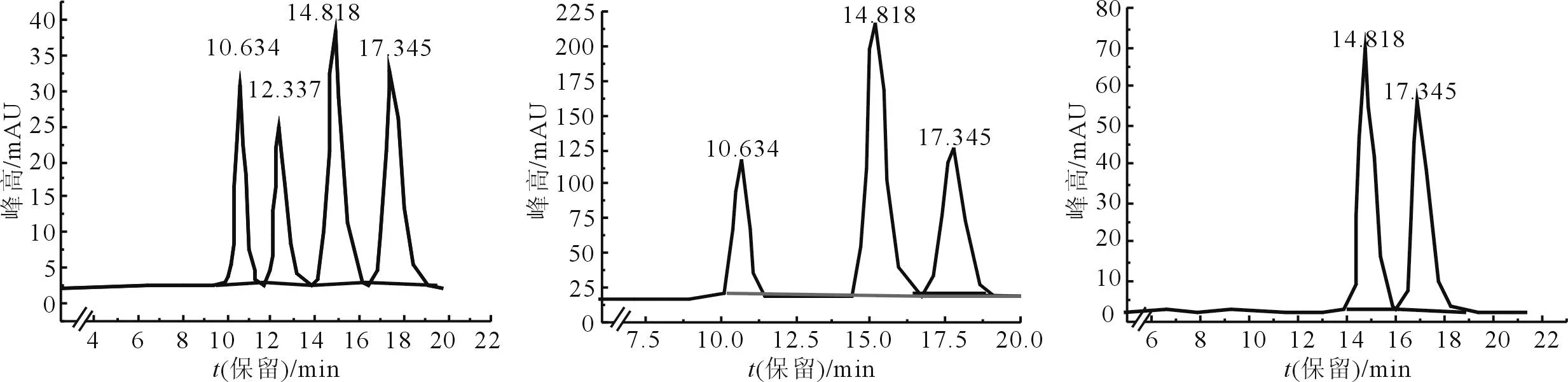
图2 相关中间体的结构
从图2可以看出,化合物1和化合物2可以被完全拆分,HPLC图谱基线平稳,转化液经处理后基本没有杂质。通过化合物1和化合物2混合物的HPLC谱图、化合物2的HPLC图谱及消旋化合物2转化12 h后的HPLC图谱结果对比分析可知,新出现的峰为化合物(R)-1的峰,转化12 h后,化合物(S)-2的峰面积基本没变,而化合物(R)-2的峰面积有所减少,且没有(S)-1的峰出现。化合物1的(R)-异构体和(S)-异构体保留时间分别为(10.334±0.300) min和(12.037±0.300) min,化合物2的(S)-异构体和(R)-异构体保留时间分别为(14.618±0.200) min和(17.045±0.300) min,误差在允许范围内。
2.2方法学分析结果2种化合物在0.25~1.25 g/L范围内线性关系良好。化合物2的线性方程为Y=24 472X-74.767,R2=0.999 5,化合物1的线性方程为Y=21 961X+404.98,R2=0.999 3;该方法测定结果的精密度较好,RSD分别为1.190%(n=6)和1.850%(n=6);化合物(R)-1的ee值为93.22%,化合物(R)-2的ee值为92.22%。化合物2和化合物1的加标回收率分别为98.170%和98.830%。
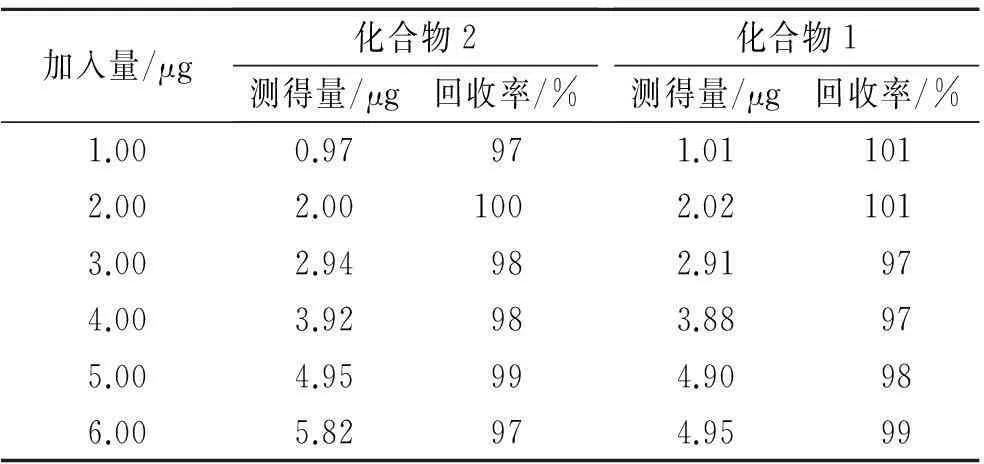
表1 加样回收实验结果
3讨论
该实验所用的正己烷和异丙醇均为色谱纯且样品中没有过多的杂质,故HPLC谱图基线平稳,色谱峰之间没有重叠,测定结果准确。使用该方法不但使化合物1、2得到了良好的分离,而且各自的2种对映异构体也基本上被分离,在实验过程中不仅可同时测定2种化合物的含量,还可以测定其ee值,有利于对转化过程进行跟踪测定,且灵敏度高。作者利用此分析方法已经对季也蒙毕赤酵母(Meyerozymaguilliermondii)HM988686.1催化利斯的明中间体拆分的转化条件进行优化,利用优化后的条件进行转化,转化速度大大提高。
[1]徐刚,文富华,买小胖,等.胆碱酯酶抑制剂(S)-卡巴拉汀及其类似物的不对称合成与活性研究[J].有机化学,2010,30(8):1185
[2]Polinsky RJ. Clinical pharmacology of rivastigmine:a new-generation acetylcholinesterase inhibitor for the treatment of Alzheimer′s disease[J].Clin Ther,1998,20(4):634
[3]Enz A,Chappuis A,Dattler A.A simple,rapid and sensitive method for simultaneous determination of rivastigmine and its major metabolite NAP 226-90 in rat brain and plasma by reversed-phase liquid chromatography coupled to electrospray ionization mass spectrometry[J].Biomed Chromatogr,2004,18(3):160
[4]Pommier F,Frigola R.Quantitative determination of rivastigmine and its major metabolite in human plasma by liquid chromatography with atmospheric pressure chemical ionization tandem mass spectrometry[J].J Chromatogr B Analyt Technol Biomed Life Sci,2003,784(2):301
[5]Kim N,Ko SB,Kwon MS,et al.Air-stable racemization catalyst for dynamic kinetic resolution of secondary alcohols at room temperature[J].Org Lett,2005,7(20):4523
[6]Han K,Kim C,Park J,et al.Chemoenzymatic synthesis of rivastigmine via dynamic kinetic resolution as a key step[J].J Org Chem,2010,75(9):3105
[7]Arava VR,Gorentla L,Dubey PK.A simple and highly efficient enantioselective synthesis of (S)-rivastigmine[J].Int J Org Chem,2011,1:26
[8]Arava RV,Gorentlaa L,Dubey PK.Facile enantioselective synthesis of (S)-Rivastigmine and (+)-NPS-R-568 a calcimimetic agent[J].Der Pharma Chemica,2011,3(1):426
[9]李永红,于梅艳,刘宏民.高效液相色谱法测定β-氨基醇类药物中间体的含量及ee值[J].郑州大学学报:医学版,2009,44(2):427
[10]可钰,袁冬冬,刘宏民.盐酸倍他洛尔的手性液相色谱法拆分及其左旋体的稳定性分析[J].郑州大学学报:医学版,2010,45(2):308
*安徽中医药大学2014年自然科学基金资助项目2014zr010
Determination ofeevalues and content of rivastigmine intermediates by RP-HPLC
LIYonghong1,2),ZHOUFangfang2),FULuping2),LIUHongmin1,2)
1)NewDrugResearch&DevelopmentCenter,ZhengzhouUniversity,Zhengzhou4500012)DepartmentofPharmaceuticalSciences,ZhengzhouUniversity,Zhengzhou450001
Key wordsrivastigmine; chiral drug intermediate; ee value
doi:10.13705/j.issn.1671-6825.2015.06.018
中图分类号TQ460.7
通信作者#,男,1960年3月生,博士,教授,研究方向:药物化学及糖化学,E-mail:liuhm@zzu.edu.cn
