疏肝健脾益肾中药联合化疗治疗肝郁型转移性三阴性乳腺癌患者疗效及安全性研究
2015-02-21王志光林丽珠
王志光,林丽珠
·专题研究·
疏肝健脾益肾中药联合化疗治疗肝郁型转移性三阴性乳腺癌患者疗效及安全性研究
王志光,林丽珠
目的 探讨疏肝健脾益肾中药联合化疗治疗肝郁型转移性三阴性乳腺癌(TNBC)患者的临床疗效及安全性。方法 收集2010年5月—2013年9月柳州市中医院肿瘤科收治的术后化疗后出现内脏转移的TNBC患者79例,采用随机数字表法分成两组,对照组40例,采用GT化疗(紫杉醇+吉西他滨);治疗组39例,采用疏肝健脾益肾中药联合化疗。评价两组临床疗效及毒副作用。结果 患者均最少完成2个周期化疗,对照组完全缓解2例(5.0%)、部分缓解16例(40.0%)、稳定13例(32.5%)、进展9例(22.5%);治疗组分别为1例(2.6%)、15例(38.5%)、16例(41.0%)、7例(17.9%);两组临床疗效比较,差异无统计学意义(Z=-0.120,P=0.904)。平均随访8.5个月,对照组及治疗组平均无进展生存期(PFS)分别为(5.7±0.5)个月、(7.5±0.7)个月,中位PFS分别为(5.2±0.3)个月、(6.5±0.6)个月。两组PFS比较,差异有统计学意义(χ2=4.627,P=0.031)。两组患者骨髓抑制发生程度比较,差异无统计学意义(Z=0.672,P=0.501);两组患者消化道毒副作用发生程度比较,差异有统计学意义(Z=1.995,P=0.046)。结论 疏肝健脾益肾法能延长肝郁型转移性TNBC化疗患者的PFS,并能减轻化疗药物的消化道毒副作用。
乳腺肿瘤;疏肝;健脾;抗肿瘤联合化疗方案;无进展生存期
王志光,林丽珠.疏肝健脾益肾中药联合化疗治疗肝郁型转移性三阴性乳腺癌患者疗效及安全性研究[J].中国全科医学,2015,18(6):620-624.[www.chinagp.net]
Wang ZG,Lin LZ.Clinical efficacy and safety of combined chemotherapy with traditional Chinese medicine for smoothing liver,invigorating spleen and tonifying kidney in the treatment of metastatic triple negative breast cancer with liver stagnation[J].Chinese General Practice,2015,18(6):620-624.

表1 两组患者一般情况比较〔n(%)〕
注:PS评分=功能状态评分
乳腺癌是当前世界上治疗规范、研究进展迅速、疗效也相对较好的肿瘤疾病之一,但对于三阴性乳腺癌(triple negative breast cancer,TNBC),目前的治疗进展相对较小,疗效也较非TNBC差很多,对于转移性TNBC,治疗手段更是相对匮乏。目前,紫杉类药物及吉西他滨已成为除蒽环类药物之外治疗转移性乳腺癌最常用化疗药物。既往有研究显示,紫杉醇联合吉西他滨对于转移性乳腺癌有较高的有效率[1-2],是既往接受过蒽环类药物化疗的TNBC患者适宜的临床选择。本研究采用疏肝健脾益肾中药联合紫杉醇及国产吉西他滨治疗肝郁型转移性TNBC患者,获得了较好的临床效果,报道如下。
1 资料与方法
1.1 临床资料 收集2010年5月—2013年9月柳州市中医院肿瘤科收治的术后化疗后出现内脏转移的TNBC患者79例为研究对象,均为女性。入选标准:(1)术后病理诊断为乳腺癌,且免疫组化显示雌激素受体(ER)、孕激素受体(PR)、原癌基因人类表皮生长因子受体2(HER-2)均阴性;(2)中医辨证存在肝郁证[3];(3)肿瘤出现内脏转移;(4)功能状态(PS)评分0~2分,预计生存期6个月以上;(5)既往蒽环类药物辅助化疗;(6) 化疗前骨髓和肝肾储备功能正常;(7) 年龄18~75岁;(8)患者及家属知情同意。排除标准:(1)只有骨转移灶,无其他内脏转移者;(2)出现脑转移者;(3)手术及辅助放化疗结束后不足3个月出现转移者;(4)不同意或无法按期进行化疗后影像学检查评价疗效者;(5)化疗不足2个周期因非医疗相关原因退出者;(6)服用中药有不良反应者。
1.2 分组 采用随机数字表法将患者分成两组,对照组40例,采用化疗,年龄(50.7±2.1)岁;治疗组39例,采用疏肝健脾益肾中药联合化疗,年龄(51.2±2.3)岁。两组年龄比较,差异无统计学意义(t=2.25,P=0.138)。两组PS评分、转移脏器、转移灶数量构成及是否绝经比较,差异均无统计学意义(P>0.05,见表1)。
1.3 治疗方法 化疗方案:紫杉醇(海南中化联合制药工业股份有限公司,国药准字:H20083956) 135~175 mg/m2,(化疗过程中出现Ⅲ度异常骨髓抑制者改用135 mg/m2)静脉滴注,d1;吉西他滨(江苏豪森药业股份有限公司,国药准字:H20030104)1 000 mg/m2,静脉滴注,d1和d8,21 d为1个周期。紫杉醇用药前进行标准的抗过敏处理:地塞米松15 mg,分别于用药前12、6 h口服,化疗前30 min应用苯海拉明50 mg肌肉注射、西米替丁400 mg静脉注射,化疗前后30 min分别予以托烷司琼5 mg静脉滴注止吐,化疗期间出现Ⅱ度以上白细胞计数降低常规使用粒集落刺激因子(G-CSF)生白治疗。治疗组化疗前3 d开始口服中药,化疗开始第1~3天暂停口服中药,第4天开始口服至第14天。以后每个周期服用中药同第1个周期。中药组成:柴胡15 g、当归15 g、白芍15 g、白术15 g、茯苓15 g、生姜15 g、薄荷6 g、炙甘草9 g、穿山甲10 g、红参12 g、鸡内金15 g、熟地30 g、山茱萸15 g、山药15 g、鹿角胶20 g、黄芪30 g,由本院药房JS-819多功能煎药机煎煮,分2次饭后半小时口服。患者最多接受6个周期的化疗。入组前均签署化疗知情同意书,肿瘤进展(PD)或患者拒绝及出现不可接受的毒副作用时终止试验。治疗方案通过医院伦理委员会批准。
1.4 评价标准 每个周期开始前行常规体格检查及血常规、血生化检查。第1次化疗前对所有可测量病灶均行CT、MRI、骨扫描等检查,记录病灶大小的基线值,以后每2个周期后对基线病灶行影像学复查,评价疗效,对于化疗临床获益者[4]初次评价后每隔4周重新进行影像学评价1次,对于未到影像学复查时间但患者出现相关临床症状,怀疑病情进展者,尽快行相关影像学检查评价。疗效评价按2009年欧洲RECIST标准[4]分为完全缓解(CR)、部分缓解(PR)、稳定(SD)、PD。毒副作用参照美国国立癌症研究所(NCI)CTCAE v3.0标准[5]。无进展生存期(PFS)指从首次化疗开始至发现疾病出现进展或患者死亡。截尾数据:规定的随访时间内,由于失访、非肿瘤性死亡、肿瘤未进展、退出研究等没有出现结果事件者称之为截尾。

2 结果
2.1 临床疗效 患者均最少完成2个周期化疗,并进行了影像学复查。两组患者瘤体总缓解率(CR+PR)分别为41.1%、45.0%。两组临床疗效比较,差异无统计学意义(Z=-0.120,P=0.904,见表2)。

表2 两组临床疗效比较〔n(%)〕
注:CR=完全缓解,PR=部分缓解,SD=稳定,PD=进展
2.2 PFS 79例患者中,随访过程中未发现肿瘤PD者至少随访至首次化疗开始后10个月。平均随访8.5个月,对照组及治疗组平均PFS分别为(5.7±0.5)个月、(7.5±0.7)个月,中位PFS分别为(5.2±0.3)个月、(6.5±0.6)个月。两组PFS比较,差异有统计学意义(χ2=4.627,P=0.031,见图1)。
2.3 毒副作用 主要毒副作用为骨髓抑制(粒细胞计数及血小板计数降低)及消化道毒副作用(恶心及呕吐)。两组患者骨髓抑制发生程度比较,差异无统计学意义(Z=0.672,P=0.501,见表3);两组患者消化道毒副作用发生程度比较,差异有统计学意义(Z=1.995,P=0.046,见表4)。
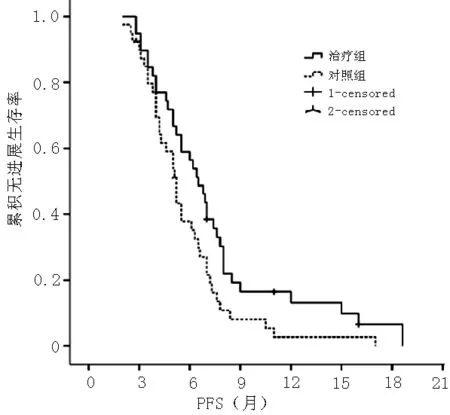
注:PFS=无进展生存期
图1 两组PFS曲线图
Figure 1 PFS curves of the two groups
表3 两组患者骨髓抑制发生程度比较〔n(%)〕
Table 3 Comparison of occurrence degree of myelosuppression between the two groups

组别例数0ⅠⅡⅢⅣ对照组402(50)7(175)13(325)11(275)7(175)治疗组393(77)6(154)16(410)9(231)5(128)
表4 两组患者消化道毒副作用发生程度比较〔n(%)〕
Table 4 Comparison of occurrence degree of gastrointestinal side effect between the two groups

组别例数ⅠⅡⅢⅣ对照组403(75)12(300)16(400)9(225)治疗组397(179)15(385)13(333)4(103)
2.4 截尾数据 79例患者中,出现截尾数据5例,其中治疗组3例,1例为随访过程中患者出现急性缺血性脑梗死、另2例为随访至PFS时患者未出现肿瘤PD;对照组2例,1例为患者2个周期化疗后因家人原因放弃继续化疗到外地寻求免疫治疗、另1例为患者化疗4个周期后联系方式变更无法继续联系。
3 讨论
近年来虽然拉帕替尼、贝伐单抗、西妥昔单抗等靶向治疗在晚期转移性TNBC治疗上取得了一定的疗效[6-8],但因其价格昂贵,并不能为我国广大患者所接受,化疗依然是我国转移性TNBC患者的主要治疗手段。欧洲临床肿瘤协会年会(ESMO)已达成共识,将以蒽环类药物及紫杉类药物为基础的化疗方案作为局部晚期TNBC的初始治疗方案[9],大部分TNBC患者在术后辅助化疗中即已使用蒽环类药物,考虑到蒽环类药物的心脏毒性累积作用,本研究化疗方案未使用含蒽环类药物方案。紫杉类药物与吉西他滨合用的有效率在45%~64%,成为既往使用过蒽环类复发转移性乳腺癌的有效、合理的选择方案[10-11]。吉西他滨与紫杉醇作用于不同的细胞周期,吉西他滨为细胞周期特异性抗代谢类抗癌药,主要作用于S期细胞,紫杉醇可作用于细胞微管/微管蛋白系统,对G2期和M期细胞敏感,故两药联合能很好地增强疗效。本研究也取得了较好的PFS及总缓解率,与国内外其他两药联合的临床试验数据相似[1-2]。
临床上转移性TNBC患者大多术后已行多次强度较大的辅助化疗,使得患者对化疗的耐受性降低,如何提高化疗的耐受性、并延长患者的生存时间对临床有重要意义,而辨证论治的指导思想使得中医药可能能够弥补化疗的不足。中医学认为,肝郁是乳腺癌发病的重要病理基础,且中医药治疗肝气郁结有较好的临床疗效,西医学难以取代,故本研究选择肝郁型这一亚型作为研究对象。《外科正宗》:“忧郁伤肝、思虑伤脾,积想在心,所愿不得者,致经络痞涩,聚结成核”指出了乳腺癌的成因。根据脏腑经络学说,乳头属足厥阴肝经、肝脉布络胸胁,宜疏泄条达。郁怒伤肝,肝失疏泄则胸胁脉络气机不利。乳房属胃,脾胃互为表里,脾伤则运化无权而痰浊内生,以至无形之气郁与有形之痰浊相互交凝,经络痞涩,日积月累,结滞乳中而成本病。肾为元气之根,冲任之本。肾气充盛则冲任脉盛,冲任之脉上贯于乳,下濡包宫。《疮疡经验全书》:“阴极阳衰,血无阳安能散,致血渗入心经而生乳岩”。故乳腺癌与肝脾肾三藏关系密切,其中又以与肝关系最大,多项临床研究也证实,气郁体质为乳腺癌患者中所占比例最大的体质类型,超过一半[12-13]。程旭锋等[14]认为,“肝气郁滞”贯穿于乳腺癌发生、发展的整个病理过程,并认为是机体免疫力下降的具体表现。李福鑫[15]、石书芳[16]运用疏肝法为主的治法对乳腺癌术后患者进行干预,不仅能够改善患者的临床症状、生活质量,还能控制肿瘤发展、延长生存期、预防复发。化疗短期内主要对消化道及骨髓功能损伤明显,且肝郁患者很易出现木克土即肝郁脾虚,脾肾功能的损伤导致患者对化疗耐受性降低,免疫力下降。
既往国内的临床研究虽然有对肝郁型乳腺癌患者进行中医干预治疗,但多是术后无瘤状态的患者,而对于综合治疗后内脏转移的TNBC患者,其治疗更为棘手,预后亦更为凶险[15-16]。国际上有针对转移性TNBC患者的临床研究[7-8],但采用的靶向药物价格昂贵,不适合我国国情。本研究将转移性TNBC患者作为研究对象,采用中药治疗联合常规化疗,其近期疗效与化疗相当。研究采用的中医治疗方案运用逍遥散方底疏肝解郁、条畅气机,红参、白术、鸡内金等药物健脾益气、顾护中土,减轻恶性呕吐等化疗期间消化道反应,熟地、山茱萸、山药、鹿角胶、黄芪等补肾填髓,益气养血,减轻骨髓抑制作用,穿山甲软坚散结,配合化疗药物加强抗癌作用,全方攻补兼施,以补为主,辅以行气、散结,与化疗联合,相得益彰。“正气存内,邪不可干,邪之所凑,其气必虚”,化疗期间配合中药健脾益肾,使得脾肾重要脏器气血充足、精血充盈,且气机畅达,降低了癌细胞(即邪气)的增殖及转移的概率,而肿瘤进展的基本条件就是癌细胞的增殖及扩散。Deng等[17]既往进行的动物实验也证实了这一中医理论,从分子水平证明了中药能对乳腺癌癌细胞发生侵袭及转移的重要物质基础基质金属蛋白酶(MMPs)及CD44的表达起到抑制作用,从而对乳腺癌的骨转移起到一定的防治作用。
综上所述,从中医学理论基础、临床实践以及分子水平不同层面为疏肝健脾益肾法改善机体对化疗毒副作用的耐受性、延长PFS提供了理论基础。但肿瘤的发生、发展以及治疗期间的毒副作用,常是多因素综合作用的结果,中西医结合的临床研究因临床干预手段较纯中医或纯西医研究复杂。本研究样本量较少,若能继续增加样本,对患者不同月经状态、不同术后转移时间、不同内脏转移、不同病理类型等因素均进行亚组分析,可能能筛选出最佳的中医获益人群,也更加符合乳腺癌个体化诊疗的发展趋势,值得在今后工作中探索。
[1] Tomao S,Romiti A,Tomao F,et al.Aphase Ⅱ trial of a biweekly combination of paclitaxel and gmecitabine in metastatic breast cancer[J].BMC Cancer,2006,6:137-143.
[2]Liao Y,Fan Y,Wan Y,et al.Acceptable but limited efficacy of capecitabine-based doublets in the first-line treatment of metastatic triple-negative breast cancer:a pilot study[J].Chemotherapy,2013,59(3):207-113.
[3] 国家中医药管理局.中医病证诊断疗效标准[M].北京:中国医药科技出版社,2012:26.
[4] Watanabe H,Okada M,Kaji Y,et al.New response evaluation criteria in solid tumours-revised RECIST guideline(version 1.1)[J].Gan To Kagaku Ryoho,2009,36(13):2495-2501.
[5]Trotti A,Colevas AD,Setser A,et al. CTCAE v3.0:development of a comprehensive grading system for the adverse effects of cancer treatment[J].Seminars in Radiation Oncology,2003,13(3):176-181.
[6]Clark O,Botrel TE,Paladini L,et al.Targeted therapy in triple-negative metastatic breast cancer:a systematic review and meta-analysis[J].Core Evid,2014,9:1-11.
[7]Hamilton E,Kimmick G,Hopkins J,et al.Nab-paclitaxel/bevacizumab/carboplatin chemotherapy in first-line triple negative metastatic breast cancer[J].Clin Breast Cancer,2013,13(6):416-420.
[8] Baselga J,Gómez P,Greil R,et al.Randomized phase Ⅱ study of the anti-epidermal growth factor receptor monoclonal antibody cetuximab with cisplatin versus cisplatin alone in patients with metastatic triple-negative breast cancer[J].J Clin Oncol,2013,31(20):2586-2592.
[9] Cardoso F,Costa A,Norton L,et al.ESO-ESMO 2nd international consensus guidelines for advanced breast cancer (ABC2) [J].Ann Oncol,2014,25(10):1871-1888.
[10] Moinpour CM,Donaldson GW,Liepa AM,et al.Evaluating health-related quality-of-life therapeutic effectiveness in a clinical trial with extensive nonignorable missing data and heterogeneous response:results from a phase Ⅲ randomized trial of gemcitabine plus paclitaxel versus paclitaxel monotherapy in patients with metastatic breast cancer[J].Qual Life Res,2012,21(5):765-775.
[11]Albain KS,Nag SM,Calderillo-Ruiz G,et al.Gemcitabine plus Paclitaxel versus Paclitaxel monotherapy in patients with metastatic breast cancer and prior anthracycline treatment[J].J Clin Oncol,2008,26(24):3950-3957.
[12] Mou WN,Li M,Xie CS.Clinical features and TCM syndromes in 78 cases with triplenegative breast cancer[J].Journal of Chinese Oncology,2014,20(2):106-109.(in Chinese) 牟微娜,李苗,谢长生.78 例三阴性乳腺癌的临床特征和中医证型分析[J].肿瘤学杂志,2014,20(2):106-109.
[13] Zhang L,Tian H,Li QQ,et al.Study on the correlation of TCM constitution type characteristics and TCM syndromes of 132 breast cancer patients[J].Yunnan Journal of Traditional Chinese Medicine and Materia Medica,2012,33(8):13-16.(in Chinese) 张莉,田欢,李清琴,等.132例乳腺癌患者中医体质特征与中医证候的相关性研究[J].云南中医中药杂志,2012,33(8):13-16.
[14] Cheng XF,Liu Q,Liu S.Treat breast cancer,s pathogenesis transformation from liver [J].Chinese Journal of Basic Medicine in Traditional Chinese Medicine,2011,17(2):151-152.(in Chinese) 程旭锋,刘琦,刘胜.从“肝”论治乳腺癌的病机转化[J].中国中医基础医学杂志,2011,17(2):151-152.
[15] Li FX.Influence of Fuzheng Shugan Xiaoai decoction on relapse and metastasis and life quality in breast cancer patients with postoperative radiation and chemotherapy[J].Chinese Journal of Experimental Traditional Medical Formulae,2013,19(7):342-345.(in Chinese) 李福鑫.扶正疏肝消癌方对乳腺癌术后放化疗患者复发转移和生存质量的影响[J].中国实验方剂学杂志,2013,19(7):342-345.
[16]Shi SF.Clinical analysis of professor CHEN Yi on treating postoperative breast cancer patients with spirit regulating and depression relieving method[J].Journal of Sichuan of Traditional Chinese Medicine,2013,31(8):12-14.(in Chinese) 石书芳.陈熠运用调神解郁法治疗乳腺癌术后临床分析[J].四川中医,2013,31(8):12-14.
[17] Deng B,Jia LQ,Gao FY,et al.Effect of Sangu Decoction on metastatic bone destruction in rats with mammary cancer[J].Chin J Integr Med,2012,18(4):304-307.
(本文编辑:陈素芳)
Clinical Efficacy and Safety of Combined Chemotherapy with Traditional Chinese Medicine for Smoothing Liver,Invigorating Spleen and Tonifying Kidney in the Treatment of Metastatic Triple Negative Breast Cancer with Liver Stagnation
WANGZhi-guang,LINLi-zhu.
DepartmentofOncology,LiuzhouHospitalofTraditionalChineseMedicine,theThirdAffiliatedHospitalofLiuzhouTraditionalChineseMedicineHospital,Liuzhou545001,China
Objective To investigate the clinical efficacy and safety of combined chemotherapy with traditional Chinese medicine (TCM) for smoothing liver,invigorating spleen and tonifying kidney in the treatment of metastatic triple negative breast cancer (TNBC) patients with liver stagnation.Methods A total of 79 TNBC patients with visceral metastasis after postoperative chemotherapy who were admitted to the Department of Oncology of Liuzhou Hospital of Traditional Chinese Medicine from May 2010 to September 2013 were randomly divided into two groups.The control group (n=40) was given GT chemotherapy (Taxol and Gemcitabine),and the treatment group (n=39) was given combined chemotherapy with TCM for smoothing liver,invigorating spleen and tonifying kidney.The clinical efficacy and side effect of the two groups were evaluated.Results Both groups were at least given two cycles of chemotherapy.In the control group,2 cases (5.0%) achieved complete remission,16 cases (40.0%) achieved partial remission,13 cases (32.5%) were stable and 9 cases (22.5%) progressed;while in the treatment group,one case (2.6%) achieved complete remission,15 cases (38.5%) achieved partial remission,16 cases (41.0%) were stable and 7 cases(17.9%) progressed.The clinical efficacy of the two groups showed no statistically significant differences (Z=-0.120,P=0.904).The two groups were followed up for an average of 8.5 months,and the progression free survival (PFS) of the control group and treatment group was(5.7±0.5) months and(7.5±0.7) months,respectively,and the median PFS was (5.2±0.3) months and (6.5±0.6) months,respectively.The PFS of the two groups showed statistically significant differences (χ2=4.627,P=0.031).The occurrence degree of myelosuppression of the two groups showed no statistically significant differences (Z=0.672,P=0.501).The gastrointestinal side effect of the two groups showed statistically significant differences (Z=1.995,P=0.046).Conclusion TCM for smoothing liver,invigorating spleen and tonifying kidney can prolong PFS of metastatic TNBC patients with liver stagnation,and can alleviate gastrointestinal side effect caused by chemotherapy.
Breast neoplasms;Soothing liver;Strengthening spleen;Antineoplastic combined chemotherapy protocols;Progression free survival
545001 广西柳州市中医院 广西中医药大学第三附属医院肿瘤一科(王志光,广州中医药大学同等学历申请博士学位人员);广州中医药大学(林丽珠)
王志光,545001 广西柳州市中医院 广西中医药大学第三附属医院肿瘤一科;E-mail:a1860@126.com
R 737.9
A
10.3969/j.issn.1007-9572.2015.06.003
2014-11-21;
2015-01-20)
