急性淋巴细胞白血病行大剂量甲氨蝶呤时血药浓度监测的临床意义
2015-02-16陈列光陆滢
陈列光 陆滢
宁波市鄞州人民医院血液科,浙江宁波315100
急性淋巴细胞白血病行大剂量甲氨蝶呤时血药浓度监测的临床意义
陈列光 陆滢▲
宁波市鄞州人民医院血液科,浙江宁波315100
目的探讨大剂量甲氨蝶呤治疗急性淋巴细胞白血病时血药浓度监测的临床意义。方法选取46例急性淋巴细胞白血病患者,使用大剂量甲氨蝶呤后,通过酶放大免疫法来测定其血药浓度,观察儿童与成人不良反应的发生情况,并分析其区别。结果儿童组的胃肠道反应和感染发生率较成人组高,差异有统计学意义(P<0.05)。CMTX48 h≤0.4 μmol/L组患者的骨髓抑制和胃肠道反应发生率低于CMTX48 h≥0.4 μmol/L组,差异有统计学意义(P<0.05)。结论MTX的不良反应主要为骨髓抑制、胃肠道反应和黏膜损伤。儿童胃肠道反应和感染的发生率高于成人。通过监测MTX血药浓度有助于及时适量调整甲酰四氢叶酸钙解救量,确保用药安全。
甲氨蝶呤;酶放大免疫法;血药浓度;不良反应
甲氨蝶呤(methotrexate,MTX)为抗叶酸类抗癌药物,目前是临床治疗急性淋巴细胞白血病(acute lymphoblastic leukemia,ALL)的常用药物之一[1,2]。有研究表明,MTX血药浓度越高,疗效越好。但由于MTX毒性反应大,选择性极差,常产生骨髓抑制、胃肠道反应及黏膜损伤等不良反应[3,4]。因此及时监测MTX血药浓度,根据MTX的血药浓度及时调整CF的解救量与时间来确保临床用药的安全具有十分重要意义[5]。本研究通过对ALL患者行大剂量MTX治疗后血药浓度的监测,来分析其浓度与不良反应率的联系,并分析儿童与成年人不良反应的区别。
1 资料与方法
1.1 一般资料
选取我院2012年5月~2014年5月治疗的46例急性淋巴细胞白血病患者,所有患者均经骨髓检查确诊,排除具有严重器质性病变的患者。其中儿童(≤14岁)27例,平均年龄(8.2±3.5)岁,平均身高(121.91± 27.19)cm,平均体重(32.26±4.61)kg,应用MTX剂量(3.12±0.97)g;成人(>14岁)19例,平均年龄(32.5±9.2)岁,平均身高(167.43±31.23)cm,平均体重(56.65±12.61)kg,应用MTX剂量(3.02±1.27)g。
1.2 给药剂量与方法
所有患者均在治疗前接受相关检查,粒细胞计数>1.5×109/L,白细胞计数≥3×109/L,血小板>100×109/L,肝肾功能的各项检查都无异常。首先用1/10的MTX(江苏恒瑞医药股份有限公司,规格0.1g,1g)剂量作为突击剂量在30 min内快速由静脉滴完,余量在23.5 h内缓慢滴入。开始滴注MTX 24~48 h后,对患者应用亚叶酸钙(CF)(江苏恒瑞医药股份有限公司,规格10 mL,1 g)静脉注射解救,15 mg/m2,6 h/次。除首次外,其余治疗选择肌注治疗,直到血浆MTX浓度低于0.1 μmol/L。治疗后需对出现的各种症状对症治疗。46例患者共接受治疗144次,其中儿童100例次,成人44例次。
1.3 血药浓度及不良反应监测
MTX滴注完记为0时,以后每24小时采集肘静脉血2 mL左右,3500 r/min离心4 min分离待测血浆,采用酶放大免疫测定法测定血浆MTX的浓度直到血药浓度低于0.1 μmol/L(线性范围为0.1~2 μmol/L)。观察治疗过程中患者出现的不良反应。本研究累计对血MTX浓度监测281次,其中48 h监测有92次,CMTX≤0.4 μmol/L 71次(A组),CMTX>0.4 μmol/L 21次(B组)。
1.4 统计学方法
采用SPSS18.0统计学软件进行分析处理,计量资料采用t检验,计数资料采用χ2检验或确切概率法。P<0.05为差异有统计学意义。
2 结果
2.1 血药浓度监测结果
给药后24 h、48 h及72 h,儿童组的与成人组的MTX血药浓度比较,差异无统计学意义(P>0.05),见表1。
表1 血药浓度监测结果(±s,μmol/L)
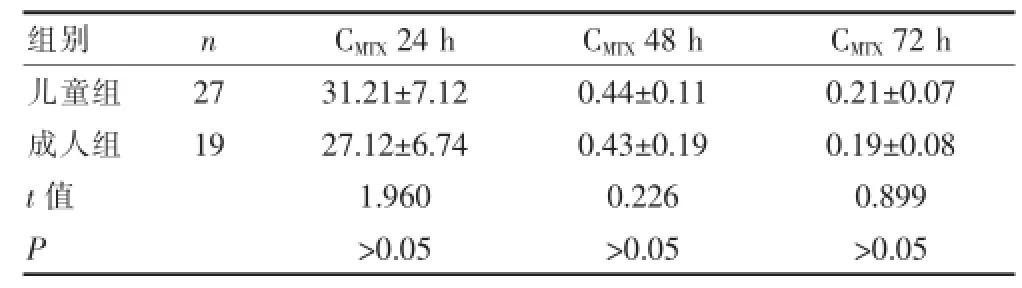
表1 血药浓度监测结果(±s,μmol/L)
组别n CMTX2 4 h CMTX4 8 h CMTX7 2 h儿童组成人组t值P 2 7 1 9 3 1 . 2 1 ± 7 . 1 2 2 7 . 1 2 ± 6 . 7 4 1 . 9 6 0 > 0 . 0 5 0 . 4 4 ± 0 . 1 1 0 . 4 3 ± 0 . 1 9 0 . 2 2 6 > 0 . 0 5 0 . 2 1 ± 0 . 0 7 0 . 1 9 ± 0 . 0 8 0 . 8 9 9 > 0 . 0 5
2.2 不良反应发生情况
对ALL患者进行治疗后,部分患者出现不良反应,主要为骨髓抑制、胃肠道反应、黏膜损伤等。具体情况如下:骨髓抑制72例次(50.00%);腹泻和呕吐等胃肠道不良反应37例次(25.69%);口腔溃疡和肛周糜烂等黏膜损伤26例次;感染(呼吸道感染)17例次;过敏反应(皮肤瘙痒、皮疹)8例次;肝功能异常(ALT升高)6例次;肾功能异常(尿素氮升高)2例次。临床上通过各种对症治疗,不良反应状况均在1~2周内消失。
2.3 儿童组与成人组不良反应比较
儿童组胃肠道反应、感染的发生率均高于成人组,差异均有统计学意义(P<0.01)。其他不良反应两组间差异无统计学意义(P>0.05),见表2。
2.4 不同血药浓度不良反应发生率情况比较
B组的骨髓抑制和胃肠道反应发生率高于A组(P<0.05或P<0.01),其他不良反应两组比较差异无统计学意义(P>0.05),见表3。
3 讨论
甲氨蝶呤能抑制叶酸代谢途径,使二氢叶酸胸腺核苷酸合成酶和亚甲基四氢叶酸还原酶的活性降低,二氢叶酸还原受阻,造成胸腺嘧啶和嘌呤合成障碍,DNA合成缺陷,从而对肿瘤细胞产生明显的抑制作用[6-8]。亚叶酸钙(CF)可以在体内转化为四氢叶酸,从而减轻MTX对机体的影响,起到解救作用[9]。
3.1 儿童与成年不良反应发生率的比较
本次研究显示应用MTX治疗后出现的不良反应主要为骨髓抑制、胃肠道反应、黏膜损伤。由于手术过程中对患者进行了充分水化、碱化尿液,所以肾损伤在本次研究中出现较少。与成人组相比,儿童组胃肠道反应和感染的发生率均明显高于成人组,差异有统计学意义,提示在对患者的治疗过程中应注意儿童胃肠道和感染发生的预防。有研究表明,可能与CF解救时间的不同有关[10]。

表2 不同年龄组患者不良反应情况比较[n(%)]

表3 不同血药浓度患者不良反应情况比较[n(%)]
3.2 不同血药浓度不良反应发生率情况比较
MTX不良反应发生率和损害程度与MTX的血药浓度和持续时间相关[11]。通过血药浓度监测,可发现MTX在体内是否发生排泄延迟,从而为后续的治疗与解救提供参考。本次研究表明CMTX48 h≤0.4 μmol/L患者骨髓抑制与胃肠道反应的发生率明显低于CMTX48 h>0.4 μmol/L组,差异有统计学意义。因此通过监测MTX的血药浓度可以避免严重不良反应的发生,确保用药安全。
临床上认为MTX中毒浓度为CMTX48 h≥1 μmol/L或CMTX72 h≥0.1 μmol/L[12]。本研究所用的酶放大免疫法操作简单、快捷、自动化程度高,适合广大临床需求。临床医生在实际工作中,通过监测MTX的血药浓度,利用药动学原理及方法,为患者提供个性化的药学服务,避免或减少毒副作用的发生,保障临床用药的安全。
[1]Fakhry C,Baiai G,Aygun N,et al.Long-term survival of a patient with leptomeningeal involvement by nasopharyngeal carcinoma after treatment with high-dose intravenous methotrexate[J].Head Neck,2012,34(2):296-300.
[2]王平,李艳玲,曹志新.大剂量甲氨蝶呤治疗急性淋巴细胞白血病的不良反应及护理对策[J].中国肿瘤临床与康复,2013,12(5):527-529.
[3]牛晓强,马军.大剂量甲氨蝶呤治疗急性淋巴细胞白血病血药浓度监测及毒性反应观察[J].中国药物与临床,2013,13(4):17-22.
[4]Csordas K,Heqyi M,Eipel OT,et al.Comparison of pharmacokinetics and toxicity after high-dose methotrexate treatments in children with acute lymphoblastic leukemia[J]. Anti-Cancer Drugs,2013,24(2):189-197.
[5]顾敏,李爽,郝良纯,等.大剂量甲氨蝶呤治疗儿童急性淋巴细胞白血病的血药浓度及影响因素分析[J].中国医科大学学报,2013,42(6):22-24.
[6]Scott JR,Ward DA,Crews KR,et al.Hypersensitivity reaction to high-dose methotrexate and successful rechallenge in a pediatric patient with osteosarcoma[J].Pediatric Blood&Cancer,2014,61(2):373-375.
[7]Chan AJ,Rajakumar I.High-dose methotrexate in adult oncology patients:A case-control study assessing the risk association between drug interactions and methotrexate toxicity[J].Journal of Oncology Pharmacy Practice,2014,20(2):93-99.
[8]徐明,许宋锋,于秀淳.骨肉瘤不含大剂量甲氨蝶呤新辅助化疗的疗效观察[J].中华肿瘤防治杂志,2015,7(2):21-23.
[9]Purizaca J,Meza I,Pelayo R.Early lymphoid development and microenvironmental cues in B-cell acute lymphoblastic leukemia[J].Arch Med Res,2012,43(2):89-101.
[10]Corporation HP.Treatment of recurrent posttransplant lymphoproliferative disorder of the central nervous system with high-dose methotrexate[J].Case Rep Transplant,2013,43(2):91-94.
[11]田飞,王燕青,白晓楠,等.大剂量甲氨蝶呤治疗淋巴瘤致急性肾衰竭1例急救护理[J].齐鲁护理杂志,2014,10(19):15-17.
[12]王捷,王建华,赵军,等.SLC19A1遗传多态性与大剂量甲氨蝶呤化疗不良反应相关性的研究[J].中国临床药理学杂志,2013,29(6):406-409.
Clinical significance of plasma concentration after high-doses methotrexate in the treatment of acute lymphoblastic leukemia
CHEN LieguangLU Ying
Department of Hematology,Yinzhou People's Hospital of Ningbo City,Ningbo315100,China
Objective To investigate the clinical significance of plasma concentration monitoring after high-doses of methotrexate in the treatment of acute lymphoblastic leukemia and lymphoma.Methods The plasma concentration of 46 patients with acute lymphoblastic leukemia were measured by an enzyme multiplied immunoassay technique.Their adverse reaction were observed.Results The incidence of gastrointestinal reaction and infection were significantly less in adults than that in children(P<0.05).Meanwhile,the incidence of myelosuppression and gastrointestinal reaction were significantly less in group with CMTX48 h≤0.4 μmol/L than that in group with CMTX48 h>0.4 μmol/L(P<0.05).Conclusion The adverse reactions of high-doses of methotrexate were mainly the gastrointestinal reaction,myelosuppression and mucosa injury.The incidence of gastrointestinal reaction and infection were less in adults than in children.The monitoring of concentration of MTX in plasma can contribute to appropriately adjust the use of CF and ensure the security and effect of MTX.
Methotrexate;EMIT;Plasma concentration;Adverse reactions
R965
A
1673-9701(2015)24-0005-03
2015-04-16)
浙江省宁波市自然科学基金项目(2014A610232)
▲通讯作者
