匹多莫德联合氯雷他定对螨过敏性哮喘患儿的长期疗效观察
2015-01-18吴杰妍广州市荔湾区芳村中医医院儿科广州510361
吴杰妍(广州市荔湾区芳村中医医院儿科,广州 510361)
匹多莫德联合氯雷他定对螨过敏性哮喘患儿的长期疗效观察
吴杰妍(广州市荔湾区芳村中医医院儿科,广州 510361)
目的 观察匹多莫德联合氯雷他定对螨过敏性哮喘患儿的长期疗效。方法 选择螨过敏性哮喘患儿104例作为研究对象。根据数字表法随机均分成观察组和对照组。2组均予以抗炎、平喘等常规治疗,服用氯雷他定;观察组在此基础上再加用匹多莫德。随访1年,对比2组长期疗效、2组血氧饱和度(SaO2)、第1秒用力呼气量与用力肺活量比值(FEV1/FVC)及最大呼气流量(PEF)以及2组不良反应。结果 观察组的总有效率为98.08%(51/52),显著高于对照组的84.62%(44/52),差异有统计学意义。2组治疗前的SaO2、FEV1/FVC及PEF相比,差异无统计学意义。治疗后1年观察组的SaO2、FEV1/FVC及PEF均显著高于对照组的水平,差异均有统计学意义。观察组的不良反应总发生率与对照组相比,差异无统计学意义。结论 将匹多莫德与氯雷他定联合治疗螨过敏性哮喘,具有较好的长期疗效,且可使患者的喘息症状得到明显控制,安全性较高。
匹多莫德;氯雷他定;螨过敏性哮喘
居室环境内的尘螨通常是导致螨过敏性哮喘的一类重要过敏原。大多数哮喘患者均对尘螨过敏,而哮喘症状的严重程度和接触尘螨的密度与时间均有明显的相关性[1]。本文将匹多莫德与氯雷他定联用治疗螨过敏性哮喘,获得了良好的长期疗效。
1 资料和方法
1.1 临床资料 选择2012年4月~2013年4月在我院接受治疗的螨过敏性哮喘患儿104例作为研究对象,男59例,女45例,年龄2~10岁,平均年龄为5.4±3.2岁。纳入标准[2]:(1)所有患儿均经过粉尘螨皮试浸液检测为阳性;(2)患儿症状均符合《支气管哮喘防治指南》中的诊断标准;(3)年龄≤10岁者。排除标准[3]:(1)有急、慢性感染性病症者;(2)有心、肝、肾等器官功能不全者;(3)有营养不良或腹泻者;(4)年龄>10岁者。根据数字表法随机分成观察组和对照组,每组各52例。其中观察组中男30例,女22例,年龄2~9岁,平均年龄为5.2±1.8岁;对照组中男29例,女23例,年龄2~10岁,平均年龄为5.5±2.6岁。2组在性别和年龄等方面相比,差异无统计学意义(P>0.05),具有可比性。
1.2 研究方法 2组均常规予以抗炎、平喘等常规治疗,服用氯雷他定(10mg/片,江苏正大天晴制药公司),体质量>30kg者,1日1次,1次1片。体质量≤30kg者,1日1次,1次半片。观察组在此基础上另服用匹多莫德(0.4g,浙江仙琚药业公司),1日2次,1次1袋。2组均治疗1个月。
1.3 观察指标 对比2组长期疗效,2组血氧饱和度(SaO2)、第一秒用力呼气量与用力肺活量比值(FEV1/FVC)、最大呼气流量(PEF)以及2组不良反应。
1.4 疗效评价 疗效评价标准[4]。显效:患儿呼吸困难及咳嗽等症状均完全缓解,且哮鸣音已全部消失,经血气检查显示为正常。有效:患儿呼吸困难及咳嗽等症状有所缓解,但哮鸣音仍存在,经血气检查显示好转,却未达到正常范围。无效:患儿的临床症状并无改善,或者反而加重。将显效及有效者的比例之和记为总有效率。
1.5 统计学方法 采用SPSS 13.0统计软件分析,数据比较采用χ2检验,计量数据以x±s表示,实施t检验。
2 结果
2.1 2组长期疗效比较 观察组的总有效率为98.08%(51∶52),显著高于对照组的84.62%(44∶52),差异有统计学意义(P<0.05)。见表1。

表1 2组长期疗效比较Tab.1 Comparison of long term effect of the two groups
2.2 2组SaO2、FEV1/FVC及PEF比较 2组治疗前的SaO2、FEV1/FVC及PEF比较,差异无统计学意义(P>0.05)。治疗后1年观察组的SaO2、FEV1/FVC及PEF均显著高于对照组的水平,差异均有统计学意义(均P<0.05)。见表2。
2.3 2组不良反应比较 观察组的不良反应总发生率与对照组相比,差异无统计学意义(P>0.05)。见表3。
表2 2组SaO2、FEV1/FVC及PEF对比Tab.2 Comparison of SaO2,FEV1/FVC and PEF of the two groups(n=52,±s)
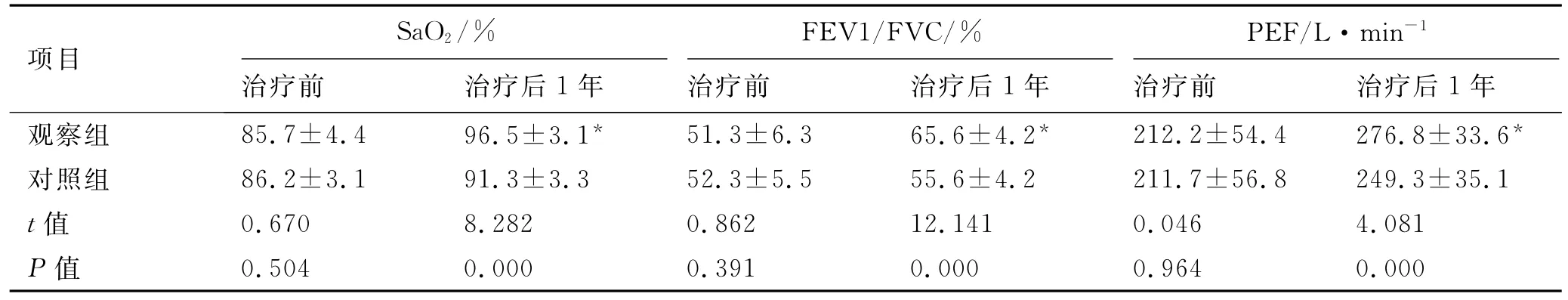
表2 2组SaO2、FEV1/FVC及PEF对比Tab.2 Comparison of SaO2,FEV1/FVC and PEF of the two groups(n=52,±s)
注:与对照组相比*P<0.05。
项目 SaO2/%治疗前 治疗后1年FEV1/FVC/%治疗前 治疗后1年PEF/L·min-1治疗前 治疗后1年观察组 85.7±4.4 96.5±3.1* 51.3±6.3 65.6±4.2* 212.2±54.4 276.8±33.6*对照组 86.2±3.1 91.3±3.3 52.3±5.5 55.6±4.2 211.7±56.8 249.3±35.1 t值 0.670 8.282 0.862 12.141 0.046 4.081 P值0.504 0.000 0.391 0.000 0.964 0.000

表3 2组不良反应比较Tab.3 Comparison of adverse reaction of the two groups(n=52)
3 讨论
据病理学研究显示[5],哮喘病理学基础为气道慢性与非特异性炎症引发的气道高反应,多类变应原均可诱发哮喘疾病的发作。有报道[6],>80%的哮喘患儿可因粉尘螨过敏。近年来发现有哮喘症状的患儿大都存在着T细胞的免疫功能异常,使得调节患儿免疫功能成为了当前较为可行的一种过敏性哮喘方向[7]。鉴于此,本文通过将匹多莫德与氯雷他定联用治疗螨过敏性哮喘,旨在分析此种联合治疗方案的长期疗效。
本文研究显示,观察组总有效率显著高于对照组,且2组治疗前的SaO2、FEV1/FVC及PEF相比,差异不显著。治疗后1年观察组的SaO2、FEV1/FVC及PEF均显著高于对照组的水平,表明治疗螨过敏性哮喘时,使用匹多莫德联合氯雷他定可获得更佳疗效[8]。氯雷他定作为非中枢神经系统相应镇静性组胺拮抗剂,可发挥出高效和选择性地拮抗机体外周H1受体的效果[9]。匹多莫德是免疫调节剂,可刺激患儿机体非特异性自然免疫和细胞免疫以及体液免疫调节有关免疫应答。匹多莫德还可调节患儿T细胞亚群,增强免疫功能,降低哮喘复发次数。氯雷他定与匹多莫德联合应用,针对性治疗方向也不同,因此发挥出较好的协同增效作用。Gaffin JM等[10]报道,匹多莫德能够快速提升吞噬细胞的活性,进而激活NK细胞,强化机体免疫作用,还可加速CD4+T细胞成熟,优化CD4+/CD8+比例,最终达到维持机体Th1/Th2免疫稳态的平衡。刘洪泱等[11]报道,増用匹多莫德治疗过敏性哮喘,总有效率为96.5%,本文为98.0%。此外,本文研究显示,观察组的不良反应总发生率与对照组相比,差异不显著,表明将匹多莫德与氯雷他定联合治疗螨过敏性哮喘,安全性较高。观察组共有5例患儿有不良反应发生,但停药后均恢复正常。Tay HL等[12]亦有类似的报道可进行佐证。
综上所述,将匹多莫德与氯雷他定联合治疗螨过敏性哮喘,具有较好的长期疗效,且可使患者的喘息症状得到明显控制,安全性较高,可推荐临床上应用。
[1]唐利群.孟鲁司特联合氨溴索雾化防治儿童支气管哮喘[J].西北药学杂志,2010,25(1):49-50.
[2]Asai-Tajiri Y,Matsumoto K,Fukuyama S,et al.Small interfering RNA against CD86during allergen challenge blocks experimental allergic asthma[J].Respir Res,2014,15(1):132-133.
[3]陈潮青,罗学虹,陈宜升,等.匹多莫德联合孟鲁司特治疗小儿反复发作性哮喘的疗效观察[J].中华全科医学,2013,11(8):1204-1205.
[4]Ciepiela O,Zawadzka-Krajewska A,Kotula I,et al.The influence of sublingual immunotherapy on several parameters of immunological response in children suffering from atopic asthma and allergic rhinitis depending on asthma features[J].Pneumonol Alergol Pol,2014,82(6):503-510.
[5]任麦青.氟替卡松气雾剂联合孟鲁斯特治疗儿童支气管哮喘的临床观察[J].西北药学杂志,2014,29(1):75-76.
[6]Wu W,Chen H,Li Y M,et al.Intranasal sirna targeting c-kit reduces airway inflammation in experimental allergic asthma[J].Int J Clin Exp Pathol,2014,7(9):5505-5514.
[7]范飞,鲍一笑,华丽,等.婴幼儿喘息急性期联合降阶梯治疗方案中氯雷他定的作用[J].中华实用儿科临床杂志,2013,28(4):274-277.
[8]Mehta P.Allergic rhinitis and bronchial asthma[J].J Assoc Physicians India,2014,62(3):23-26.
[9]张德信,董蕾,孙秀珍,等.成人过敏性难治性支气管哮喘患者血清维生素D水平的相关临床研究[J].中华哮喘杂志:电子版,2013,7(4):12-15.
[10]Gaffin J M,Kanchongkittiphon W,Phipatanakul W,et al.Reprint of:Perinatal and early childhood environ-mental factors influencing allergic asthma immunopathogenesis[J].Int Immunopharmacol,2014,7(14):380-384.
[11]刘洪泱,谢林艳,周林福,等.支气管哮喘变应原特异性免疫治疗研究进展[J].中华结核和呼吸杂志,2013,36(6):450-454.
[12]Tay H L,Plank M,Collison A,et al.MicroRNA:Potential biomarkers and therapeutic targets for allergic asthma[J].Ann Med,2014,13(1):1-7.
Long-term outcomes observation of pidotimod combined with loratadine in the treatment of children with mite allergic asthma
WU Jieyan(Department of Pediatirics,Liwan District Fangcun Hospital of Traditional Chinese Medicine,Guangzhou 510361,China)
Objective To observe the long-term outcomes of pidotimod combined with loratadine in the treatment of children with mite allergic asthma.Methods Children with mite allergic asthma 104cases were selected as the research objects.According to the figures,the cases were randomly divided into observation group and control group.Conventional treatment for the two groups were routinely anti-inflammatory,and anti-asthma.In the control group foratadine was taken.Based on this in the observation group pidotimod was administered 1year of follow-up,the two groups of long-term effect and the adverse reactions were compared.Results The total effective rate of observation group was 98.08%(51/52),significantly higher than the control group of 84.62%(44/52).1year after the treatment of the observation group′s SaO2,FEV1/FVC and PEF were significantly higher than the level of the control group.The total incidence of adverse reaction rate of the observation group compared with the control group,had no significant difference.Conclusion Pidotimod combined with loratadine in mite allergic asthma,with good long-term effects,and can make breathing symptoms be controlled with high safety.
pidotimod;loratadine;mites allergic asthma
10.3969/j.issn.1004-2407.2015.04.025
R985
A
1004-2407(2015)04-0405-04
2014-12-15)
