盐酸小檗碱明胶纳米粒的制备
2015-01-18李小第张海龙黄小艳西安交通大学医学部第二附属医院药剂科西安70004西安交通大学药学院西安7006
李小第,张海龙,黄小艳,王 妮,鲍 和,高 阳*(.西安交通大学医学部第二附属医院药剂科,西安 70004;.西安交通大学药学院,西安 7006)
盐酸小檗碱明胶纳米粒的制备
李小第1,张海龙2,黄小艳2,王 妮2,鲍 和1,高 阳2*(1.西安交通大学医学部第二附属医院药剂科,西安 710004;2.西安交通大学药学院,西安 710061)
目的 制备盐酸小檗碱明胶纳米粒。方法 以明胶为囊材,采用单凝聚法制备盐酸小檗碱明胶纳米粒,并通过单因素实验优化其最佳制备工艺。结果 盐酸小檗碱纳米粒最佳制备工艺条件为:明胶质量浓度为10g·L-1,凝聚剂体积分数为81.25%,滴定速度为2mL·min-1,搅拌速度为600r·min-1,投料比(盐酸小檗碱与明胶的质量比)为2∶4,交联剂体积分数为10%。结论 该制备工艺简便可行,制得的盐酸小檗碱纳米粒有较明显的缓释效果。
盐酸小檗碱;明胶;纳米粒
盐酸小檗碱俗称黄连素,是从黄连、黄柏等植物中提取出的一种异喹啉类生物碱。其抗菌谱广,对金黄色葡萄球菌、溶血性链球菌、志贺氏痢疾杆菌、弗氏和淋球菌均有抗菌作用,还有增强白血球的吞噬作用,临床上主要用于治疗肠道感染、腹泻。近年来有研究表明,盐酸小檗碱具有多种药理学活性,例如对中枢神经系统、糖尿病、心血管系统、肿瘤等都有不同程度的治疗效果,有着十分广阔的应用前景[1]。但盐酸小檗碱溶解度低,易被胃肠道中的黏蛋白吸附[2],最终会导致口服后生物利用度较低,难以达到发挥药理作用的有效浓度。且盐酸小檗碱作为一种季铵盐类,不宜静脉滴注和肌肉注射,否则易引起过敏性休克、药疹等不良反应[3]。因此,盐酸小檗碱在临床上的应用受到限制。
近年来,纳米给药系统越来越受到关注,将药物包裹于纳米粒中,不仅可以调节释药速度,改善药物在体内的分布,提高生物利用度,而且还可以减少毒性和不良反应[4-6]。而明胶是由动物骨头、皮肤和筋腱熬制而成,无毒,生物相容性好,可生物降解[7],且表面存在大量-NH2和-OH,为进一步载药提供了活性位点[8],是一种常用的天然高分子载体材料。因此本实验以明胶为囊材,采用单凝聚法制备盐酸小檗碱明胶纳米粒,通过优化盐酸小檗碱纳米粒的处方及制备条件来获得其最佳制备工艺,再对制得的纳米粒进行表征,最后,对制得的盐酸小檗碱纳米粒的体外释药行为进行了初步考察。
1 仪器与试药
1.1 仪器 DF-101S集热式恒温加热磁力搅拌器(河南省予华仪器有限公司);Malvern Nano-ZS 90型马尔文粒度分布仪(Malvern);KQ5200型超声波清洗机(昆山舒美科技有限公司);AL204电子天平(梅特勒-托利多仪器(上海)有限公司);pH计PB-10(赛多利斯科学仪器(北京)有限公司);
1.2 试药 盐酸小檗碱(西安冠宇生物技术有限公司);明胶(北京寰宇科技有限公司);乙二醛(阿拉丁试剂有限公司,批号A1305107);甘氨酸(阿拉丁试剂有限公司,批号D1307075);无水乙醇(天津市富宇精细化工有限公司,分析纯)。
2 方法
2.1 明胶纳米粒的制备 用双蒸水配制一定质量浓度的明胶水溶液,加热充分溶胀后,用1mol·L-1氢氧化钠溶液调节pH至7.0。精密称取一定量的盐酸小檗碱加入到明胶溶液中,37℃水浴、600 r·min-1磁力搅拌,再超声数分钟后缓慢加入凝聚剂,随后逐滴加入100μL乙二醛溶液(交联剂)交联固化5min,再缓慢加入500μL 15mg·mL-1甘氨酸溶液中和多余的乙二醛。
2.2 盐酸小檗碱标准曲线的绘制
2.2.1 盐酸小檗碱紫外最大吸收波长的确定 用乙醇为溶剂配制适当质量浓度的盐酸小檗碱标准溶液,以空白无水乙醇作为参比,在紫外分光光度计上进行全量程扫描,确定盐酸小檗碱的最大吸收波长。
2.2.2 盐酸小檗碱标准曲线的绘制 精密称取50 mg盐酸小檗碱原药,置于50mL的量瓶中,加入无水乙醇溶解并稀释至刻度,摇匀。准确移取该溶液1 mL,置于10mL量瓶中,用无水乙醇定容,再分别精密吸取0.2,0.3,0.4,0.5,0.6,0.7,0.8,0.9,1.0,1.1和1.2mL,置于10mL量瓶中,加入无水乙醇稀释至刻度,摇匀,即得一系列盐酸小檗碱标准溶液。最后用紫外分光光度计于盐酸小檗碱最大吸收波长处分别测定各盐酸小檗碱标准溶液的吸光度值。
2.3 纳米粒制备工艺的优化 以凝聚剂的种类、搅拌速度、凝聚剂的体积分数、凝聚剂的滴定速度、囊材明胶的质量浓度、投料比(盐酸小檗碱与明胶的质量比)和交联剂乙二醛的体积分数为主要考察因素,如表1所示,以制得的纳米粒溶液乳光强弱、一定时间内体外释放度及平均粒径为评价指标,单因素实验优化盐酸小檗碱明胶纳米粒的制备工艺。

表1 制备盐酸小檗碱明胶纳米粒的影响因素Tab.1 The influence factors of preparation of berberine hydrochloride-loaded gelatin nanoparticles
2.4 盐酸小檗碱明胶纳米粒体外释放行为的考察
采用透析法进行纳米粒体外释放度的研究[9]。分别精密吸取阴性对照组溶液(盐酸小檗碱溶液)、阳性对照组溶液(制备小檗碱纳米粒处方的简单混合)及各条件下制备的盐酸小檗碱明胶纳米粒溶液各1mL,置于预处理过的透析袋中,封好两端后置于盛有50mL释放介质(pH 7.4PBS缓冲溶液)的锥形瓶中,于37℃恒温水浴,以200r·min-1磁力搅拌,分别在不同时间点15,30,60,90,120,150,180,210,240,270,300,330和360min各吸取释放介质1mL,同时向锥形瓶中补充相同体积的PBS缓冲溶液。用紫外分光光度计测定各时间点取出的样品溶液的吸光度,并计算盐酸小檗碱的含量,计算各时间点的累积释放率。计算公式如下:
累积释放率=(透析外液药物总量/纳米粒药物总量)×100%。
2.5 粒径及粒度分布测试 用马尔文激光粒度分析仪测定盐酸小檗碱明胶纳米粒粒径分布。将准备好的待测盐酸小檗碱明胶纳米粒溶液进样,得到纳米粒粒径分布及其平均粒径结果。
3 实验结果
3.1 紫外分光光度法制备盐酸小檗碱标准曲线 扫描结果显示,盐酸小檗碱在340nm处有最大吸收,以不同质量浓度的盐酸小檗碱为横坐标、吸光度为纵坐标绘制标准曲线,得标准曲线方程:Y=0.062 9 X+0.006 4(r=0.999 2,n=3),结果表明,盐酸小檗碱质量浓度在2~12.0μg·mL-1范围内线性关系良好。
3.2 单因素考察法优化盐酸小檗碱明胶纳米粒制备工艺
3.2.1 凝聚剂的影响 采用硫酸钠和乙醇2种不同的凝聚剂,固定其他条件(搅拌速度为600r·min-1,明胶质量浓度为10g·L-1,投料比为2∶4,凝聚剂滴定速度为2mL·min-1,交联剂体积分数为20%),以纳米粒的乳光效果为初步评价指标,考察凝聚剂对纳米粒制备工艺的影响。实验结果发现,硫酸钠作凝聚剂的条件更加苛刻,不易出现纳米粒溶液特有的乳光现象,而乙醇作凝聚剂时,乳光明显。因此,我们选用乙醇作为凝聚剂进行进一步考察。
3.2.2 搅拌速度的影响 采用搅拌速度为200,400和600r·min-1,固定其他条件(凝聚剂体积分数为81.25%,明胶质量浓度为10g·L-1、投料比为2∶4、凝聚剂滴定速度为2mL·min-1、交联剂体积分数为20%),以纳米粒的乳光效果为评价指标,考察转速对纳米粒制备工艺的影响。结果发现,搅拌速度为200r·min-1制备纳米溶液,不易出现乳光,容易产生片状沉淀,搅拌速度为400r·min-1制备的纳米溶液乳光不强烈,常温下放置,容易析出沉淀,而搅拌速度为600r·min-1,制备的纳米溶液乳光状态良好,且较稳定。说明转速越高,凝聚成的纳米粒分散性更好,不容易聚集形成沉淀。而实验中发现搅拌速度大于600r·min-1,溶液容易飞溅,因此,我们选用600r·min-1的搅拌速度进行进一步研究。
3.2.3 凝聚剂(乙醇)体积分数的影响 采用体积分数分别为81.25%和100%的乙醇溶液为凝聚剂,固定其他条件(搅拌速度为600r·min-1,明胶质量浓度为10g·L-1,投料比为2∶4,凝聚剂滴定速度为2 mL·min-1,交联剂体积分数为20%),以一定时间内体外释放度为评价指标,考察凝聚剂体积分数对纳米粒制备工艺的影响。结果显示,体积分数分别为81.25%和100%的乙醇溶液为凝聚剂制备的盐酸小檗碱纳米粒6h累积释放率分别约为81.35%和89.72%,说明凝聚剂体积分数为81.25%的乙醇制得的盐酸小檗碱纳米粒的缓释效果较体积分数100%的乙醇更优,因此,我们选用体积分数为81.25%的乙醇溶液为凝聚剂进行进一步研究。
3.2.4 明胶质量浓度的影响 采用质量浓度分别为10,30和50g·L-1的明胶溶液,固定其他条件(搅拌速度为600r·min-1,凝聚剂体积分数为81.25%,投料比为2∶4,凝聚剂滴定速度为2mL·min-1,交联剂体积分数为20%),以一定时间内体外释放度为评价指标,考察明胶质量浓度对纳米粒制备工艺的影响。结果显示,质量浓度分别为10,30和50g·L-1的明胶溶液制得的盐酸小檗碱纳米粒6h累积释放率分别约为81.35%,85.03%和86.56%。说明随着明胶质量浓度的增加,制得的盐酸小檗碱纳米粒的体外缓释作用随之降低,且以质量浓度为10g·L-1的明胶为囊材制得的纳米粒有较好的缓释效果。因此,选择质量浓度为10g·L-1的明胶进行进一步研究。
3.2.5 投料比(盐酸小檗碱与明胶的质量比)的影响采用投料比分别为1∶4,2∶4和3∶4,固定其他条件(搅拌速度为600r·min-1,凝聚剂体积分数为81.25%,明胶质量浓度为10g·L-1,凝聚剂滴定速度为2mL·min-1,交联剂体积分数为20%),以一定时间内体外释放度为指标,考察投料比对明胶纳米粒制备工艺的影响。结果显示,投料比为1∶4,2∶4和3∶4条件下,制备的盐酸小檗碱纳米粒6h累积释放率分别约为93.16%,81.35%和95.69%。说明投料比为2∶4制得的纳米粒具有更好的缓释效果。因此,我们选用投料比为2∶4进行进一步研究。
3.2.6 凝聚剂滴定速度的影响 凝聚剂滴定速度分别设为1,2和3mL·min-1,固定其他条件(搅拌速度为600r·min-1,凝聚剂体积分数为81.25%,明胶质量浓度为10g·L-1,投料比为2∶4,交联剂体积分数为20%),以一定时间内体外释放度为指标考察凝聚剂滴定速度对纳米粒制备工艺的影响。结果显示,凝聚剂滴定速度为1,2和3mL·min-1制备得到的盐酸小檗碱纳米粒6h累积释放率分别约为91.23%,81.35%和90.78%。说明当凝聚剂滴定速度为2mL·min-1时,明胶纳米粒有较好的缓释效果。
3.2.7 交联剂(乙二醛)体积分数的影响 采用体积分数分别为10%和20%的乙二醛溶液,固定其他条件(搅拌速度为600r·min-1,凝聚剂体积分数为81.25%,明胶质量浓度为10g·L-1,投料比为2∶4,凝聚剂滴定速度为2mL·min-1),以纳米粒的粒径分布及平均粒径为评价指标,考察交联剂的浓度对纳米粒制备工艺的影响。结果显示,交联剂乙二醛体积分数为10%和20%条件下,制得的盐酸小檗碱纳米粒平均粒径分别为209.50和2 053.97nm。说明降低乙二醛溶液体积分数,可大大减小纳米粒的粒径。
3.2.8 最佳工艺的确定 精密称取一定质量明胶加双蒸水配成质量浓度为10g·L-1的明胶溶液,加热充分溶胀后,用1mol·L-1氢氧化钠溶液调节溶液pH至7.0,取2mL质量浓度为10g·L-1的明胶溶液,置于25mL烧杯中,在37℃、600r·min-1的条件下,加入精密称取的一定量盐酸小檗碱(盐酸小檗碱与明胶质量比为2∶4),搅拌数分钟后再超声使其分散均匀。随后逐滴加入8mL体积分数为81.25%的乙醇溶液(滴定速度为2mL·min-1),再逐滴滴加100μL体积分数为10%的乙二醛溶液,交联固化5min,加入15mg·mL-1甘氨酸500μL中和多余的乙二醛。盐酸小檗碱明胶纳米粒制备的最佳工艺条件见表2。
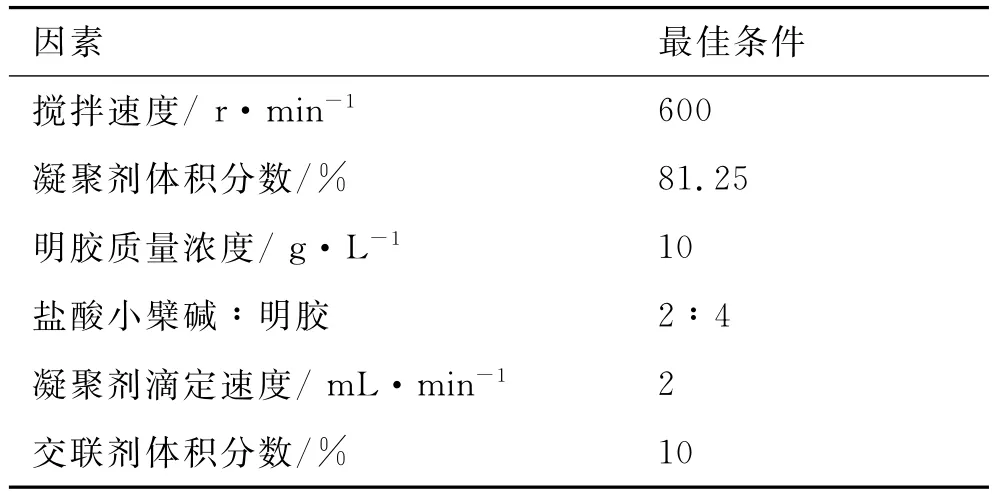
表2 盐酸小檗碱明胶纳米粒制备的最佳工艺条件Tab.2 The optimal conditions for the preparation of berberine hydrochloride-loaded gelatin nanoparticles
3.2.9 体外释药行为的考察 模拟体内条件,以磷酸盐缓冲溶液(pH 7.4)为释放介质,考察阴性对照品溶液、阳性对照溶液在最佳制备工艺条件下制得的盐酸小檗碱明胶纳米粒在6h内的体外释药行为,结果见表3和图1。结果显示,阴性对照组释药较快,在2h药物已基本释放完全,累积释药率达到101.1%±0.65%,而阳性对照组和纳米粒组3h后释放曲线趋于稳定,6h的累积释药率分别为90.65%±0.25%和80.26%±1.26%,经统计学分析,在纳米粒组与阳性对照组的6h累积释放率具有显著性差异。说明优化条件下制得的盐酸小檗碱纳米粒有一定的缓释效果。
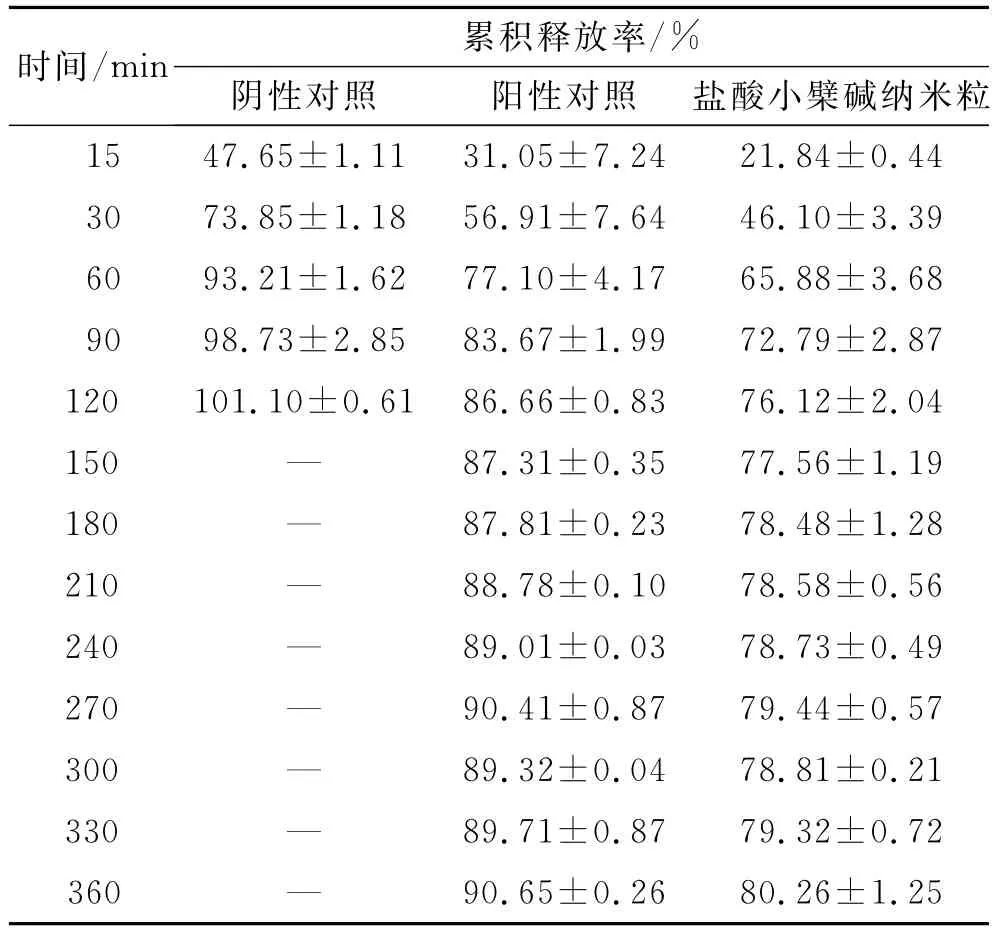
表3 盐酸小檗碱明胶纳米粒体外释放实验结果Tab.3 Results of berberine hydrochloride-loaded gelatin nanoparticles release tests in vitro
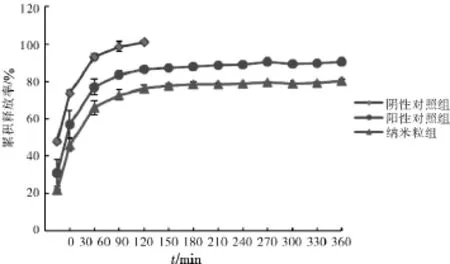
图1 盐酸小檗碱纳米粒体外释放曲线Fig.1 The in vitro release profile of berberine hydrochlorideloaded gelatin nanoparticles
3.2.10 粒径及粒度分布的考察 通过马尔文激光粒度仪测最佳工艺条件下制得的盐酸小檗碱明胶纳米粒的粒径分布,结果如图2。结果表明,制得的盐酸小檗碱纳米粒粒径分布较均匀,平均粒径为209.5nm。
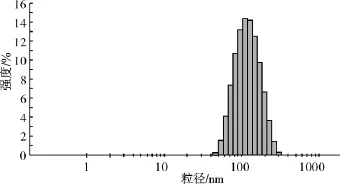
图2 盐酸小檗碱明胶纳米粒粒径分布Fig.2 The size distribution of the berberine hydrochlorideloaded gelatin nanoparticles
4 讨论
单凝聚法是相分离法的一种,是指只用一种高分子作为壁材,将芯材分散到溶有壁材的水溶液中,然后加入凝聚剂(如乙醇、丙酮等强亲水性有机溶剂或无机盐),由于大量水与凝聚剂结合,使壁材的溶解度降低而凝聚成囊[10]。单凝聚法因是在水中成囊,主要适合于难溶性药物的微囊化,但并非所有的不溶于水的药物都适合单凝聚法,该法要求药物难溶于水,但也不能过分疏水,否则仅形成不含药物的空囊。而盐酸小檗碱难溶于冷水,但其在热水中有一定的溶解度,因此盐酸小檗碱适合于单凝聚法。且目前尚没有关于盐酸小檗碱明胶纳米粒的制备的相关报道,为了提高盐酸小檗碱的水溶性及改善其体内外释药行为,本研究采用单凝聚法制备盐酸小檗碱明胶纳米粒,结果表明,优化条件后制得的明胶纳米粒粒径较小,分布均匀,且有较明显的缓释效果。
本实验研究发现,凝聚剂的种类、体积分数、明胶溶液的质量浓度、投料比、凝聚剂的滴定速度、交联剂的体积分数是影响单凝聚法制备盐酸小檗碱明胶纳米粒的主要因素。在考察明胶质量浓度对盐酸小檗碱明胶纳米粒制备影响时发现,当滴加凝聚剂(体积分数为81.25%的乙醇)体积相同时,明胶质量浓度越大,溶液越浑浊,越容易析出絮状沉淀。据文献报道,以乙醇为凝聚剂,采用单凝聚法制备明胶微囊时,明胶质量浓度越高,乙醇用量越少[11]。主要原因可能是由于明胶不溶于乙醇,明胶量越多,越容易析出沉淀。在考察交联剂浓度对盐酸小檗碱纳米粒制备的影响时发现,体积分数为20%的乙二醛制得的纳米粒比体积分数为10%的乙二醛制得的纳米粒粒径大得多。Kommareddy等以明胶为囊材、乙醇为凝聚剂,采用单凝聚法制备硫醇化明胶纳米粒时发现,未添加交联剂制得的纳米粒粒径小于加入交联剂制得的纳米粒[12]。因此,交联剂的浓度可能是影响粒径大小的一个重要因素,交联剂添加过多,会使纳米粒聚集粘连在一起,导致粒径过大。在研究凝聚剂滴定速度对盐酸小檗碱纳米粒制备影响时发现,凝聚剂(体积分数为81.25%的乙醇)的滴定速度对盐酸小檗碱纳米粒的制备有着非常重要的影响。凝聚剂滴定速度过快,纳米粒易粘连成团,容易导致溶液浑浊,滴定速度过慢会使制得的纳米粒溶液乳光不明显,且缓释效果也减弱。并且随着凝聚剂滴加的量逐渐增多,纳米粒溶液乳光越明显,但凝聚剂加入量过多时,溶液中有片状沉淀物析出。因此,在采用该方法制备明胶纳米粒过程中,需精准把控凝聚剂的滴加量和滴定速度。通过实验我们获得了单凝聚法制备盐酸小檗碱的最佳工艺,为以后该制剂的研究奠定了基础。参考文献:
[1]王丽峰,张思培,曹颖,等.盐酸小檗碱鼻用凝胶的研究[J].天津中医药大学学报,2014,33(1):36-38.
[2]陈俊威,谭丽蓉,李伟恩,等.正交实验法优选盐酸小檗碱脂质体制备工艺[J].实用医技杂志,2007,14(14):1868-1870.
[3]林爱华,李鸿燕,刘奕明,等.小檗碱壳聚糖纳米粒的制备及其体外释药特性研究[J].中国药房,2007,18(10):755-757.
[4]李波.阿仑膦酸明胶纳米粒的研制及相关生物学特性的实验研究[D].西安:第四军医大学,2007.
[5]胡亚男,易涛,许岩.载格列吡嗪的聚β-氨基酯纳米粒的制备及含量测定[J].西北药学杂志,2013,28(3):296-299.
[6]李方园,姜永莉,成颖.PLGA纳米粒抗肿瘤药物载体的研究进展.[J].西北药学杂志,2013,28(6):656-660.
[7]余丽丽,李仲谨,朱雷,等.阿司匹林明胶微球的粒径及其影响因素[J].陕西科技大学学报:自然科学版,2008,26(1):46-49.
[8]丁素丽,朱以华,杨晓玲.纳米明胶粒子的制备及其表面改性[J].华东理工大学学报:自然科学版,2004,30(5):523-526.
[9]侯君.盐酸小檗碱固体脂质纳米粒的制备[J].中国药学杂志,2008,38(8):315-317.
[10]王莹.以明胶为基质的苦参碱类磁性微球制备及其特性研究[D].天津:天津大学,2012.
[11]Gu X L,Zhu X,Kong X Z,et al.Comparisons of simple and complex coacervations for preparation of sprayable insect sex pheromone microcapsules and release control of the encapsulated pheromone molecule[J].J Microencapsul,2010,27(4):355-364.
[12]Kommareddy S,Amiji M.Preparation and evaluation of thiol-modified gelatin nanoparticles for intracellular DNA delivery in response to glutathione[J].Bioconjugate Chem,2005,16(6):1423-1432.
Preparation of berberine hydrochloride-loaded gelatin nanoparticles
LI Xiaodi1,ZHANG Hailong2,Huang Xiaoyan2,WANG Ni2,BAO He1,GAO Yang2*(1.Department of Pharmacy,the Second Affiliated Hospital,Health Science Center,Xi′an Jiaotong University,Xi′an 710004,China;2.School of Pharmacy,Xi′an Jiaotong University,Xi′an 710061,China)
Objective To prepare berberine hydrochloride-loaded gelatin nanoparticles.Methods Berberine hydrochloride-loaded gelatin nanoparticles were prepared by using gelatin as coating materials by simple coacervation,and the preparation process was optimized by the single-factor experiments.Results The optimal conditions for the preparation of berberine hydrochloride-loaded gelatin nanoparticles were as follows:the concentration of gelatin,10g·L-1;the volume fraction of coagulant,81.25%;the titration speed of coagulant,2mL·min-1;the stirring speed,600r·min-1;the mass ratio of berberine hydrochloride and gelatin,2∶4;the volume fraction of curing agent,10%.Conclusion The preparation process of the berberine hydrochloride-loaded gelatin nanoparticles was simple and practical,and the gelatin nanoparticles prepared under the optimal conditions had an obvious sustained-release effect.
berberine hydrochloride;gelatin;nanoparticles
10.3969/j.issn.1004-2407.2015.04.021
R944
A
1004-2407(2015)04-0393-05
2014-11-21)
中央高校基本科研业务费专项资金资助项目
李小第,男,主管药师
*通信作者:高阳,女,副教授
