RP-HPLC法测定逍遥丸 (水丸)中芍药苷、苯甲酸和苯甲酰基总苷
2015-01-18李向阳屠万倩杨明杰
李向阳, 高 洁, 屠万倩, 杨明杰
(1.河南省食品药品检验所,河南郑州450003;2.郑州铁路职工技术学院,河南郑州450052;3.河南省中医药研究院,河南郑州450004;4.河南中医学院,河南郑州450008)
RP-HPLC法测定逍遥丸 (水丸)中芍药苷、苯甲酸和苯甲酰基总苷
李向阳1, 高 洁2, 屠万倩3, 杨明杰4
(1.河南省食品药品检验所,河南郑州450003;2.郑州铁路职工技术学院,河南郑州450052;3.河南省中医药研究院,河南郑州450004;4.河南中医学院,河南郑州450008)
目的建立反相高效液相色谱法定量测定8家企业生产的逍遥丸中芍药苷、游离苯甲酸和苯甲酰基总苷。方法逍遥丸甲醇提取液分析采用Agi1ent Ec1ipse XDBC18色谱柱(4.6mm×250mm,5μm),测定芍药苷和苯甲酸的流动相为乙腈 (A)-0.1%磷酸溶液 (B),梯度洗脱;苯甲酰基总苷以总苷碱水解为苯甲酸计算,色谱条件同上。结果芍药苷和游离苯甲酸进样量分别在0.060 8~0.760μg(r=0.999 8)、0.009 6~0.120 0μg(r=0.999 7)范围内与峰面积线性关系良好,平均回收率 (n=6)为97.3% (RSD=2.2%)和97.2% (RSD=2.2%);苯甲酰基总苷在0.020 32~0.304 8μg范围内线性关系良好 (r=0.999 6),平均回收率 (n=6)为96.6% (RSD=2.8%)。结论建议增加苯甲酰基总苷的定量测定可有助于更好地控制逍遥丸的内在质量。
逍遥丸;芍药苷;苯甲酸;苯甲酰基总苷;反相高效液相色谱法
逍遥丸 (水丸)是 《中国药典》2010年版一部收载的常用复方中药,由柴胡、当归、白芍、炒白术、茯苓、炙甘草和薄荷七味中药组成,具有疏肝健脾、养血调经的功效,用于肝郁脾虚所致的郁闷不舒、胸胁胀痛、头晕目眩、食欲减退、月经不调等症的治疗[1]。随着逍遥丸的临床应用和药理作用研究的深入,其主治病症不断扩大,现已被应用于抑郁症、围绝经期综合症、乳腺增生症、慢性肝炎、肠易激综合症、慢性前列腺炎等多种疾病的治疗[2]。
白芍是逍遥丸 (水丸)中起养血柔肝作用的重要药物。白芍主要含有芍药苷、苯甲酰羟基芍药苷、芍药苷元酮、氧化芍药苷、羟基芍药苷、苯甲酰芍药苷、芍药新苷、羟基苯甲酰芍药苷、白芍苷R1、乙酰芍药苷、4-O-没食子酰白芍苷、没食子酰芍药苷、没食子酸及苯甲酸等多种单萜及苷类成分[3-4]。白芍苷类成分具有降脂、抗氧化、抗炎、对肝损伤的保护作用和调节免疫等多种作用,是逍遥丸 (水丸)中的重要活性部位[5-8]。据文献报道白芍的主要质控成分为芍药苷,但研究发现以芍药苷单一指标的质控模式不能准确反映药材内在质量[9],因此,已有研究报道以多种苷类单体为定量指标,控制白芍药材质量[10-11],或根据白芍中苷类成分的化学结构多含有苯甲酰基、可水解为苯甲酸的特性,将白芍饮片及提取物水解后测定总苷的量[12~14]。在现行逍遥丸 (水丸) 的质量标准中用芍药苷作为定量指标,不能全面反映药品的内在质量。考虑到白芍中含有多种苯甲酰基苷类成分,可将其水解为苯甲酸,HPLC法测定水解后苯甲酸的总量,减去游离苯甲酸量,即可反映出药品中苯甲酰基苷类成分的含有量。为准确测定并计算出逍遥丸 (水丸)中苯甲酰基总苷的量,应测定样品中游离的苯甲酸量,同时考虑到白芍中所含游离的苯甲酸是白芍中的无效成分,且会增加肝脏解毒负担,长期摄入一定量后产生不良反应,一般被视为白芍中的有害成分,其在药品中的含有量也应予以检测和控制[15-16]。为确保临床用药的安全有效性,采用反相高效液相色谱法,分别测定了不同生产厂家生产的多批次逍遥丸 (水丸)中芍药苷、游离苯甲酸及苯甲酰基总苷 (以苯甲酸计)的量。
1 仪器与试药
日本岛津LC2010高效液相色谱仪;ASS150超声波提取器 (济宁科特超声电子有限责任公司);LIBROR-160DPT万分之一分析天平(日本岛津);AE240十万分之一分析天平(瑞士METTLER公司)。
芍药苷对照品 (批号110736-201035)、苯甲酸对照品 (批号100419-200801)均购自中国药品生物制品检定所;逍遥丸 (水丸)(山西华康药业股份有限公司,批号分别为20100401、20120101、20120301;亚宝药业大同制药有限公司,批号20100504;四川和润制药有限公司,批号120203;承德颈复康药业集团有限公司,批号100610;赤峰丹龙药业有限公司,批号20100415;山西开元制药有限公司,批号20100101,20100602;宁夏启元国药有限公司,批号090515;广西来宾金钱草药业有限公司,批号090902,090903);甲醇、乙腈为色谱纯 (德国Merck公司),水为超纯水,其余试剂均为分析纯。
2 方法与结果
2.1 芍药苷和游离苯甲酸测定
2.1.1 色谱条件 Agi1ent Ec1ipse XDB C18色谱柱(4.6 mm×250 mm,5μm);流动相为乙腈(A)-0.1%磷酸水溶液 (B),梯度洗脱 (0~15 min,15%A;15~18 min,15%→25%A;18~33 min,25%A);体积流量1.0 mL/min;柱温30℃;进样量10μL;检测波长230 nm。理论塔板数按芍药苷峰计算应不低于3 000。
2.1.2 对照品溶液的制备 精密称取芍药苷和苯甲酸对照品,加甲醇制成每1 mL分别含芍药苷30.4μg、苯甲酸4.8μg的混合溶液,作为对照品溶液。
2.1.3 供试品溶液的制备 取本品适量,研细,取约0.4 g,精密称定,置具塞锥形瓶中,精密加入甲醇50 m L,称定质量,超声处理30 min,放冷,再称定质量,用甲醇补足减失的质量,摇匀,滤过,续滤液用0.45μm微孔滤膜滤过,即得。
2.1.4 阴性对照试验 按处方比例,制备缺白芍阴性对照药,按 “2.1.3”项下方法操作,制备缺白芍阴性样品溶液。分别取混合对照品溶液、供试品溶液及阴性样品溶液各10μL,按 “2.1.1”项下色谱条件进行检测,色谱图见图1。供试品色谱中,可清晰检出芍药苷和苯甲酸色谱峰,缺白芍阴性对照无干扰。
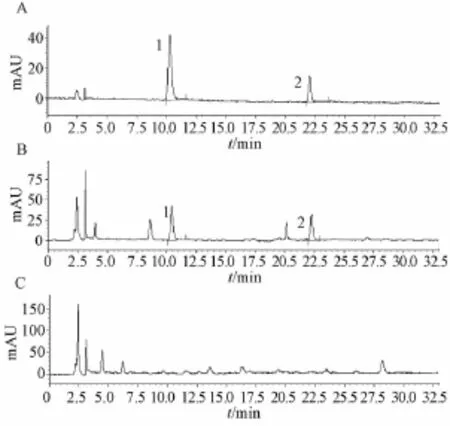
图1 芍药苷和游离苯甲酸测定HPLC色谱图Fig.1 HPLC chromatogram s of paeoniflorin and benzoic acid
2.1.5 线性关系考察 精密吸取 “2.1.2”项下的对照品溶液2、5、10、15、20、25μL,分别注入液相色谱仪,测定。以进样量X(μg)为横坐标,峰面积Y为纵坐标,进行线性回归,得芍药苷和苯甲酸的回归方程分别为Y=1.106×106X+ 1.007×103(r=0.999 8),Y=6.061×106X-5.378×103(r=0.999 7)。结果表明芍药苷在0.060 8~0.760μg、苯甲酸在0.009 6~0.120 0 μg范围内呈良好的线性关系。
2.1.6 精密度试验 吸取同一供试品溶液,按“2.1.1”项下色谱条件连续重复进样6次,测定芍药苷和苯甲酸的峰面积并计算RSD值,结果芍药苷和苯甲酸的RSD值分别为0.85%和1.3%。表明仪器精密度较好。
2.1.7 稳定性试验 取同一供试品溶液,分别于0、2、4、6、8、10 h注入液相色谱仪,测定芍药苷和苯甲酸的峰面积并计算RSD值,结果芍药苷和苯甲酸的RSD值分别为1.1%和1.4%。表明供试品溶液在10 h内稳定。
2.1.8 重复性试验 取逍遥丸 (批号120203),按 “2.1.3”项下方法平行制备6份供试品溶液,按“2.1.1”项下色谱条件进行测定。芍药苷和苯甲酸的平均含有量分别为6.434 mg/g和1.008 mg/g,RSD值分别为1.7%和1.3%,表明本法重复性较好。
2.1.9 加样回收率试验 取已知含有量的逍遥丸(批号120203)0.2 g,精密称定,精密加入芍药苷为0.028 8 mg/mL、苯甲酸为0.004 0 mg/mL的对照品混合溶液50 m L,以下按 “2.1.3”项下操作,制备加样供试品溶液。按 “2.1.1”项下方法测定分析,计算芍药苷和苯甲酸的加样回收率,结果见表1。
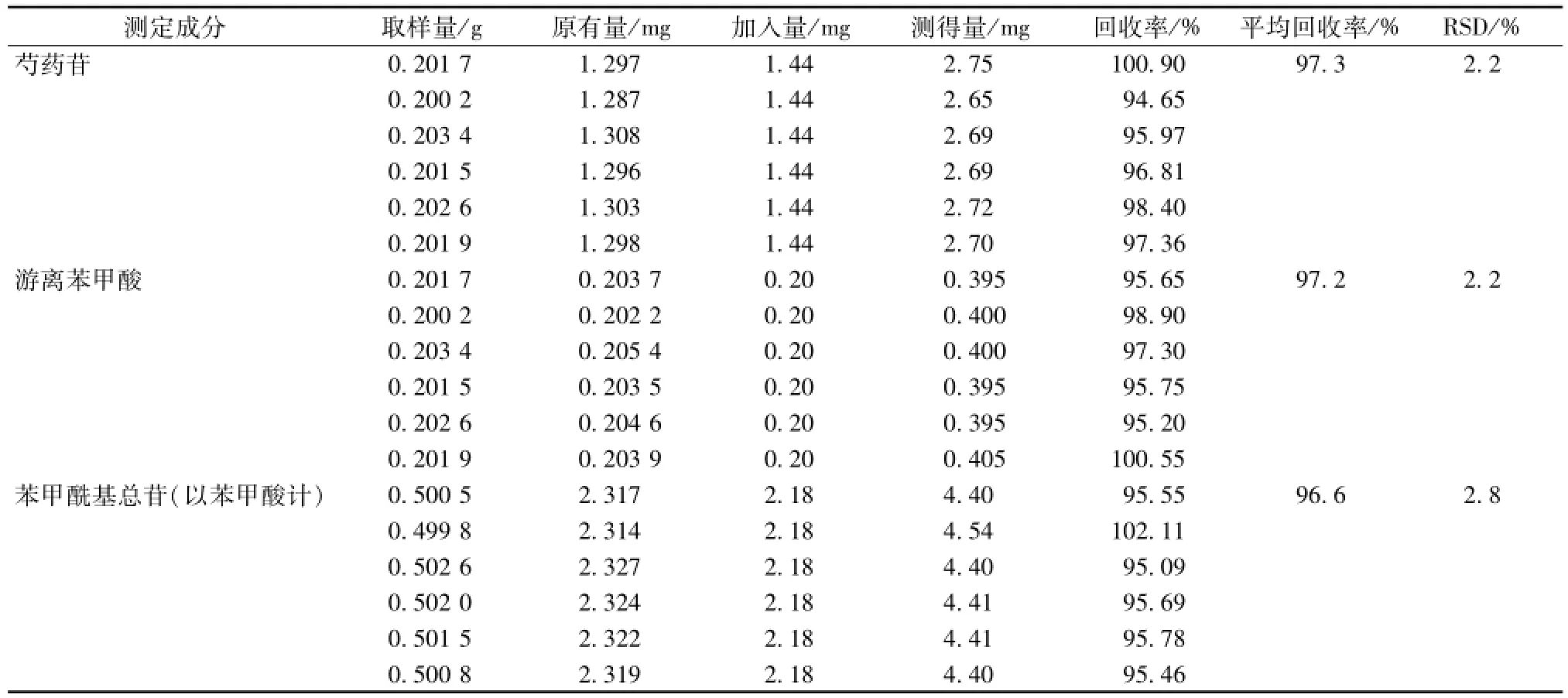
表1 加样回收率试验结果Tab.1 Results of recovery tests
2.1.10 样品测定 取逍遥丸样品,按 “2.1.3”项下方法制备供试品溶液,按 “2.1.1”项下方法测定,结果见表2。

表2 样品测定结果(n=3)Tab.2 Resu lts of determ ination
2.2 苯甲酰基总苷 (以苯甲酸计)测定
2.2.1 色谱条件 同 “2.1.1”项下方法。
2.2.2 对照品溶液的制备 精密称取苯甲酸对照品适量,加甲醇制成每1mL含苯甲酸10.16μg的溶液,作为对照品溶液。
2.2.3 供试品溶液的制备 取本品适量,研细,取约1.0 g,精密称定,置具塞锥形瓶中,精密加入甲醇50 mL,称定质量,超声处理30 min,放冷,再称定质量,用甲醇补足减失的质量,摇匀,滤过,精密吸取续滤液25 mL,水浴蒸干,残渣加1%氢氧化钠溶液10 mL溶解,置具塞试管中,水浴加热1 h,放冷,精密吸取1 mL,置10 mL量瓶中,加流动相8mL,摇匀,用磷酸溶液调节pH为3~4,用流动相稀释至刻度,摇匀,用0.45μm微孔滤膜滤过,即得。
2.2.4 阴性对照试验 按处方比例,制备缺白芍阴性对照样品,按 “2.2.3”项下方法操作,制备缺白芍阴性样品溶液。分别取对照品溶液、供试品溶液及阴性样品溶液各10μL,按 “2.1.1”项下色谱条件进行检测,色谱图见图2。供试品色谱中,可清晰检出苯甲酸色谱峰,缺白芍阴性对照无干扰。
2.2.5 线性关系考察 精密吸取 “2.2.2”项下的对照品溶液2、5、10、15、20、30μL,分别注入液相色谱仪,测定。以进样量X(μg)为横坐标,峰面积Y为纵坐标,进行线性回归,得回归方程Y=5.625×106X-6.171×103(r= 0.999 6)。表明苯甲酸在0.020 32~0.304 8μg范围内呈良好的线性关系。
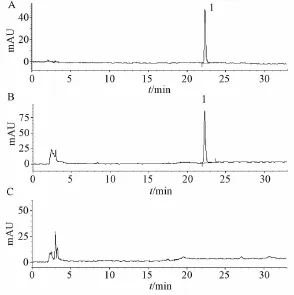
图2 苯甲酰基总苷测定HPLC色谱图Fig.2 HPLC chromatogram s of total benzoy l glucosides
2.2.6 精密度试验 吸取同一供试品溶液,按“2.1.1”项下色谱条件连续重复进样6次,测定苯甲酸的峰面积并计算RSD值,结果苯甲酸的RSD值为1.1%。表明仪器精密度较好。
2.2.7 稳定性试验 取同一供试品溶液,分别于0、2、4、6、8、10 h注入液相色谱仪,测定苯甲酸的峰面积并计算RSD值,结果苯甲酸的RSD值为1.1%。表明供试品溶液在10 h内稳定。
2.2.8 重复性试验 取逍遥丸 (批号120203),按 “2.2.3”项下方法平行制备6份供试品溶液,按 “2.1.1”项下色谱条件进行测定总苯甲酸的量,减去已测定的游离苯甲酸的量,计算苯甲酸的量,即为苯甲酰基总苷 (以苯甲酸计)的量。结果平均含有量和RSD值分别为4.631 mg/g和2.8%,表明本法重复性较好。
2.2.9 加样回收率试验 取已知含有量的逍遥丸(批号120203),取约0.5 g,精密称定,精密加入0.043 6 mg/m L的苯甲酸对照品溶液50 mL,以下按 “2.2.3”项下操作,制备加样供试品溶液。按“2.1.1”项下方法测定分析,计算苯甲酸的加样回收率,结果见表1。
2.2.10 样品测定 取逍遥丸样品,按 “2.2.3”项下方法制备供试品溶液,按 “2.1.1”项下方法测定,测定总苯甲酸量,减去游离苯甲酸量后,计算苯甲酰基总苷 (以苯甲酸计)的量,结果见表2。
3 讨论
3.1 测定指标的确定 逍遥丸 (水丸)由柴胡、白芍等七味药制成,现行质量标准中仅以白芍中的芍药苷单体成分为指标进行定量控制,显然不够科学,不能全面反映药品内在质量。考虑到白芍中含有多种苯甲酰基苷类成分,是逍遥丸 (水丸)中重要的生物活性成分,将逍遥丸水解后测定苯甲酸总量,扣除游离苯甲酸量,以反映药物中苯甲酰基总苷的量,结合芍药苷单体的测定,可以更好地控制药品中白芍苷类成分的量。另外,由测定结果可知,多厂家生产的逍遥丸 (水丸)中可检出具有毒副作用的游离苯甲酸,为确保临床用药的安全性,应在逍遥丸 (水丸)质量标准中增加相应的检测方法,控制苯甲酸的量。因此,本实验测定了逍遥丸 (水丸)中芍药苷、游离苯甲酸和苯甲酰基总苷 (以苯甲酸计)的量。
3.2 流动相的优选 据参考文献,采用HPLC法测定总苯甲酸、游离苯甲酸和芍药苷含有量。在试验中,摸索了流动相配比,为简化实验操作,用甲醇超声处理供试品,采用梯度洗脱法同时测定了供试品中的芍药苷和游离苯甲酸;样品水解后,采用相同的色谱条件测定苯甲酸总量。按照文中方法,待测成分均峰形对称,与相邻峰可达较好的分离度,确保了测定的准确。
3.3 供试品溶液的制备 根据芍药苷和游离苯甲酸的理化性质,用甲醇超声提取制备供试品溶液。在实验中,分别对超声时间、甲醇加入量等因素进行了考察和比较,根据实验结果,确定了芍药苷和游离苯甲酸测定的供试品溶液的制备方法。根据苯甲酰基总苷的理化性质和化学结构特点,采用甲醇超声提取,碱水加热水解的方法制备总苷中苯甲酸测定用供试品溶液。在实验中,分别比较了氢氧化钠溶液的浓度、加入量、加热水解时间等参数,根据实验结果,确定了样品中苯甲酰基总苷供试品溶液的制备方法。
3.4 小结 本实验采用高效液相色谱法测定了8个厂家生产的12批次逍遥丸 (水丸)中芍药苷、苯甲酸和苯甲酰基总苷 (以苯甲酸计)的量,结果所有批次样品中芍药苷含有量均符合 《中国药典》2010年版一部逍遥丸 (水丸)项下芍药苷量不得低于2.5 mg/g的有关规定。除2批次样品中游离苯甲酸量过低无法准确定量外,10批样品中均检出游离的有害成分苯甲酸,建议今后应在逍遥丸 (水丸)的质量评价方法中增加相关项目检测,保证临床用药的安全性。同时,不同厂家和批次的样品中苯甲酰基总苷测定结果差异较大,芍药苷单体的含有量与苯甲酰基总苷含有量无明显相关性,提示苯甲酰基总苷的含有量差异可能与样品中所含除芍药苷外的其他苷类成分有关,增加苯甲酰基总苷的定量测定可有助于更好地控制逍遥丸的内在质量。本实验所建立方法操作简便,重复性好,丰富了逍遥丸 (水丸)的定量质控手段,可为该药物的全面质量评价提供参考依据。
[1]国家药典委员会.中华人民共和国药典:2010年版一部[S].北京:中国医药科技出版社,2010:995-996.
[2]夏小玉,邵 辉,沈红薇,等.逍遥丸的临床研究进展[J].陕西中医,2011,26(9):1436-1437.
[3]吴 芳,杜伟锋,徐珊珊,等.白芍化学成分及质量评价方法研究进展[J].浙江中医药大学学报,2012,36(5):613-615.
[4]谭菁菁,赵庆春,杨 琳,等.白芍化学成分研究[J].中草药,2010,41(8):1245-1248.
[5]刘月华,吕俊华.白芍总苷的降血脂、抗氧化作用及对脂肪肝的防治研究[J].海南医学院学报,2012,18(2):158-161.
[6]李宜川,刘国玲,张玉霞,等.白芍总苷对NAFLD大鼠肝脏NF-κB/p65蛋白表达及羟脯氨酸含量的影响[J].聊城大学学报:自然科学版,2013,24(4):62-66.
[7]冯文林,伍海涛,罗超华.白芍总苷在消化系统疾病中的药理研究进展[J].时珍国医国药,2012,23(7):1778-1779.
[8]李冰菲,王 娟,张碧丽.白芍总苷治疗肾脏疾病的药理作用和临床应用研究进展[J].现代药物与临床,2013,28(5):811-814.
[9]杜伟锋,胡淑珍,吴 芳,等.不同级别杭白芍中3个有效成分的考察[J].中成药,2014,36(2):358-362.
[10]李伟铭,赵月然,杨燕云,等.HPLC波长切换法同时测定白芍饮片中9个成分的含量[J].药物分析杂志,2011,31(12):2208-2212.
[11]郑敏霞,陈 喆,刘 培,等.白芍中芍药苷及其衍生物的UPLC-MS/MS分析[J].中国中药杂志,2011,36(12):1641-1643.
[12]刘敏彦,高秀强,王 永,等.高效液相色谱法测定白芍药材中白芍总苷的含量[J].中国药业,2008,17(5):22-23.
[13]刘玉红,陈 燕,易进海.HPLC测定白芍总苷的含量[J].华西药学杂志,2002,17(4):295-296.
[14]瞿白露,禹文峰,任凤莲,等.基于碱水解反应-荧光光度法测定白芍总苷的含量[J].理化检验:化学分册,2010,46(9):1040-1042.
[15]陈科敏,吴巧凤.杭白芍和亳白芍中苯甲酸的含量测定[J].中草药,2004,35(9):1064.
[16]李越峰,严兴科.赤芍和白芍不同部位芍药苷和苯甲酸的含量分析研究[J].时珍国医国药,2012,23(3):519-520.
Determ ination of paeoniflorin,benzoic acid and total benzoyl glucosides in Xiaoyao Pills by RP-HPLC
LIXiang-yang1, GAO Jie2, TUWan-qian3, YANGMing-jie4
(1.Henan Institute of Food and Drug Control,Zhengzhou 450003,China;Zhengzhou Kailway Vocational and Technical College,Zhengzhou 450052,China;3.Henan Academy of Traditional Chinese Medicine,Zhengzhou 450004,China;4.Henan College of Traditional Chinese Medicine,Zhengzhou 450008,China)
AIMTo estab1ish an HPLC method for determining the contents of paeonif1orin,free benzoic acid,and tota1benzoy1g1ucosides(with benzoic acid as contro1)in Xiaoyao(water)Pi11s produced by eightmanufactories.METHODSThe ana1ysis of Xiaoyao Pi11smethano1ic extractwas performed on Agi1ent Ec1ipse XDB C18co1umn(4.6 mm×250 mm,5μm).The mobi1e phase for simu1taneous determining paeonif1orin and benzoic consisted of acetonitri1e(A)-0.4%phosphoric acid(B)in gradient e1ution mode at the f1ow rate of 1.0 m L/min.The detection wave1ength was set at 230 nm.Using the method of a1ka1ine hydro1ysis,the tota1benzoy1 g1ucosides in Xiaoyao Pi11swere hydro1yzed into benzoic acid,determined by HPLC,and ca1cu1ated as benzoic acid content.The chromatographic conditionswere the same as the above.RESULTSThe 1inear ranges of paeonif1orin and free benzoic acid were in the ranges of0.060 8-0.760μg(r=0.999 8)and 0.009 6-0.120 0μg(r= 0.999 7),respective1y.The average recovery rates(n=6)were97.3%(RSD=2.2%)and 97.2%(RSD= 2.2%),respective1y.The 1inear range of benzoy1g1ucosides was in the ranges of 0.020 32-0.304 8μg(r=0.999 6),and the average recovery rate(n=6)was 96.6%(RSD=2.8%).CONCLUSIONThemethod is simp1e,accurate and sensitive,and can be used for the qua1ity contro1of Xiaoyao Pi11s.
Xiaoyao Pi11s;paeonif1orin;benzoic acids;benzoy1g1ucosides;RP-HPLC
R927.2
A
1001-1528(2015)08-1722-06
10.3969/j.issn.1001-1528.2015.08.019
2014-08-25
李向阳(1968—),男,副主任药师,主要从事药品检验、中药质量分析研究。Te1:(0371)63388283,E-mai1:1ixia632@126.com
