石膏用量对麻黄入血生物碱类的影响
2015-01-18霍慧灵李汉成任孟月马钦海谭晓梅罗佳波
霍慧灵, 李汉成, 任孟月, 马钦海, 谭晓梅,2, 罗佳波,2*
(1.南方医科大学中医药学院,广东广州510515;2.南方医科大学广东省中药制剂重点实验室,广东广州510515)
石膏用量对麻黄入血生物碱类的影响
霍慧灵1, 李汉成1, 任孟月1, 马钦海1, 谭晓梅1,2, 罗佳波1,2*
(1.南方医科大学中医药学院,广东广州510515;2.南方医科大学广东省中药制剂重点实验室,广东广州510515)
目的采用UPLC-MS/MS探讨不同用量石膏配伍麻黄对麻黄中移行入血生物碱类成分药动学的影响。方法将24只大鼠随机分成4组,各组分别灌胃麻黄-石膏不同配比 (1∶0,1∶1,1∶2,1∶4)水煎液后,于不同时间点采血,所得血药浓度-时间数据经DAS 3.2.2得出相关药动学参数。结果4组的药时曲线下面积 (AUC0-t)、达峰时间(tmax)有显著差异。与单味麻黄组相比,麻黄-石膏1∶1与1∶2组去甲基麻黄碱、去甲基伪麻黄碱和麻黄碱AUC0-t减少,麻黄-石膏1∶2与1∶4组此三成分tmax均缩短,但对于伪麻黄碱和甲基麻黄碱差异无统计学意义。在麻黄-石膏合用组中,随着石膏用量的加大,5种麻黄类生物碱的药动学变化整体表现为t1/2z、MRT、Vz/F逐渐增加,tmax、CLz/F逐渐减少。结论石膏用量的改变可对麻黄中效毒成分的药动学行为产生规律性的影响,与传统医学中麻黄石膏配比用药的临床经验相吻合。
麻黄;石膏;生物碱;剂量配比;药动学
目前,通过定量分析配伍后化学成分在机体内的变化规律,从其生物药剂学特征探索药效发挥的物质基础,已成为中医配伍理论研究的重点和热点。但是中药成分复杂,一方一药往往难以得出规律性的认识,而药对虽组成简单却代表着系列衍生方的核心特征,其中蕴含着丰富的客观规律[1-2]。
麻黄-石膏作为中医常用药对,当两药用量比例不同时,君臣不一,功效迥异,适应证有所差异:①麻黄量大于石膏,如大青龙汤,重在发散郁热,治疗寒邪束表、汗不得出、热不得越而形成的里有郁热之证;②麻黄用量小于石膏,如麻杏石甘汤,主清泻肺热;③麻黄石膏用量相等,如越婢汤,则为发越水气[3-4]。麻黄-石膏功效的改变是否与体内效毒成分的动态变化相吻合?不同剂量比例存在的变化规律是否与增效减毒的配伍内涵相关?为此,本研究借助UPLC-MS/MS手段,比较临床常用的麻黄-石膏剂量配比 (1∶0、1∶1、1∶2、1∶4)对自麻黄移行入血特征成分去甲基麻黄碱、去甲基伪麻黄碱、麻黄碱、伪麻黄碱和甲基麻黄碱药动学参数的影响,从药动学角度阐释麻黄-石膏剂量配比的合理性,以期为该药对的传统配伍理论提供现代科学依据。
1 仪器与材料
1.1 仪器 UPLC-MS/MS系统(Agi1ent 1290 Infinity-G6410,美国安捷伦公司);统计软件DAS 3.2.2;1/10万天平(美国DENVER公司);涡旋振荡混合器 (上海沪西分析仪器厂);HC-3018R高速冷冻离心机 (安徽中科中佳科学仪器有限公司)。
1.2 药品 麻黄为麻黄科植物草麻黄Ephedra sinica Stapf的干燥草质茎 (产地吉林,20101002),石膏为硫酸盐类石膏族矿物Gypsum(产地湖北,20110712),药材均购自广东致信中药饮片有限公司,经南方医科大学中药鉴定教研室马骥教授鉴定为正品。化学对照品盐酸麻黄碱(ephedrine hydroch1oride,171241-201007)、盐酸伪麻黄碱(pseudoephedrine hydroch1oride,171237-200807)、盐酸甲基麻黄碱(methy1ephedrine hydroch1oride,171247-200301)和盐酸金刚烷胺 (内标,100426-201002)均购自中国食品药品检定研究院;盐酸去甲基麻黄碱(norephedrine hydroch1oride,纯度≥98%)和盐酸去甲基伪麻黄碱(norpseudoephedrine hydroch1oride,纯度≥98%)为市售。
1.3 试剂 乙腈 (色谱纯,Merck公司);甲酸(分析纯,Tedia公司),乙醚、二氯甲烷均为市售分析纯。
1.4 实验动物 SPF级雄性SD大鼠24只,体质量 (220±20)g,购于南方医科大学实验动物中心,许可证号SCXK(粤)2011-0015。
2 方法
2.1 检测条件
2.1.1 色谱条件 色谱柱Agi1ent Zorbax SB-C18(3.5μm,2.1 mm×100 mm);柱温25℃;体积流量0.4 mL/min;流动相为乙腈(A)-0.1%甲酸水(B),梯度洗脱 (0~3 min,3%A;3~5 min,3%~4%A;5~7 min,4%A;7~7.5 min,4%~18%A;7.5~9 min,18%A;9~9.1 min,18% A→3%A;9.1~14.5 min,3%A)。
2.1.2 质谱条件 采用电喷雾离子源;喷雾电压4 000 V;毛细管温度350℃;气体体积流量8.0 L/min;正离子方式检测;扫描方式为MRM模式,用于定量分析的监测离子去甲基麻黄碱/去甲基伪麻黄碱m/z 152.1>134.1(Fragmentor=75,Co11ision Energy=8)、麻黄碱/伪麻黄碱m/z 166.1>148.1(88,12)、甲基麻黄碱m/z 180.2>162.1(110,12)和内标m/z152.2>135.1(95,20)。
2.2 混合对照溶液的制备 分别取去甲基麻黄碱(NME)、去甲基伪麻黄碱 (NMP)、麻黄碱 (E)、伪麻黄碱 (PE)和甲基麻黄碱 (ME)对照品适量,用甲醇溶解并定容,制成质量浓度分别为212.40、219.90、2 441.0、1 022.4、407.1μg/mL的对照品贮备液。精密量取各对照品贮备液适量,用甲醇稀释成分别含去甲基麻黄碱21.240、去甲基伪麻黄碱21.990、麻黄碱244.10、伪麻黄碱102.24和甲基麻黄碱40.710μg/mL的混合对照品,依次逐级稀释得系列溶液,于4℃冰箱保存备用。
2.3 灌胃用药液的制备 结合前期药效学实验[5]的煎煮方法与用药剂量,依不同比例 (1∶0、1∶1、1∶2、1∶4)分别称取麻黄36 g、石膏 (0、36、72、144 g),加1 680mL蒸馏水,先加入麻黄浸泡30 min,煮20 min,放入石膏继续煎煮30 min,保持微沸,四层纱布过滤,滤液减压回收溶剂,残渣用适量水溶解,制成相当于麻黄药材质量浓度为0.5 g/mL的药液,于4℃保存备用。
采用HPLC[5]测得单味麻黄水煎液中去甲基麻黄碱、去甲基伪麻黄碱、麻黄碱、伪麻黄碱和甲基麻黄碱的含有量 (以每1 g麻黄生药量计)依次为0.172 0、0.289 2、5.144、1.942、0.393 6 mg/g(n=6);麻黄-石膏1∶1中对应5种成分的含有量为0.172 3、0.289 9、5.152、1.949、0.395 8 mg/g(n=6);麻黄-石膏1∶2为0.172 4、0.290 4、5.158、1.951、0.397 2 mg/g(n=6);麻黄-石膏1∶4为 0.172 6、0.290 3、5.162、1.951和0.397 4 mg/g(n=6)。经统计分析,各成分在4组间均无显著差异 (P>0.05),即本研究中石膏剂量的变化不影响麻黄生物碱类成分的体外溶出。
2.4 给药与血样采集 将大鼠随机分成4组 (单味麻黄、麻-石1∶1、麻-石1∶2、麻-石1∶4,n= 6),给药前禁食12 h,自由饮水,眼眶静脉丛采血0.5 mL作为零时间点。按4 g/kg(以麻黄生药量计)分别灌胃给予药液,于给药后0.08、0.25、0.5、1、1.5、2.5、4、6、8、10、12、24、36和48 h眼眶静脉取血,置预先肝素化的 EP管中,4 000 r/min离心10 min,分离血浆,-80℃保存待测。
2.5 血样预处理 取上述血浆100μL,加入2.264μg/mL内标溶液40μL,再加入甲醇50μL、饱和Na2CO3溶液40μL,涡旋混匀30 s,加乙醚-二氯甲烷(3∶2,V/V)1.2 mL,涡旋2 min后4 000 r/min离心10 min,分取上清液。加乙醚-二氯甲烷(3∶2,V/V)1.2 mL重复萃取1次,合并上清液,以N2流吹干,残留物用乙腈-0.1%甲酸水 (3∶97)涡旋复溶,14 000 r/min离心10 min,取上清液10μL进样分析。
2.6 方法学考察
2.6.1 专属性 在建立的分析方法下,去甲基麻黄碱、去甲基伪麻黄碱、麻黄碱、伪麻黄碱、甲基麻黄碱和内标的保留时间分别为3.1、3.6、4.9、5.5、6.1、8.8 min,达到基线分离,血浆中物质不干扰5种生物碱与内标的测定,见图1。

图1 血浆样品LC-MS图Fig.1 Typical LC-MS chromatogram s of five alkaloids in rat p lasma
2.6.2 标准曲线与定量下限 取空白血浆100μL,加入系列对照品混合溶液50μL,除不加甲醇外,按 “2.5”项操作,每一质量浓度双样本分析,以待测物与内标物峰面积的比值为纵坐标,样品中待测物质量浓度为横坐标,用加权最小二乘法进行回归分析,求得标准曲线去甲基麻黄碱y=0.001 406x+ 0.000 513 4(r2=0.997 5)、去甲基伪麻黄碱y= 0.001 664x+0.000 587 2(r2=0.999 0)、麻黄碱y=0.001 165x+0.006 688(r2=0.991 9)、伪麻黄碱y=0.001 469x+0.001 815(r2=0.997 1)和甲基麻黄碱y=0.000 957 1x+0.000 175 8(r2= 0.996 7),分别在0.53~1 062、0.55~1 099.5、6.10~12 205、2.56~5 112、和1.02~2 035.5 ng/mL线性关系良好,最低定量为0.53、0.55、6.10、2.56和1.02 ng/mL。
2.6.3 精密度与准确度 按上述方法制备线性范围内5种生物碱低、中、高3个质量浓度的质量控制样品 (QC)(去甲基麻黄碱1.06、53.10、531.0 ng/mL;去甲基伪麻黄碱1.10、54.98、549.8 ng/mL;麻黄碱12.21、610.25、6 102.5ng/mL;伪麻黄碱5.11、255.60、2 556.0 ng/mL和甲基麻黄碱2.04、101.78、1 017.8 ng/m L),每一质量浓度5样本分析,连续测定3 d,根据当日的随行标曲算得QC样品质量浓度,与配制质量浓度比较,计算日内、日间精密度 (RSD)和准确度(RE)。结果,日内RSD<9.9% (低质量浓度<18.2%)、日间 RSD<3.6% (低质量浓度 <16.7%)、RE均在 ±9.7% (低质量浓度 ± 16.3%)之间。
2.6.4 提取回收率和基质效应 按 “2.6.3”项制备低、中、高3个质量浓度的血浆样品各5份(溶液A)。另取空白血浆100μL,除不加系列溶液和内标外,按 “2.5”项操作,向得到的上清液中加入相应质量浓度的溶液50μL和内标40μL,涡旋混合,N2流吹干,残留物复溶 (溶液B)。另取纯水100μL,按 “溶液B”法操作得溶液C,以每一质量浓度两种处理方法的峰面积比值计算提取回收率 (A/B)与基质效应 (B/C),结果见表1,符合相关的体内分析要求。
2.6.5 稳定性考察 按 “2.6.3”项制备低、中、高3个质量浓度的血浆样品各5份,考察样品处理后室温放置12 h,处理前3次冻融循环和-80℃保存15 d的稳定性。结果表明,处理后室温放置12 h后血浆浓度的RE在±10.5% (低质量浓度±15.2%)内,处理前3次冻融循环后 RE在±11.5% (低质量浓度±16.0%)内,-80℃保存15 d后RE在±13.0% (低质量浓度± 16.0%)内,其RSD<10.9% (低质量浓度<16.7%),稳定性良好。

表1 去甲基麻黄碱、去甲基伪麻黄碱、麻黄碱、伪麻黄碱、甲基麻黄碱和内标的提取回收率与基质效应(n=5)Tab.1 Recoveries and m atrix effects of five alkaloids and IS.(n=5)
3 结果
3.1 药动学参数 大鼠灌胃单味麻黄、麻黄-石膏1∶1、麻黄-石膏1∶2、麻黄-石膏1∶4水煎液后,5种麻黄类生物碱 (去甲基麻黄碱、去甲基伪麻黄碱、麻黄碱、伪麻黄碱、甲基麻黄碱)的药-时曲线如图2。经DAS 3.2.2处理,得主要药动学参数,见表2。
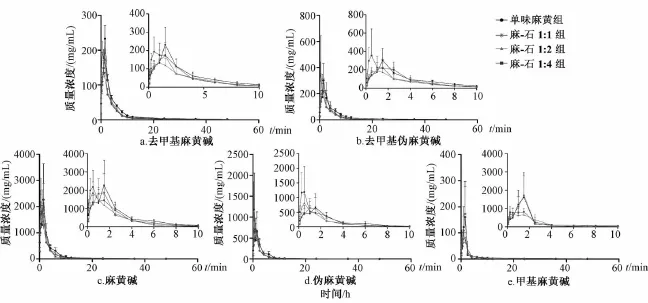
图2 大鼠分别灌胃麻黄-石膏不同配比水煎液 (1∶0;1∶1;1∶2;1∶4)后平均血药浓度-时间曲线(,n=6)Fig.2 M ean p lasm a concentration-tim e profiles for five alkaloids in rat p lasma after oral adm inistration of different doses of gypsum in Ephedrae Herba-Gypsum Decoction(,n=6)
3.2 数据分析 借助SPSS 13.0统计软件,采用One-way ANOVA比较多组之间药动学参数的均值,以LSD法(方差齐性)与Games-Howe11法(方差不齐)进行多重比较。结果显示,各组组内5种麻黄类生物碱的吸收趋势(AUC0-t/Dose)均为去甲基麻黄碱≈去甲基伪麻黄碱>麻黄碱≈伪麻黄碱≈甲基麻黄碱 (见图3)。4组的AUC0-t、tmax有显著差异 (P<0.05),但Cmax变化不明显。其中与单味麻黄相比,对于成分去甲基麻黄碱、去甲基伪麻黄碱和麻黄碱,麻黄-石膏1∶1与1∶2时吸收程度下降 (AUC0-t减少),麻黄-石膏1∶2与1∶4时吸收速率提高 (tmax缩短)。成分伪麻黄碱和甲基麻黄碱虽存在上述变化,但无统计学意义。此外,在3个麻黄-石膏合用组中,随着石膏用量的加大,5种麻黄类生物碱的药动学行为变化整体表现为参数t1/2z、MRT、Vz/F逐渐增加,tmax、CLz/F逐渐减少。
表2 灌胃麻黄-石膏不同配比水煎液后去甲基麻黄碱、去甲基伪麻黄碱、麻黄碱、伪麻黄碱和甲基麻黄碱的药动学参数(,n=6)Tab.2 Pharmacokinetic parameters of five alkaloids in rat p lastm a after oral adm inistration of d ifferent doses of gypsum Ephedrae Herda-Gypsum Decoction(,n=6)

表2 灌胃麻黄-石膏不同配比水煎液后去甲基麻黄碱、去甲基伪麻黄碱、麻黄碱、伪麻黄碱和甲基麻黄碱的药动学参数(,n=6)Tab.2 Pharmacokinetic parameters of five alkaloids in rat p lastm a after oral adm inistration of d ifferent doses of gypsum Ephedrae Herda-Gypsum Decoction(,n=6)
注:与单味麻黄组比较,1)P<0.05;与麻-石1∶1组比较,2)P<0.05;与麻-石1∶2组比较,3)P<0.05
化合物 组别AUC0-t/(ng·h·mL-1)C max/(ng·mL-1)Tmax/h t1/2z/h MRT/h(CLz/F)/(mL·h-1·kg-1)(Vz/F)/(L·kg-1)去甲基麻黄碱 单味麻黄 851.6±80.8 233.5±92.4 1.67±0.41 17.60±7.36 6.64±0.93 0.77±0.05 19.89±9.07麻-石∶1 565.3±201.21) 177.8±67.8 1.58±0.50 4.39±2.411) 3.48±1.011) 1.32±0.94 7.38±4.081)麻-石∶2 542.0±118.01) 138.8±30.4 0.92±0.381,2) 5.48±5.081) 3.84±1.541) 1.12±0.27 7.81±5.881)麻-石∶4 750.0±94.82,3) 214.3±71.0 0.92±0.491,2) 17.49±5.682,3)5.51±1.002,3) 0.86±0.09 21.66±7.012,3)去甲基伪麻黄碱 单味麻黄 1 283±126 305.4±126.2 1.67±0.41 17.76±8.18 7.38±0.94 0.86±0.05 22.29±11.08麻-石∶1 776.8±284.41) 235.3±89.2 1.50±0.55 3.21±1.261) 3.42±1.091) 1.70±1.30 6.27±1.61麻-石∶2 759.3±145.11) 201.3±42.9 0.92±0.381,2) 2.82±1.921) 3.38±0.581) 1.26±0.251) 5.04±3.551)麻-石∶4 1 122±2312,3) 387.2±275.0 0.92±0.491,2) 7.61±7.03 3.53±1.111) 1.00±0.21 10.08±6.97麻黄碱 单味麻黄 7 139±1 386 2 335±1 348 1.42±0.67 16.30±4.95 5.44±0.83 2.87±0.50 68.87±26.00麻-石∶1 4 756±1 9591) 2 006±1 006 1.25±0.27 1.02±0.561) 2.20±0.371) 4.24±1.51 6.26±4.571)麻-石∶2 5 380±8471) 1 907±552 0.58±0.201,2) 9.02±4.392) 4.12±1.282) 4.51±0.721) 59.35±30.482)麻-石∶4 6 317±899 2 287±789 0.38±0.141,2) 23.56±8.902,3)5.49±1.132) 3.42±0.49 115.1±44.42)伪麻黄碱 单味麻黄 2 253±458 769.7±414.3 1.25±0.76 14.83±5.10 4.96±0.49 3.49±0.70 73.79±27.61麻-石∶1 1 635±718 701.2±349.8 1.08±0.38 2.07±1.471) 2.18±0.421) 5.33±3.33 13.74±6.921)麻-石∶2 1 745±318 831.5±290.3 0.54±0.25 4.64±3.891) 2.63±0.881) 3.92±0.76 26.55±20.621)麻-石∶4 2 528±6152,3) 1 350±810 0.33±0.132) 39.17±16.452,3)5.11±1.242,3) 2.69±0.473) 158.3±83.32,3)甲基麻黄碱 单味麻黄 325.7±162.3 168.5±134.5 1.33±0.26 45.58±31.15 6.45±2.21 4.66±2.06 284.8±177.2麻-石∶1 256.9±127.0 172.6±105.6 1.50±0.00 2.68±2.24 1.61±0.251) 6.48±2.92 24.30±22.11麻-石∶2 276.3±60.9 88.58±25.75 0.83±0.59 22.05±18.58 7.22±2.162) 4.83±1.05 140.8±102.4麻-石∶4 336.0±59.8 100.9±18.7 0.83±0.59 61.09±38.622)9.68±1.061,2,3)3.33±0.59 271.6±125.02)
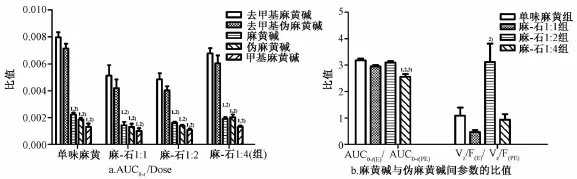
图3 灌胃麻黄-石膏不同配比水煎液后去甲基麻黄碱、去甲基伪麻黄碱、麻黄碱、伪麻黄碱和甲基麻黄碱的药动学参数比值(,n=6)Fig.3 Ratios of pharmacok inetic parameters of five alkaloids in rat p lasma after oral adm inistration of different doses of gypsum in Ephedrae Herba-Gypsum Decoction(,n=6)
4 讨论
4.1 移行入血成分的选择 前期研究[3]借助HPLC发现不同配比的麻黄-石膏水煎液中存在10个共有峰,经已有对照品参照确认了其中5个成分去甲基麻黄碱、去甲基伪麻黄碱、麻黄碱、伪麻黄碱和甲基麻黄碱,它们所涵盖的药毒理学作用[6-12],恰与麻黄 “发汗解热、宣肺平喘、利水消肿”的功效对应,亦与其 “峻烈”之药性吻合。它们虽均属麻黄类生物碱,化学结构相似但效毒强度有所区别,体现在发汗平喘功效,麻黄碱≈ 甲基麻黄碱>伪麻黄碱 (伪麻黄碱对支气管平滑肌存在双向调节);利尿功效,伪麻黄碱>麻黄碱;兴奋中枢神经功效,麻黄碱>伪麻黄碱>甲基麻黄碱 (甲基麻黄碱几乎无中枢兴奋作用);去甲基麻黄碱主要用于增强身体机能。为此麻黄-石膏不同配比下功效侧重的改变,可能与效毒成分药动学行为变化随之产生不同比例物质群有关。故本实验选取去甲基麻黄碱、去甲基伪麻黄碱、麻黄碱、伪麻黄碱和甲基麻黄碱作为研究石膏剂量变化对麻黄移行入血成分药动学影响的主要检测指标。
4.2 检测方法的建立 按试验剂量灌服大鼠后所得含药血浆浓度较低,过去HPLC、GC-MS[13-14]难以测定,故采用灵敏度较高的LC-MS/MS定量分析5种麻黄类生物碱的含量。经正负离子扫描发现5成分均在正离子模式下有较好的响应,且根据其分子离子峰与产物离子完成Fragmentor和co11ision等参数优化,最低定量限可达纳克级。此外,对甲醇-水、乙腈-水流动相进行系统探索,发现乙腈-水中加入适量甲酸可改善峰型亦提高待测物的质谱响应,尚能实现去甲基麻黄碱/去甲基伪麻黄碱、麻黄碱/伪麻黄碱同分异构体在色谱上良好分离。针对血样预处理常用的方法,考察了蛋白沉淀法、液液萃取法与SPE固相萃取法,结果采用乙醚-二氯甲烷 (3∶2)萃取时待测物的内源性物质干扰相对较少,回收率较高。本实验所建立的同时测定生物样品中去甲基麻黄碱、去甲基伪麻黄碱、麻黄碱、伪麻黄碱和甲基麻黄碱的LC/MS-MS较以往的方法灵敏、快速,能满足中药麻黄乃至含麻黄生物碱药品的体内成分监测,指导临床安全用药。
4.3 麻黄石膏不同配比下的药动学行为 实验结果表明石膏剂量的改变可对麻黄中效毒成分 (去甲基麻黄碱、去甲基伪麻黄碱、麻黄碱、伪麻黄碱和甲基麻黄碱)的药动学行为产生规律性影响。结合传统医学对麻黄石膏临床用药的认识,加之检测指标的效毒差异 (见 “4.1”项),发现与麻黄-石膏1∶1比,当1∶2、1∶4时,成分麻黄碱、伪麻黄碱与甲基麻黄碱吸收速率加快、滞留时间延长,表观分布容积增加,吸收程度升高,生物利用度提高,与麻黄量少于石膏功效重在解热平喘相衔接,但临床常用比例为1∶2,原因可能在于1∶4时去甲基麻黄碱、麻黄碱的药代特征趋于单味麻黄,而麻黄属 “峻烈”之品[15],不良反应的发生率相应提高。对于麻黄-石膏1∶1时,尽管麻黄碱与伪麻黄碱的生物利用度有所下降,可是两成分间AUC0-t、Vz/F的比值分别为2.9∶1与0.5∶1,均较麻黄-石膏1∶2与单味麻黄低 (见图3),引用概念 “中药药效物质的叠加作用”[16],推测互为同分异构体的麻黄碱与伪麻黄碱结构极其相似,可能具有相同的药效基团,在相同的利尿作用靶点上相互竞争,麻黄-石膏1∶1时伪麻黄碱较麻黄碱占据份额提升,“此消彼长”,平喘作用降低的同时利尿效应增强,实现麻黄量等于石膏重在发越水气(利尿)的目的。此外麻黄配伍石膏,可使成分麻黄碱、去甲基麻黄碱的AUC0-t、Cmax减少,消除速率加快,一定程度上降低了毒副作用的风险。
本研究从药动学方面证实临床麻黄-石膏据“证”定 “比”的科学性与合理性,至于其剂量改变导致参数变化的机制尚不明确,本课题组猜想:(1)结构相似的麻黄生物碱类成分在特定的条件下可实现相互间的转化,其转化程度除与药物本身有关,还受到所处环境的作用; (2)石膏的加入可使体内药物作用靶点的内环境发生改变,如pH、离子浓度、渗透压等理化性质; (3)由于石膏加入量的不同,所引起的生物体内环境变化程度有所差异,即使同一剂量对不同靶标位置的影响亦有所区别,从而实现对特定靶点 (如肺、肾、脑、心等组织器官)中麻黄药效/毒成分群比例的调节,达到麻黄解热、平喘、利尿功效的偏颇。为了进一步验证本课题组的构想,实验后期将分析剂量配比对麻黄类生物碱体内组织分布、对石膏移行入血元素药动学的影响,可为麻黄-石膏 “增效减毒”的配伍内涵提供更为翔实的数据支撑。
[1]胥庆华.中药药对大全[M].北京:中国中医药出版社,2001.
[2]王胜鹏,胡杨洋,陈锐娥,等.中药药对的系统研究(Ⅱ)-药效与药动学研究[J].世界科学技术:中医药现代化,2012,14(2):1322-1328.
[3]张保伟.《伤寒杂病论》中麻黄石膏用量比与其作用关系探讨[J].河南中医,2003,23(1):7-8.
[4]李晨光,贾 波,张建伟.基于现代医案探讨麻黄与石膏的配伍特点[J].江西中医药,2010,41(8):20-22.
[5]梅 芬.麻黄-石膏药对配伍的化学成分、药效及代谢组学研究[D].广州:南方医科大学,2013.
[6]李佳莲,方 磊,张永清,等.麻黄的化学成分和药理活性的研究进展[J].中国现代中药,2012,14(7):21-27.
[7]王艳宏,王秋红,夏永刚,等.麻黄化学拆分组分的性味药理学评价-麻黄化学拆分组分 “辛温”发汗、利水作用的实验研究[J].中国中医药科技,2011,18(6):489-491.
[8]王艳宏,王秋红,夏永刚,等.麻黄化学拆分组分的性味药理学评价-化学拆分组分的制备及其解热作用的研究[J].中医药信息,2011,28(5):7-10.
[9]王艳宏,王秋红,夏永刚,等.麻黄化学拆分组分的性味药理学评价-麻黄化学拆分组分 “辛宣苦泄”平喘作用的研究[J].中国实验方剂学杂志,2011,17(24):136-139.
[10]黄云珍.麻黄与麻黄碱的共性与区别[J].江西中医学院学报,2007,19(6):54-55.
[11]刘维国,刘兴君,姜晓威.甲基麻黄碱的药理作用研究进展[C]第二十二届航天医学年会暨第五届航天护理年会论文汇编.北京:中国航天科工集团公司,2006:372.
[12]潘国华,孙晓如.国外对麻黄及其制剂的安全性评价[J].中国药物警戒,2007,4(2):111-117.
[13]朱全红,陈飞龙,白 霜,等.GC-MS法测定尿液中麻黄汤代谢产物麻黄类生物碱的浓度[J].药物分析杂志,2005,25(9):1030-1034.
[14]Chen Y,Li X,Chen F L,et al.Simu1taneous determination of ephedra a1ka1oids in traditiona1Chinesemedicines by high-performance 1iquid chromatography[J].Acta Chromatogr,2012,24(3):475-487.
[15]钟赣生.中药学[M].北京:中国中医药出版社,2012.
[16]徐 风,杨东辉,尚明英,等.中药药效物质的 “显效形式”、“叠加作用”和 “毒性分散效应”[J].世界科学技术:中医药现代化,2014,16(4):688-703.
Effect of gypsum dosage on p lasm a concentration of Ephedrae Herba alkaloids
HUO Hui-1ing1, LI Han-cheng1, REN Meng-yue1, MA Qin-hai1, TAN Xiao-mei1,2, LUO Jia-bo1,2*
(1.School of Chinese Medical Sciences,Southern Medical University,Guangzhou 510515,China;2.Guangdong Provincial Key Laboratory of Chinese Medicine Pharmaceutics,Southern Medical University,Guangzhou 510515,China)
AIMTo investigate the effect of the various gypsum dosages on pharmacokinetic changes of the p1asma concentration of Ephedrae Herba a1ka1oids by UPLC-MS/MS.METHODSTwenty-four SD ratswere random1y divided into four groupsand ora11y administered with EphedraeHerba-gypsum(1∶0,1∶1,1∶2,1∶4,m/ m)decoction.Their b1ood was co11ected at different time points,and the main pharmacokinetic parameters were ca1cu1ated by DAS 3.2.2 software.RESULTSSignificant differences in AUC0-tand tmaxwere observed among four groups.The 1∶1 and 1∶2 groups shared AUC0-tdecreases of norephedrine,norpseudoephedrine and ephedrine as compared to the 1∶0 group,whi1e 1∶2 and 1∶4 groups had shortened tmax,but no variation in their contents of pseudoephedrine and methy1ephedrine.With the gypsum dosage increased,the genera1 pharmacokinetic changes of the five Ephedrae Herba a1ka1oidsmanifested as the increases in t1/2z,MRT and Vz/F,but the decreases in tmaxand CLz/F.CONCLUSIONEphedrae Herba f1uctuating efficacy or toxicity due to change in gypsum dosage may exp1ain the regu1ar ratio a1eration in c1inica1administration of Ephedrae Herba and gypsum.
Ephedrae Herba;gypsum;a1ka1oids;dosage;pharmacokinetics
R966
A
1001-1528(2015)08-1689-07
10.3969/j.issn.1001-1528.2015.08.012
2014-10-18
国家自然科学基金重点项目 (81030066)
霍慧灵 (1989—),女,硕士,从事中药复方制剂组方原理及配伍规律研究。Te1: (020)61689112,E-mai1:hh1study@ 163.com
