正交实验优选高乌头解毒的炮制工艺研究
2015-01-17胡昌江侯桃霞马贝红孙政华刘峰林
李 芸, 胡昌江, 侯桃霞, 马贝红, 孙政华, 刘峰林
(1.成都中医药大学,四川成都611137;2.甘肃中医学院,甘肃兰州730000)
正交实验优选高乌头解毒的炮制工艺研究
李 芸1,2, 胡昌江1*, 侯桃霞2, 马贝红2, 孙政华2, 刘峰林2
(1.成都中医药大学,四川成都611137;2.甘肃中医学院,甘肃兰州730000)
目的探讨毒性中药高乌头炮制解毒的最佳工艺,为高乌头的质量标准制订提供科学依据。方法采用L9(34)正交设计法,以总生物碱和高乌甲素的量为考察指标,选择辅料种类、加热方式及加热时间3个因素 (每因素3水平),优选最佳炮制工艺。结果最佳炮制工艺为加入10%甘草汁,127℃0.15 MPa加压蒸5 h。结论优选的高乌头最佳炮制工艺稳定,合理。
高乌头;单因素;正交设计;炮制工艺
高乌头是毛莨科乌头属植物高乌头Aconitum sinomontanum Nakai的干燥根,又名九连环、麻布七,分布于我国甘肃、青海、陕西、四川等地,为我国中西部地区的民间草药,主要用于风寒湿痹、脘腹冷痛、跌打损伤,外用杀灭寄生虫等[1-4],现收载于 《甘肃省中药材标准》(2009年版)。高乌头生品有毒,己被多部文献记载[1-4]。高乌头虽与乌头同科同属,但其毒性成分不同于乌头,高乌头基本不含极毒的乌头碱[5],从迄今分离的27种化学成分中也未得到乌头碱[6-7]。高乌甲素 (也叫刺乌头碱,拉帕乌头碱)是高乌头抗炎镇痛的主要有效成分,也是其毒性成分[8-10]。
我国自古就认为高乌头 “辛热有大毒”,其临床应用受限,须炮制以解毒,才能保证临床安全有效。目前,高乌头炮制解毒尚未见报道。本课题以总生物碱和高乌甲素的量为考察指标,采用正交设计法,探讨高乌头炮制解毒过程,优选高乌头炮制解毒的最佳炮制工艺。
1 仪器与试药
1.1 仪器 Waters-2695型高效液相仪、2998二极管阵列检测器 (PAD);UV-3300型紫外可见分光光度计 (上海美谱达仪器有限公司);BT 125D电子天平 (赛多利斯科学仪器北京有限公司);LDZX-30FA立式压力蒸汽灭菌器(上海中安医疗器械厂)。
1.2 试药 高乌头购自甘肃省天祝藏族自治县,由中药鉴定教研室杨抚德教授鉴定为高乌头Aconitum sinomontanum Nakai的根,别名麻布七。氢溴酸高乌甲素对照品购自甘肃神龙药业股份有限公司,批号20001001,纯度97.50%。甲醇、乙腈为色谱纯,其他试剂均为分析纯。0.1%溴甲酚绿的制备:精密称取溴甲酚绿0.500 0 g,用0.05 mol/L NaOH溶液8.75mL研磨,加蒸馏水溶解到500 mL(pH= 6.0±0.2),过滤,以三氯甲烷除去脂溶性杂质。醋 (镇江香醋pH为4~5,镇江市恒康调味品厂)。甘草汁的制备[11]:取甘草180 g,加12倍量水,煎煮1 h,过滤,药渣再用10倍量水煎煮1 h,过滤,合并两次滤液,浓缩至甘草汁体积与甘草质量比为3:1,即得。
2 炮制工艺评价方法的建立
2.1 总生物碱测定方法的建立
2.1.1 溶液的制备
2.1.1.1 对照品贮备液的制备 精密称取氢溴酸高乌甲素11.10 mg,置于50 mL量瓶中,加入醋酸-醋酸钠缓冲液稀释至刻度,作为对照品溶液,备用。
2.1.1.2 供试品溶液的制备 取高乌头粉末0.2 g,精密称定,加入乙醚-三氯甲烷 (3:1)20 mL、氨试液1 mL,摇匀放置过夜,过滤,药渣用乙醚-三氯甲烷 (3:1)洗涤3次,合并滤液,减压回收溶剂,水浴60℃蒸干,残渣用三氯甲烷定容至25 m L。
2.1.2 线性关系考察[12]精密量取对照品贮备液0.5、1.0、1.5、2.0、2.5、3.0、4.0 m L分别置分液漏斗中,分别加醋酸-醋酸钠缓冲液至10 mL,另取醋酸-醋酸钠缓冲液10 mL置于分液漏斗中作为空白对照。在上述分液漏斗中分别加入10 mL溴甲酚绿溶液,振摇5 min,静置10 min,用三氯甲烷提取3次,每次10 mL,合并三氯甲烷提取液,用干燥滤纸滤过于50 mL量瓶中,并用三氯甲烷稀释至刻度,在413 nm处测定吸光度,以吸光度 (A)对质量浓度(C)进行线性回归,氢溴酸高乌甲素在 4.44~17.76 μg/mL线性关系良好,回归方程为A=41.977C-0.100 4,r=0.995 2。
2.1.3 精密度试验 精密吸取对照品溶液2 mL,连续测定6次,吸光值的RSD为0.3%。
2.1.4 稳定性试验 取供试品溶液按照标准曲线项下的方法进行操作,分别在1、10、20、30、60、90、120、180、240、360 min测定吸光度,结果RSD为1.4%,供试品溶液在6 h内稳定。
2.1.5 重复性试验 取同一药材样品,平行6份,依法测定,结果平均含有量为3.4%,RSD为2.6%。
2.1.6 加样回收率试验 取已知含有量的高乌头药材0.1 g,精密称定,精密加入氢溴酸高乌甲素对照品溶液(0.315 2mg/mL)7mL,按供试品溶液的制备方法制备供试品溶液,依线性关系考察项下的方法进行测定吸光度,结果平均回收率为91.8%,RSD为2.5%。
2.2 氢溴酸高乌甲素测定方法的建立
2.2.1 溶液的制备
2.2.1.1 醋阴性对照溶液的制备 取醋0.2 mL(制备样品时醋的用量),挥干,按供试品溶液的制备方法依法制备。
2.2.1.2 甘草汁阴性对照溶液的制备 取甘草汁0.1 mL,挥干,按供试品溶液的制备方法制备阴性对照溶液。
2.2.1.3 对照品溶液的制备 精密称取氢溴酸高乌甲素对照品7.5 mg,置25 mL量瓶中,加甲醇溶解并定容至刻度,摇匀,即得。
2.2.1.4 供试品溶液的制备 取高乌头样品 (过50目筛)约0.5 g,精密称定,置三角瓶中,加甲醇15 mL,超声15 min,滤过,滤渣再加10 m L甲醇,超声15 min,滤液合并于25 mL量瓶中,用甲醇定容至刻度,即得。
2.2.2 色谱条件 ZORBAX SB-C18色谱柱(4.6mm×250 mm,5μm);以甲醇-0.05 mol/L NaH2PO4溶液(45:55)为流动相;体积流量为1.0 mL/min;进样量10μL;检测波长252 nm;柱温为30℃。
2.2.3 系统适用性试验 分别取对照品溶液、样品溶液及阴性对照溶液,照上述色谱条件,各进样10μL,结果见图1,氢溴酸高乌甲素的保留时间为12.234 min。结果表明各阴性对照溶液色谱在与对照品色谱相应位置上无干扰。理论塔板数按氢溴酸高乌甲素计算不低于5 000。
2.2.4 线性关系考察 精密吸取对照品溶液0.5、1、5、10、15、20、25μL注入液相色谱仪,测定峰面积,以峰面积 (Y)对进样量 (X)进行线性回归,氢溴酸高乌甲素在0.15~7.5μg范围内线性关系良好,回归方程Y=237 512 X-53 646,r=0.999 9。
2.2.5 精密度试验
2.2.5.1 日内精密度 精密吸取对照品溶液10μL连续进样5次,其峰面积的RSD为0.5% (n=5)。
2.2.5.2 日间精密度 取同一样品溶液 (生品饮片),在相同条件下连续3日进样,其峰面积的RSD为1.6%。
2.2.6 重复性试验 取5份样品 (生品饮片)各0.5 g,精密称定,按供试品溶液的制备方法制备溶液,依法测定,结果氢溴酸高乌甲素的平均含有量为0.595%,RSD为2.8% (n=5)。
2.2.7 加样回收率试验 精密称取已知含有量的样品 (生品饮片)5份各0.25 g,精密加入对照品溶液5 mL(质量浓度0.3mg/mL),按供试品溶液的制备方法制备,依法测定,结果见表1。

表1 加样回收试验结果
3 炮制工艺研究
3.1 单因素试验 高乌头的炮制解毒工艺参数与是否加入辅料及所加辅料用量,采用何种加热方式,以及加热时间长短都密切相关,因此,本实验首先确定一定的影响因素及水平范围(如药材软化方式,水煮制时间,甘草汁及米醋用量,其中,水煮制时间的确定也意味着甘草汁和米醋煮制时间的确定,在确定的时间内再选择甘草汁和米醋的用量),再采用正交设计优选炮制工艺的最佳组合。
3.1.1 软化方式的选择 称取高乌头药材3份,每份150 g(下同),抢水法洗净,分别采用泡、漂、润3种方法软化,透心后,切碎段(约5 mm),阴干,结果3种软化方法总生物碱的量均有不同程度的损失,但润法损失最少,故选择润法作为最佳软化方法。
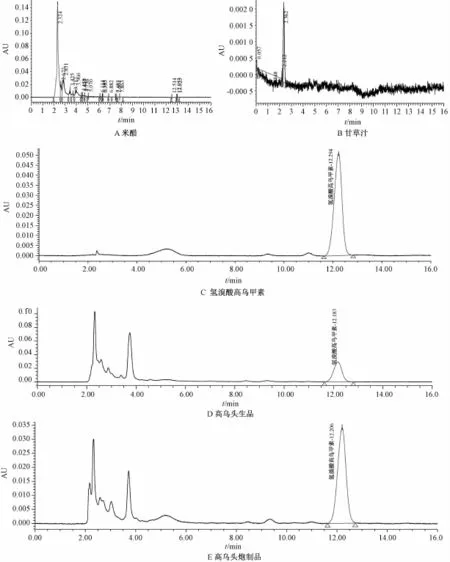
图1 对照品(C)、阴性对照(A、B)及样品(D、E)的HPLC色谱图
3.1.2 水煮制时间的选择 取软化切制后的生品饮片4份,分别加水煎煮2、4、6、8 h,煮至药透水干,取出,干燥,测定总生物碱量,见图2,结果,煮4 h总生物碱损失较少,这为后续甘草汁和米醋煮制所采用时间提供依据,也为正交设计加热时间的范围提供参考。
3.1.3 甘草汁用量的考察 取软化切制后的干燥饮片5份,分别加入5%、10%、15%、20%、25%的甘草汁,搅拌均匀,加水没过药面,先武火后文火,煮制4 h,药透汁尽,取出,干燥,依法测定含量(除去甘草的干扰),见图3,结果:加入10%甘草汁时,炮制效果理想,因此,正交设计可选用10%甘草汁炮制。

图2 煎煮时间考察
3.1.4 米醋用量的考察 取软化切制后的干燥饮片4份,分别加入5%、10%、20%、30%的醋,搅拌均匀,煮制4 h,至
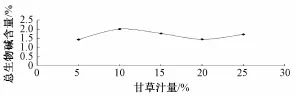
图3 甘草汁用量考察
药透水干,取出,干燥,测定(去除米醋的干扰),见图4,结果说明:加入20%醋时,总生物碱量最高,故辅料醋的用量为20%时炮制效果最佳。
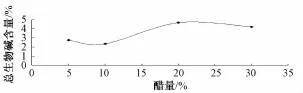
图4 米醋用量考察
3.2 正交设计试验 在文献调研及单因素考察的基础上,以辅料类型、加热方式和加热时间为考察因素,以总生物碱和高乌甲素的量为指标,进行正交设计安排实验,因素水平见表2。

表2 因素水平
3.2.1 正交设计试验安排与结果 采用L9(34)表安排试验,计算总生物碱 (折干)和高乌甲素 (折干)的百分含有量,实验结果见表3,方差分析结果见表4。
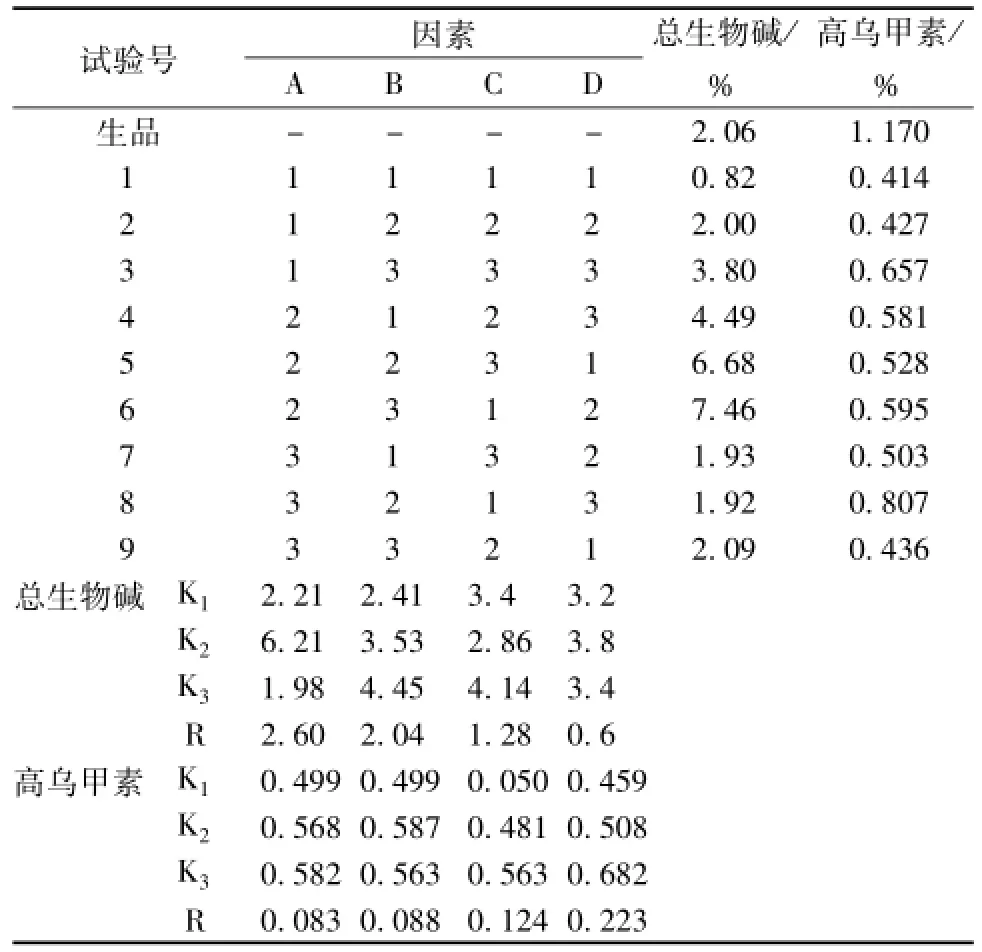
表3 L9(34)正交试验结果
3.2.2 方差分析 利用SPSS 17.0统计软件进行方差分析,结果见表4。
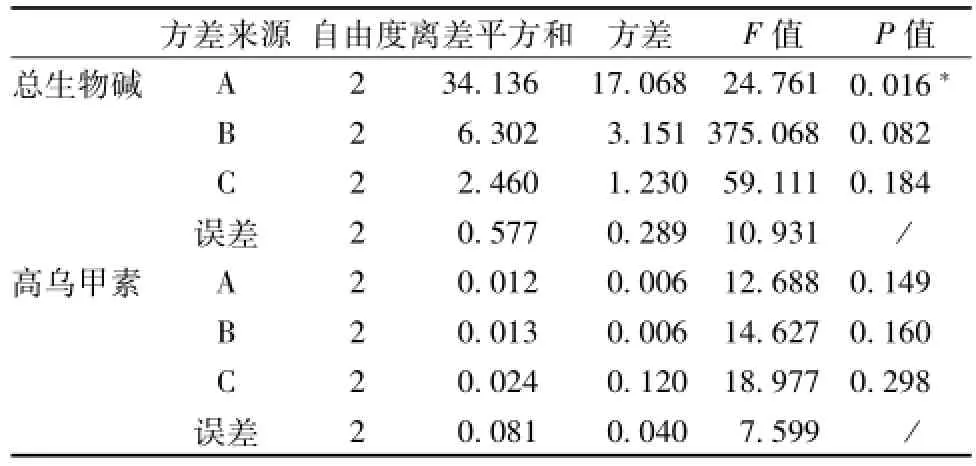
表4 方差分析结果
方差分析结果表明:按α=0.05,A因素 (辅料类型)对总生物碱量 (P=0.016)具有显著性影响;辅料、加热方式和加热时间三因素对高乌甲素含量均无显著性影响。对总生物碱:A、B、C三因素对其影响顺序为A>B>C,选择最高的水平,其最优组合为A2B3C3;对高乌甲素:A、B、C三因素对其影响顺序为C>B>A,选择 “适中”的水平,其最优组合为A2B3C2。
综合两个考察指标的方差分析结果,又考虑到该实验是选择高乌头炮制解毒增效的炮制工艺,总生物碱是其发挥药效的物质基础,高乌甲素既是镇痛抗炎的药效成分又是毒性成分,故应该选择总生物碱量高而高乌甲素量 “适中”的参数为其最佳炮制工艺,最佳组合为A2B3C3,即高乌头生品饮片加入10%甘草汁,127℃0.15 MPa加压蒸5 h。
3.2.3 验证试验 为考察该工艺的合理性、稳定性,按照正交试验优选的工艺条件验证3批,分别测定总生物碱及高乌甲素的量,结果总生物碱量分别为7.78%、7.76%、7.71%;高乌甲素的量分别为 0.601%、0.599%、0.589%。3次测定结果均优于正交试验各工艺结果,说明该高乌头的炮制工艺合理可行。
4 讨论
4.1 解毒辅料及加热方式的选择 高乌头的炮制,文献《中华本草》记载: “拣去杂质,洗净,稍闷,切片,晒干,本品有毒,使用慎用”,但炮制如何解毒未能明确,为此,笔者参照乌头的炮制方法,分别采用清水煮和加辅料(甘草汁和米醋)煮、常压蒸和加压蒸等方法,选用正交设计实验,能够更全面地考察其炮制工艺,保证工艺的可靠性和稳定性。
4.2 辅料米醋和甘草汁的作用 使用辅料解毒,是炮制毒性中药的重要手段。实验中使用米醋,主要起解毒[14]作用,同时醋具有酸性,能与药物中所含的游离生物碱结合成盐,而使有效成分易于煎出;甘草汁主要起解毒作用。甘草的解毒早在 《神农本草经》中就有记载,历代炮制有毒药物如半夏、川乌等都用甘草水煮。甘草的解毒主要是甘草甜素水解后释放出葡萄糖醛酸与含有羟基或羧基的毒物结合而解毒。此外,甘草苷是表面活性剂,能增加其他不溶于水物质的溶解度,起一定的增溶作用。
4.3 考察指标的选择 毒性中药的炮制必须兼顾去毒和存效两个方面,因此考察指标的选择也必须反映这两方面。实验曾选择总生物碱和酯型生物碱的含有量分别代表药效和毒性指标,但在采用改良盐酸羟胺-高氯酸铁比色法测定酯型生物碱时,可能由于空间位阻等因素导致该显色反应不能定量进行,无法定量测定酯型生物碱。但考虑到高乌甲素既是镇痛抗炎的有效成分,又具有一定的毒性,可作为毒性指标,在选择最佳炮制工艺时,尽量选择总生物碱含有量高而高乌甲素含有量又不能太低 (适中)的因素水平作为最适宜的炮制解毒工艺。本实验从保证疗效和降低毒性两个方面优选炮制工艺,更具有合理性,但这仅是化学评价指标,而通过炮制是否确实达到 “减毒存效”的目的,有待药理实验进一步证明。因此,高乌头 “适中”的炮制工艺还应结合毒性和药效学指标进行综合评价。
[1]甘肃省食品药品监督管理局,甘肃省中药材标准[S]. 2009:117-118.
[2]江苏新医学院.中药大辞典:下册[M].上海:上海科技出版,1993:2225-2226.
[3]国家中医药管理局,中华本草编委会.中华本草:第七卷[M].上海科技出版社,1999:1746-1747.
[4]杨仓良.毒药本草[M].中国中医药出版社,1993:473.
[5]贺江萍,王 彤,董伟林.高效液相色谱法测定高乌头和雾灵乌头中乌头碱的含量[J].天津医科大学学报,1998,(3):261-262.
[6]谢海辉,韦璧瑜.高乌头的化学成分及其药理作用研究进展[J].天然产物研究与开发,2010,22(B08):232-235,154.
[7]Yuan C L,Wang X L.Isolation of active substances and bioactivity of Aconitum sinomontanum Nakai[J].Nat Pro Res,2012,26(22):2099–2102.
[8]陈丽娟,唐希灿,王美瑛,等.刺乌头碱的毒性和致畸作用研究[J].上海实验动物科学,1989,9(1):5-7.
[9]魏华波,范艾玲,秦争平.注射用氢溴酸高乌甲素致耳毒性不良反应2例[J].中国医院药学杂志,2012,32(17):1413-1414.
[10]任媛媛,王 鹏,詹 妮.二萜生物碱生物活性和毒性的研究概况[J].中国实验方剂学杂志,2010,16(11):210-213.
[11]毛淑杰,李先端,顾雪竹,等.中药炮制辅料-醋的规范化示范性研究[J].中国中药杂志,2006,31(22):1916-1918.
[12]吴延吉.甘肃高乌头有效部位的研究[D].天津:天津大学,2007.
[13]李 飞,张世臣,杨 蕾,等.正交设计法优选乌头炮制工艺[J].北京中医药大学学报,1998,21(1):38-39.
[14]张姗姗,孙立立,石典花,等.不同炮制方法对甘遂急性毒性影响的研究[J].中成药,2012,34(11):2178-2180.
R283
B
1001-1528(2015)04-0905-05
10.3969/j.issn.1001-1528.2015.04.050
2014-08-07
甘肃省自然科学基金项目 (1107RJZA242);甘肃中医学院中青年基金项目 (ZQ2011-8)
李 芸(1973—),女,博士生,主要从事中药炮制学的教学和科研工作。E-mail:liyunherb@163.com
*通信作者:胡昌江(1952—),男,教授,博士生导师,主要从事中药炮制学的教学和科研工作。E-mail:hhccjj@hotmail.com
