回药哈黑里里方提取物纳米乳及其原位凝胶滴鼻液的研究
2015-01-16周成铭王亚楠张立明王文苹张万年
周成铭, 王亚楠, 张立明,2,3, 王文苹,2,3*, 张万年,2,3*
(1.宁夏医科大学药学院,宁夏银川750004;2.宁夏回药现代化工程技术研究中心,宁夏银川750004;3.宁夏医科大学回医药现代化省部共建教育部重点实验室,宁夏银川750004)
回药哈黑里里方提取物纳米乳及其原位凝胶滴鼻液的研究
周成铭1, 王亚楠1, 张立明1,2,3, 王文苹1,2,3*, 张万年1,2,3*
(1.宁夏医科大学药学院,宁夏银川750004;2.宁夏回药现代化工程技术研究中心,宁夏银川750004;3.宁夏医科大学回医药现代化省部共建教育部重点实验室,宁夏银川750004)
目的制备哈黑里里方 (乳香、胡椒、没药等)提取物纳米乳及其原位凝胶滴鼻液。方法用哈黑里里方超临界流体提取物、肉豆蔻酸异丙酯与乳化剂制备纳米乳,载入以去乙酰结冷胶为主要基质的体系得到鼻用原位凝胶液,采用伪三元相图选择纳米乳处方,并综合评价滴鼻液的性能。结果以吐温80-甘油 (2∶1)为混合乳化剂在伪三元相图纳米乳区的面积最大,当提取物∶混合乳化剂∶水质量比为0.20∶0.40∶0.40时制得的纳米乳平均粒径60.3 nm;以0.5%去乙酰结冷胶为基质、0.2%海藻酸钠为增黏剂时体系的胶凝行为最适,载纳米乳原位凝胶液与人工鼻液混合能形成强度、持水性和流变性均良好的凝胶。结论所得离子敏感型纳米乳原位凝胶滴鼻液粒径细小、稳定,适合性也符合鼻腔给药需求。
哈黑里里方;提取物;纳米乳;原位凝胶;滴鼻液
回医药学是阿拉伯医药学与中国医药学高度融合的民族性医药学,是东西方医药文化交流的结晶,具有深厚的回民族特色,尤其擅用香药[1]。哈黑里里方载于回医药学典籍 《回回药方》[2],由乳香、胡椒、没药、五倍子、番栀子花蕊 (西红花)、扁豆、撒额因 (阿魏)、芦荟、白荜拨、麝香、腽肭脐 (海狗肾)组成,将上述药材碾成粉末与勿忘草水调和,滴鼻用。研究[3]证实,哈黑里里方能够改善缺血性脑卒中后遗症患者症状,并能积极有效地干预该症病理进程。但该方工艺粗糙、用药量大、使用不便,为了改进剂型和工艺使之更符合现代用药需求。课题组前期采用超临界流体萃取法对处方药材进行提取[4],药材出油率为5.45%(g/g),采用GC-MS法分析提取物(油)成分,其中胡椒碱、愈创醇、没食子酸等在该药材提取物中占的比例较高。针对提取物的特性以及给药需求,本研究利用纳米乳和原位凝胶制剂技术对方剂提取物进行处置,并对所得制剂质量进行初步评价。
1 仪器与试药
PL203电子分析天平 (上海精密科学仪器有限公司);NICOMPTM380 ZLS亚微粒径分析仪(美国PSS公司);漩涡混合器 (太仓市科教器材厂);DV-Ⅲ流变仪(美国博勒飞公司);PHS-3 E型pH计 (上海仪电科学仪器股份有限公司)。
哈黑里里方提取物 (宁夏医科大学药学院自制);肉豆蔻酸异丙酯 (国药集团化学试剂有限公司,20130107);1,2-丙二醇 (天津市瑞金特化学品有限公司,20130504);吐温-80(Tween-80,天津市大茂化学试剂厂,20131026);Triton X-100(北京索莱宝科技有限公司,20130608);D-α生育酚聚乙二醇琥珀酸酯 (TPGS,武汉国邦达医药化工有限公司,G20140201);甘油 (天津市大茂化学试剂厂,20130414);聚乙二醇400(PEG-400,天津市大茂化学试剂厂,20130504);去乙酰结冷胶(Deacetylated gellan gurn,DGG,浙江天伟生化工程有限公司,130725);海藻酸钠 (天津市大茂化学试剂厂,F20130925);水为去离子水 (自制),其余试剂均为分析纯 (国药集团化学试剂有限公司)。
2 方法与结果
2.1 纳米乳的处方筛选
2.1.1 伪三元相图的制备[5]室温下,以肉豆蔻酸异丙酯:提取物 (1∶1)做为油相,将混合乳化剂与油相依次按照1∶9、2∶8、3∶7、4∶6、5∶5、6∶4、7∶3、8∶2、9∶1(m/m)不同比例混匀后逐滴加水,并涡旋混匀,当体系由暗黄色油体变为半透明有蓝色乳光时为临界点[6],计算各相变点时混合乳化剂、油相、水相的重量百分比,利用ORIGIN7.5软件绘制伪三元相图(阴影部分为纳米乳区)。
2.1.2 乳化剂的筛选 固定助乳化剂为甘油,乳化剂与助乳化剂比值Km为2∶1,分别以TPGS、TritonX-100和Tween-80为乳化剂绘制伪三元相图,结果见图1。

图1 不同乳化剂的伪三元相图Fig.1 Pseudoternary phase diagram s of different emulsifiers
由图1可知,纳米乳区域面积大小依次为Tween-80>TritonX-100>TPGS,其中以Tween-80作为乳化剂与挥发油混合稀释后乳化效果最佳,能形成均匀稳定的纳米乳,故选择Tween-80为乳化剂。2.1.3 助乳化剂的筛选 固定乳化剂为Tween-80,Km=2∶1,分别以1,2-丙二醇、PEG-400和甘油为助乳化剂绘制伪三元相图,结果见图2。
由图2可知,纳米乳区域面积大小依次为甘油>PEG-400>1,2-丙二醇,甘油助乳化效果最佳。且甘油具有保湿作用、无毒无刺激,适于鼻腔给药,因此选择甘油为助乳化剂。
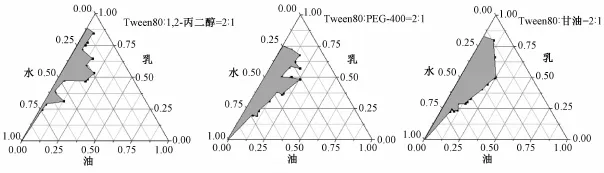
图2 不同助乳化剂的伪三元相图Fig.2 Pseudoternary phase diagrams in different auxiliary emulsifiers
2.1.4 Km值的确定 分别将Tween-80与甘油按照Km=1∶2、1∶1、2∶1的比例混合,绘制伪三元相图,结果见图3。

图3 不同Km的伪三元相图Fig.3 Pseudoternary phase diagram s of different Km values
由图3可知,当Km=2∶1时所得相图中纳米乳区域面积最大,当油相比例高达25%时仍可形成纳米乳。继续增加乳化剂用量可能乳化效果更佳,但考虑到乳化剂用量过大可能带来的刺激性问题,故将纳米乳处方中的Km值定为2∶1。
2.1.5 纳米乳处方的确定 根据上述结果,称取适量油相 (肉豆蔻酸异丙酯 ∶提取物=1∶1),然后将混合乳化剂(Tween-80∶甘油=2∶1)加入到油相中,涡旋均匀,逐滴加水到混合油相当中;当油-乳-水0.20∶0.40∶0.40时,体系载药量较高,形成的纳米乳外观半透明、具淡蓝色乳光,且此时乳化剂用量相对较低。
2.2 纳米乳的初步评价
2.2.1 外观 哈黑里里方提取物如图4-a所示;纳米乳如图4-b所示。
由图4可知,提取物 (图4-a)为暗红色黏稠状油体、气味芳香,与混合乳化剂混匀,采用滴水法制得纳米乳 (图4-b)为有蓝色乳光半透明的液体,流动性良好。

图4 提取物和纳米乳外观图Fig.4 Appearance of extract and its nanoemulsion
2.2.2 粒径及Zeta电位的测定 采用NICOMPTM380 ZLS亚微粒径分析仪分别测定纳米乳的粒径分布和Zeta电位。由图5知,平均粒径 (60.3± 10.8)nm,PI(Polydispersity Index)0.277± 0.15。Zeta电位(-1.63±0.02)mV,可能是由于吐温是非离子表面活性剂。
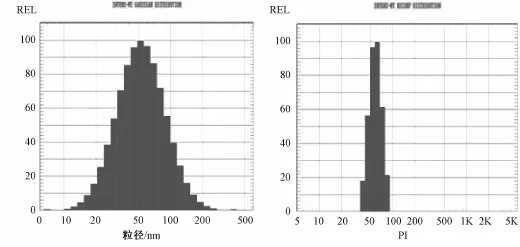
图5 纳米乳的粒径和PIFig.5 Particle size and PIof nanoemulsion
2.2.3 离心稳定性考察 12 000 r/min离心20 min后纳米乳与离心前相比无明显差异,体系不分层、无沉淀、均匀半透明,较稳定。
2.3 鼻用原位凝胶的制备
2.3.1 人工鼻液的配制 根据文献[7]配制,使1 L去离子水中含氯化钠7.91 g、碳酸氢钠2.56 g、氯化钾3.68 g和氯化钙0.51 g,溶解混匀即得。
2.3.2 凝胶基质的筛选 参考文献[8]方法,分别以不同浓度的DGG为基质、海藻酸钠为增黏剂配制凝胶溶液,将凝胶液与人工鼻液按比例 (V/ V,25∶7)混匀,体系迅速胶凝 (30 s),使用DV-Ⅲ流变仪考察体系的黏度变化 (63号转子,25℃,转速50 r/min),结果见图6。
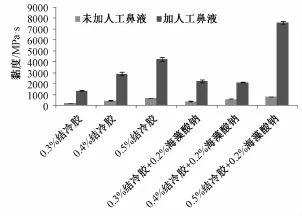
图6 原位凝胶材料及浓度对体系胶凝行为的影响Fig.6 Effect of in-situ gel on system atic gelling behavior of the system
原位凝胶系统在体外为低黏度的流体,生理条件下如温度,pH值等,自身将会产生溶液—凝胶的相转变[9]。由图6可知,凝胶黏度随DGG质量分数增大而增大,0.2%海藻酸钠的加入能进一步提高体系黏度。与人工鼻液混合后,体系黏度迅速提高。其中,含0.5%DGG和0.2%海藻酸钠的体系与人工鼻液混合前后的黏度差值最大,形成的凝胶稳定。低黏度的溶液滴入鼻腔后容易流出,且鼻纤毛的清除作用会使制剂滞留时间短,而黏度太高不易滴出和使用,因此选择“0.5%DGG+ 0.2%海藻酸钠”作为凝胶基质。
2.3.3 载纳米乳鼻用原位凝胶制备 将0.67 g油相、0.89 g Tween-80和0.44 g甘油加至试管中涡旋混匀,逐滴加入去离子水至形成纳米乳,再将含0.5%DGG及0.2%海藻酸钠的凝胶液与纳米乳以3∶1(V/V)的比例混合均匀,即得纳米乳原位凝胶剂。
2.4 原位凝胶的体外评价
2.4.1 外观 考察载纳米乳原位凝胶液与人工鼻液混合前后的外观,结果见图7。

图7 制剂胶凝前后的外观图Fig.7 Preparation appearance before and after being m ixed w ith artificial nasal drops
由图7可知,未加人工鼻液的纳米乳原位凝胶液 (图7-a)为略带乳光的半透明黏性溶液、流动性良好;加人工鼻液后体系 (图7-b)凝胶化、颜色加深,倒置后不下流。
2.4.2 黏度测定 采用 《中国药典》2010年版二部附录ⅥG项下黏度测定第二法,测得原位凝胶液的平均黏度 (470.27±0.57)MPa·s(n=3),与人工鼻液混合后平均黏度骤升至 (5014.33± 30.44)MPa·s(n=3)。表明体系具有良好的胶凝性能。
2.4.3 pH测定 取适量凝胶样品用去离子水稀释100倍,用PHS-3E型pH计测得纳米乳原位凝胶的平均pH值为5.57±0.04(n=3),与正常人鼻腔分泌液pH值 (5.5~6.5)相近[10],无刺激性,适合鼻腔给药。
2.4.4 原位凝胶强度考察[11]取原位凝胶样品加入含有适量人工鼻液试管中,置于120 r/min(37℃)条件下气浴振荡,观察并记录凝胶溶蚀所需的时间。结果凝胶溶蚀时间为 (59±0.57)min(n=3)。这是因为所制备的凝胶为水凝胶,在弱酸性环境中,凝胶中高分子链变得卷曲,链间的疏水作用增强,从而使凝胶与水的作用减弱,导致凝胶溶蚀。Giammona等[12]采用PHEA为主体材料制得的凝胶也表现出同样的性质。
2.4.5 原位凝胶持水性考察[13]取原位凝胶与人工鼻液1∶1混合,静置1 min,转移至超滤离心管内管中 (避免破坏凝胶表面),称重 (记为m0),以4 000 r/min离心,于不同时间点取出内管分别称重 (记为m),以m/m0的值反应原位凝胶在外力作用下持水能力随时间的变化。结果发现凝胶在外力离心作用下30 min后持水率接近100%,凝胶持水性能良好。
2.4.6 流变学性质考察 采用DV-Ⅲ流变仪,分别考察原位凝胶在加入人工鼻液前后剪切速率增大时黏度和剪切应力的变化情况。控制温度为25℃,选择小量样品适配器 (SC4-31号转子),结果见图8。
由图8可知,未加人工鼻液条件下,黏度和剪切应力随剪切率的变化均不显著;加入人工鼻液后体系形成凝胶,黏度随剪切率增大而变稀,剪切应力随剪切速率增大迅速上升。随着剪切力作用的增加,体系的黏度减小,但当体系黏度降低到一定值后,黏度的变化趋于平稳,可能是由于凝胶具有剪切变稀的特性,剪切速率增大破坏了凝胶规则的空间结构,降低其黏度。
3 讨论
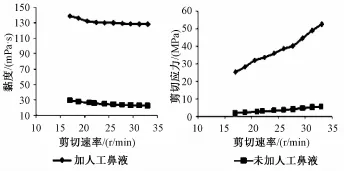
图8 剪切速率对体系黏度和剪切应力的影响Fig.8 Effect of shear rate on viscosity and shear stress of the system
原位凝胶有pH敏感、温度敏感和离子敏感[14]3种类型。其中,pH敏感型原位凝胶体外情况下一般为酸性,较低的pH对于鼻部刺激性较大,不宜鼻部给药;温度敏感型原位凝胶配方所需基质浓度高、常温下黏度大,不易滴出。鼻用原位凝胶必需于鼻黏膜呈现良好的胶凝能力及药物缓释作用,且无明显鼻黏膜刺激性。本研究结合DGG的阳离子响应特性和鼻腔的富阳离子环境,制备离子敏感型鼻用原位凝胶。DGG是一种对阳离子敏感的线性多糖,接触生理浓度的阳离子 (Na+、K+、Ca2+)时,结构中的葡萄糖醛酸被中和,结构发生阳离子介导的凝聚,形成半固体凝胶态[15]。人鼻腔分泌物富含Na+、K+、Ca+阳离子,离子浓度相对固定[16],使其能够在鼻腔形成黏度理想的凝胶。
实验结果表明,以0.5%DGG和0.2%海藻酸钠制备的凝胶基质最为适宜,既具有离子敏感特性,又避免黏度过高给制备及使用带来不便。流变学结果显示,所制原位凝胶具有假塑性流体学特性,即黏度随剪切率增大而降低 (切稀作用),这种流变学特性对对鼻腔的刺激较小,更易被患者接受;另外,这种流变学特性也使凝胶溶液易于搅拌、灌装,从而降低工业化生产的难度和成本。
4 结论
本研究针对回药哈黑里里方的鼻腔给药需求及提取物特点,将提取物制成纳米乳并载入离子型原位凝胶液中,不仅能使提取物高度分散为纳米级、利于透过鼻黏膜吸收入脑,且能显著延长给药局部的滞留时间、可望改善生物利用度,该制剂体系黏度小、便于制备和使用。本研究为回医药经方的现代研究和应用提供参考,也为相关新产品开发奠定了基础。
参考文献:
[1]张占武,刘敬霞.回医香药理论简述及临床应用[J].宁夏医科大学学报,2013,36(1):3-5.
[2]牛 阳.回药方研究[M].银川:黄河出版传媒集团阳光出版社,2010.
[3]刘耀龙,马晓东,丁小龙,等.试论 《回回药方》治疗脑系疾病滴鼻剂的剂型特点[J].西部中医药,2012,25(9):135-136.
[4]黎颖君,宋伟峰.超临界二氧化碳流体萃取三叶青藤挥发油成分分析[J].中国医药导报,2012,9(22):26-27.
[5]Shafiq-un-Nabi S,Shakeel F,Talegaonkar S,et al.Formulation development and optimization using nanoemulsion technique:a technical note[J].AAPS Pharm Sci Tech,2008,8(2):E1-E6.
[6]姜素芳,张雪萍,周学军.丹皮酚自微乳的制备和评价[J].中成药,2012,34(5):835-838.
[7]Carlfors J,Edsman K,Petersson R,et al.Rheological evaluation of Gelrite in situ gels for ophthalmic use[J].Eur JPharm Sci,1998,6(2):113-119.
[8]Cao SL,Ren XW,Zhang Q Z,etal.In situ gelbased on gellan gum as new carrier for nasal administration of mometasone furoate[J].Int JPharm,2009,365(1-2):109-115.
[9]陈两绵,王锦玉,仝 燕,等.黏膜给药原位凝胶的研究进展[J].中国实验方剂学杂志,2008,14(8):76-80.
[10]苏崇周,张正侯,韩绍哲,等.鼻炎、鼻窦炎鼻腔分泌物溶菌酶及pH值测定[J].中华耳鼻咽喉科杂志,1987,22(1):61.
[11]曹师磊,徐 丰,蒋新国,等.离子敏感鼻用原位凝胶的制备及其兔消除动力学[J].中国药学杂志,2007,42(11):844-847.
[12]Pitarresi G,Casadei M A,Mandracchia D,et al.Photocrosslinking of dextran and polyaspartamide derivatives:a combination suitable for colon-specific drug delivery[J].JControl Release,2007,119(3):328-338.
[13]Mao R,Tang J,Swanson B G.Water holding capacity and microstructure of gellan gels[J].Carbohyd Polym,2001,46(4):365-371.
[14]陶 涛,岳 鹏,赵 雁,等.石杉碱甲鼻用原位凝胶喷雾剂的制备及稳定性研究[J].中国新药杂志,2006,15(22):1950-1954.
[15]Robinson G,Manning C E,Morris E R.Conformation and physical properties of the bacterial polysaccharide Gellan,Welan and Rhamsan[M].London:Royal Society of Chemistry,1991:22-33.
[16]Lorin M I,Gaerlan P F,Mandel ID.Quantitative composition of nasal secretions in normal subjects[J].J Lab Clin Med,1972,80(2):275-281.
Nanoemulsion and in-situ gel nasal drops of Haheililiextract
ZHOU Cheng-ming1, WANG Ya-nan1, ZHANG Li-ming1,2,3, WANGWen-ping1,2,3*,ZHANGWan-nian1,2,3*
(1.Schoolof Pharmacy,Ningxia Medical University,Yinchuan 750004,China;2.Ningxia Engineering&Technology Research Center For Modernization of HuiMedicine,Yinchuan 750004,China;3.Ningxia Medical University,Key Laboratory of Hui EthnicMedicineModernization,Ministry of Education,Yinchuan 750004,China)
AIMTo prepare nasal drops composed of nanoemulsion and in-situ gel of the oil fraction extracted from Hahelili Formula(Olibanum,Piperis Fructus,Myrrha,etc).METHODSThe oil fraction was obtained by supercritical fluid extraction.The nanoemulsion of oil extractwas prepared using isopropylmyristate and emulsifiers according to pseudo-ternary phase diagrams.The nanoemulsion was loaded into deacetylated gellan gum to form in-situ gel system for nasaladministration,and the performance of in-situ gelwas evaluated.RESULTSThe co-surfactant system of tween-80 and glycerinum(2∶1)showed themaximum nanoemulsion area.Themean particle size of obtained nanoemulsion was60.3 nm at 0.20∶0.40∶0.40 ratio of oil extract,emulsifier and water. The nanoemulsion-loaded in situ gel,consisting of0.5%gellan gum and 0.2%sodium alginate as gellingmaterials,showed favorable gel formation.Strong gelwith excellentwater-binding capacity and rheological property could be formed after being mixed with artificial nasal drops.CONCLUSIONThe obtained nanoemulsion possesses small particle size and good stability,and the in situ gel system shows excellentgelling property which canmeet the requirementof intranasal administration.
Hahelili Formula;extract;nanoemulsion;in situ gel;intranasal administration
R944
:A
:1001-1528(2015)06-1210-06
10.3969/j.issn.1001-1528.2015.06.012
2014-10-15
国家科技支撑项目 (2013BAI11B07);宁夏回族自治区科技攻关计划项目 (2013)
周成铭 (1987—),男,硕士,研究方向为新型载药材料及给药系统。Tel:18295076567,E-mail:z_dahai0806@126.com
*通信作者:王文苹 (1977—),女,博士,教授,研究方向为新型载药材料及给药系统。Tel:(0951)-6880581,E-mail:wangwenpingg@sina.com张万年 (1947—),男,教授,博士生导师,研究方向为药物分子设计及抗肿瘤药物。Tel: (0951)6980189,E-mail:zhangwnk@sina.com
