降血压水包油微乳巴布剂的制备
2015-01-13张广唱郭殷锐武哲丽
张广唱, 郭殷锐, 王 剑, 武哲丽*
(1. 广州中医药大学 广东省中医治法与中药创制研究重点实验室,广东 广州510006;2. 广州中医药大学,广东广州510006)
降血压水包油微乳巴布剂是由吴茱萸和川芎两味药组成,对高血压、心绞痛等疾病的治疗具有显著效果。吴茱萸Evodia rutaecarpa 具有散寒止痛、降逆止呕、助阳止泻之功效。外用贴于涌泉穴具有引火下行作用,临床常用于治疗高血压、头痛等疾病[1]。吴茱萸碱(evodiamine,EVO)和吴茱萸次碱(rutaecarpine,RUT)是其主要的有效活性成分,现代药理研究发现其具有降压、强心、抗心律失常、抗血栓等作用[2-3]。川芎具有行气活血,祛风止痛功效,临床上广泛用于头痛、冠心病、高血压等,其所含有效成分为川芎嗪和阿魏酸等[4]。
微 乳 (microemulsion,ME) 也 称 纳 米 乳(nanoemulsion)是粒径为10 ~100 nm,由水、油、表面活性剂和助表面活性剂组成的一种流动、透明、热力学稳定、均质性的液体。其主要优点在于可增加难溶性药物的溶解度、延长作用时间、口服或外用均可提高生物利用度[5-6],表面活性剂HLB值在8 ~18 可以形成O/W 型微乳。巴布剂(cataplasm)系指将药物加入水溶性高分子化合物作为基质所制成的贴膏剂。相对于其他外用贴膏,巴布剂具有载药量大,透气性、保湿性好,刺激性小,应用方便等优点[7]。由于吴茱萸中有效成分吴茱萸碱、吴茱萸次碱为脂溶性,难溶于水,而巴布剂基质主要由水溶性基质组成,脂溶性成分难于通过水溶性基质进入皮下发挥药效。而采用O/W 微乳技术,可有效提高脂溶性有效成分的经皮透过率。本实验在确定降血压水包油微乳的最佳处方及用量基础上,以初黏力、内聚力、皮肤追随性、外观性状和反复揭贴性为考察指标,采用正交试验设计优选降压水包油微乳巴布剂基质配比。
1 仪器与试药
1.1 仪器 HH-50L 循环水反应釜(开封市宏兴科教仪器厂);RE-3005 旋转蒸发仪(巩义市予华仪器有限公司);YB-P6 型智能透皮仪(天津药典标准仪器厂);KQ-500DE 型数控超声波清洗器(昆山市超声仪器有限公司);AUI220 分析天平(广州湘仪机电设备有限公司);LC-20A 高效液相色谱仪(岛津,日本);QYYS-20A 超纯水机(重庆前沿水处理设备有限公司);LY-105N 型管式离心机(辽阳阳光制药机械有限公司);SS 型三足式离心机(张家港市润星机械厂);FY-6032 初黏性测试仪(深圳市方源仪器有限公司);WN801 激光粒度分析仪(济南微纳仪器有限公司);8S-1 磁力搅拌器(常州普天仪器制造有限公司)。
1.2 试药 冰片(阿拉丁,批号11182);明胶(天津市大茂化学试剂厂,批号20140810);卡波姆(天津市大茂化学试剂厂,批号20140116);酒石酸(天津市大茂化学试剂厂,批号20140305);甘油(天津市大茂化学试剂厂,批号20140312);Viseomate-NP800 (天津市福晨化学试剂厂);甘羟铝(天津市富于精细化工有限公司,批号20140215)。乙醇(天津市致远化学试剂有限公司,批号20140512);乙腈(色谱纯,Dikma,批号608001003);四氢呋喃(天津市大茂化学试剂厂,批号20140206);冰醋酸(天津市致远化学试剂有限公司,批号20140208);肉豆蔻酸异丙酯(阿拉丁,批号110270);吐温-80 (天津市大茂化学试剂厂,批号20140316);CO-40 氢化蓖麻油(天津市大茂化学试剂厂,批号20140309);氯化钠(天津市致远化学试剂有限公司,批号20131009)。吴茱萸(广州南北行中药饮片有限公司,批号20140503G322);川芎(广州南北行中药饮片有限公司,批号20140506G106)。
2 方法与结果
2.1 川芎、吴茱萸有效部位的提取及分离
2.1.1 吴茱萸提取分离[8]将4.5 kg 吴茱萸置烘箱干燥24 h,再置于循环水反应釜中,加入10 倍量70%乙醇,80 ℃加热回流2 h,提取3 次,将提取液浓缩至含生药量1 g/mL,放置于4 ℃冰箱10 d,将浓缩液离心,离心药液减压浓缩。所得浓缩液经D101 大孔树脂纯化,弃3 BV 纯水与20%乙醇洗脱液,收集70%乙醇洗脱液,浓缩至浸膏状,浸膏经乙酸乙酯萃取3 次,乙酸乙酯萃取部位挥去有机溶剂,冷藏备用。
2.1.2 川芎提取分离[9]将10 kg 川芎置烘箱干燥24 h,加入足量70%乙醇渗漉,至浸出液颜色近无色为止,离心,收集上清液减压浓缩至浸膏状。加入少量蒸馏水溶解浸膏,经D101 树脂纯化,弃3 BV 纯水与20%乙醇洗脱液,收集70%乙醇洗脱液,减压浓缩至浸膏,冷藏备用。
2.2 降压水包油微乳的制备 精密称取吴茱萸和川芎精制提取物,加入肉豆蔻酸异丙酯,水浴加热溶解,加入适量95%乙醇助溶,再加入乳化剂搅拌均匀,再加入助乳化剂,在25 ℃恒温磁力搅拌器边搅拌边滴加超纯水,至微乳形成澄清透明流动性良好的微乳。记录乳液由稀变稠和再由稠变稀相变点水的用量,以确定微乳区界限。
2.3 水包油微乳处方的优选 根据微乳形成的基本原理和预试验初步确定如下试验用数据。表面活性剂与助表面活性剂的内部比(Km值)为1 ∶1、2 ∶1、3 ∶1。表面活性剂和助表面活性剂混合溶液与油相以9.5 ∶0.5、9 ∶1、8 ∶2、7 ∶3、6 ∶4、5 ∶ 5、4 ∶6、3 ∶7、2 ∶8、1 ∶9、0.5 ∶9.5 比例进行设组,作为试验用统一数据。Origin 8.0 软件对数据进行处理并绘制拟三元相图,结果见表1。
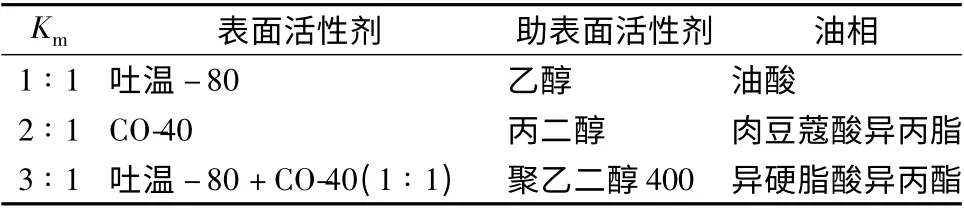
表1 水包油微乳处方因素Tab.1 Prescription factors for oil-in-water microemulsion
2.3.1 油相的选择 分别称取3 份等量的吴茱萸和川芎干燥精制提取物,加入等量的油酸、异硬脂酸异丙脂和肉豆蔻异丙脂,搅拌均匀后超声1 h,放置24 h,离心,取上清液,HPLC 测定吴茱萸碱、吴茱萸次碱和阿魏酸的含有量。结果3 种有效成分在肉豆蔻酸异丙酯中溶解度最大,因此选肉豆蔻酸异丙酯作为油相。
2.3.2 表面活性剂的选择 选用HLB 值为8 ~18的表面活性剂,即吐温-80、CO-40、吐温-80 与CO-40 混合体系 (1 ∶1)。经过预实验可知吐温-80与CO-40 混合体系形成的水包油微乳区较大,因此选用吐温-80 与CO-40 (1 ∶1)混合体系作为表面活性剂。
2.3.3 助表明活性剂的选择及其微乳体系的制备现象
2.3.3.1 吐温-80-CO-40-聚乙二醇400-肉豆蔻酸异丙酯体系 按照“2.2”项方法制备微乳,该体系在Km=1 ∶1、Km=2 ∶1、Km=3 ∶1 时,都不能形成澄清透明微乳。
2.3.3.2 吐温-80-CO-40-乙醇-肉豆蔻酸异丙酯体系 按照“2.2”项方法制备微乳,当Km=1 ∶1时,该体系在9.5 ∶0.5、9 ∶1、8 ∶2 比例形成澄清透明微乳,在7 ∶3 比例形成半透明乳液,其余比例形成凝胶。Km=2 ∶1 时,该体系在9.5 ∶0.5、9 ∶1、8 ∶2 比例形成澄清透明微乳,在7 ∶3 比例形成半透明乳液,其余比例形成凝胶。Km=3 ∶1时,该体系在9.5 ∶0.5、9 ∶1 比例形成澄清透明微乳,在8 ∶2、7 ∶3 比例形成半透明乳液。其余比例形成凝胶。但该体系所形成的澄清透明微乳在室温下暴露放置一天会变浑浊,稳定性差。
2.3.3.3 吐温-80-CO-40-丙二醇-肉豆蔻酸异丙酯体系 按照“2.2”项方法制备微乳,当Km=1∶1 时,该体系在9.5 ∶0.5、9 ∶1 比例能形成澄清透明微乳,在8 ∶2 比例形成半透明乳液,其余比例形成凝胶。Km=2 ∶1 时,该体系在9.5 ∶0.5、9 ∶1、8 ∶2 比例能形成澄清透明微乳,在7 ∶3 比例形成半透明乳液。其余比例形成凝胶。Km=3 ∶1 时,该体系在9.5 ∶0.5、9 ∶1 能形成澄清透明微乳,在8 ∶2、7 ∶3 比例形成半透明乳液,其余比例形成凝胶。该体系所形成的微乳较稳定,室温暴露放置性状不变。故选用丙二醇作为该体系的助表面活性剂。
2.3.4 Km值的选择 分别固定Km为1 ∶1、2 ∶1、3 ∶1,将表面活性剂和助表面活性剂的混合溶液与油相按9.5 ∶0.5、9 ∶1、8 ∶2、7 ∶3、6 ∶4、5 ∶5、4 ∶6、3 ∶7、2 ∶8、1 ∶9、0.5 ∶9.5 比例磁力搅拌混匀,室温下磁力搅拌时向混合液中滴加定量蒸馏水,观察体系由稀变稠和由稠变稀的临界点并记录水的用量。计算临界点体系各相组成部分的比例,origin 8.0 软件作伪三元相图,并计算相应相图的O/W 型微乳区面积,结果见图1 (水作为一个顶点,表面活性剂与助表面活性剂的总量作为一个顶点,油作为一个顶点,所形成的左下角闭合区域为O/W 微乳区)。不同Km下的O/W 型微乳的面积是Km=2 ∶1 >Km=3 ∶1 >Km=1 ∶ 1,故选择Km=2 ∶1,并从图中微乳区内选混合表面活性剂溶液与油相在9.5 ∶0.5 比例所对应的处方量作为水包油微乳配方,即吐温-80 ∶CO-40 ∶ 丙二醇∶肉豆蔻酸异丙酯∶水= 3.2 ∶3.2 ∶ 3.2 ∶0.5 ∶15.6。通过该微乳处方对吴茱萸和川芎提取物溶解度的考察,最佳溶解量均为0.15 g。
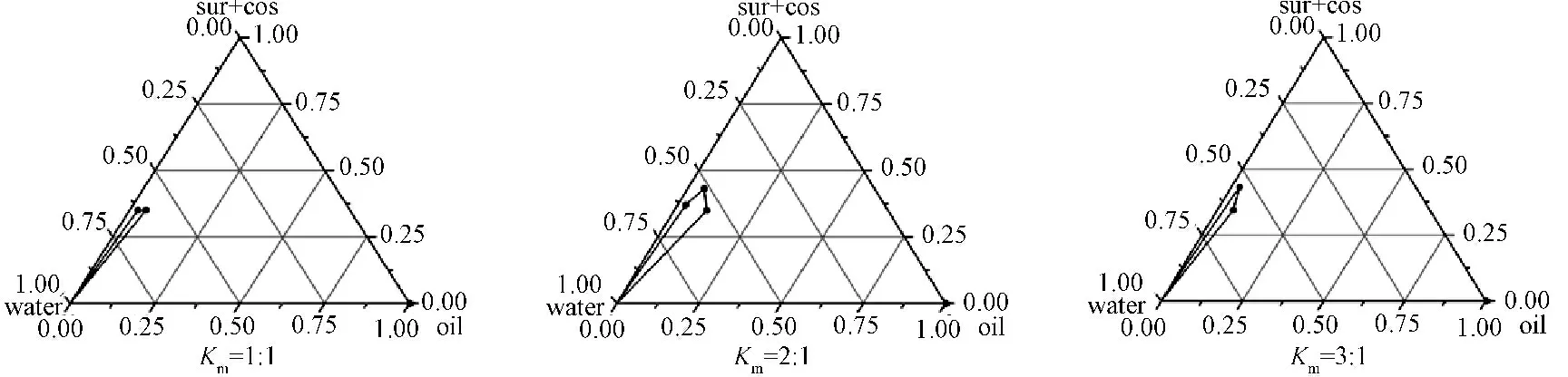
图1 不同Km值的伪三元相图Fig.1 Pseudo ternary phase diagrams with different Km
2.3.5 微乳类型的鉴定 15 000 r/min 离心15 min,不分层。采用染色法[10],用油溶性染料苏丹红和水溶性染料亚甲蓝在微乳中红色和蓝色的扩散速度快慢来判断微乳的类型,若红色扩散快于蓝色则为W/O 型微乳,反之为O/W 型微乳。结果,按上述方法制备微乳配方离心不分层,蓝色快于红色,即为水包油微乳。
2.3.6 粒度检测 测试温度25 ℃,分散介质为水,介质黏度8.904 × 10-4Pa·s,介质折射率1.333,角度90.0 Deg,延迟时间5 μs。测试结果Xav =50.57 nm,分散指数PI =0.470 2,见图2。

图2 微乳粒径检测条件及结果Fig.2 Condition and result of microemulsion particle size test
2.4 水包油微乳巴布剂的制备 将1 g 卡波姆用水定容至100 mL,充分搅拌,放置24 h 使其完全溶胀成1%卡波姆凝胶备用。先量取甘油置于烧杯中,然后加入NP-800,搅拌均匀,再加入甘羟铝(先用水溶解)搅拌1 min,作为A 相。另外取一烧杯加入水和明胶,80 ℃水浴溶解,待充分溶解后加入酒石酸,作为B 相。再取一定量制备好的微乳加入卡波姆(用三乙醇胺调至中性),两者混合均匀作为C 相。然后先将B 相加入A 相中,搅拌5 min 至均匀。再将C 相加入混合均匀的A 相中搅拌10 min,至膏体均匀没有结块。再加入促渗剂冰片(适量无水乙醇溶解),搅拌5 min,促渗剂分布均匀即可涂布成10 cm ×10 cm 大小,背面朝上放置一天晾干成型。
2.5 基质处方评分指标考察 参考文献[11],本实验选用双面拒水无纺布作为巴布剂的背衬材料,并以内聚力、初黏力、皮肤追随性、反复揭贴性和外观性状为综合考察指标。
2.5.1 内聚力测定[12]将3 cm ×3 cm 的巴布剂贴在垂直不锈钢板上,下端2 cm 处挂700 g 的砝码,记录巴布剂滑移直至脱离的时间,用秒表记数。
2.5.2 初黏力测定[13]参照2010 年版《中国药典》一部贴膏剂黏附力测定法第一法。取供试品3片,置于倾斜角30°的倾斜板中央,膏面向上,斜面上部10 cm 及下部15 cm 用0.025 mm 厚的涤纶薄膜覆盖,中间留出5 cm 膏面,分别取不同规格的钢球,自斜面顶端自由滚下。供试品中,3 片应有2 片或2 片以上能在测试段上粘住钢球,如有1片不能黏住,再用较小一号的钢球试验,应能黏住;如有1 片能黏住,而另2 片只能黏住较小一号的钢球,则应另取3 片复试。
2.5.3 感官评分 ①皮肤追随性:取成型巴布剂3 片,每次取一片贴于手背,用力甩动10 次未脱落者为满分20 分。②外观性状:色泽均匀,膏体表面光洁,无颗粒感为满分20 分。③反复揭贴性:反复揭贴10 次后仍保持良好的黏性为满分20 分。
2.5.4 评分标准[14]感官评分总分60 分,包括外观性状、皮肤追随性和反复揭贴性这3 个指标,各满分为20 分;初黏力满分20 分;内聚力满分20 分。综合评分为感官评分、初黏力和内聚力的总和,满分100 分。具体见表2。
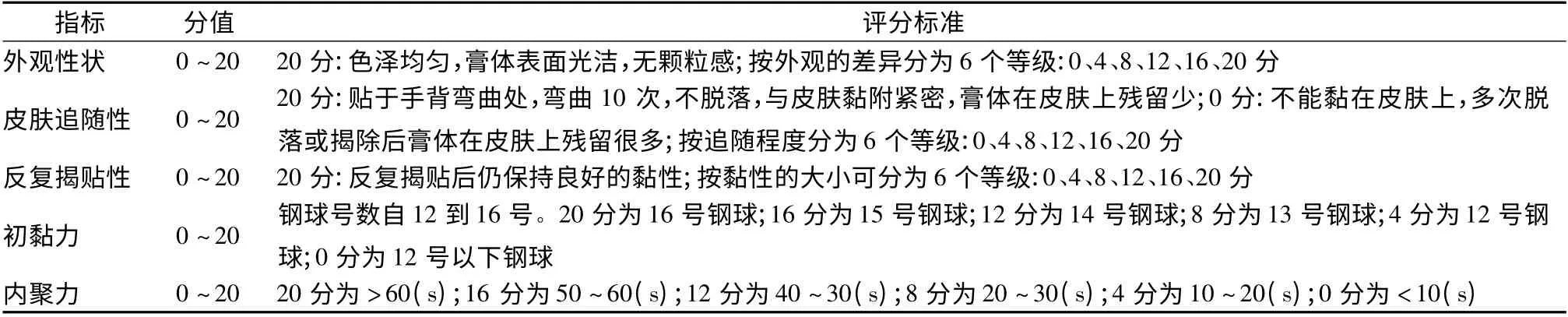
表2 巴布剂评分标准Tab.2 Criteria for scoring cataplasm
2.6 正交试验优化水包油微乳巴布剂基质处方根据预试验,初步确定微乳、NP-800、水和酒石酸作为微乳巴布剂的基本骨架,用量比例为20 ∶2 ∶18 ∶0.05。以甘羟铝,甘油,卡波姆,明胶作为考察因素。基于处方的单因素考察确定水平范围,采用L9(34)正交表进行实验设计。因素水平见表3,正交试验结果见表4,方差分析结果见表5。
实验结果表明,影响微乳巴布剂质量影响程度依次为B >A >C >D,以极差最小的D 因素为误差项进行方差分析,影响因素B (甘羟铝)是影响水包油微乳巴布剂的主要因素,A 因素(甘油)为次要因素,C 因素(明胶)影响不显著,结合直观分析结果,确定正交试验优选制备工艺为A2B1C2D4,即NP-800 ∶甘油∶甘羟铝∶水∶明胶∶酒石酸∶卡波姆∶微乳=2 ∶13 ∶0.04 ∶18 ∶4.5 ∶0.05 ∶6 ∶20。
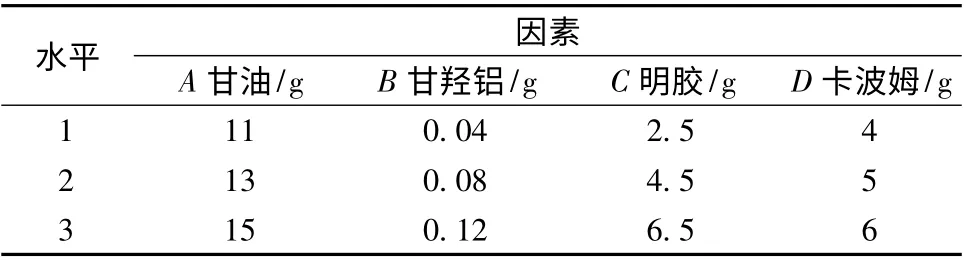
表3 因素水平Tab.3 Factors and levels
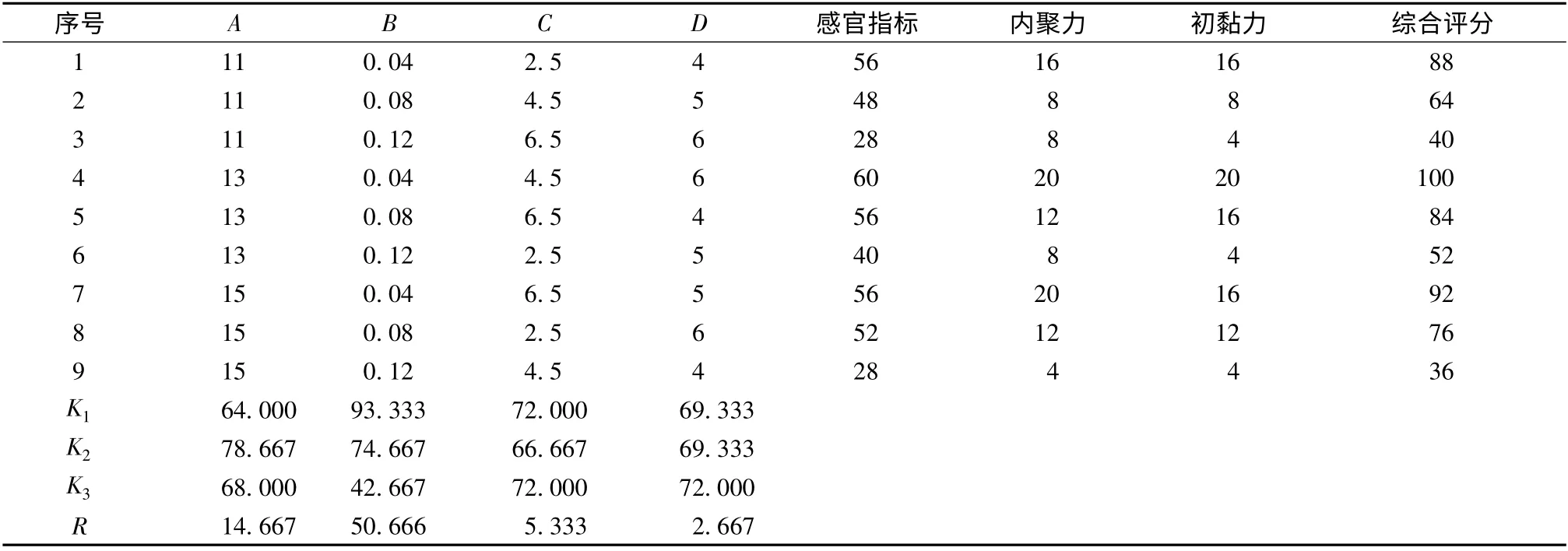
表4 正交试验结果(n=3)Tab.4 Result of orthogonal tests (n=3)
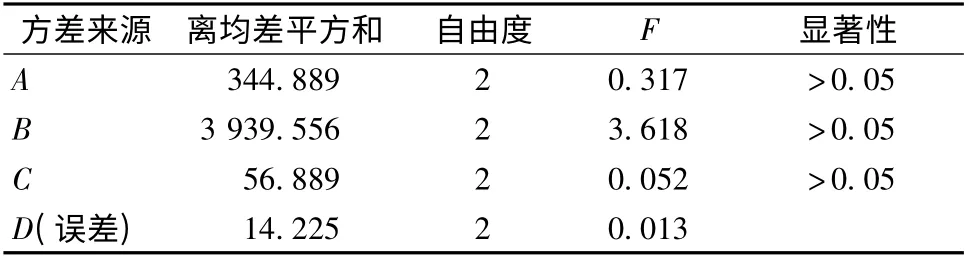
表5 方差分析结果Tab.5 Result of variance analysis
2.7 最佳处方的验证 以优选的工艺条件制备3批样品,测定其评价指标,并进行综合评定。结果以优化处方工艺制备的微乳巴布剂物理性能良好,综合评分高,表明所选工艺合理、可行。验证试验结果见表6。

表6 验证试验结果Tab.6 Result of verification tests
2.8 配方稳定性考察 把制备好的微乳巴布剂室温下存放30 d,膏体保湿性、黏性、柔软性均符合巴布剂的质量标准要求。
3 讨论
利用水包油微乳技术与常规巴布剂结合,可以使吴茱萸和川芎脂溶性有效成分更容易通过水溶性巴布剂基质进入皮下。在水包油微乳巴布剂的制备研究过程发现其质量控制的一些关键问题:水的用量是影响巴布剂药物释放的关键因数,它可以使皮肤角质层水化,增加皮肤的通透性,而且对膏体的黏性也有一定的影响。含水量太少会影响药物释放,降低黏性,太多则会使膏体太软,内聚力不足。甘羟铝是巴布剂的交联剂,它的用量对巴布剂的膏体的黏性影响最大。用量过低,会造成膏体内聚力小,容易产生残留,过量则会造成膏体过硬,黏性过小。在制备微乳巴布剂过程中,已有的巴布剂配方不适合微乳巴布剂的制备,原因可能是微乳含有大量的表面活性剂和助表面活性剂,给巴布剂的制备造成了一定的困难。微乳巴布剂膏体的形成过程对基质的混合顺序、混合速度、混合方法有较高要求。
本实验只验证了几种油相和表面活性剂、助表面活性剂形成微乳的工艺在巴布剂上的应用,研究发现乙醇作为助表面活性剂较容易形成微乳,但其稳定性差,容易挥发,故不适合微乳的制备。本实验对其他微乳材料的工艺研究只能提供参考和方法。现在国际上对微乳作为药物载体的应用前景的态度十分乐观,而中药有效成分大多数是脂溶性成分,特别是巴布剂制备中,亲水性基质限制了巴布剂的制备和推广,因此开发新的微乳制备工艺并将微乳工艺更好的应用在巴布剂制备上是未来的巴布剂发展方向之一。
[1] 许敏利. 吴茱萸粉调醋敷涌泉治疗高血压疗效观察[J]. 按摩与康复医学:中旬刊,2012,3(11):369.
[2] 胡长平,李元建. 吴茱萸碱和吴茱萸次碱的药理学研究进展[J]. 中国药理学通报,2003,19(10):1084-1087.
[3] 龚慕辛,王智民,张启伟,等. 吴茱萸有效成分的药理研究进展[J]. 中药新药与临床药理,2009,20 (2):183-184.
[4] 金玉青,洪远林,李建蕊,等. 川芎的化学成分及药理作用研究进展[J]. 中药与临床,2013,4(3):44-45.
[5] Pouton C W. Formulation of self-emulsifying drug delivery systems[J]. Adv Drug Deliv Rev,1997,25(1):47-58.
[6] Kawakami K,Yoshikawa T,Hayashi T,et al. Microemulsion formulation for enhanced absorption of poorly soluble drugs. II.In vivo study[J]. J Control Release,2002,81(1-2):75-82.
[7] 李 晋,胡晋红,朱全刚,等. 酮洛芬巴布剂的研制及体外透皮研究[J]. 药学服务与研究,2006,6(5):338-341.
[8] Wang C,Wang M W,Tashiro S,et al. Evodiamine induced human melanoma A375-S2 cell death partially through interleukin 1 mediated pathway[J]. Biol Pharm Bull,2005,28(6):984-989.
[9] 刘 旭,杨雪梅,徐江平,等. 正交试验对川芎提取工艺的筛选研究[J]. 广东药学,2003,16(13):3-5.
[10] Ho H O,Hsiao C C,Sheu M T. Preparation of microemulsions using polyglycerol fatty acid esters as surfactant for the delivery of protein drugs[J]. J Pharm Sci,1996,85(2):138-143.
[11] 刘淑芝,郭春燕,金日显. 中药巴布剂研究思路与方法[J]. 中国实验方剂学杂志,2007,13(5):62-64.
[12] 柳正青,胡晋红,朱全刚,等. 盐酸格拉司琼巴布剂基质处方设计[J]. 中国新药杂志,2006,15(17):1467-1470.
[13] 国家药典委员会. 中华人民共和国药典:2010 年版一部[S]. 北京:中国医药科技出版社,2010:附录74.
[14] 薛宝娟,龙致贤,王玉蓉. 均匀设计法优选玄麝止痛巴布剂基质配方研究[J]. 中药新药与临床药理,2008,19(6):499-501.
