酸浸-摇床重选预处理对钴矿石生物浸出的影响
2015-01-12杨洪英佟琳琳陈国宝金哲男
刘 伟,杨洪英,佟琳琳,陈国宝,金哲男
(东北大学 材料与冶金学院, 沈阳 110819)
本文所研究的钴矿石为国外某矿山选矿过程中的中间产品,该矿石中金属矿物主要为硫铜钴矿、黄铁矿、黄铜矿、斑铜矿等,脉石主要为石英、斜长石、硅酸钙、碳酸钙、碳酸镁等,含量(质量分数)达80%以上,其中碳酸钙、碳酸镁等可溶性碱性脉石含量约占脉石总量的30%.若采用传统火法冶炼工艺回收钴,不但成本高、污染环境,而且此工艺的附加产品—硫酸会使该矿山火法冶炼系统生产的硫酸无法消耗的形势更加严峻.细菌冶金技术被誉为21世纪矿产资源加工的战略性技术,在处理低品位、难处理矿产资源方面具有成本低、环境污染小等优势,且无附加产品硫酸的生成.经过众多学者的不懈努力[1~6],生物浸出提钴工艺不断发展与完善,继铜、金、铀之后第四个实现产业化[7].因此,采用微生物浸出技术从矿石中回收钴对该矿山是一个理想的选择.
在生物浸出过程中,大量可溶性碱性脉石的存在将造成浸出体系酸度不稳定,影响矿物浸出.同时过多的可溶性钙盐的溶解会导致矿浆中CaSO4达到饱和浓度而呈固体析出,并沉积于矿粒表面,阻碍矿物进一步氧化溶解[8].针对该钴矿石原料中含有大量可溶性碱性脉石的特点,本文提出酸浸—摇床重选除可溶性碱性脉石的预处理方案.此方案可将矿石中的可溶性碱性脉石除去,防止在生物浸出过程中因可溶性碱性脉石的溶解而对浸出造成的不良影响,提高钴的浸出速率与浸出率.同时硫酸的使用也会解决该矿山大量硫酸无法消耗的问题.该工艺为此类矿物的开发利用提供了一条新的途径.
1 实验材料与方法
1.1 实验材料
(1)矿样.本研究所用矿样为国外某矿山选矿过程中的中间产品,其化学成分见表1.通过工艺矿物学研究表明,该矿石中含钴矿物为硫铜钴矿(如图1所示),大部分为单体硫铜钴矿,还有部分为连生体.铜矿物主要为黄铜矿、斑铜矿、辉铜矿、铜蓝等.硫化铁矿物主要为黄铁矿.黄铜矿与黄铁矿的赋存状态与硫铜钴矿相似,大部分为单体矿物,少部分为连生体.斑铜矿、辉铜矿、铜蓝主要以与其他硫化矿物或脉石矿物连生形式赋存,单体出现的很少.脉石矿物主要为石英、斜长石、硅酸钙、碳酸钙、碳酸镁等.

图1 硫铜钴矿的SEM图与EDS能谱分析Fig.1 SEM image and EDS analysis of carrollite

(2)菌种与培养基.实验所用菌种为ZY101菌,该菌种是以氧化亚铁硫杆菌为主的混合菌.经过驯化,该菌种具有优良的抗钴特性.采用9K培养基,各组分的质量浓度分别为:(NH4)2SO43.00 g·L-1,K2HPO40.10 g·L-1,KCl 0.50 g·L-1,MgSO4·7H2O 0.50 g·L-1,Ca(NO3)20.01 g·L-1,FeSO4·7H2O 44.3 g·L-1.
(3)实验设备与仪器.HZQ-QX型恒温振荡箱,TU-1901双光束紫外可见分光光度计,SSX-550型扫描电子显微镜,矿用6-S曲波面摇床,TG-WS台式离心机等.
1.2 实验方法
1.2.1 酸浸—摇床重选预处理
将 1 000 g 原矿石加入酸浸槽中,加入3 L水调浆.滴加稀硫酸溶液(浓硫酸与蒸馏水按照1∶1的体积比配制),控制矿浆pH值在1.5~2.0之间,直至矿浆pH值稳定.利用生成的硫酸钙沉淀与矿物的密度不同,通过摇床重选将生成的硫酸钙沉淀与矿物分离除去.矿物烘干、细磨至粒度为小于38 μm占80%,备用,简称酸浸矿.
1.2.2 生物浸出实验
向200 mL培养至稳定初期的菌液中加入20 g酸浸矿(对比试样则加入相同质量的原矿).调节矿浆的初始pH值为1.5(原矿试样要待其pH值稳定在1.5不变时停止调节),在温度为44 ℃、转速为180 r/min的恒温振荡箱中进行浸出,并定时监测Fe2+、Co2+、TFe等离子浓度.Co2+质量浓度用亚硝基R盐光度法测定,Fe2+质量浓度用重铬酸钾滴定法测定,TFe质量浓度用三氯化钛还原—重铬酸钾滴定法测定.
2 结果与讨论
表2所列为酸浸—摇床重选预处理实验结果,该结果为5组平行实验的平均值.经过酸浸—摇床重选预处理后,酸浸矿中钙含量(质量分数)由8.61%降至2.87%,去除率达74.32%;钴含量(质量分数)由1.25%上升至1.62%,损失率为0.15%.可见,经过预处理大量的可溶性钙盐被除去,防止了浸出过程中生成的CaSO4由于浓度达到饱和而呈固体析出,沉积于矿粒表面的现象.同时钴的损失率仅为0.15%,没有造成有价金属的大量损失.

表2 酸浸—摇床重选预处理实验结果
图2为浸出过程中Fe2+的质量浓度ρ(Fe2+)变化曲线图.浸出过程中,含铁硫化矿物在Fe3+与细菌的共同作用下氧化分解释放出Fe2+[9,10],Fe2+通过细菌细胞壁上的微孔渗透到细胞壁内进入周质间隔,在那里被氧化成Fe3+后反渗出细胞壁[11,12].在浸出过程中,含铁硫化矿物氧化分解释放出Fe2+与细菌氧化Fe2+生成Fe3+这两个反应同时进行,ρ(Fe2+)主要由这两个因素决定.当前者速度大于后者时,ρ(Fe2+)升高,反之则降低.浸出初期,含铁硫化矿物(如黄铁矿)在Fe3+与细菌的共同作用下,氧化分解释放出Fe2+,同时Fe3+被还原成Fe2+.而此时由于细菌被转移到新的环境后有一个适应的过程,生长繁殖处于诱导期,氧化Fe2+的能力较弱,因此ρ(Fe2+)迅速增大.但随着ρ(Fe2+)的增大体系电位迅速下降,而在低电位下,黄铁矿的氧化速率极其缓慢[8,13],释放的Fe2+量很微小.同时细菌通过氧化Fe2+获得能源,不断生长繁殖,活性增强,氧化Fe2+速率加快,因此ρ(Fe2+)达到最大值后逐渐降低,呈下降趋势.当溶液中的Fe2+全部被氧化,并且矿物新释放出的Fe2+也被细菌迅速氧化时,溶液中ρ(Fe2+) 降为零.在图2中,浸出12天后酸浸矿体系中的ρ(Fe2+) 降为零,而原矿体系则滞后两天,在浸出14天后才降为零,说明酸浸矿体系中细菌的活性要好于原矿体系.

图2 Fe2+的质量浓度变化曲线图Fig.2 Concentrations of ferrous ion during leaching process
图3为浸出体系TFe的质量浓度ρ(TFe)变化曲线图,从图中可见,两个体系的ρ(TFe)均呈先下降而后开始缓慢上升,在浸出12天时迅速上升的趋势.这是因为在氧化初始阶段,由于大量Fe2+的存在,体系处于低电位状态下,作为铁的主要来源的黄铁矿在低电位下的氧化速率极其缓慢,释放出的铁量很微小.同时,溶液中的Fe3+会水解生成黄钾铁矾沉淀而使铁量下降[14],因此体系的ρ(TFe)下降.随着体系的氧化还原电位逐渐上升,细菌活性逐渐增强,黄铁矿的氧化速率增大,释放出的铁量增加,ρ(TFe)逐渐增加.浸出12天后,浸出体系电位达到550 mV的高电位并继续上升,同时细菌生长繁殖进入对数期,活性最强,因此黄铁矿氧化分解速率大幅加快,释放的铁量迅速增大,ρ(TFe)迅速上升.
由于原矿中含有大量的可溶性碱性脉石,矿石加入后碱性脉石的溶解使浸出体系的酸度不稳定,促进了铁矾沉淀的生成.经测量,在矿石加入调节初始pH值期间,原矿体系中ρ(TFe)由8.94 g·L-1迅速降至7.84 g·L-1,而酸浸矿体系中ρ(TFe) 不变,说明由于酸度的不稳定原矿体系生成了大量铁矾沉淀.酸浸矿通过预处理已将可溶性碱性脉石除去,加入后不会造成体系酸度不稳定,因此生成的铁矾沉淀的量很小,浸出3天后ρ(TFe) 降至8.49 g·L-1即开始逐渐上升.浸出结束时,酸浸矿体系ρ(TFe)为12.10 g·L-1,而原矿体系仅为8.60 g·L-1.因此,经过酸浸—摇床重选预处理除去可溶性碱性脉石后,可减少铁矾沉淀的生成量,避免大量的铁矾沉淀吸附于矿物表面阻碍矿物进一步氧化分解,有利于钴的浸出.
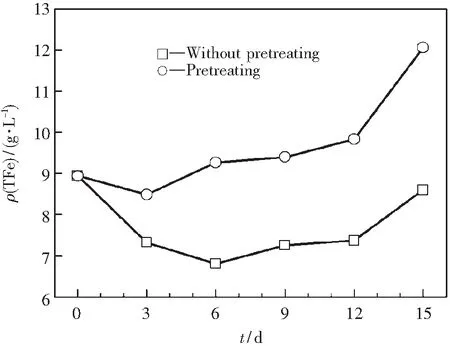
图3 TFe的质量浓度变化曲线图Fig.3 Concentrations of total iron during leaching process
原矿体系与酸浸矿体系生物浸出结果见图4及表3.酸浸矿体系钴浸出率为87.7%,原矿体系钴浸出率为52.5%,经过预处理钴浸出率提高35.2%,平均钴浸出速率提高29.4 mg·L-1·d-1,效果十分显著.对原矿体系浸出渣进行扫描电镜分析发现,部分矿粒表面吸附着大量沉积物,该沉积物经EDS能谱分析确定为CaSO4(见图5),说明在浸出过程中因大量可溶性钙盐溶解产生的CaSO4沉淀会沉积于矿粒表面,阻碍矿物与细菌和氧化剂接触,不利于矿物的氧化分解.通过对比试验可知,原矿石经过酸浸—摇床重选预处理,避免了可溶性碱性脉石的溶解造成浸出体系酸度不稳定,减少了铁矾沉淀生成量,同时也避免了钙盐溶解产生的硫酸钙沉淀沉积于矿物表面阻碍Fe3+与细菌对矿物的进一步作用,提高了钴的浸出率.经过酸浸—摇床重选预处理不但使该钴矿石适合采用微生物浸出技术回收钴,而且也缓解了该矿山大量硫酸无法消耗的情况.

图4 钴浸出率曲线图Fig.4 Leaching efficiency of cobalt
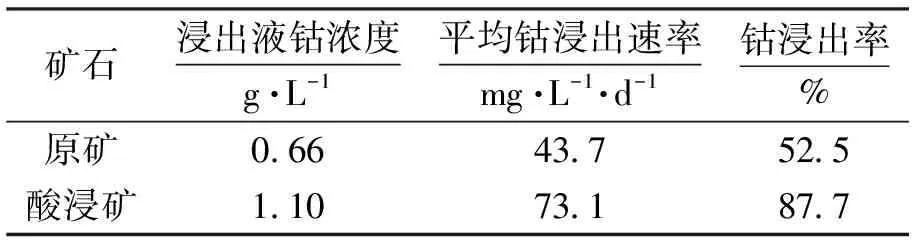
矿石浸出液钴浓度g·L-1平均钴浸出速率mg·L-1·d-1钴浸出率%原矿066437525酸浸矿110731877

图5 原矿浸出渣的SEM、EDS分析Fig.5 SEM image and EDS analysis of the raw ore leaching residue
3 结 论
(1)经过酸浸—摇床重选预处理,酸浸矿中钙含量(质量分数)由8.61%降至2.87%,去除率达74.32%;钴含量(质量分数)由1.25%上升至1.62%,损失率仅为0.15%,没有大量损失.经过预处理不但使该含钴矿石适合采用微生物浸出技术提取钴,而且也缓解了该矿山大量硫酸无法消耗的情况.
(2)原矿经过酸浸—摇床重选预处理除去可溶性碱性脉石,避免了因其溶解造成浸出体系酸度的不稳定,减少了铁矾沉淀的生成量,同时也避免了硫酸钙沉淀的生成,有利于钴的浸出.酸浸矿体系钴浸出率为87.7%,钴浸出率提高35.2%,平均钴浸出速率提高29.4 mg·L-1·d-1,效果显著.
[1] Behera S K, Panda P P, Singh S,etal. Study on reaction mechanism of bioleaching of nickel and cobalt from lateritic chromite overburdens[J]. International Biodeterioration & Biodegradation, 2011, 65: 1035-1042.
[2] D’hugues P, Cezac P, Cabral T,etal. Bioleaching of cobaltiferous pyrite: a continuous laboratory-scale study at high solids concentration[J]. Minerals Engineering, 1997, 10 (5): 507-527.
[3] Ahonen L, Tuovinen O H. Bacterial leaching of complex sulfide ore samples in bench-scale column reactors[J]. Hydrometallurgy, 1995, 37 (1):1-21.
[4] 温建康,阮仁满. 高砷硫低镍钴硫化矿浸矿菌的选育与生物浸出研究[J]. 稀有金属,2007,31(4):537-542.
(Wen Jiankang, Ruan Renman. Selection of bioleaching bacteria and bioleaching high arsenic/sulur, low-grade nikel/cobalt sulfide ore[J]. Chinese Journal of Rare Metals, 2007, 31 (4):537-542.)
[5] Yang C R, Qin W Q, Lai S S,etal. Bioleaching of a low grade nickel-copper-cobalt sulfide ore [J]. Hydrometallurgy, 2011, 106: 32-37.
[6] 刘伟,杨洪英,刘媛媛,等. 含钴矿石摇瓶生物浸出比较试验的研究[J]. 东北大学学报(自然科学版),2013,34(11):1606-1609.
(Liu Wei, Yang Hongying, Liu Yuanyuan,etal. Comparison of the bioleaching and chemical leaching of cobaltiferous ores[J]. Journal of Northeastern University (natural science), 2013, 34 (11): 1606-1609.)
[7] Rohwerder T, Gehrke T, Kinzler K,etal. Bioleaching review part A: Progress in bioleaching: fundamentals and mechanisms of bacterial metal sulfide oxidation[J]. Appl Microbiol Biotechnol, 2003, 63: 239-248.
[8] 杨显万,沈庆峰,郭玉霞. 微生物湿法冶金[M]. 北京:冶金工业出版社,2003:117-126.
(Yang Xianwan, Shen Qingfeng, Guo Yuxia. Microorganism hydrometallurgy[M]. Beijing: Metallurgical Industry Press, 2003: 117-126.)
[9] Tributsch H. Direct versus indirect bioleaching[J]. Hydrometallurgy, 2001, 59: 177-185.
[10] Crundwell F K. How do bacteria interact with minerals[J]. Hydrometallurgy, 2003, 71: 75-81.
[11] Hansford G S, Vargas T. Chemical and electrochemical basis of bioleaching processes[J]. Hydrometallurgy, 2001, 59(2/3): 135-145.
[12] Mason L J, Rice N M. The adaptation of Thiobacillus ferrooxidans for the treatment of nickel iron sulphide concentrates[J]. Minerals Engineering, 2002, 15(11): 795-808.
[13] Riekkola-Vanhanen M, Heimala S. Electrochemical control in the biological leaching of sulfidic ores[J]. Biohydrometall Technology, 1993, 1: 561- 570.
[14] Deveci H, Akcil A, Alp I. Bioleaching of complex zinc sulphides using mesophilic and thermophilic bacteria: comparative importance of pH and iron[J]. Hydrometallurgy, 2004, 73: 293-303.
