HPLC 法同时测定不同栽培年限亳芍中芍药苷和芍药内酯苷的含量
2015-01-08陈乃东陈乃富谢小乐
陈乃东 ,陈 翰,陈乃富,2,李 清,陈 琼,谢小乐
1皖西学院生物与制药工程学院;2皖西中药与天然药物工程技术研究中心,六安 237012;3 安徽医科大学,合肥 230032
亳芍(Bozhou Peony Paeonia lactiflora),即亳白芍,是芍药科植物芍药或其变种毛果芍药栽培品的根[1],为安徽道地药材之一,主产安徽省亳州地区。味苦、酸、甘,性微寒,具养血敛阴柔肝止痛、平抑肝阳等功效[2],以芍药总苷为主要活性成分,其中芍药苷和芍药内酯苷约占总苷70%以上[3]。现代药理研究表明,芍药苷具有增加冠脉流量,扩张冠状动脉,对抗急性心肌缺血,抑制血小板凝聚及降低血压等作用[4],芍药内酯苷具有镇痛、镇静、抗惊厥作用[5-7]。芍药苷和芍药内酯苷的含量对亳芍临床用药具有重要影响。
中药的活性成分积累与栽培年限密切相关。截止目前,有关白芍中芍药苷和芍药内酯苷的含量研究主要集中在不同提取方法和不同产地的含量比较[8-10],尚未见栽培时间对亳芍主要活性成分芍药苷、芍药内酯苷积累的影响的报道。
本文建立了一种同时测定芍药苷和芍药内酯苷的检测方法,在此基础上,对不同生长年限亳芍中的芍药苷及芍药内酯苷进行含量变化研究,为探讨中药亳芍的最佳药材采收时期、规范化种植、质量评价及临床用药提供依据。
1 仪器与材料
分析天平(FA1004 型,中国上海精科有限公司),超声清洗器,Lanbo Service 4000 高效液相色谱仪(EZchrom Elite 软件,UV4000 二极管阵列检测器,美国Lanbo 公司),循环水式多用真空泵(SHB-3S 型,郑州长城科工贸有限公司)。标准对照品芍药苷(含量测定用,含量≥98%,批号:B10091)、芍药内酯苷(含量测定用,含量≥98%,批号:B10102)均购自上海士锋生物科技有限公司。乙腈(色谱纯,上海星可高纯溶剂有限公司),水为市售娃哈哈纯净水,其余试剂均为国产分析纯。
实验材料亳芍2013 年8 月于亳芍道地产区安徽省亳州市6 个不同的亳芍种植基地,品种经皖西中药与天然药物工程技术研究中心陈乃东博士鉴定为毛茛科植物芍药Paeonia lactiflora Pall.干燥的根。6 个不同栽培基地分别挖取栽培1~7 年的亳芍,共42 个样品,洗净,去皮,晾干,备用。
2 方法与结果
2.1 对照品溶液的配制
以50% 乙醇配制成浓度125.0 μg/mL、22.5 μg/mL 芍药苷和芍药内酯苷对照品溶液适量,0.45 μm 微孔滤膜过滤、备用。
2.2 供试品溶液的制备
精密称取亳芍粉末0.5 g,置50 mL 容量瓶中,加50%的乙醇35 mL,60 ℃超声处理(240 W,45 kHz)30 min,冷却,加50%的乙醇定容至刻度,过滤,精密量取续滤液2 mL 以50%的乙醇定容到8 mL,微孔滤膜过滤,得供试品溶液。
2.3 色谱条件
Waters Symmetry C18色谱柱(4.6 mm×150 mm,5 μm),流动相为乙腈(A)-0.1%磷酸水溶液(B),梯度洗脱程序如下:0~5 min,5%~10%A;10~15.0 min,10~15%A;15.0~17.0 min,15~30%A;17~30.0 min,30%A;30.0~35.0 min,30~100%A;35~40.0 min,100%A。流速:1.0 mL/min;检测波长:230 nm;柱温为30 ℃。
在上述色谱条件下,对照品和供试品溶液HPLC 检测结果如图1 所示。
2.4 方法学考察
2.4.1 线性关系考察
分别紧密吸取2.1 项下配制的芍药苷、芍药内酯苷对照品溶液各1、5、10、15、20 μL,注入高效液相色谱仪,按2.3 项下色谱条件,测定芍药苷、芍药内酯苷峰面积,平行测定三次,取平均峰面积。以色谱峰面积为纵坐标(Y),对照品质量进样量(μg)为横坐标(X),分别得到的芍药苷和芍药内酯苷回归方程:y=1.2 ×1010x-3.5 ×106,R2=0.9960;y=1.1 ×106x-3.9×105,R2=0.9994。结果表明,芍药苷和芍药内酯苷在0.1250~2.5000 μg 和0.0225~0.4500 μg 范围内,分别与对应峰面积呈良好的线性关系。
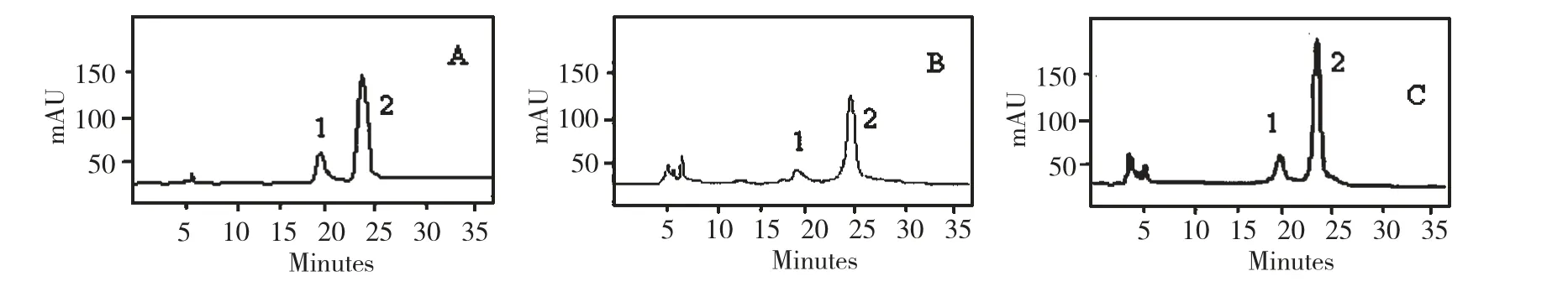
图1 芍药苷和芍药内酯苷混合对照品溶液(A)、样品溶液(B)及样品溶液与对照品混合溶液(C)的HPLC 图谱Fig.1 HPLC chromatograms of mixed standards (A),Bozhou Penoy (B)and mixed solution of standards and Bozhou Penoy sample (C)
2.4.2 稳定性试验
称取亳芍样品适量,按2.2 项下方法制备供试品溶液,精密吸取供试品溶液10.0 μL,分别于0、4、8、12、16、20、24、48 h 进样。结果表明芍药内酯苷、芍药苷峰面积的RSD 分别为0.96%和0.85%,说明样品溶液在48 h 内稳定较好。
2.4.3 重复性试验
称取同一批次亳芍样品粉末6 份,按2.2 项方法制备供试品溶液,精密吸取10.0 μL,按2.3 色谱条件测定。结果显示芍药内酯苷和芍药苷峰面积的RSD 分别为1.83%、1.79%,表明本测定方法重复性良好。
2.4.4 精密度试验
精密吸取2.1 项项下配制的芍药苷和芍药苷内酯对照品溶液各10.0 μL,按2.3 项述方法,连续进样6 次,测得二者峰面积RSD 均小于1.5%,说明仪器精密度良好。
2.4.5 回收率试验
精密称取0.5 g 已知含量的亳芍样品粉末9份,每3 份一组,依次精密加入高、中、低3 个水平芍药苷对照品5.0、1.0、0.1 mg 和药内酯苷2.0、0.5、0.1 mg,按2.2 项方法制备供试品溶液,按2.3 项方法进行测定,计算回收率。结果芍药内酯苷的平均回收率为101.30%,RSD 为2.57%;芍药苷的平均回收率为100.56%,RSD 为2.10%。
2.5 样品含量测定
精密称取栽培1~7 年的亳芍样品粉末各0.5 g,按2.2 项方法制备成供试品溶液,精密吸取10.0 μL 按2.3 项方法进行测定,测得不同栽培年限的亳芍中芍药苷和芍药内酯苷HPLC 色谱图(图2),记录芍药苷和芍药内酯苷的峰面积,利用建立的芍药苷和芍药内酯苷标准曲线,计算样品中芍药苷和芍药内酯苷的含量(图3)。
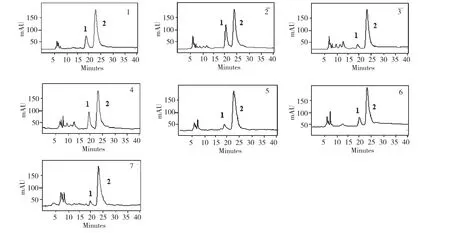
图2 不同株龄的亳芍芍药苷、芍药内酯苷HPLC 检测结果Fig.2 HPLC analysis of paeoniflorin and albiflorin in different years-old of Bozhou Peony P.Lactiflora
1~7 年株龄亳芍的芍药苷含量依次为:3.26 ±0.20%、4.97 ± 0.18%、5.84 ± 0.20%、3.57 ±0.06%、3.38 ± 0.12 %、3.37 ± 0.07%、2.70 ±0.03%。1~7 年株龄亳芍的芍药内酯苷含量分别为:0.66 ±0.09%、1.71 ±0.09%、0.48 ±0.07%、0.83 ±0.02%、0.48 ±0.02%、0.47 ±0.03%、0.27±0.04%。上述检测结果表明,亳芍中芍药内酯苷的含量远少于芍药苷,芍药苷和芍药内酯苷的含量因株龄的不同存在一定差异。1~7 年株龄亳芍,以3 年株龄的芍药苷含量最多,2 年株龄的芍药内酯苷含量最多。

图3 不同株龄的亳芍芍药苷和芍药内酯苷含量Fig.3 The contents of paeoniflorin and albiflorin from different years-old of Bozhou Peony P.Lactiflora
株龄1~7 年的亳芍中芍药苷和芍药内酯苷含量的方差分析显示,芍药苷在1~3 年含量呈递增趋势,3 年后含量降低,4~7 年株龄的芍药苷含量差别无统计学意义(表1),说明栽培3 年后,亳芍中芍药苷含量趋于稳定;芍药内酯苷在1~2 年呈递增趋势,2 年后含量降低,5~7 年含量平稳无统计学意义(表2),说明随着栽培年限增加,芍药内酯苷含量趋于稳定。上述结果分析表明,如以芍药苷含量为评价标准,以栽培3 年的亳芍药材品质较好。如以芍药内酯苷为依据,亳芍栽培2 年做药效果较好。
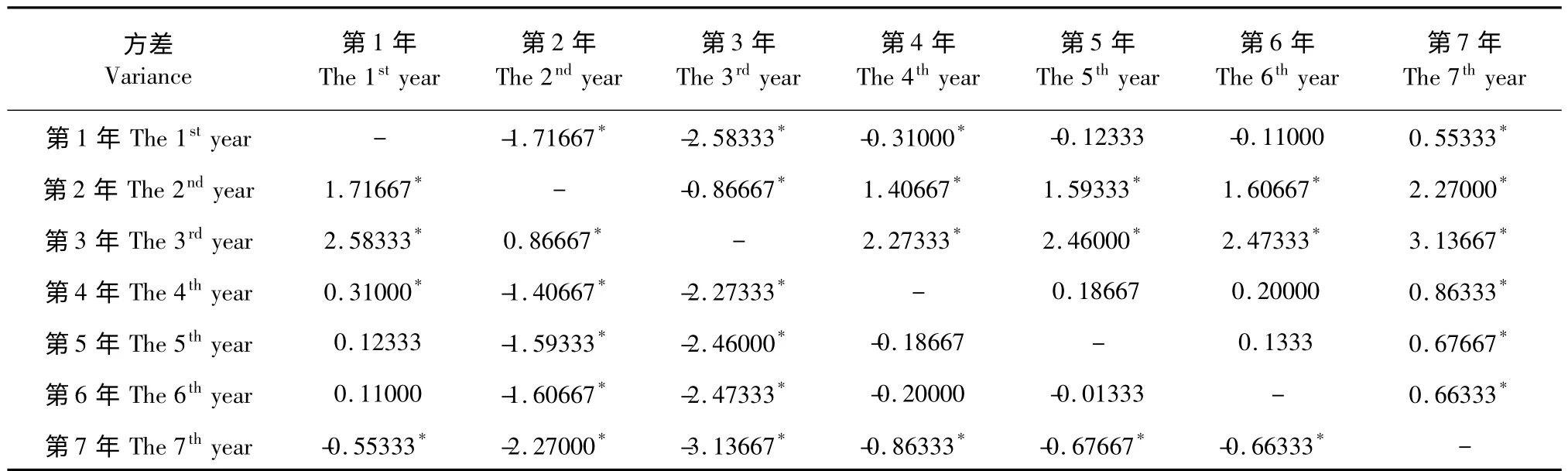
表1 不同生长年限的亳芍芍药苷含量方差分析结果Table 1 The ANOVA results of paeoniflorin contents in Bozhou Peony P.lactiflora with different growth years
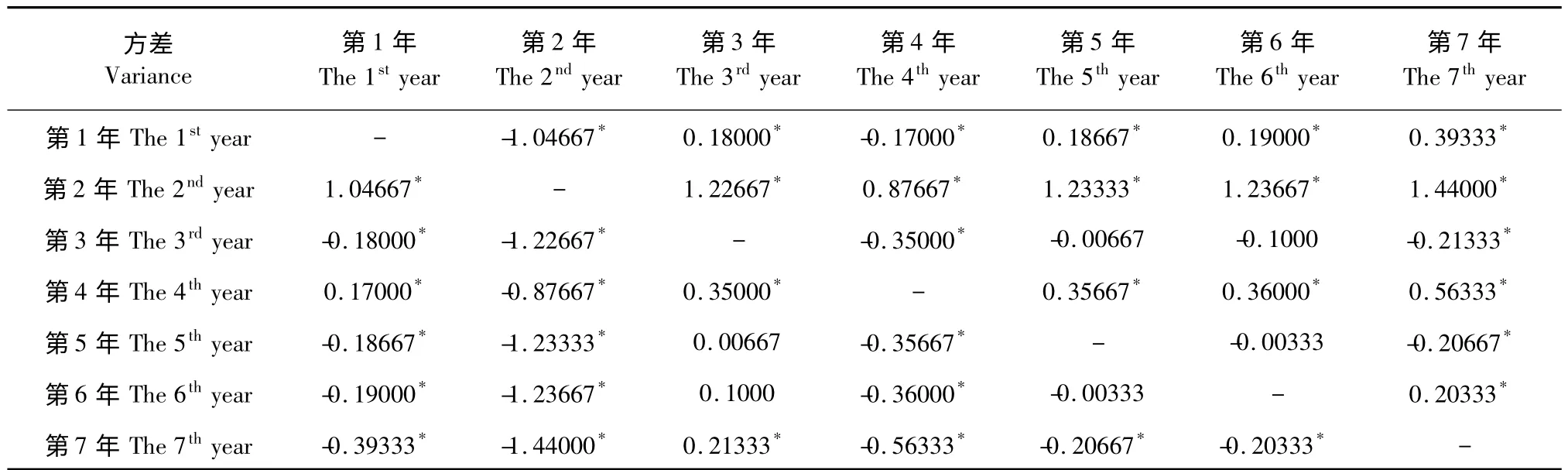
表2 不同生长年限的亳芍芍药内酯苷含量方差分析结果Table 2 The ANOVA results of albiflorin contents in Bozhou Peony P.lactiflora with different growth years
3 结论
首次对不同生长年限的安徽道地药材——亳芍中芍药苷和芍药内酯苷含量进行对比研究,研究发现三年株龄亳芍中芍药苷含量最高,两年株龄芍药内酯苷含量最多。研究结果对亳芍采收时期的确定、质量标准研究和亳芍的药物作用机制及临床应用提供新的参考依据。
1 Sun J(孙婕),Ling NS(凌宁生).Comparison of the determination methods for paeoniflorin in Radix paeoniae Alba.Chin Tradit Herb Drugs,2004,35:1372-1374.
2 The State Pharmacopoeia Commission.Pharmacopoeia of People's Republic of China (Part I).2005.109.
3 Zhang XY(张晓燕),Li X(李铣),Gong JH(工金辉).A study on the chemical constituents of Paeonia lactiflora Pall.J Shenyang Pharm Univ,2001,18:30-32.
4 Liu YX(刘鹰翔),Ma YZ(马玉卓).Advances in research of chemistry and pharmacology of Radix paeoniae Alba.Chin Tradit Herb Drugs,1995,26:437-440.
5 Lee B,Shin YW,Bae EA,et al.Antiallergic effect of the root of Paeonia lactiflora and its constituents paeoniflorin and paeonol.Arch Pharm Res,2008,31:445-450.
6 Xiao L,Wang YZ,Liu J,et al.Effects of paeoniflorin on the cerebral infarction,behavioral and cognitive impairments at the chronic stage of transient middle cerebral artery occlusion in rats.Life Sci,2005,784:413-420.
7 Tomoda M,Matsumoto K,Shimizu N,et al.An acidic poly-saccharide with immunological activities from the root of Paeonia lactiflora.Biol Pharm Bull,1994,17:1161-1164.
8 Jeon MH,Kwon HJ,Jeong JS,et al.Detection of albiflorinand paeoniflorin in Paeoniae radix by reversed-phase high-performance liquid chromatography with pulsed amperometric detection.J Chromatogr A,2009,1216:4568-4573.
9 Huang SJ(黄山君),Yang QW(杨琪伟),Shi YH(石燕红),et al.Simultaneous assay of paeoniflorin and albiflorin in Paeoniae Radix Alba by QAMS.China J Chin Mater Med,2011,19:780-783.
10 Kim N,Park KR,Park IS,et al.Application of novel HPLC method to the analysis of regional and seasonal variation of the active compounds in Paeonia lactiflora.Food Chem,2006,96:496-502.
