Mn 掺杂TiO2负载木质活性炭纤维可见光降解甲醛的研究
2015-01-08马晓军
陈 印,马晓军
(天津科技大学包装与印刷工程学院,天津 300222)
在日常生活中甲醛无处不在,例如木家具、涂料、服装、水泡鱿鱼、汽车内部材料等都会释放甲醛,其中室内空气中的甲醛是危害人体健康的主要污染物[1–2],由此导致的鼻窦癌、鼻咽癌、肺癌以及白血病等患者与日俱增,2004 年国际癌症研究机构将甲醛归属为一级致癌物质.至今人们去除室内甲醛的方法有开窗通风、物理吸附法、光催化降解法、空调净化法、离子净化法等[3–6],其中将物理吸附和光催化剂TiO2相结合效果显著,既可以解决吸附法二次污染的弊端,同时可以解决光催化剂降解低浓度甲醛速率慢的问题,充分发挥了吸附和光降解的协调作用.但是,由于TiO2禁带宽度高达3.2,eV(锐钛矿),造成TiO2负载光催化材料只有在紫外光激发条件下才能发挥光催化作用,太阳光中90%,以上的可见光没有被利用起来,不仅太阳能利用率低,而且影响了光催化效果,限制了光催化材料的应用范围.为此近年来学者们着重研究在可见光下也可以发挥降解作用的改性TiO2负载光催化材料[7–11],使得降解甲醛过程不再受紫外光的限制,不仅降低了使用门槛,同时有利于提高光催化性能.
本文以具有良好吸附性能的木质活性炭纤维为载体,选用具有可见光降解效果的Mn 掺杂TiO2为光催化剂,成功制备了Mn 掺杂TiO2负载活性炭纤维材料,考察了Mn 掺杂浓度、光照时间、光照强度、甲醛初始浓度和样品用量对甲醛降解的影响,为利用掺杂改性TiO2负载材料降解甲醛提供借鉴.
1 材料与方法
1.1 实验原料
杉木木粉;苯酚、磷酸、六次甲基四胺、MnSO4·H2O、钛酸丁酯、无水乙醇、冰乙酸、氢氧化钠、碘、碘化钾、乙酸铵、乙酰丙酮、重铬酸钾、淀粉(指示剂)、硫代硫酸钠、盐酸、甲醛等均为分析纯;蒸馏水为实验室自制.
1.2 Mn掺杂TiO2负载木质活性炭纤维的制备
将蒸馏水、4,mL 冰乙酸先后滴入120,mL 的无水乙醇获得混合溶液 A,将溶液 A 加入到 6,mL MnSO4·H2O 溶液获得混合溶液B.将180,mL 无水乙醇与20.4,g 钛酸丁酯充分混合得到浅黄色透明溶液C.将溶液B 缓慢加入到溶液C,并放入40,℃水浴锅中机械搅拌3,h,静置一段时间得到Mn 掺杂TiO2溶胶.其中蒸馏水加入量根据n(Mn+Ti)∶n(H2O)=1∶4 确定,MnSO4·H2O 含量根据n(Mn)∶n(Ti)为0∶1、1∶600、1∶300、1∶100、1∶50 确定.
将实验室制备的木质活性炭纤维(WACFs)[12]散开后均匀浸入溶胶中,经过30,min 振荡、30,min 静置处理后取出,放入真空管式炉中,在 N2保护下450,℃煅烧90,min,从而获得Mn 掺杂TiO2负载木质活性炭纤维光催化复合材料(Mn/TiO2-WACFs).
1.3 表征与光催化性能评价
1.3.1 表征
将干燥处理后的样品粘在样品台上进行真空喷金处理,采用日本电子株式会社(JEOL)JSM–7500F型冷场发射扫描电子显微镜观察样品表面形态.加速电压1,kV,分辨率3.0,nm.
XRD 表征参见本课题组前期研究成果[13].
1.3.2 Mn/TiO2-WACFs 光催化降解甲醛性能评价
依据HJ601—2011《水质·甲醛的测定·乙酰丙酮分光光度法》配制质量浓度为9.38,mg/L 的甲醛标准溶液,取数支25,mL 具塞比色管,分别加入0.5、1.00、3.00、5.00、8.00,mL 甲醛标准溶液,加水至25,mL,然后加入2.5,mL 按照标准配制的乙酰丙酮溶液,摇匀后放入60,℃水浴锅中加热15,min,取适量冷却后溶液在波长414,nm 处测得吸光度,并绘制标准曲线,通过标准曲线获得回归方程y=4.452,4,x-0.046,3,R2=0.999(x 代表吸光度;y 代表甲醛溶液的质量浓度,mg/L),因此可以通过吸光度测量值计算甲醛溶液的质量浓度,以便考察甲醛降解率.
取质地均匀、大小相同且充分干燥后的薄块状杉木木片0.5,g,放入100,mL 一定质量浓度的甲醛溶液中浸泡18,h,取出木片后立即置入250,mL 的具塞窄口透明玻璃瓶中,同时加入一定质量的Mn/TiO2-WACFs 样品,盖紧瓶盖后放入密闭的黑暗环境中30,min,使木片中的甲醛充分挥发扩散,然后放在一定功率的螺旋状节能灯下进行照射,节能灯与瓶保持45°夹角,两者之间需用滤光片(只可以透过大于等于400,nm 波长的光)隔开,目的是获得可见光,避免紫外光的干扰,一段时间后用100,mL 蒸馏水在40,℃恒温水浴锅中萃取木片及光催化剂中的甲醛1,h[14],取甲醛萃取液25,mL 并加入2.5,mL 乙酰丙酮溶液,采用乙酰丙酮显色法在分光光度计上测得的吸光度计算甲醛溶液的质量浓度,依据式(1)算甲醛降解率D.
式中:ρ0、ρ1分别为浸泡木片前后甲醛溶液的质量浓度,mg/L;ρ2、ρ3分别为木片和光催化剂吸附甲醛的质量浓度,mg/L.
2 结果与讨论
2.1 材料的表面形态
WACFs 与Mn/TiO2-WACFs 的扫描电镜图如图1 所示.由图1 可以看出:木质活性炭纤维表面平整光滑,而负载Mn 掺杂TiO2的纤维表面存在大面积间断的沉积物,说明Mn/TiO2光催化剂以薄片状薄膜形态包裹在纤维表面,具有良好的复合结构.此外,Mn/TiO2-WACFs 表面仍有基材裸露,保留了纤维丰富孔隙的特性,有利于后续的吸附和光催化反应.Mn/TiO2-WACFs 薄膜出现裂纹、边缘翘起现象,这是由于高温煅烧过程中胶体和纤维的热收缩程度不同.煅烧初始阶段,无定型TiO2薄膜形成的同时,由于部分受热挥发的钛酸丁酯与水蒸气迅速发生水解反应,造成WACFs 表面存在容易脱落的颗粒状TiO2.
2.2 Mn掺杂浓度对甲醛降解率的影响
在甲醛初始质量浓度9.38,mg/L、节能灯功率65,W、光照时间4,h、Mn/TiO2-WACFs 用量40,mg 的条件下,不同Mn 掺杂浓度样品降解甲醛的降解率曲线如图2 所示.

图2 Mn掺杂浓度对甲醛降解率的影响Fig.2 Effect of Mn doping concentration on the degradation rate of formaldehyde
由图2 可知:随着Mn 掺杂浓度的提高,甲醛降解率先增大后减小.当n(Mn)∶n(Ti)为1∶100 和1∶300 时,甲醛降解率最大,都为58%,;n(Mn)∶n(Ti)为1∶600 和1∶50 时甲醛降解率略微降低,分别为55%,和56%,,这可能是由于Mn 含量过少时替代的Ti 较少,填充不完整,而过多的Mn 离子团聚在TiO2表面,容易为电子-空穴对提供复合中心,这两种情况都不利于降解甲醛.此外所有Mn 掺杂样品降解甲醛效果均高于纯TiO2负载样品,降解率最大高出11%,,这印证了Mn 掺杂有利于提高TiO2可见光区域的光催化活性,使甲醛降解率普遍升高.由于n(Mn)∶n(Ti)=1∶300 样品中添加的Mn 质量极少,只有17,mg,而n(Mn)∶n(Ti)=1∶100 样品中达到51,mg,前者相对后者容易出现较大的称量误差,所以后续讨论中所选样品均为后者.
2.3 光照时间对甲醛降解率的影响
在甲醛初始质量浓度9.38,mg/L、节能灯功率65,W、Mn/TiO2-WACFs 用量40,mg,n(Mn)∶n(Ti)=1∶100 的条件下,光照时间对甲醛降解率的影响如图3 所示.

图3 光照时间对甲醛降解率的影响Fig.3 Effect of lighting time on the degradation rate of formaldehyde
由图3 可知:光照时间越长,Mn/TiO2-WACFs 样品对甲醛的降解效果越好;在光照时间6,h 时,甲醛降解率达到66%,.在光照后的1,h 内,甲醛减少了44%,,降解效率最高;而当光照时间在1~2.5,h 时间段内,甲醛降解率增加幅度相对较小,只增加了5%,;光照时间在2.5~4,h 和4~5.5,h 两个时间段内,甲醛降解率增加幅度相对稳定,分别增加了9%,和8%,.甲醛降解率出现上升走势,主要是因为刚开始反应的1,h 内,木质活性炭纤维在避光时间内吸附了反应瓶内木片释放的大量甲醛气体,使富集在Mn/TiO2-WACFs 周围的甲醛浓度很高,有利于降解反应的进行,所以降解的甲醛量多,以至于在光照反应的1~2.5,h 时,Mn/TiO2-WACFs 周围的甲醛浓度相对较低,所以降解率开始较低,属于吸附和光催化速率相互调节的过程,光照时间2.5~5.5,h 区间,纤维吸附和Mn 掺杂TiO2光降解甲醛速率相对平衡,所以甲醛降解效果稳定上升.
2.4 光照强度对甲醛降解率的影响
在甲醛初始质量浓度9.38,mg/L、光照时间4,h、Mn/TiO2-WACFs 用量160,mg、n(Mn)∶n(Ti)=1∶100 条件下,通过节能灯光源功率的改变,调节光照强度的大小,从而获得光照强度对甲醛降解率的影响曲线,结果如图4 所示.由图4 可知:随着光照强度的增加,甲醛降解率先增大后减小;当节能灯功率为65,W 时,甲醛降解率最大,达到70%,.这是由于光照强度增大,Mn/TiO2接受的能量越大,受激发产生的电子-空穴对数量增加,从而反应过程中起主要降解作用的自由基·OH 增多,所以甲醛降解效果越好.但是,当光照强度增加到一定程度以后,由于TiO2利用光能量有限,而且过多的电子-空穴对、中间氧化物等容易出现竞争复合现象,所以甲醛降解率没有继续增高[15].

图4 光照强度对甲醛降解率的影响Fig.4 Effect of illumination intensity on the degradation rate of formaldehyde
2.5 甲醛初始浓度对甲醛降解率的影响
在光照时间4,h、Mn/TiO2-WACFs 用量160,mg、节能灯功率65,W、n(Mn)∶n(Ti)=1∶100 的条件下,甲醛初始浓度对甲醛降解率的影响如图5 所示.由图5 可知:随着甲醛初始质量浓度的提高,甲醛降解率逐渐增大.反应 4,h 后,甲醛初始质量浓度9.38,mg/L 时比4.69,mg/L 时的降解率提高了50%,,提高幅度最大;而甲醛质量浓度18.76,mg/L 时比9.38,g mg/L 时降解率提高了2%,,甲醛质量浓度28.14,mg/L 时比18.76,mg/L 时降解率提高了7%,,两者提高的幅度都较小.这是由于甲醛初始浓度很低时,短时间内活性炭纤维吸附量和吸附速率相对较低,富集到Mn/TiO2-WACFs 周围的甲醛浓度相应较低,所以光降解甲醛的反应速率也会较低,最后导致相同时间内甲醛降解率较低.
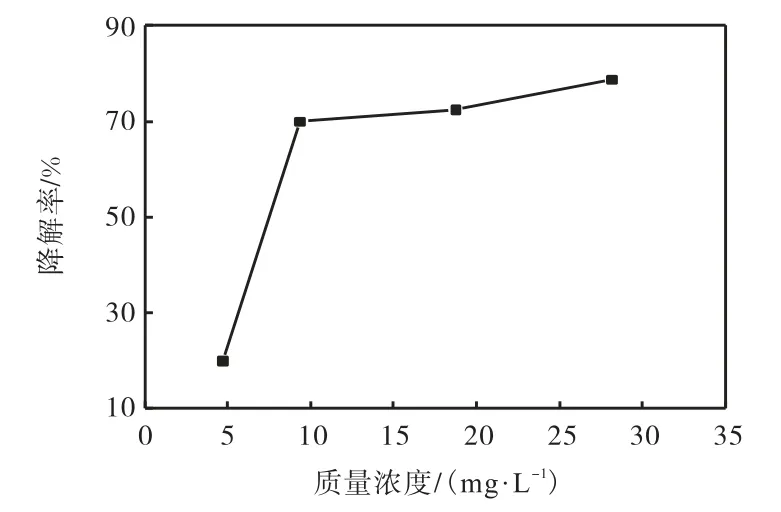
图5 甲醛初始浓度对甲醛降解率的影响Fig.5 Effect of initial concentration on the degradation rate of formaldehyde
2.6 样品用量对甲醛降解率的影响
在甲醛初始质量浓度9.38,mg/L、节能灯功率65,W、光照时间4,h、n(Mn)∶n(Ti)=1∶100 的条件下,Mn/TiO2-WACFs 用量对甲醛降解率的影响如图6 所示.
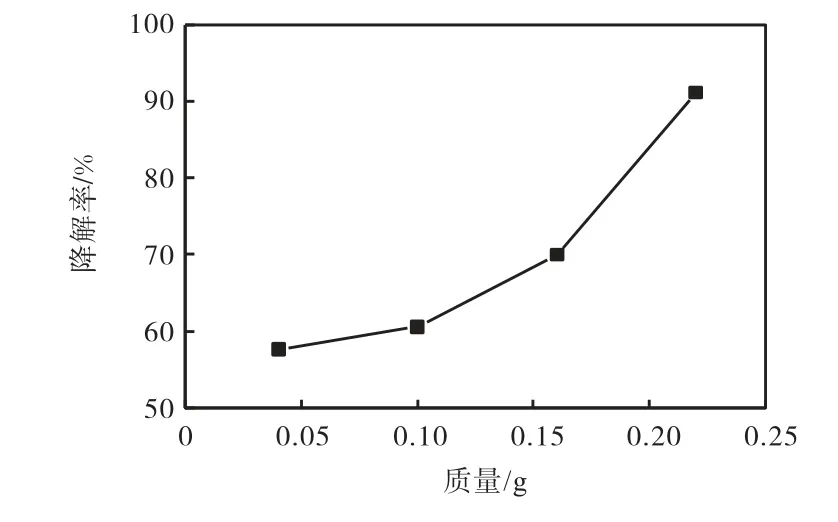
图6 样品用量对甲醛降解率的影响Fig.6 Effect of Mn/TiO2-WACFs doses on the degradation rate of formaldehyde
由图6 可知:随着Mn/TiO2-WACFs 用量的增多,甲醛降解率表现出增大的趋势,且增加幅度也逐渐增大,反应4,h 后,用量为0.22,g 的样品甲醛降解率最大,为91%,,且增幅也最大,比0.16,g 样品用量时的甲醛降解率增大了21%,.这说明样品用量的增大有利于降解甲醛.但值得注意的是,Mn/TiO2-WACFs 用量不是越大越好.用量过多,容易造成活性炭纤维分散不开的问题,以至于有些纤维上负载的Mn/TiO2被其他纤维遮挡,接收不到光的照射,难以发挥光降解性能.
3 结论
以木质活性炭纤维为载体制备Mn 掺杂TiO2负载活性炭纤维材料,考察可见光下其对甲醛的降解效果.研究发现:随着光照时间的延长、Mn/TiO2-WACFs 用量的增多和甲醛初始质量浓度的增大,Mn/TiO2-WACFs 在可见光下对气态甲醛的降解效果逐渐增强;随着Mn 掺杂浓度和光照强度的提高,Mn/TiO2-WACFs 对气态甲醛的降解效果先增大后减小.在光照强度65,W、光照时间4,h、甲醛初始质量浓度9.38,mg/L、n(Mn)∶n(Ti)=1∶100、Mn/TiO2-WACFs 用量 0.22,g 的条件下,甲醛降解率高达91%,.
[1]罗晓红,顾艳.室内甲醛污染对人类健康影响的研究进展[J].职业与健康,2011,27(21):2501-2503.
[2]候一宁,王安,王燕.二氧化钛-活性炭纤维混合材料净化室内甲醛污染[J].四川大学学报:工程科学版,2004,36(4):41-44.
[3]Oda T,Takahashi T,Yamaji K.Nonthermal plasma processing for dilute VOCs decomposition[J].IEEE Transactions on Industry Applications,2002,38(3):873-878.
[4]南璇.室内甲醛去除方法综述[J].中国涂料,2013,28(12):7–9.
[5]张顺喜,杨洁.室内甲醛污染治理实验研究[J].环境工程学报,2008,2(11):1539–1541.
[6]梁文俊,李坚,李洁,等.高频放电法对甲醛去除性能研究[J].北京工业大学学报,2008,34(6):617–620.
[7]Di Lanbo,Zhang Xiuling,Xu Zhijian,et al.Atmospheric-pressure cold plasma for preparation of high performance Pt/TiO2photocatalyst and its mechanism[J].Plasma Chemistry and Plasma Processing,2014,34(2):301–311.
[8]Magagnin L,Bernasconi R,Leffa S,et al.Photocatalytic and antimicrobial coatings by electrodeposition of silver/TiO2nano-composites[J].ECS Transactions,2013,45(8):1–6.
[9]Teoh W Y,Maedler L,Amal R,et al.Modifying bandgap of Tio2-based nanoparticles by cation doping[C]// Proceedings of 2005 AIChE Annual Meeting.Cincinnati:American Institute of Chemical Engineers,2005:3141.
[10]Kim Jungwon,Choi Wonyong.TiO2modified with both phosphate and platinum and its photocatalytic activities[J].Applied Catalysis B :Environmental,2011,106(1/2):39–45.
[11]马云飞,陈宗家.泡沫镍负载改性TiO2降解甲醛[J].环境工程学报,2014,8(5):2040–2044.
[12]Li Dongna,Ma Xiaojun,Liu Xinyan,et al.Preparation and characterization of nano-TiO2loaded bamboo-based activated carbon fibers by H2O activation[J].BioResources,2014,9(1):602–612.
[13]Chen Yin,Ma Xiaojun.Preparation of visible-light active Mn-doped TiO2photocatalyst and its photodegradation of methylene blue from solution[J].Advanced Materials Research,2014,989:531–535.
[14]王涵,张华,张文华,等.负载纳米MnO2的吸附纤维室温下对甲醛的吸附分解[J].高分子材料科学与工程,2012,28(1):158–162.
[15]Bahnemann D W.Mechanisms of organic transformations on semiconductor particles[J].Solar Energy Materials and Solar Cells,1991,24(3):564–583.
