基于KGdF4:Tb3+纳米材料检测四环素的生物传感新方法
2014-12-25吴世嘉王周平
段 诺, 吴世嘉, 王周平
(1.江南大学 食品学院,江苏 无锡 214036;2.食品科学与技术国家重点实验室,江南大学,江苏 无锡 214122)
四环素(Tetracycline,Tc)是四环素类抗生素的一种,是由放线菌属产生的一类广谱抗生素,对革兰氏阴性菌和阳性菌、立克次氏体等均有抑菌作用[1]。近年来,四环素被广泛应用于饲料添加剂,一方面能够有效地预防和治疗鱼类、畜禽类的疾病,另一方面可促进其生长速度,控制生殖周期和繁育能力。然而一些不法分子为了经济效益,常滥用这类药物,致使其在动物性食品中大量残留,不仅危害人体健康,而且更为严重的是畜禽产品中残留较低浓度的四环素类抗生素容易诱导各种致病菌产生耐药性,不利于对人类和畜禽类疾病的治疗[2-4]。目前,国内外对于四环素残留常用的检测方法有微生物法[5]、薄层层析法[6]、液相色谱法[7-9]、酶联免疫法[10-11]等。上述方法均具有灵敏度高、重复性好等特点。然而上述方法也存在耗时、设备昂贵、样品前处理步骤繁琐等缺点。因此构建快速、准确、灵敏的食品安全检测新方法新技术,对于实现四环素的超痕量检测具有重要意义。
镧系元素掺杂的新型纳米材料KGdF4:Ln3+纳米粒子是一类具有显著荧光发射的粒子,相比于传统的荧光染料和量子点,KGdF4:Ln3+纳米粒子具有以下显著的优点:较长的荧光寿命,可以很好的消除散射光对于荧光检测的干扰、较大的斯托克斯位移(>50 nm)、较窄的荧光发射峰形(<10 nm)、低毒性以及很高的抗光漂白性[12-13]。目前KGdF4:Ln3+纳米粒子在生物大分子检测分析、医疗诊断分析等方面具有比较广泛的应用。
氧化石墨烯也是一类具有非常良好的电子、机械和热性能的纳米材料,近年来备受关注[14]。研究表明,单链DNA可以通过π-π共轭大量的吸附在氧化石墨烯的表面[15]。而由于磷酸骨架中的核苷酸碱基的遮蔽作用,导致氧化石墨烯对于DNA双链以及折叠的DNA复合物的吸附能力相对较弱[16]。与此同时,氧化石墨烯具有较宽的紫外吸收,是一种高效的荧光淬灭剂,这些特性使得氧化石墨烯成为一种优良的检测平台[17-18]。
作者利用KGdF4:Ln3+纳米粒子作为荧光分子,氧化石墨烯作为荧光淬灭分子,结合适配体与目标物质的高亲和力和高特异性识别,构建了一种灵敏、高效的荧光共振能量转移体系检测四环素的方法。
1 材料与方法
1.1 材料与试剂
四环素标准品:购自上海晶纯科技股份有限公司;氟化铵、氯化钾、氯化钠、乙二醇、戊二醛等:购自国药集团化学试剂有限公司;聚丙烯亚胺:购自梯希爱(上海)化成工业发展有限公司;GdCl3·6H2O、TbCl3·6H2O、亲和素:购自 Sigma 公司;牛奶样品:购自无锡华润万家超市。四环素适配子[19]5'-biotin-CGT ACG GAA TTC GCT AGC CCC CCG GCA GGC CAC GGC TTG GGT TGG TCC CAC TGC GCG TGG ATC CGA GCT CCA CGT G-3':由生工生物工程(上海)有限公司合成。
1.2 仪器与设备
紫外可见分光光度计UV-1800:日本岛津公司;冷冻离心机:德国eppendorf公司;ZD-85气浴恒温振荡器:上海比朗仪器有限公司;JEM2100透射电镜:日本JEOL公司;荧光光谱仪FLUORMAX-4:美国HORIBA公司;X射线衍射仪D8:德国布鲁克AXS有限公司;傅立叶变换红外光谱仪Nicolet iS10:美国赛默飞公司;Direct-Q3超纯水系统:美国Millipore公司。
1.3 氧化石墨烯的制备
在Hummers方法的基础上做改进[20],利用石墨粉末得到氧化石墨烯。称取2 g石墨薄片和1.6 g NaNO3,在冰浴状态下加入67.5 mL浓硫酸中。随后缓慢加入 9 g KMnO4反应溶液中,35℃搅拌 30 min。随后560 mL温水缓慢加入溶液中形成糊状,再加入 30%H2O2,室温条件下连续搅拌5 d,溶液逐渐变为亮黄色。最后将悬液离心,用去离子水清洗多次,在真空干燥箱中70℃干燥得到氧化石墨烯片层。
1.4 镧系元素掺杂的KGdF4:Tb3+纳米材料的制备
将 2.0 mmol KCl、1.0 mmol GdCl3·6H2O、0.01 mmol TbCl3·6H2O、1 mL(300 mg/mL)聚丙烯亚胺以及20 mL乙二醇加入至100 mL圆底烧瓶中,充分搅拌至所有固体溶解。另取8 mmol NH4F加入至烧杯中,并加入20 mL乙二醇,放入40℃水浴锅中恒温搅拌至固体全部溶解。后将溶解的NH4F逐滴加入至圆底烧瓶中,充分搅拌1 h,形成悬浮液。将悬浮液转入至高温反应釜中,放入电热鼓风干燥箱195℃恒温加热4 h。反应结束后将产物分装入离心管中,10 000 r/min离心15 min。弃上清液,沉淀用乙醇以及超纯水超声清洗三次。最后成品烘干,研成粉末保存,即制得镧系元素掺杂的KGdF4:Tb3+纳米粒子。
1.5 KGdF4:Tb3+纳米粒子-四环素适配体复合物的制备
将 15 mg KGdF4:Tb3+纳米粒子于 5 mL PBS 中超声分散 20 min,之后加入 1.25 mL(1.06 g/mL)戊二醛,37℃恒温振荡2 h。然后用PBS超声清洗三次 (9 000 r/min、10 min)。 所得沉淀于0.9 mL PBS中重悬,加入0.1 mL(1 mg/mL)亲和素,37℃恒温振荡6 h。反应结束后用结合缓冲液 (20 mmol/L Tris-HCl、100 mmol/L NaCl、5 mmol/L KCl、2 mmol/L MgCl2、1 mmol/L CaCl2、pH 7.0)清洗 3 次,加入 20 μL(10 μmol/L)生物素化的四环素适配体,37℃恒温振荡2 h。之后用结合缓冲液清洗3次(9 000 r/min、10 min),再用结合缓冲液配制成1 mg/mL的体系,构成KGdF4:Tb3+纳米粒子-四环素适配体复合物。放入4℃冰箱保存备用。
1.6 四环素检测
配制不同浓度的四环素标准样品(0.5、1、5、10、20、50、100 ng/mL), 分别与上述制备的 KGdF4:Tb3+纳米粒子-四环素适配体复合物于37℃孵育1 h,然后加入氧化石墨烯(100 μL,1 mg/mL),37 ℃继续孵育1.5 h。最后使用荧光光谱仪FLUORMAX-4测定样品荧光光谱,设定激发波长273 nm,考察发射峰543 nm处荧光强度。
1.7 牛奶样品中四环素加标回收实验
利用建立的方法对牛奶中的四环素进行检测,对牛奶样品的处理方法为:取10 mL牛奶,在10℃下7 000 r/min离心10 min,完全去除上层脂肪层。将得到的样本用去离子水1∶20稀释,再经过一次性注射式滤器过滤,最终得到待测溶液。配制不同浓度的四环素标准溶液加入待测溶液中,利用本设计方法检测其中四环素的含量,计算检测值,得到回收率。
2 结果与分析
2.1 四环素的检测原理
KGdF4:Tb3+纳米粒子的表面富含氨基,并通过戊二醛法与亲和素进行连接,之后再与生物素化的四环素适配体进行结合,构成荧光供体探针。同时我们制备得到了氧化石墨烯单片层,通过紫外扫描发现其在300~700 nm之间存在广泛的紫外吸收区,并且与制备得到的KGdF4:Tb3+材料的荧光发射谱重叠,也就意味着氧化石墨烯可以作为能量受体淬灭KGdF4:Tb3+纳米粒子的荧光。据此设计了一个荧光共振能量转移体系检测四环素的方法,技术原理见图1。将KGdF4:Tb3+-四环素适配体荧光供体探针与氧化石墨烯共同孵育,由于π-π堆积作用,适配体(单链DNA)就会被固定到氧化石墨烯片层表面,致使KGdF4:Tb3+荧光被氧化石墨烯淬灭。当加入目标物质四环素时,四环素与荧光供体探针上的适配体发生特异性结合从而降低了适配体表面电荷,使得这部分适配体不具备与氧化石墨烯π-π共轭结合的能力,从而不会吸附在氧化石墨烯片层表面,KGdF4:Tb3+荧光得以保留,据此可实现四环素的定量检测。

图1 基于荧光共振能量转移的四环素检测原理图Fig.1 Schematic representation of the detection of tetracycline using FRET
2.2 材料表征
所制备的KGdF4:Tb3+纳米粒子的荧光光谱见图2a所示,在激发波长273 nm下,KGdF4:Tb3+纳米粒子在540 nm左右处有显著的发射峰。利用TEM对KGdF4:Tb3+纳米粒子的形貌进行表征,由图2b可见,KGdF4:Tb3+纳米粒子在水中分散性良好,颗粒都趋于球形,粒径在25~30 nm左右,且分布较为均匀。对KGdF4:Tb3+纳米粒子进行X射线衍射表征,结果见图2c所示。该纳米粒子粉末的X射线衍射图谱可以完全索引到KGdF4的纯立方相,可以表明该粉末具有高度结晶的KGdF4晶体存在,没有其他晶体杂质的干扰。对KGdF4:Tb3+纳米粒子进行红外光谱表征。聚乙烯亚胺在KGdF4:Tb3+纳米粒子的合成过程中包覆于材料表面,为该材料提供了丰富的氨基与亚氨基,使其形貌良好,生物相容性佳。如图2d所示,在1 396 cm-1处的红外峰为C-N键的伸缩振动,2 950、2 856 cm-1处的红外峰分别为C-H键的非对称与对称伸缩振动。在1 625 cm-1处的显著红外峰为氨基中N-H键的特征峰,由此可以表征聚乙烯亚胺的成功包被,使得KGdF4:Tb3+纳米粒子的表面具有丰富的活性基团,可为后续的亲和素连接提供基础,并可大幅的改良其在水中的分散性与生物相容性。


图2 KGdF4:Tb3+纳米粒子荧光光谱图 (a), 透射电镜图(b),X 射线衍射图谱(c)和红外光谱光谱图(d)Fig.2 Fluorescence spectra (a),TEM image (b),XRD image (c),FT-IR spectra ofKGdF4:Tb3+nanoparticles(d)
2.3 氧化石墨烯的表征
从图3a可以清楚的看到氧化石墨烯片层的薄片,以及特有的褶皱和卷边的现象,可以确认氧化石墨烯单片层制备成功。另外,测定了氧化石墨烯的紫外吸收光谱,由图3b中看到,氧化石墨烯具有非常宽泛的紫外吸收大约包含了从300~700 nm的范围,而恰好此范围与KGdF4:Tb3+纳米粒子的荧光发射光谱重叠,这意味着KGdF4:Tb3+纳米粒子发射的荧光将被氧化石墨烯吸收从而发生荧光淬灭。

图3 氧化石墨烯透射电镜图(a)和紫外吸收光谱图(b)Fig.3 TEM image (a) and UV-visible absorption spectrum(b) of graphene oxide
2.4 KGdF4:Tb3+纳米粒子与亲和素连接的表征
本实验中KGdF4:Tb3+纳米粒子-四环素适配体复合物由KGdF4:Tb3+纳米粒子与四环素适配体构成,二者的连接通过亲和素与生物素的特异性结合来完成。其中四环素适配体5'端修饰了生物素,KGdF4:Tb3+纳米粒子与亲和素则按照1.5所述方法进行连接。利用紫外-可见吸收光谱对其是否成功连接进行了表征。由图4中曲线A可以看出,亲和素在未与KGdF4:Tb3+纳米粒子连接之前在280 nm处有明显的紫外吸收峰;当亲和素与KGdF4:Tb3+纳米粒子进行孵育之后,离心收集所得上清液的紫外吸收图谱见曲线B。此时在亲和素280 nm处的紫外特征吸收峰峰值大幅降低。从而表明亲和素已成功固定到KGdF4:Tb3+纳米粒子的表面。

图4 亲和素原液(曲线A)与孵育后上清液(曲线B)的紫外-可见吸收图谱Fig.4 UV-visible absorption spectrum of avidin(curve A)and the supernatant after incubation(curve B)
2.5 荧光共振能量转移体系
如图5所示,连接了四环素适配体的KGdF4:Tb3+纳米粒子作为能量供体探针,当能量供体探针与氧化石墨烯连接后,KGdF4:Tb3+纳米粒子荧光被氧化石墨烯淬灭 (曲线A),而将无适配体修饰的KGdF4:Tb3+纳米粒子与氧化石墨烯混合扫描荧光图谱 (曲线B),KGdF4:Tb3+纳米粒子荧光强度略有下降。由此可以推断,KGdF4:Tb3+纳米粒子荧光的淬灭是因为适配体修饰后KGdF4:Tb3+纳米粒子通过ππ效应能够吸附到石墨烯表面,从而拉近了能量供体与能量受体间的空间距离,导致了荧光共振能量转移现象的发生。由此表明,具有适配体功能化的荧光生物探针是本实验建立的关键要素。

图5 KGdF4:Tb3+纳米粒子-适配体复合物与氧化石墨烯孵育后的荧光光谱(a)和KGdF4:Tb3+纳米粒子与氧化石墨烯孵育后的荧光光谱(b)Fig.5 Fluorescence spectra of KGdF4:Tb3+-aptamer after the incubation with graphene oxide (a),fluorescence spectra of the KGdF4:Tb3+after the incubation with graphene oxide(b)
2.6 线性范围与检测限
根据实验原理检测体系中不存在被测物四环素时荧光强度为最低值,随四环素质量浓度增加体系荧光强度随之增强,在最佳实验条件下,KGdF4:Tb3+纳米粒子在543 nm处的荧光发射峰与四环素质量浓度在0.5~100 ng/mL范围内呈现良好的线性关系 (图6a)。回归方程为y=430.0x+75 095(R2=0.993),最低检出限(3S/N)为 0.25 ng/mL,其中 y 为荧光强度,x为四环素质量浓度。10次重复检测10ng/mL的四环素溶液以评价该方法的精密度,其相对标准偏差为2.5%,因此本实验具较好的灵敏度与准确性。图6b为加入不同质量浓度四环素的荧光图谱。
2.7 特异性研究
为了评价本实验方法对于四环素的特异性,实验考察了与四环素类似的抗生素:金霉素、土霉素、强力霉素与氯霉素在此方法下的检测效果。在所构建的检测系统中,分别加入10 ng/mL的四环素、金霉素、土霉素、强力霉素与氯霉素,测定该检测体系荧光值,结果见图7。四环素在该检测体系中引起的荧光强度的变化远远高于其余四种物质。这是因为四环素适配体与四环素发生特异性结合,导致荧光共振能量转移体系破坏,荧光强度大幅的恢复;而四环素适配体对于其余四种物质不具备高亲合力,此时四环素适配体修饰的荧光纳米粒子仍大量的被氧化石墨烯所吸附,体系中的荧光被大幅的淬灭。综上所述,基于四环素适配体与四环素的高度特异性使得该检测方法具有良好的选择性。

图6 四环素质量浓度与体系荧光强度的标准曲线(a)和不同四环素质量浓度条件下体系的荧光图谱(b)Fig.6 Standard curve of the fluorescence intensity versus the tetracycline concentration(a),typical recording output for the detection of different concentrations of tetracycline using the developed method(b)

图7 四环素检测方法的特异性分析Fig.7 Specificity analysis of tetracycline detetion
2.8 加标回收实验
表1所示为本文方法测得的四环素质量浓度与应用传统高效液相色谱法所得的四环素质量浓度,二者结果基本一致,高效液相色谱法所得回收率在95.3%~102%之间,该实验方法所得回收率在96.1%~102.5%之间,说明本法可用于实际样品的检测。
3 结语
根据氧化石墨烯的紫外吸收光谱与KGdF4:Tb3+纳米粒子的荧光光谱相重叠这一现象,结合单链适配体与氧化石墨烯的π-π共轭作用及其与目标物质的高亲和力和高特异性,构建了一种利用荧光共振能量转移体系检测四环素的方法。本研究制备的KGdF4:Tb3+纳米粒子是一种低度的,具有良好生物相容性的绿色纳米材料,适配体为体外合成,成本低,稳定性好,特异性强。因而该方法操作简单、灵敏度高,可以作为检测四环素的备选方法。
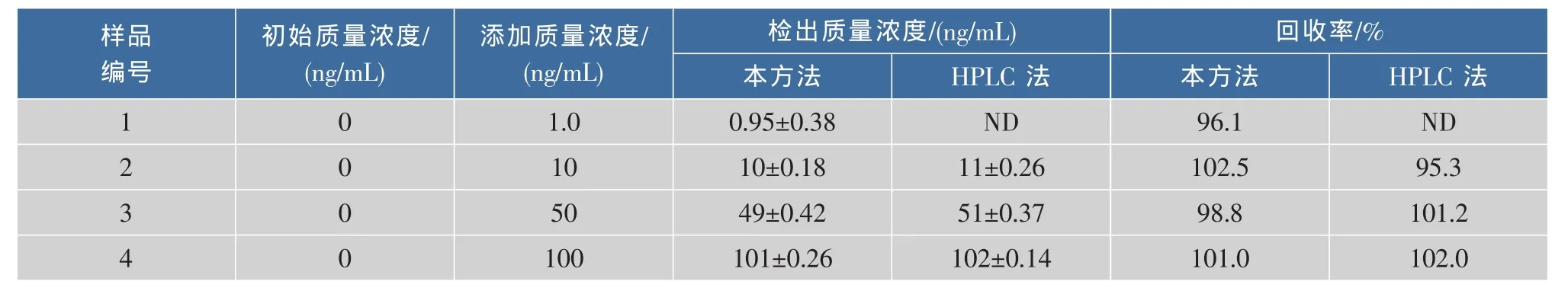
表1 牛奶样品中四环素的检测回收率(n=5)Table 1 Recovery of tetracycline detection in milk samples(n=5)
[1]陈一资,胡滨.动物性食品中兽药残留的危害及其原因分析[J].食品与生物技术学报,2009,28(2):162-166.CHEN Yizi,HU Bin.Reasons&harm of animal medicine remainder to animal material food[J].Journal of Food Science and Biotechnology,2009,28(2):162-166.(in Chinese)
[2]李银生,曾振灵.兽药残留的现状与危害[J].中国兽药杂志,2002,36(1):29-33.LI Yinsheng,ZENG Zhenling.Present situation and the harm of veterinary drug residue[J].Chinese Journal of Veterinary Drug,2002,36(1):29-33.(in Chinese)
[3]Slana M,Dolenc M S.Environmental risk assessment of antimicrobials applied in veterinary medicine-A field study and laboratory approach[J].Environmental Toxicology and Pharmacology,2013,35(1):131-141.
[4]黄邦富.兽药残留的危害及原因分析[J].福建畜牧兽医,2008,30(2):39.HUANG Banfu.The harm of veterinary drug residue and reason analysis[J].Fujian Animal Husbandry and Veterinary,2008,30(2):39.(in Chinese)
[5]Kurittu J,Lonnberg S,Virta M,et al.A Group-specific microbiological test for the detection of tetracycline residues in raw milk[J].Journal of Agricultural and Food Chemistry,2000,48:3372-3377.
[6]Choma I M.TLC Determination of tetracyclines in milk[J].Journal of Planar Chromatography,2000,13:261-265.
[7]Cinquina A L,Longo F,Auastasi G,et al.Validation of a high-performance liquid chromatography method for the determination of oxytetracycline,tetracycline,chlortetracycline and doxycycline in bovine milk and muscle[J].Journal of Chromatography A,2003,987(1/2):227-233.
[8]罗庆,孙丽娜,胡筱敏.固相萃取-高效液相色谱法测定畜禽粪便中罗红霉素和 3种四环素类抗生素 [J].分析试验室,2014,33(8):885-888.LUO Qing,SUN Lina,HU Xiaomin.Simultaneous determination of roxithromycin and three tetracyclines in manure by highperformance liquid chromatography with a diode-array detector[J].Chinese Journal of Analysis Laboratory,2014,33(8):885-888.(in Chinese)
[9]岳振峰,邱月明,林秀云,等.高效液相色谱串联质谱法测定牛奶中四环素类抗生素及其代谢产物[J].分析化学,2006,34(9):1255-1259.YUE Zhenfeng,QIU Yueming,LIN Xiuyun,et al.Determination of multi-residues of tetracyclines and their metabolites in milk by high performance liquid chromatography-tandom positive-ion electrospray ionization mass spectrometry[J].Chinese Journal of Analytical Chemistry,2006,34(9):1255-1259.(in Chinese)
[10]檀尊社,陆恒,邵伟,等.胶体金免疫层析法快速检测水产品中四环素类药物残留[J].西北农业学报,2010,19(8):32-37.TAN Zunshe,LU Heng,SHAO Wei,et al.Nanocolloidal gold-based immunoassay for rapid detection of tetracy residue in aquatic products[J].Acta Agriculturae Boreali-Occidentalis Sinica,2010,19(8):32-37.(in Chinese)
[11]陈玲,万宇平,邵兵,等.牛奶中β-内酰胺和四环素类抗生素二联检测试纸条的初步研究[J].食品与生物技术学报,2012,31(7):776-783.CHEN Ling,WAN Yuping,SHAO Bing.Study about combo detection strip of β-lactams and tetracyclines in milk[J].Journal of Food Science and Biotechnology,2012,31(7):776-783.(in Chinese)
[12]Ju Q,Tu D,Liu Y S,et al.Amine-functionalized lanthanide-doped KGdF4nanocrystals as potential optical/magnetic multimodal bioprobes[J].Journal of the American Chemical Society,2012,134(2):1323-1330.
[13]Ju Q,Tu D,Liu Y S,et al.Lanthanide-doped inorganic nanocrystals as luminescent biolabels[J].Combinatorial Chemistry&High Throughput Screening,2012,15(7):580-594.
[14]马文石,周俊文,程顺喜.石墨烯的制备与表征[J].高校化学工程学报,2010,24(4):719-722.MA Wenshi,ZHOU Junwen,CHENG Shunxi.Preparation and characterization of graphene [J].Journal of Chemical Engineering of Chinese Universities,2010,24(4):719-722.(in Chinese)
[15]杨文荣.功能化石墨烯在生物医学研究中的应用[J].云南民族大学学报:自然科学版,2011,20(5):327-332.YANG Wenrong.Functional grarhene:A novel plateform for biomedical applications[J].Journal of Yunnan University of Nationlities:Natural Sciences Edition,2011,20(5):327-332.(in Chinese)
[16]吴呈珂,郑立庆,冯素玲.基于氧化石墨烯识别特定双螺旋 DNA[J].分析试验室,2013,32(4):52-55.WU Chengke,ZHENG Liqing,FENG Suling.Sequence specific recognition of double-stranded DNA with graphene oxide[J].Chinese Journal of Analysis Laboratory,2013,32(4):52-55.(in Chinese)
[17]胡耀娟,金娟,张卉,等.石墨烯的制备、功能化及在化学中的应用[J].物理化学学报,2010,26(8):2073-2086.HU Yaojuan,JIN Juan,ZHANG Hui,et al.Graphene:systhesis,functionalization and applications in chemistry[J].Wuli Huaxue Xuebao,2010,26(8):2073-2086.(in Chinese)
[18]许春萱,吴志伟,曹凤枝,等.羧基化石墨烯修饰玻碳电极测定水样中的痕量铅和镉[J].冶金分析,2010,30(8):30-34.XU Chunxuan,WU Zhiwei,CAO Fengzhi,et al.Determination of trace lead and cadmium in water sample with carbonylated graphene modified glassy carbon electrode[J].Metallurgical Analysis,2010,30(8):30-34.(in Chinese)
[19]Niazi J H,Lee S J,Gu M B.Single-stranded DNA aptamers specific for antibiotics tetracyclines[J].Bioorganic&Medicinal Chemistry,2008,16(15):7245-7253.
[20]Hummers W S,Offeman R E.Preparation of graphitic oxide[J].Journal of the American Chemical Society,1958,80:1339.
