纳米零价铁去除水中微量N-亚硝基二甲胺的研究
2014-12-14李咏梅同济大学环境科学与工程学院污染控制与资源化研究国家重点实验室上海200092
杨 娟,李咏梅 (同济大学环境科学与工程学院,污染控制与资源化研究国家重点实验室,上海 200092)
纳米零价铁去除水中微量N-亚硝基二甲胺的研究
杨 娟,李咏梅*(同济大学环境科学与工程学院,污染控制与资源化研究国家重点实验室,上海 200092)
采用纳米零价铁催化降解水中微量N-亚硝基二甲胺(NDMA),并研究了溶解氧、纳米铁投加量、NDMA初始浓度、初始pH值、温度对纳米铁降解NDMA的影响.结果表明,纳米铁可以在中性厌氧条件下有效降解NDMA,作用效果远胜于普通铁粉;其对NDMA的去除速率随着纳米铁投加量的增加而增大,但与NDMA初始浓度无关;pH值降低或温度升高均有利于NDMA的降解.纳米铁降解NDMA存在一个启动期,启动期的长短与pH值和反应温度有关,提前活化纳米铁能有效提高反应速率.NDMA的降解产物主要是DMA和NH4+,其他产物如UDMH需进一步确认.
NDMA;纳米零价铁;厌氧;pH值;降解产物
N-亚硝基二甲胺(NDMA)是一种新型消毒副产物,主要产生于氯胺消毒过程.NDMA的慢性毒性作用可引起肝癌、肺癌、以及神经系统的损伤,致癌风险远高于卤代消毒副产物[1].世界癌症研究机构(IARC)将其定为2A类致癌物[2].研究发现NDMA存在于奶酪、腌制熏制食品(尤其是鱼、肉)中,另外酒精饮品、化妆品、烟草烟雾、人体体内均可检测出NDMA[3].NDMA也广泛存在于工业产品中,例如火箭燃料、橡胶制品、润滑油、除草剂、杀虫剂等[4].根据美国的调查,城市的污水处理厂氯消毒过程中产生的NDMA的量在 20~400ng/L[2],有时甚至能达到 1000ng/L[5].鉴于NDMA的高致癌性,一些国家和地区制定了NDMA的饮用水公共健康标准.加拿大全国范围内NDMA的饮用水卫生标准为40ng/L[6],美国加利福尼亚州为 3ng/L[7],日本为 100ng/L[8].去除水中 NDMA的方法有很多种,包括生物降解[9-10],光降解[11-13],光催化氧化[14-16],高级氧化[17-18],催化还原[19-21]等,其中金属还原法是催化还原的重要部分.
近20年来,纳米零价铁(NZVI)颗粒由于其粒径小,比表面积大,表面活性强而受到国内外学者广泛关注,其在环境领域的应用研究与日俱增.目前,NZVI及其双金属颗粒已成功用于修复被有机氯化物、硝基苯类、硝酸盐、高氯酸盐、重金属等污染的地下水,并表现出比普通零价铁更独特的优势.Gui等[19]研究普通铁粉对NDMA的降解,发现铁降解NDMA的过程符合伪一级动力学,其平均半衰期约为(13±2)h.Zhang等[23]研究表明,NZVI可用于去除地下水中的 NDMA.Lin等[24]研究发现 Al2(SO4)3可以提高 NZVI对NDMA的去除率.但对NZVI降解微量NDMA的具体研究鲜见报道,NZVI的作用是否优于普通铁粉也未知.本试验研究了NZVI对于NDMA的降解情况及其影响因素,以期为 NZVI用于NDMA去除提供理论依据.
1 材料与方法
1.1 试剂与仪器
NDMA 标准品(Chemservice,99+%,美国),乙腈(Mok,HPLC 级,德国),超纯水(由 Millipore Milli-Q system制得);还原铁粉及其他药品均为分析纯,购自国药集团试剂有限公司,其中还原铁粉的平均粒径 42.5µm.纳米零价铁购自阿拉丁(纯度>99.9%),粒径分布范围为(50±20)nm,比表面积为20m2/g.
所用仪器包括气浴恒温振荡器(ZD-85),高效液相色谱仪(Aglient 1200),总有机碳分析仪(岛津,CPH型),真空冷冻干燥机,透射电镜(JEM2010),激光粒度仪(MS3000h),紫外分光光度计,pH计等.
1.2 试验方法
用超纯水配置100µg/L的NDMA溶液,不调pH值,溶液pH值为6.5左右.在125mL锥形瓶中加入100mL上述NDMA溶液,连续氮吹30min,去除溶液中的溶解氧,加入0.75gNZVI颗粒或普通铁粉颗粒,密闭后放入气浴恒温振荡器中避光震荡,调节振荡器温度维持在 25℃,转速为200r/min.定时取样,样品经0.22µm滤膜过滤分离NZVI颗粒,从而终止反应,所得水样以备分析.在研究NDMA降解产物的实验中,将NDMA浓度提升至10mg/L,其余条件均不变.
好氧条件下,NDMA溶液不经过氮吹,锥形瓶开口置于恒温震荡器中震荡;分别改变单因素变量NZVI投加量、NDMA初始浓度、pH值、恒温振荡器温度,研究这些因素对 NZVI作用效果的影响.溶液 pH值用 0.1mol/L的 H2SO4和NaOH溶液调节.
1.3 分析方法
采用高效液相色谱法定量分析测定 NDMA浓度,色谱柱为 C18柱(250mm×4.6mm,填料粒径5µm,Supelco),流动相体积比为乙腈/水=5/95,总流量为 1mL/min,紫外检测波长为 230nm;DMA用4%异硫氢酸苯酯衍生化后用高效液相色谱法分析测定[18];氨氮浓度用纳氏试剂分光光度法测定[25],总有机碳(TOC)和总有机氮(TN)用总有机碳分析仪(TOC-VCPH,日本岛津)分析.
2 结果与讨论
2.1 NZVI与普通铁粉的处理NDMA的效果比较
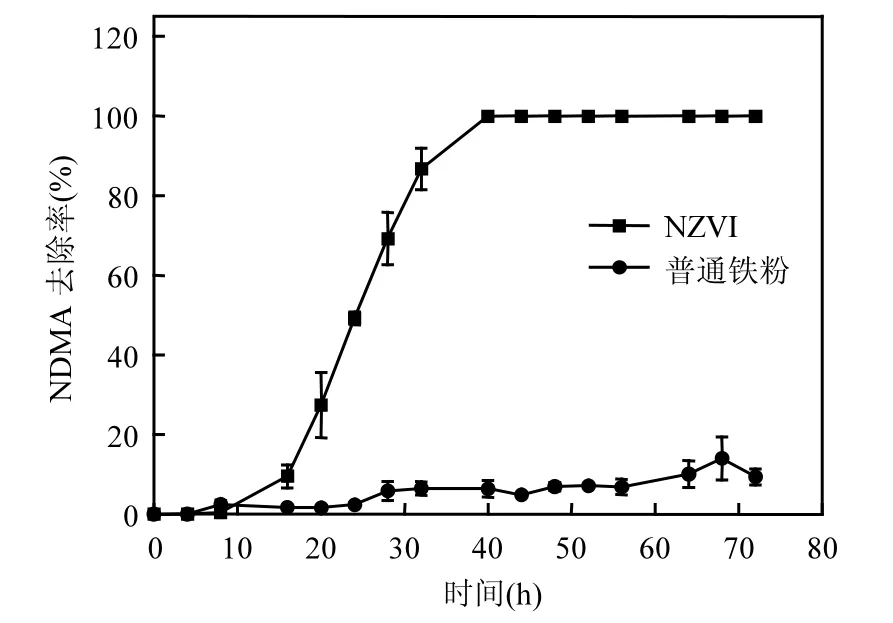
图1 NZVI与普通铁粉去除NDMA效果比较Fig.1 Comparison of NDMA reduction by NZVI and commercial iron powders
图1显示了NZVI与普通铁粉在相同条件下对NDMA的不同去除效果.中性条件下普通铁粉在72h内对100µg/L的NDMA几乎没有去除效果,而NZVI则可获得99%以上的去除率.李海莹等[26]研究NZVI的脱硝反应中证明了NZVI之于普通铁粉的优越性,并认为这是由于球形颗粒的比表面积与直径成反比,随着颗粒变小,粒子比表面积显著增大,增加了与反应物的接触面积,加大了活性原子的碰撞几率;同时表面原子所占的百分比显著提高,使纳米粒子的物理化学活性大幅度提高,从而对污染物有较高的去除率.
2.2 NZVI降解NDMA的影响因素
2.2.1 溶解氧 图2为厌氧和好氧条件下NZVI对 NDMA 去除率的影响.NZVI颗粒初始投加量为 7.5g/L,反应 72h,在好氧和厌氧的情况下,初始浓度为100µg/L的NDMA的去除率分别为32%和100%.在天然水体中,与纳米铁发生腐蚀反应的主要是溶解氧和水[27],其反应式如式(1)、式(2)所示.试验测得好氧条件下,溶液中的溶解氧维持在7.6~9.4mg/L之间.溶解氧的存在,使NZVI发生式(1)的反应,O2会与H2O竞争NZVI,使溶液中产生活化氢的反应受阻;同时,O2作为一种强氧化剂,氧化性远高于NDMA,能与活化氢快速反应,从而阻碍了NDMA的还原.在厌氧条件下,溶液中不存在溶解氧,NZVI只与 H2O反应,生成的活化氢可以顺利还原NDMA,使NDMA得到有效降解.因此,厌氧条件更有利于 NZVI去除 NDMA.以下试验均在厌氧条件下进行.
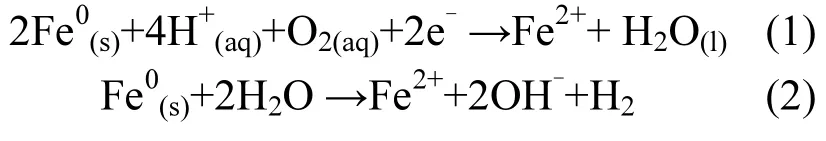
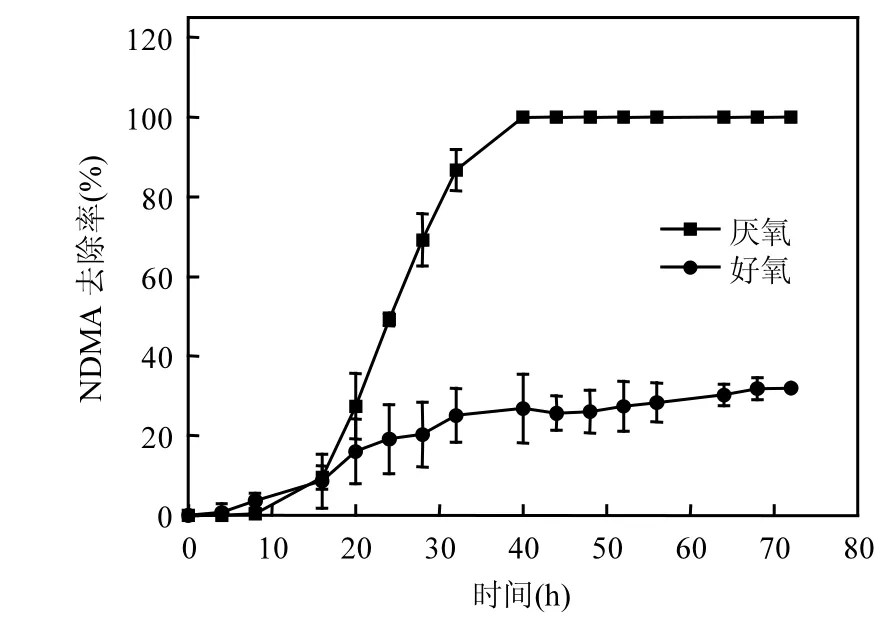
图2 厌氧和好氧条件下NDMA去除率的比较Fig.2 Comparison of NDMA reduction under aerobic and anaerobic conditions
2.2.2 NZVI投加量 图3为不同NZVI投加量对于NDMA去除率的影响.NZVI初始投加量由2.5g/L增加到 5.0g/L,反应 72h,初始浓度为100µg/L的 NDMA 的去除率由不足 10%增至99%以上;当 NZVI初始投加量增加到 7.5g/L,NDMA的去除时间可以大大缩短,在40h内去除率即可达到 99%以上;继续增大初始投加量至10.0g/L,NDMA的去除速率继续增大,但与投加量为 7.5g/L相比差异不显著.其原因在于 NZVI和水中NDMA的反应是固液界面上的反应,其反应速率和NZVI的表面形态和表面积有关,NZVI的投加量越大,其表面积也越大,可供反应的活性位点越多,对于 NDMA 的去除效果就越好,去除速率也会越快.但在NDMA初始浓度一定的情况下,所需的反应活性位点数量也是一定的,NZVI粉增加到一定投加量时,反应活性位点基本可满足NDMA降解的需要,其降解速率也不会再有明显的增加.
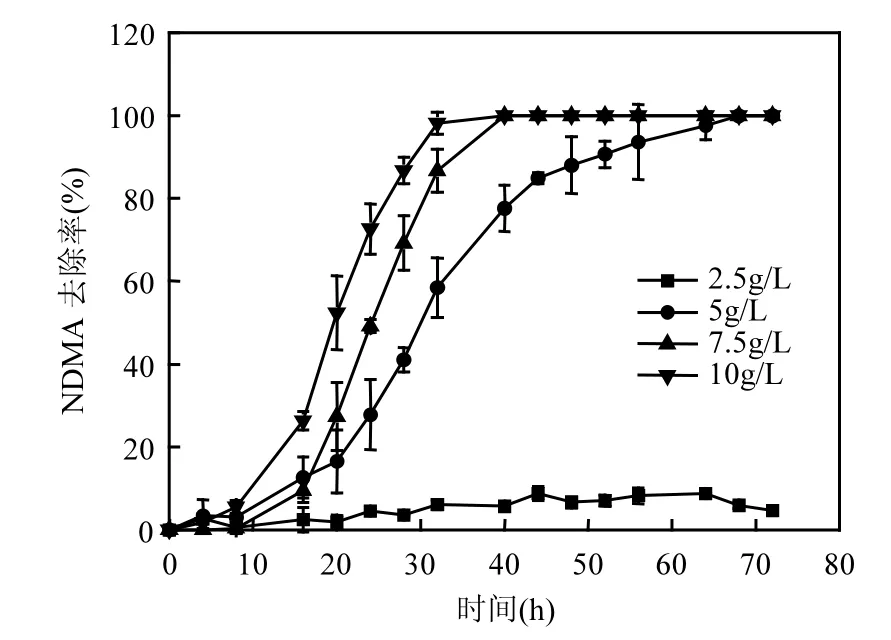
图3 NZVI投加量对NDMA去除率的影响Fig.3 The effect of initial NZVI dose on the reduction of NDMA
2.2.3 NDMA初始浓度 试验考察了不同NDMA初始浓度对NDMA去除率的影响,结果如图 4所示.当 NDMA 初始浓度由 100µg/L增至1000µg/L时,NDMA的去除率均达到99%以上,去除速率没有明显的变化.其原因是NZVI的投加量为 7.5g/L时,其活性位点的数量可以完全满足1000µg/L的NDMA的需要.事实上,在NDMA完全降解后继续在溶液中投加NDMA,剩余的NZVI仍可有效降解NDMA,NZVI的作用效果是可以持续的.同时,与NZVI的初始投加量相比,NDMA的浓度非常低,其浓度变化对NZVI的作用效果影响不显著,故其反应速率没有明显变化.
由图3和图4可以看出,NZVI降解NDMA的过程中,前 8~12h内 NDMA几乎不降解,之后NDMA浓度开始快速下降.因此,推测NZVI的作用可分为两个阶段,启动阶段和反应阶段.在启动阶段,由于NDMA的浓度非常小,在µg/L级,反应体系主要为 NZVI与水的反应,反应产生活化氢并缓慢积累,等到活化氢积累到一定程度才能够与NDMA发生还原反应,之后溶液中的活化氢维持在所需浓度,使 NDMA 持续缓慢降解.为了验证这一推测,在NZVI与水反应12h(活化)后再加入100µg/L的NDMA,结果如图5所示,经活化后NZVI对NDMA的降解率在6h内达到95%以上,降解速率显著加快,且不存在启动期.
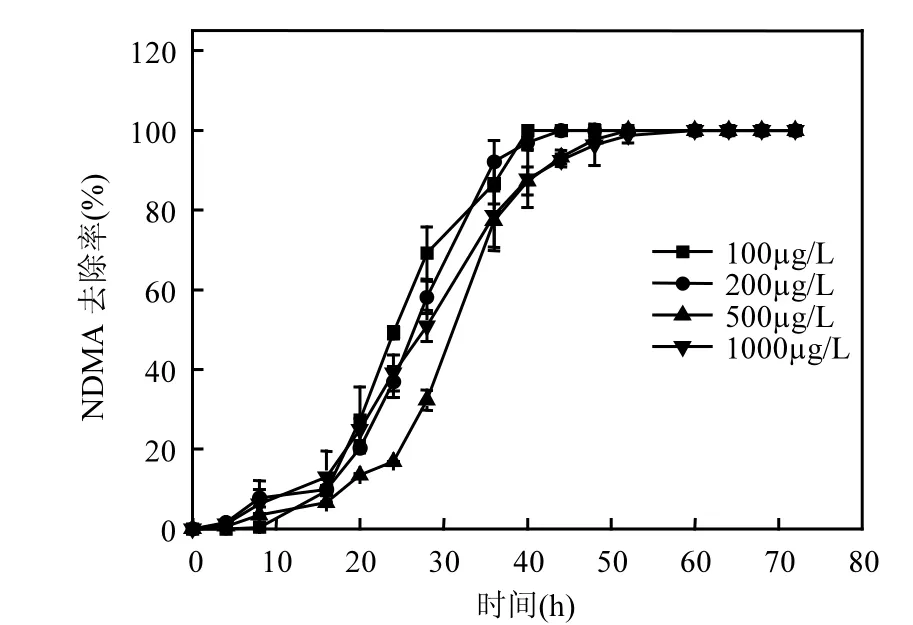
图4 NDMA初始浓度对NDMA去除率的影响Fig.4 The effect of initial NDMA concentration on the reduction of NDMA
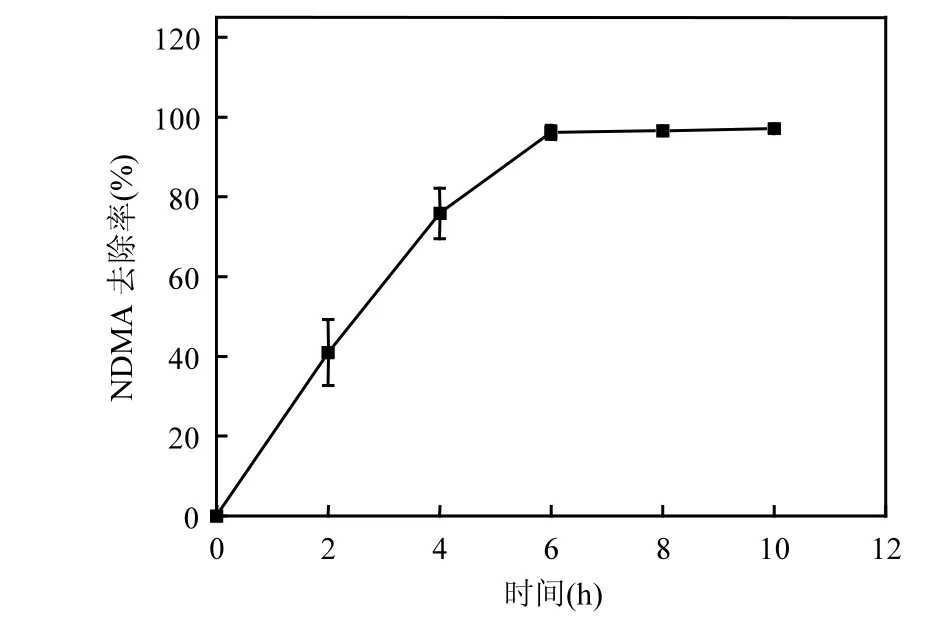
图5 NZVI活化12h对NDMA的去除率Fig.5 The reduction of NDMA when NZVI was activated for 12h
2.2.4 初始pH值 图6显示了不同初始pH值对 NDMA去除率的影响.溶液初始 pH值越低,NDMA降解的启动期越短,NDMA的去除率能越快地达到 99%以上.目前,NDMA 的还原机理主要是催化加氢.在酸性条件下,水中氢离子越多,被NZVI还原生成的活化氢原子越多,反应速率越快.同时,根据 Lee等[12]的研究,在溶液初始pH值较低时,NDMA呈质子化,质子化的NDMA具有更高的活性,更容易被还原.随着溶液 pH值的升高,产生的活化氢原子减少,反应速率逐渐下降.另外,Shu等[28]研究表明,当溶液为碱性时,溶液中的氢氧根离子与亚铁离子生成氢氧化亚铁沉积在NZVI的表面上,占据了NZVI的活性位点,阻碍亚铁离子的释放和活化氢的生成,pH 值越高,阻碍作用越显著.在pH<10的条件下,NZVI仍然有残留的活性位点可以和水反应产生一部分活化氢,用于还原NDMA.当pH=11时,NZVI与水的反应被彻底阻止,或是产生的活化氢与溶液中的OH-反应,从而无法还原NDMA.
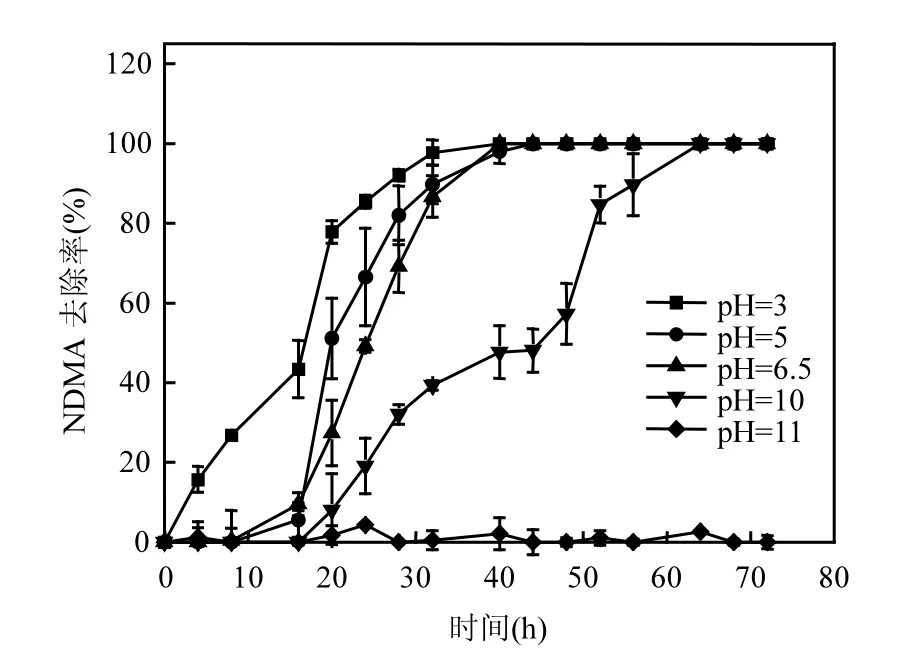
图6 初始pH值对NDMA去除率的影响Fig.6 The effect of initial pH on the reduction of NDMA
2.2.5 温度 图7显示了不同温度对NDMA去除率的影响.随着反应温度的升高,NDMA 降解的启动期缩短,NDMA的去除速率加快.这是由于温度升高一方面可以提高反应物的活化分子数,另一方面能够加快活化氢的产生速率,从而加快反应的进行.
2.3 NDMA降解动力学
NZVI降解NDMA的过程分为启动阶段和反应阶段,在启动阶段,NDMA 基本不降解,因此,对最佳反应条件下([Fe]0=7.5g/L,pH=6.5,转速=200r/min, T=25℃)反应阶段NZVI降解NDMA的过程进行了动力学分析.发现尽管NDMA初始浓度不同,但反应阶段NDMA的降解基本符合拟一级动力学模型,其动力学常数kobs用公式(3)确定.
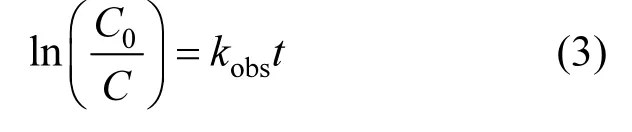
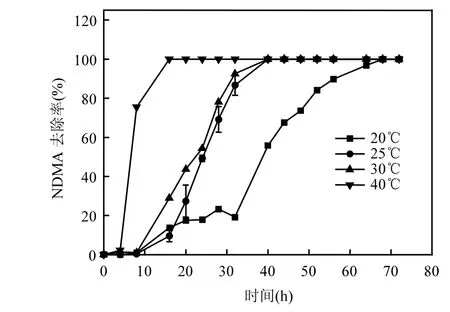
图7 温度对NDMA去除率的影响Fig.7 The effect of temperature on the reduction of NDMA
如表1所示,NDMA初始浓度变化对反应速率常数没有显著影响.进一步分析不同 pH值条件下的拟合参数,发现在酸性和中性条件下,NDMA的降解基本符合拟一级动力学模型,且pH 值越低,动力学常数 kobs越大,反应速率越快.而在碱性条件下,NDMA的降解不适合用拟一级动力学模型解释,这可能是受到碱性溶液中沉积在NZVI表面的氢氧化亚铁的影响.
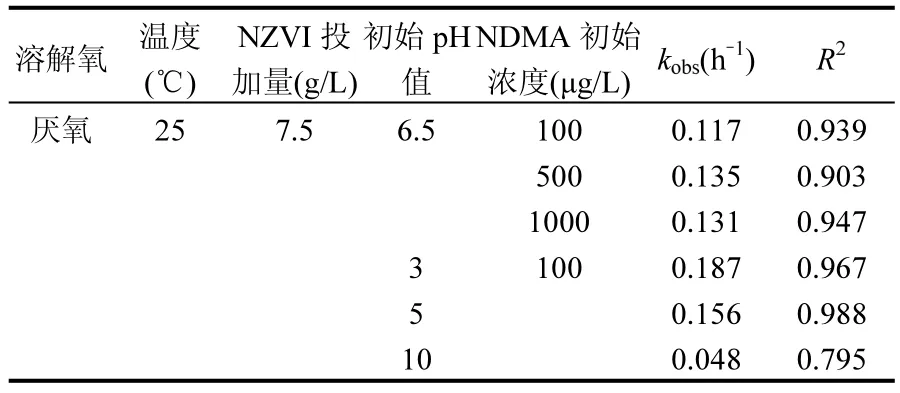
表1 不同条件下NZVI去除NDMA的拟一级动力学方程参数Table 1 Pseudo first-order kinetics parameters for reduction of NDMA with NZVI at different initial conditions
2.4 NZVI的表征
透射电镜(TEM)分析结果如图 8所示.反应前,NZVI颗粒为规则球形,整体成链状,存在一定的团聚现象,但因为团聚物具有较高的空隙率,对NZVI颗粒的整体比表面积影响不大[29],基本不影响 NZVI与反应物的接触,对反应没有影响.NZVI在厌氧条件下降解NDMA反应过程中,对反应72h的NZVI体系进行取样,经冷冻干燥后用TEM进行形貌观测.发现NZVI表面被明显腐蚀,由规则的球形变为不规则的块状结构,颗粒间蓬松的链状变得密实,因此比表面积减小,反应速率减慢.

图8 NZVI的透射电镜图:(a) 反应前,(b)反应后Fig.8 The TEM image of nanoscale Fe0particles: (a)before reaction (b)after reaction
2.5 NDMA降解产物
研究表明,还原降解NDMA的产物主要为偏二甲肼(UDMH)、二甲胺(DMA)、氨氮()、可能还会有二甲基二氮烯((CH3)2N2)、甲烷(CH4)、氮气(N2)等[30].本研究对中性条件下 NZVI(活化12h后使用)降解NDMA的产物进行了研究,测定了溶液中残留 NDMA的浓度及二甲胺(DMA)浓度的变化,并计算了氮质量平衡,如图 9所示.氨氮()的测定由于受到干扰数值偏大(计算其测试浓度高于理论投加氮含量),未能得到准确数值,但由于DMA和氨氮由同一个N=N键断裂得到,所以氨氮的浓度应该与DMA的浓度相近[22].根据产物的氮质量平衡计算,发现DMA的氮含量只占投加的理论氮含量的 20%左右,加上氨氮后氮含量也不过为40%,另有 60%的氮质量损失.因此,除了这两种产物之外,还有其他降解产物存在.测定溶液中的实际TN和TOC后,发现反应前后,TN和TOC基本没有发生变化,说明NDMA的降解产物中不存在CH4和N2等气体物质.根据Han等[22]的研究,在中性条件下用零价锌降解 NDMA,在所得 56%的氮质量平衡中,中间产物偏二甲肼(UDMH)占了48%,为NDMA的主要还原产物.而在氨氮的测定中,排除了溶液中铁离子的影响后,氨氮的测定可能是受到含-NH2的有机物的影响.因此,推测在损失的氮质量中可能还存在UDMH,但由于UDMH标样难以获得,需要进一步分析确认.

图9 反应过程中NDMA及其降解产物DMA的变化Fig.9 Changes of NDMA and its product DMA during NDMA reduction with NZVI
3 结论
3.1 在中性厌氧条件下,NZVI能有效去除水中微量NDMA,7.5g/L的NZVI反应40h,NDMA去除率可以达到100%,与普通铁粉降解NDMA相比具有很大的优越性.溶液中的溶解氧对NDMA的降解有显著的影响,厌氧条件更有利于 NZVI去除NDMA,且NZVI投加量越大,NDMA的去除效果越好.
3.2 在厌氧条件下,NZVI通过Fe0-H2O体系发生明显腐蚀,并团聚成密实结构.Fe0-H2O反应产生活化氢,积累到一定程度后与溶液中的NDMA发生催化加氢反应.活化氢积累的过程为启动期.
3.3 pH值对NZVI降解NDMA具有一定的影响.酸性条件有利于活化氢的产生,能够缩短启动期,加快NDMA的降解速率;随着pH值的增高,活化氢的生成反应受阻,启动期延长,NDMA的降解速率降低.NDMA的初始浓度对NZVI降解NDMA的速率基本没有影响.温度升高有利于NDMA 的降解,温度越高,反应的启动期越短,反应速率越快.
3.4 在酸性和中性条件下,NDMA的降解符合拟一级动力学模型,且pH值越低,动力学常数kobs越大,反应速率越快.
3.5 中性条件下,NDMA的还原产物主要为DMA和氨氮,另外可能有UDMH等中间产物存在,需要进一步研究确定.
[1]吕 娟,李咏梅.NDMA在水处理过程中产生与去除的研究进展 [J]. 水资源与水工程学报, 2011,22(3):58-62.
[2]Integrated Risk Information System (IRIS), United States Environmental Protection Agency (EPA), N-Nitrosodimethylamine (CASRN 62-75-9). http://www.epa.gov/iris/subst/0045.htm, 2012.
[3]Najm I, Trussell R R.NDMA Formation in Water and Wastewater[J]. American Water Works Association. 2001,93(2):92–99.
[4]古 楠,刘永东,钟儒刚.N-亚硝基二甲胺(NDMA)的环境过程和毒理效应 [J]. 生态毒理学报, 2013,8(3):338-343.
[5]Gan J, Bondarenko S, Ernst F, et al. Leaching of N-nitrosodimethylamine (NDMA)in turfgrass soils during wastewater irrigation [J]. Journal of Environmental Quality,2006,35(1):277– 284.
[6]Health Canada. N-nitrosodimethylamine (NDMA)in drinking water. http://www.hc-sc.gc.ca/ewh-semt/pubs/water-eau/ndma/index-eng.php, 2011.
[7]California Department of Public Health. NDMA and other nitrosamines–drinking water issues. http://www.cdph.ca.gov/certlic/drinkingwater/pages/NDMA.aspx, 2013.
[8]Sakai H, Takamatsu T, Kosaka K, et al. Effects of wavelength and water quality on photodegradation of N-Nitrosodimethylamine(NDMA)[J]. Chemosphere, 2010,89(6):702-707.
[9]Sharp J O, Sales C M, LeBlanc J C, et al. An inducible propane monooxygenase is responsible for N-nitrosodimethylamine degradation by Rhodococcus sp. strain RHA1 [J]. Applied and Environmental Microbiology, 2007,73(21):6930–6938..
[10]Sharp J O, Sales C M, Cohen L A. Functional characterization of propane-enhanced N-nitrosodimethylamine degradation by two actinomycetales [J]. Biotechnology and Bioengineering., 2010,107:924–932.
[11]Sakai H, Takamatsu T, Kosaka K, et al. Effects of wavelength and water quality on photodegradation of N-Nitrosodimethylamine(NDMA)[J]. Chemosphere, 2012,89(6):702–707.
[12]Lee C, Choi W, Kim Y G, et al. UV photolytic mechanism of N-nitrosodimethylamine in water: dual pathways to methylamine versus dimethylamine [J]. Environment Science and Technology,2005,39(7):2101–2106.
[13]Genuinoa H C, Njagia E C, Benbowa E M, et al. Enhancement of the photodegradation of N-nitrosodimethylamine in water using amorphous and platinum manganese oxide catalysts [J]. Journal of Photochemistry and Photobiology A: Chemistry, 2011,217(2/3):284–292.
[14]Xu B B, Chen Z L, Qi F, et al. Inhibiting the regeneration of N-nitrosodimethylamine in drinking water by UV photolysis combined with ozonation [J]. Journal of Hazardous Materials,2009,168(1):108–114.
[15]黄露溪,沈吉敏,徐冰冰,等.UV/H2O2降解水中微量NDMA的效能研究 [J]. 中国给水排水, 2010,26(5):104-108.
[16]Hiramoto K, Ryuno Y, Kikugawa K. Decomposition of N-nitrosamines, and concomitant release of nitric oxide by Fenton reagent under physiological conditions [J]. Mutation Research -Genetic Toxicology and Environmental Mutagenesis, 2002,520:103-111.
[17]Lee C, Yoon J, Von G U. Oxidative degradation of N-nitrosodimethylamine by conventional ozonation and the advanced oxidation process ozone/hydrogen peroxide [J]. Water Research, 2007,41(3):581–590.
[18]Lv J, Li Y M, Song Y. Reinvestigation on the ozonation of N-nitrosodimethylamine: Influencing factors and degradation mechanism [J]. Water Research, 2013,47(14):4993–5002.
[19]Gui L, Gillham R W, Odziemkowski M. Reduction of N-nitrosodime-thylamine with granular iron and nickel-enhanced iron.1.Pathways and knetics [J]. Environment Science and Technology, 2000,34(16):3489-3494.
[20]Frierdich A J, Sharpley J R, Strathmann T J. Rapid Reduction of N-Nitrosamine Disinfection Byproducts in Water with Hydrogen and Porous Nickel Catalysts [J]. Environment Science and Technology, 2008,42(1):262-269.
[21]Davie M G, Shih K, Pacheco F A, et al. Palladium-Indium Catalyzed Reduction of N-Nitrosodimethylamine: Indium as a Promoter Metal [J]. Environment Science and Technology,2008,42(8):3040-3046.
[22]Han Y, Chen Z L, Tong L N, et al. Reduction of NNitrosodimethylamine with zero-valent zinc [J]. Water Research,2013,47(1,1):216-224.
[23]Zhang W X.Nanoscale iron particles for environmental remediation: An overview [J]. Journal of Nanoparticle Research,2003,5:323–332.
[24]Lin L, Xu B, Lin Yi-Li, et al. Reduction of NNitrosodimethylamine (NDMA)in aqueous solution by nanoscale Fe/Al2(SO4)3[J]. Water, Air and Soil Pollution, 2013,224(1632):2-9.
[25]国家环境保护局水和废水监测分析方法 [M]. 4版.北京:中国环境科学出版社, 2002:105-284.
[26]李海莹,王 薇,金朝晖,等.纳米铁的制备及其对污染地下水的脱硝研究 [J]. 南开大学学报(自然科学版), 2006,39(1):8-13.
[27]Crane R A, Scott T B. Nanoscale zero-valent iron: Future prospects for an emerging water treatment technology [J]. Journal of Hazardous Materials, 2012,211–212:112–125.
[28]Shu H Y, Chang M C, Chen C C, et al. Using resin supported nano zero-valent iron particles for decoloration of Acid Blue 113azo dye solution [J]. Journal of Hazardous Materials, 2010,184(1-3):499–505.
[29]Hwang Y H, Kim D G, Shin H S. Mechanism study of nitrate reduction by nano zero valent iron [J]. Journal of Hazardous Materials, 2011,185(2/3):1513–1521.
[30]韩 莹.零价锌还原降解水中 N-亚硝基二甲胺的效能与机理研究 [D]. 哈尔滨:哈尔滨工业大学, 2009.
Removal of trace n-nitrosodimethylamine using nanoscale zero-valent iron.
YANG Juan, LI Yong-mei*(State Key Laboratory of Pollution Control and Resources Reuse, College of Environmental Science and Engineering, Tongji University, Shanghai 200092, China). China Environmental Science, 2014,34(7):1696~1702
Removal of trace N-Nitrosodimethylamine (NDMA)using nanoscale zero-valent iron (NZVI)was studied as a potential technology. Effects of dissolved oxygen, initial concentration of NZVI, initial NDMA concentration, pH and temperature on the degradation of NDMA was investigated. NDMA was effectively removed by NZVI from deoxygenated solution under neutral condition, while the removal of NDMA was limited using common commercial iron powders. The removal rate increased with the increase of initial NZVI dosage, while the effect of initial NDMA concentration is not remarkable. Lower pH and higher temperature facilitated the reduction of NDMA with NZVI. There existed a lag period for the reduction of NDMA and the lag time was influenced by pH and temperature. When NZVI was pre-activated in water for 12h, the removal rate of NDMA was sharply improved. The main degradation products were DMA and NH4+;other products, such as UDMH, need further investigation.
N-Nitrosodimethylamine;nanoscale zero-valent iron;anaerobic;pH;degradation product
X523
A
1000-6923(2014)07-1696-07
2013-10-29
国家自然科学基金资助项目(50878165)和新世纪优秀人才支持计划(NCET-08-0103)
* 责任作者, 教授, liyongmei@tongji.edu.cn
杨 娟(1988-),女,浙江绍兴人,同济大学硕士研究生,主要从事污水处理和资源化研究.
