N,N-乙基苄基苯胺合成新工艺
2014-12-11陈伟东张红艳郑鑫梁金建英
陈伟东 张红艳 郑鑫梁 金建英
(1、3浙江闰土股份有限公司 浙江绍兴 312300)
(2.浙江新丰环保科技有限公司 浙江绍兴 312300)
(4.上虞市通利流体控制有限公司 浙江绍兴312352)
N,N-乙基苄基苯胺是用于制造酸性淡绿SF以及其他蓝色染料的重要中间体[1]。目前工业上主要工艺为:在反应釜中,投入N-乙基苯胺,一边冷却一边加入氯化苄,然后于100℃下保温反应12h。用氢氧化钠溶液中和洗涤后,经真空蒸馏即得成品。我们通过加入适量催化剂,采用合成与分离一步进行的方法,对该产品进行了工艺改进,得到高收率、高纯度的N,N-乙基苄基苯胺[2~4]。按照此方法可以缩短反应时间,减少原料消耗,同时简化工业单元操作,具有可观的经济效益。
一、实验部分
1.试剂及投料表:
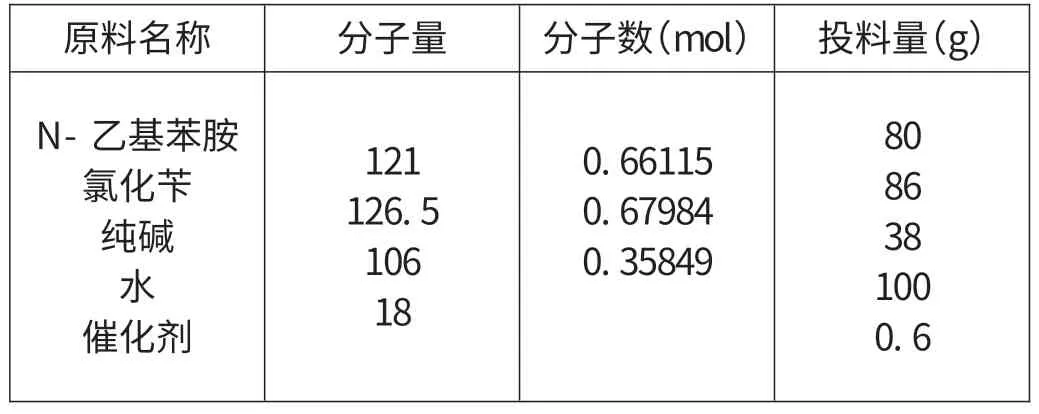
原料名称分子量分子数(mol)投料量(g)N-乙基苯胺121 0.66115 80氯化苄126.50.6798486纯碱1060.3584938水18100催化剂0.6
2.仪器:JJ-1增力电动搅拌器,智能数显控温仪,GC-14C型高效气相色谱仪。
3.实验原理:N-乙基苯胺和氯化苄在纯碱溶液下进行反应,反应生成的盐酸与纯碱反应吸收,从而使反应正向进行。再通过添加少量催化剂,加快反应速度,同时提高反应产物的纯度和收率[5-7]。反应的方程式如下:

4.实验方法:将水及纯碱溶解好后加入装有回流冷凝管的500ml三口烧瓶中,再加入N-乙基苯胺,氯化苄,催化剂,搅拌均匀,升温至适当温度后反应。取样,进行H PGC分析,合格后鼓泡吹出多余氯化苄,静置分层,上层油相液体即为产品。
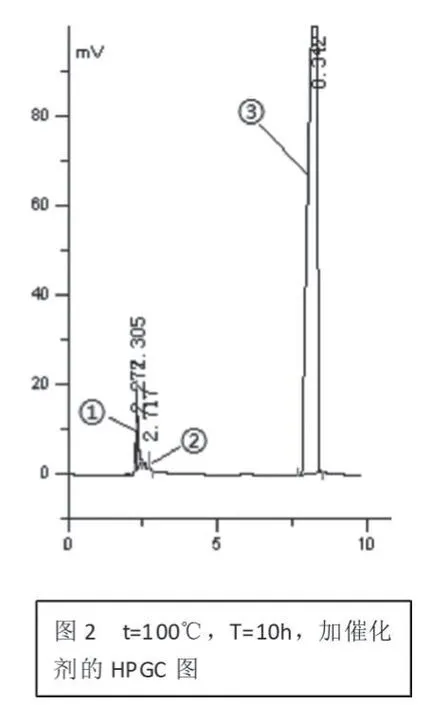
5.分析条件及方法:柱温190℃,气化室280℃,检测室280℃,柱前压100M Pa。此分析条件下得到了理想的高效气相色谱图,如图1和图2所示。主要峰是:①氯化苄,②N-乙基苯胺,③N,N-乙基苄基苯胺。其具体位置通过标准样得到证实。
二、结果与讨论
为了探索最佳反应条件,我们改变反应温度、反应时间以及催化剂的加入等因素,考察了这些因素的改变对于反应的影响。
1.反应温度对反应的影响
反应时间10h,加催化剂,在不同反应温度下原料与产物浓度的变化的结果如表1所示,趋势如图3所示。
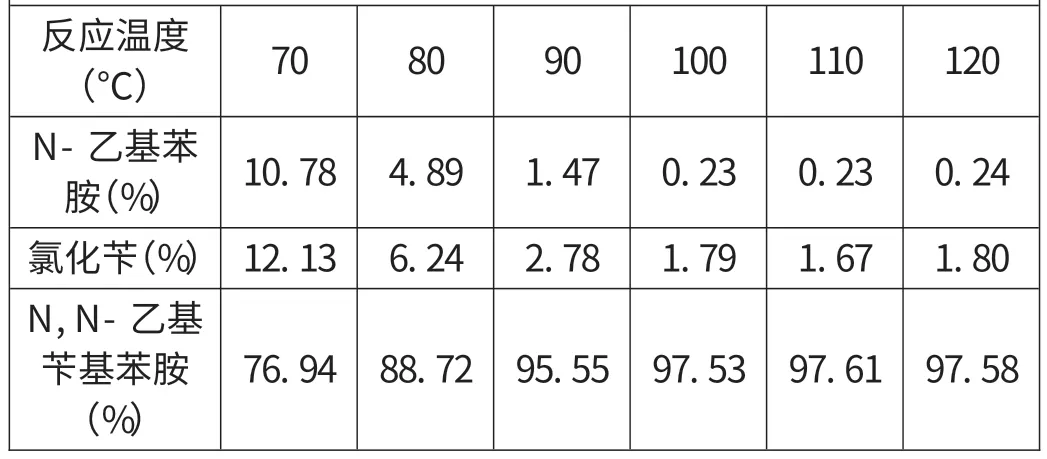
表1 反应温度与H PGC的关系
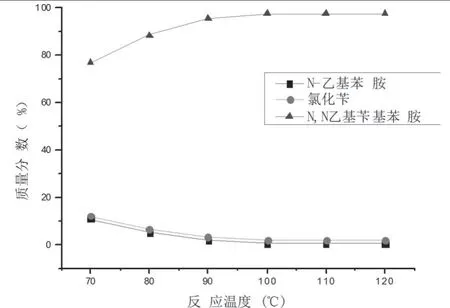
图3反应温度对原料及产物浓度的影响Fig 3

结果表明,在70~100℃,随着反应温度的提高,原料浓度呈现下降趋势,而产物浓度呈现上升趋势;该反应与普通化学反应一样,随着温度的上升,分子活化能提高,原料分子之间更容易碰撞,反应速度加快,因此产物浓度随温度的升高而上升。而反应温度超过100℃后,原料浓度并未呈现显著下降趋势,而产物浓度也并未呈现出显著上升趋势;其主要原因在于分子活化能对产物浓度的影响达到极限,分子间碰撞程度的加强不足以再提高产物的浓度。综上所述,反应温度为100℃,既可以达到较高的收率,又可以节约能源。因此,选择反应温度为100℃为最佳。
2.反应时间对反应的影响
反应温度100℃、加催化剂,在不同反应时间下的原料及产物浓度随反应时间变化的结果如表2所示,趋势如图4所示。

表2 反应时间与H PGC的关系

图4 反应时间对原料及产物浓度的影响Fig 4
结果表明,在10h之前,随着反应时间的增加,产物浓度呈现增加趋势,而原料浓度呈现下降趋势。而10h之后产物浓度几乎不再增加,主要原因在于10h产物产率几乎达到极限,因此随着反应时间的延长,产物浓度几乎不再增加。因此选择反应时间10小时较为理想。
3.催化剂对反应的影响
反应温度100℃,催化剂对产物产率的影响结果如表3所示,趋势如图5所示
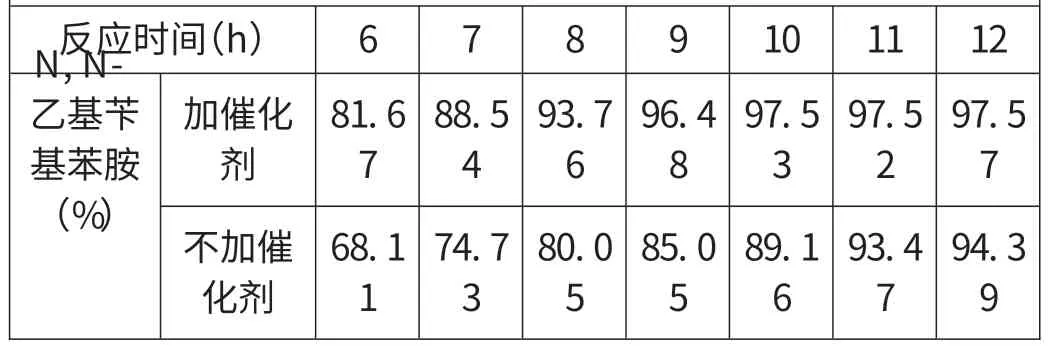
表3 反应时间与反应转化率的关系
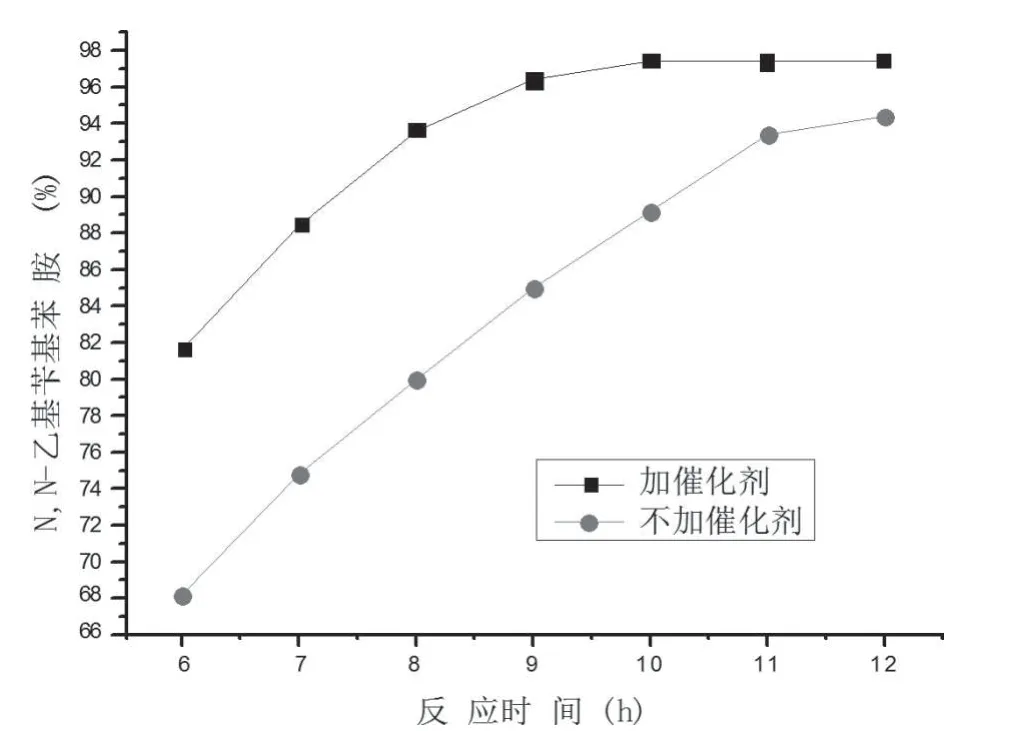
图5 催化剂对产物浓度的影响Fig 5
由图5可知,催化剂的加入,不仅可以大大缩短反应时间,提前达到终点,并且在相同的反应时间内,产物浓度也获得较高的提高,这是由于本反应为有机相和无机相两液相间反应,催化剂的加入于两相间反应有利。采用加入较少的催化剂而获得较快的反应速度,不仅可以大大缩短反应时间,提高单位生产效率,而且有利于降低劳动成本,显著提高经济效益。
4.稳定性实验
反应温度定为100℃,反应时间定为10小时,加入催化剂,连续进行6批稳定性实验,具体试验结果如表4。

编号产品重(g)收率(%)H PGC(%)1 136.53 97.87 97.53 2 136.44 97.81 98.47 3 136.78 98.05 97.63 4 136.22 97.65 98.15 5 136.92 98.15 98.23 6 136.36 97.75 97.78平均136.54 97.88 97.97
结果表明在该反应条件下,反应产物收率较高,并且也相对稳定,收率平均值为97.88%,收率标准差为0.171561,离散度为0.146667。
结论
1.采用N-乙基苯胺和氯化苄在纯碱溶液中进行反应的方法,既可以及时吸收反应产生的盐酸,使反应正向进行,又控制了反应的PH条件,避免了氯化苄在高温强碱条件下水解产生苯甲醇而耗用大量的氯化苄。
2.通过在反应中添加少量催化剂,使反应速率加快,减少反应时间,同时也较大的提高了反应的转化率,具有客观的经济效益。3.该工艺采用合成与分离一步进行的方法,简化了工业单元操作,节约了生产成本,避免了多步操作带来的物料损失。
[1]杨新玮等,分散染料,化工工业出版社,10.(1989).
[2]何立,高立江,方标等.N-氰乙基苯胺清洁生产工艺[J].广东化工,2012,39(3):53-54,21.
[3]胡玉桥.N-乙基苄基苯胺的合成及微波有机合成反应的研究[D].大连理工大学,1995.
[4]华东理工大学.苄基取代的苯胺类化合物及其应用:中国,CN201410052487.8[P].2014-5-14.
[5]任宝晶;N-乙基-N-苄基苯胺合成工艺研究[J];皮革化工;1997年02期.
[6]李应成,胡玉桥,李攻本,袁云程,蒋育林;N-乙基-N-苄基苯胺合成方法的改进[J];合成化学;1997年02期.
[7]刘翠华,赵秀祯,尹静梅,高大彬;N,N-乙基苄基苯胺合成研究[J];染料工业;1998年03期.
