纳米碳引导腹腔镜中低位直肠癌根治术临床疗效探讨
2014-12-04佘盛飞曾莲英
佘盛飞 曾莲英
直肠癌手术中利用腹腔镜对直肠侧方的淋巴结探测效果不佳,手术时常常忽略了此部分的病变,容易对直肠癌患者产生不良的影响[1-3]。纳米碳引导腹腔镜中低位直肠癌根治术能够对直肠侧方的淋巴结进行识别并清除,从而有效降低复发率。本文旨在探究以纳米碳作为手术时的示踪剂,利用腹腔镜进行中低位直肠癌手术进行治疗的效果,现报道如下。
1 资料与方法
1.1 一般资料 将2006年6月-2012年6月90例直肠癌患者随机分为治疗组36例和对照组54例。两组患者的性别、年龄、TNM分期等基本资料比较差异均无统计学意义(P>0.05),见表1,具有可比性。所有患者对研究知情且同意,符合研究要求,研究经过医院伦理委员会批准实施。
1.2 研究方法 治疗组36例患者采用纳米碳引导下腹腔镜中低位直肠癌根治术治疗,对照组54例患者采用传统的腹腔镜手术进行治疗。对两组患者术中各项指标及术后并发症情况等进行统计和对比分析。
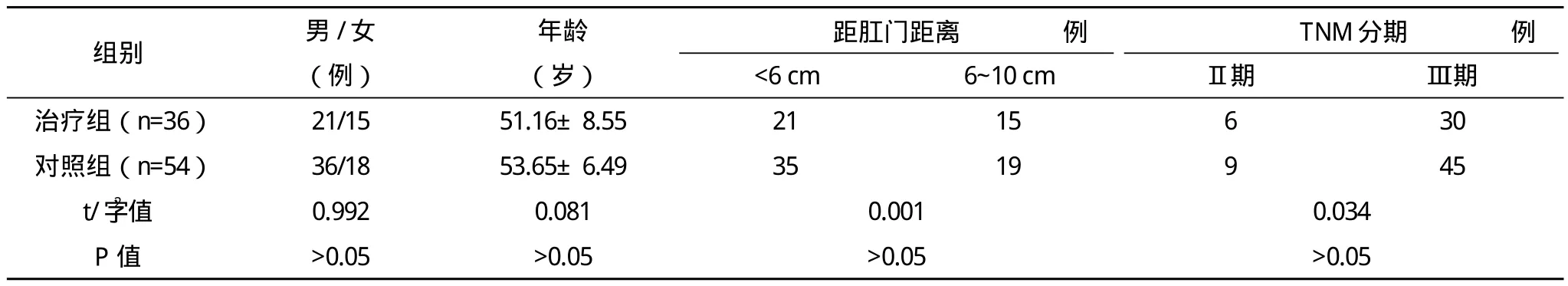
表1 两组患者基线资料比较
治疗组:首先,进行常规的四孔法建立气腹。建立气腹后利用腹腔镜进行探查。分离到肿瘤处,再将1 mL纳米碳慢慢注入肿瘤周围。然后,对全直肠系膜进行切除。切除后观察直肠侧方有无淋巴结染色,然后再对染色的淋巴结进行检获。对照组:首先,进行常规的四孔法建立气腹,并进行腹腔镜下探查。其次,在腹腔镜下对患者的乙状结肠进行分离[4-5]。然后,再进行肠系膜下动脉及静脉的处理。再对直肠根部的淋巴结进行清扫,并将直肠全系膜切除至距离肿瘤远端5 cm处。利用腹腔镜对直肠进行处理。在患者左下腹取4~5 cm大小的切口,提出患者直肠,并对直肠及肿瘤等病变部位进行切除。然后,对固定肠道吻合器进行缝合。缝合后将其置入腹腔内并实行关腹操作。最后,在腹腔镜监视下进行直结肠吻合,术区放置引流,并缝合关闭盆腔。
1.3 统计学处理 本文研究结果采用SPSS 21.0统计软件对得到的数据进行分析。计量资料以(x-±s)表示,采用t检验,计数资料采用x2检验,P<0.05为差异具有统计学意义。
2 结果
2.1 两组手术指标比较 治疗组患者手术时间、术中出血量、胃肠道恢复时间短于对照组,差异有统计学意义(P<0.05),肿块距下缘距离两组比较差异无统计学意义(P>0.05),见表2。
2.2 两组检获淋巴结数量比较 治疗组患者平均检获的淋巴结数、平均小于5 cm的淋巴结数量、平均阳性淋巴结检获数多于对照组,差异均有统计学意义(P<0.05),见表3。
表2 两组患者手术指标对比(±s)
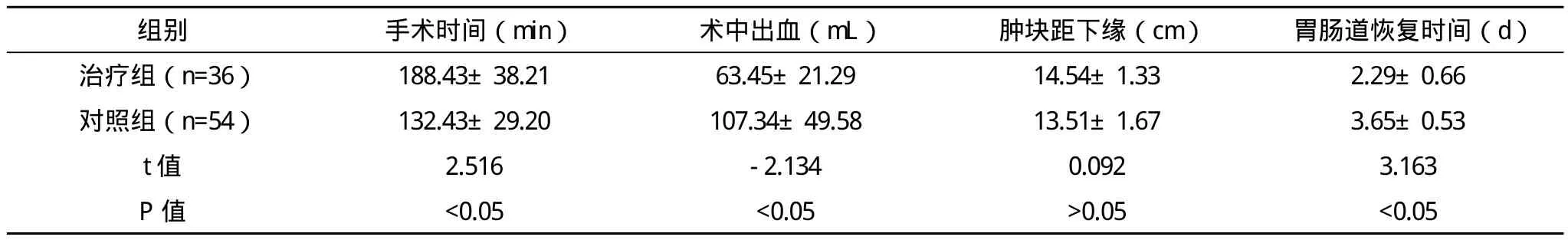
表2 两组患者手术指标对比(±s)
组别 手术时间(min) 术中出血(mL) 肿块距下缘(cm) 胃肠道恢复时间(d)治疗组(n=36) 188.43±38.21 63.45±21.29 14.54±1.33 2.29±0.66对照组(n=54) 132.43±29.20 107.34±49.58 13.51±1.67 3.65±0.53 t值 2.516 -2.134 0.092 3.163 P值 <0.05 <0.05 >0.05 <0.05
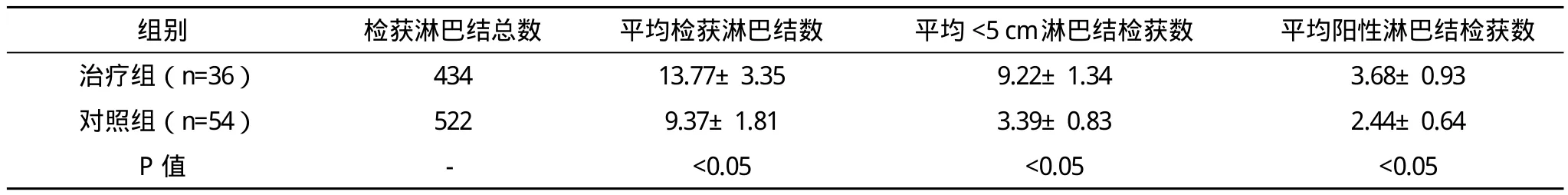
表3 两组患者检获的淋巴结数量比较 个
2.3 术后并发症 治疗组患者术后并发症发生率为8.33%,对照组为11.11%,两组比较差异无统计学意义(x2=1.018,P>0.05),见表4。
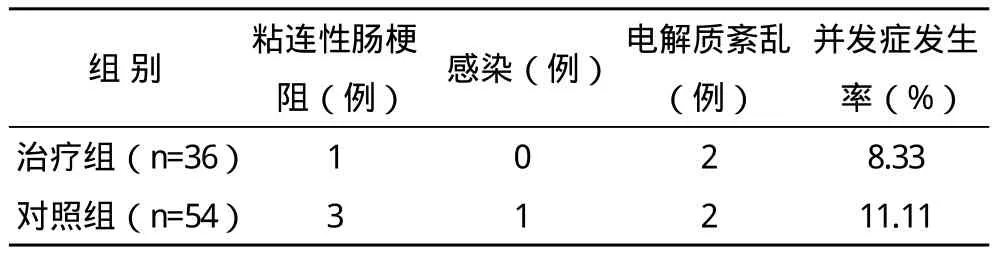
表4 两组患者术后并发症情况比较
3 讨论
3.1 手术注意事项 术中对患者进行纳米碳注射,由于肛门镜空间狭小[6-8],所以在进行注射前应该充分扩肛。注射纳米碳时应将针尖在直肠黏膜下潜行一段距离后再缓慢推注示踪剂。纳米碳注射应掌握好注射的剂量[9-10],纳米碳注射剂量不足将导致区域淋巴结的染色效果不佳,影响术中对淋巴结的摘除。而注射过多则会导致手术区域染色过重,进而影响手术效果[11-13]。手术中应保持术区的清洁,手术间歇清晰[14-16]。
3.2 纳米碳引导手术治疗的优点 利用腹腔镜对直肠癌进行手术治疗容易由于腹腔镜探测不到直肠侧方的淋巴结而导致病变部位清理不干净,从而出现术后再次病变的可能性,为患者的再次治疗带来一定难度。而将纳米碳作为示踪剂,将直肠侧方的病变部位标记出来,术中就能够有效的对病变部位进行清理,从而降低术后复发的可能性。纳米碳注射后,会被巨噬细胞吸附,带入毛细淋巴管系统之内[17-19],并在淋巴结处聚集,将其染为黑色,同时由于纳米碳的直径大于毛细血管直径,因此作为示踪剂的纳米碳不会进入毛细血管内[20-21]。腹腔镜手术手触觉丢失的劣势,利用纳米碳作为示踪剂引导,可以弥补回来,主要就是依赖纳米碳对于淋巴组织的良好特异性[22-24]。从本文研究结果可以看出,纳米碳引导下腹腔镜中低位直肠癌根治术对淋巴结的清理较彻底。纳米碳引导下腹腔镜中低位直肠癌根治术由于切口较小,手术操作的时间较长,但是术中出血量较小,比较安全。而传统的方式虽然进行手术的时间较短,但出血量大,增加了手术的风险。且患者术后也无明显的并发症发生。结果显示,治疗组患者手术时间、术中出血量、胃肠道恢复时间短于对照组,创伤性更小。同时纳米碳引导下实施腹腔镜手术并未增加并发症发生率,表明此种术式保证了安全性。
本文研究结果表明,利用纳米碳进行引导下腹腔镜中低位直肠癌根治术的效果比腹腔镜下中低位直肠癌根治术的效果明显,此手术对淋巴结的检获数量高,且无明显并发症产生安全性高,临床上对直肠癌患者手术时可推广此方法。
[1]史衍辉,夏璐,南林,闫兵,等.纳米碳引导下腹腔镜中低位直肠癌根治术的近期疗效分析[J].中华临床医师杂志,2012,6(21):6682-6684.
[2]Zhen-Jie Wang, Keizo Ohnaka, Makiko Morita, et al.Dietary polyphenols and colorectal cancer risk:The Fukuoka colorectal cancer study[J].World Journal of Gastroenterology, 2013,19(17):2683-2690.
[3]王宜民,王芳.单吻合器在中低位直肠癌保肛手术中的应用体会[J].中国医学创新,2012,9(21):131-132.
[4]Gacci M, Saleh O, Cai T, et al.Quality of life in women undergoing urinary diversion for bladder cancer:results of a multicenter study among long-term disease-free survivors[J].Health and quality of life outcomes, 2013, 11(1):43.
[5]叶平江,郭贵龙,应晓江,等.腹腔镜与开腹结直肠癌根治术对机体免疫系统影响的比较研究[J].中国内镜杂志,2011,17(5):478-484.
[6]刘三刚,魏兴科,李亚彬.吻合器在中低位直肠癌保肛术中的应用[J].中国医学创新,2011,8(24):45-46.
[7]Chang-Ming Gao, Toshiro Takezaki, Jian-Zhong Wu, et al.CYP2E1 Rsa Ⅰpolymorphism impacts on risk of colorectal cancer association with smoking and alcohol drinking[J].World Journal of Gastroenterology, 2007,13(43):5725-5730.
[8]陈鸿源,王亚楠,薛芳沁,等.腹腔镜下静脉输液针注射法纳米碳淋巴示踪技术在胃癌根治术中的应用[J].中华胃肠外科杂志,2014,20(05):457-460.
[9]白雪峰,王平瑜,张俊杰,等.腹腔镜辅助中低位直肠癌保肛手术36例临床观察[J].中国医学创新,2011,8(30):118-119.
[10]Matthiessen P, Hallbook O, Rutegard J,et al.Defunctioning stoma reduces symptomatic anastomotic leakage after low anterior resection of the rectum for cancer:a randomized multicenter trial[J].Ann Surg,2007,246(54):207-214.
[11]史衍辉,夏璐,南林,等.纳米碳引导下腹腔镜中低位直肠癌根治术的近期疗效分析[J].中华临床医师杂志(电子版),2012,6(21):6682-6684.
[12]Darlene Veruttipong, Amr S Soliman, Samuel F Gilbert,et al.Age distribution, polyps and rectal cancer in the Egyptian populationbased cancer registry[J].World Journal of Gastroenterology,2012,18(30):3997-4003.
[13]郑圣明.全直肠系膜切除术治疗低位直肠癌104例临床分析[J].中外医学研究,2014,12(12):137-139.
[14]Shahriar Nikpour, Ali Ali Asgari.Colonoscopic evaluation of minimal rectal bleeding in average-risk patients for colorectal cancer[J].World Journal of Gastroenterology,2008,14(42):6536-6540.
[15]许辉,周赤龙,李裕标,等.完全腹腔镜下超低位直肠癌保肛根治术后直肠肛管功能对比分析[J].肿瘤研究与临床,2014,26(3):175-177,182.
[16]ZHOU JiaLiang, JIANG Zhi, WANG ZhengWu, et al.MicroRNA-142-3p is frequently up regulated in colorectal cancer and may be involved in the regu lation of cell proliferation[J].Chinese science bulletin,2013,58(23):2836-2845.
[17]章斐然,李威,王怀明,等.腹腔镜全直肠系膜联合经肛门内括约肌切除治疗低位直肠癌的疗效探讨[J].中华普通外科学文献(电子版),2014,8(3):204-208.
[18]Aravind Suppiah, John Greenman.Clinical utility of anti- p53 autoantibody:Systematic review and focus on colorectal cancer[J].World Journal of Gastroenterology,2013,19(29):4651-4670.
[19]封义兵,舒亦斌,余泽兵.直肠拖出双吻合器21例超低位直肠癌保肛手术应用[J].肿瘤学杂志,2009,15(3):265-266.
[20]Kirwan W O, Turnbull R B Jr, Fazio V W, et al.Pull-through operation with delayed anastomosis for rectal cancer[J].Br J Surg,1978,65(10):695-698.
[21]李海,尹耀兴,李扬,等.直肠拖出双吻合器超低位直肠癌保肛术的应用[J].西南国防医药,2010,20(1):61-62.
[22]刘永安,黎艳芳,陶琦,等.直肠拖出双吻合器保肛术治疗超低位直肠癌临床报道[J].中国普通外科杂志,2012,21(10):1308-1309.
[23]Rolv-Ole Lindsetmo, Yong-Geul Joh, Conor P Delaney.Surgical treatment for rectal cancer:An international perspective on what the medical gastroenterologist needs to know[J].World Journal of Gastroenterology, 2008,14(21):3281-3289.
[24]陈斌,林奎生,陈进渠,等.经肛门拖出切除联合双吻合器技术在低位直肠癌保肛术中的临床研究[J].实用癌症杂志, 2011,26(3):297-298.
