HIV 初筛实验不同策略的选择及其在临床应用中的评价*
2014-11-21吴志奇刘雁雁倪芳宋为娟谢而付徐华国南京医科大学第一附属医院检验学部南京210029
吴志奇,刘雁雁,倪芳,宋为娟,谢而付,徐华国(南京医科大学第一附属医院检验学部,南京 210029)
艾滋病是由人类免疫缺陷病毒(HIV)感染引起的一种全球性传染病。目前尚无有效的预防性疫苗,早期诊断对于控制艾滋病疫情就显得尤为重要。HIV 的实验室诊断主要依靠血清学检测,适用于HIV 感染窗口期后至艾滋病患者死亡的整个过程。HIV 抗体检测是HIV 血清学检测的常规方法,是艾滋病诊断的一项重要指标,分为筛查试验和确证试验[1]。目前临床HIV 抗体筛查试验常用的方法是酶联免疫吸附试验(ELISA)和快速检测试验。ELISA 是最早应用在HIV 抗体初筛实验中血清学检测技术,其检测试剂已经历经了第一代、第二代、第三代和第四代产品。目前国内的医院大多使用的是第三代ELISA 检测试剂,其敏感性和特异性较前两代检测试剂有了很大的提高,但还是有假阳性和假阴性结果报道,尤其是在感染窗口期[2]。第四代ELISA 试剂是在第三代ELISA 试剂的基础上,加入了p24抗原的检测。P24是HIV 病毒的主要核蛋白,形成病毒核心颗粒的外层。P24抗原是人感染HIV时血液中最早出现的抗原,在抗体产生前数周出现。P24抗原检测的加入使得第四代ELISA 试剂能够更早期地发现HIV的感染,提高HIV 感染窗口期的检出率,减少HIV 在人群中传播的危险[3-4]。目前,第四代ELISA 检测试剂已经开始应用于临床,但实际临床应用效果还有待评估。本文就2010年1月至2014年4月在南京医科大学第一附属医院就诊患者的331968份HIV 筛查样本做回顾性分析研究,对HIV 第三代ELISA、第四代ELISA、或(和)胶体金免疫层析法与HIV 检测确证试验蛋白印迹试验(WB)进行了比较分析,现将结果报道如下。
1 资料与方法
1.1 一般资料检测者来自2010年1月至2014年4月在南京医科大学第一附属医院门诊及住院的就诊者,共计331968份血清样本。通过第三代ELISA 试剂对HIV 抗体进行筛查,胶体金进行复检。332例初筛阳性(反应性)样本送南京市疾病预防控制中心使用第四代ELISA 试剂进行复检及WB 确证。189例HIV 抗体确证阳性,年龄5~79岁,男女比例为155∶34。
1.2 仪器与试剂 MICROLAB STAR VENUS 加样系统,MICROLAB FAME分析系统,试剂由上海科华生物工程股份有限公司提供。BIO-Benchmark Plus酶标仪,试剂由生物梅里埃公司提供。
1.3 方法 ELISA 方法根据s/co值判断结果。s/co≥1为阳性(反应性),s/co<1为阴性(无反应性)。胶体金免疫层析法,在30min内出现两条带为阳性(反应性)。WB蛋白印迹试验严格按照说明书的要求操作。
1.4 统计学处理应用SPSS17.0进行统计学分析,计数资料组间比较采用四格表χ2检验。以P<0.05为差异有统计学意义。
2 结果
2.1 ELISA 第三代、第四代试剂检测结果比较通过比较可以看出,第三代ELISA 试剂与第四代ELISA 试剂的差异有统计学意义。第四代ELISA 与胶体金组合后,确证阳性符合率较第三代ELISA 与胶体金组合提高了3.91%。见表1。

表1 ELISA 第三代第四代试剂检测结果比较
2.2 筛查阳性样本s/co值的分布情况从332例两代试剂检测s/co值的分布情况中可以看出,第四代ELISA 试剂HIV抗体阳性的s/co值集中分布在较高的数值,更易于判断,并且没有漏检。见表2。
2.3 ELISA+胶体金试验复检与确证结果比较从表3中可以看出,联合胶体金检测,避免了第三代ELISA 试剂的漏检。

表2 筛查阳性样本s/co值的分布情况(n)
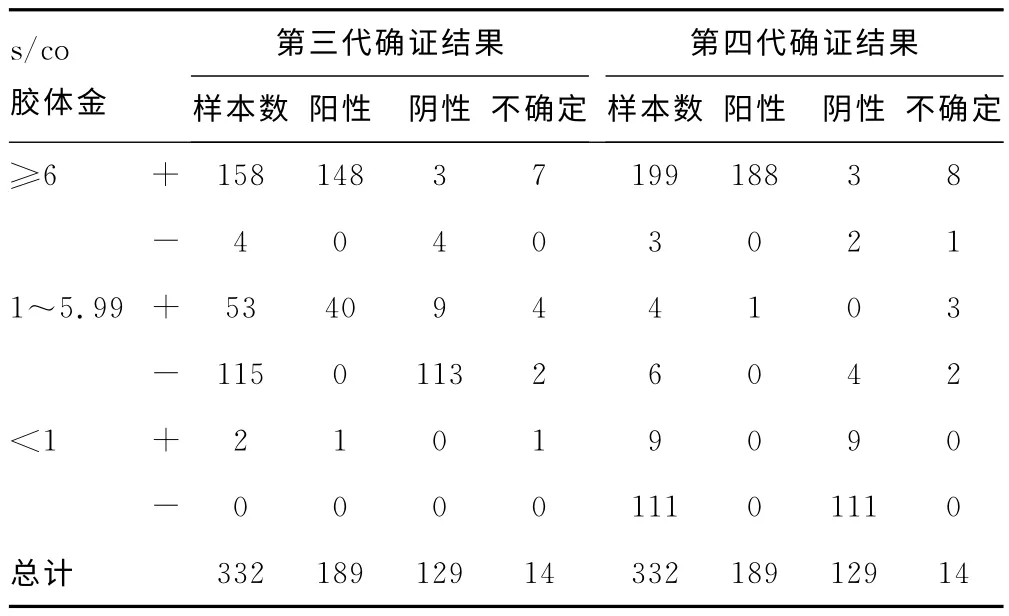
表3 ELISA+胶体金试验复检与确证结果比较(n)
2.4 WB条带结果332例初筛阳性标本中,第三代ELISA试剂筛查漏检1例阳性和1例不确定标本。第四代ELISA 试剂检测该2例标本的s/co值分别为17.65和1.81。WB确证结果表明该2例标本均包含p24条带。见表4。

表4 两代试剂筛查不一致WB条带结果
3 讨论
检测所用试剂是影响ELISA 检测结果的关键因素。随着科技的发展,HIV ELISA 检测试剂包被的抗原已从第一代的全病毒裂解物,发展为目前的以基因重组和多肽抗原包被和标记的第三代ELISA 双抗原夹心法试剂,可检测的亚型包括HIV-1、HIV-2和HIV-1型的O 亚型[1]。第四代ELISA 检测试剂则在此基础上增加了p24抗原检测系统,可同时检测HIV p24抗原和HIV-1/2抗体。与第三代试剂相比,可缩短窗口期4~5d[3]。从表1中可以看出,第四代ELISA 试剂的假阳性样本数明显低于第三代ELISA 试剂,阳性样本的确证阳性符合率也明显高于第三代ELISA 试剂,两者比较,差异有统计学意义(P<0.05)。当第三代ELISA 检测试剂与胶体金联合使用后,确证阳性符合率由57.27%提高到88.73%,与第四代ELISA 试剂比较,差异无统计学意义(P>0.05)。189例确证阳性标本中,第三代ELISA 试剂检测漏检1例阳性标本,与梁启忠等[5]报道的第三代ELISA 试剂有漏检现象相符。从表2和表3的s/co值的分布可以看出,第三代ELISA 试剂与第四代ELISA 试剂的差别明显。胶体金的加入,避免了第三代ELISA 试剂的漏检。
HIV 初次感染人体后,产生短暂的病毒血症,血液中先出现的是p24抗原,数周内产生p24抗体,随后出现gp160、gp120、gp41抗体[6]。抗体出现后在体内形成抗原抗体复合物,p24抗原浓度降低,所以血液中可以先检测到抗原,之后检测到抗体。HIV 阳转期间,WB能检测到p24和gp160这两条带。如果WB出现p24和gp160条带,可以作为判断HIV 初期感染的重要依据[7]。从表4中可以看出,患者2检测结果显示,第三代ELISA 试剂为s/co高值阴性,第四代ELISA 试剂为s/co低值阳性,WB条带显示为gp160、p24(±),提示HIV特异性抗体滴度低,由于第三代ELISA 只能检测抗体,所以显示s/co<1。而第四代ELISA 试剂增加了p24抗原检测,提高了检测灵敏度,显示s/co>1,判断为阳性,可以为临床诊断提供帮助。该患者为年轻男性,因为不明原因发热而收治于感染科,CD4+的T 淋巴细胞为每微升434个。新报告HIV 感染者中,有半数是来源于早期感染阶段的传播[8]。欧美等发达国家利用第四代产品进行HIV 抗体与p24抗原的检测。通过p24抗原的检测,进一步提高了HIV 检测的灵敏度和特异度,并用于对新生儿HIV 的初筛[9]。患者1为中年男性,因发热,肺部感染收治于感染科,有活动性肺结核,为男男性接触人群(MSM)。检测结果显示,第三代ELISA 试剂为s/co低值阴性,期间另外再抽血复查,且重复多次检测,排除人为因素及偶然误差的影响。第四代ELISA 试剂为s/co高值阳性,WB 条带显示为gp160、gp120、p66、p55、p51、gp41、p39、p31、p24、p17。出现第三代ELISA 试剂检测结果为阴性,原因为何,需要进一步的探讨和研究。
目前希望能找到一种灵敏度特异度都达到最佳的试剂或是组合,然而各种试验方法都有着不同的优缺点和特性。因此,如何科学合理地使用规则判定结果,既避免假阳性的产生,又防止真阳性的漏检,就显得极为重要了。根据不同的样本类型,不同的筛查人群选择适宜的试验方法是这次研究分析的目的。
ELISA 作为筛查试剂,价格便宜,性能稳定,适合大样本量的检测,又以数值来判断结果,有利于实现检测的自动化。因其较高的灵敏度和特异度,为HIV 检测筛查的首选方法[7]。第四代ELISA 诊断试剂是在第三代ELISA 试剂“双抗原夹心”,可同时检测HIV 特异性IgG 和IgM 抗体的基础上,增加了对p24抗原的检测,对HIV 感染窗口期的检测强于第三代ELISA 试剂[10]。
胶体金免疫层析试验是应用于HIV 抗体筛查中的快速检测试验。该方法检测的灵敏度和特异度都较高,检测结果易于判断,试剂便于携带和保存。因此胶体金法比较适合性病门诊等一些有检测需求但检测样本量少的地方,可以实现随到随测;因其方法简单,便于掌握,在条件允许的情况下,建议个人在有了高危行为后,也可尝试着进行自我检测;同时也可以作为大样本量实验室初筛阳性后的复检试验,依据ELISA 所得s/co值结合胶体金结果判断是否进行WB确证。
通过本次分析和比较,ELISA+胶体金的组合是目前条件下优先的初筛复检方案。第三代ELISA+胶体金组合虽可以在减少假阳性的同时避免假阴性的产生,但在检验流程上容易出现偏差,需要在临床样本的检测中格外小心,遇到可疑样本时多与临床医生沟通交流,以免造成不必要的漏检。第四代ELISA+胶体金的组合,即可以明显提高确证阳性符合率,又有利于HIV 感染窗口期的检测,可推荐作为临床实验室HIV优选筛查方案。
在本次回顾性分析总结所讨论的问题中,存在着一些不足,在今后的工作中需要进一步研究探讨,尤其是结果出现特殊情况的样本,对统计结果进行分析补充,以期发现和制订出更为合理的HIV 筛查检测方案,为艾滋病的诊断提供科学依据。
[1]尚红,张子宁.人免疫缺陷病毒感染的实验室检测[J].中华检验医学杂志,2006,29(7):669-670.
[2]段惠玲,林霞,黄静,等.窗口期弱阳性抗体血清在选择抗-HIV 检测试剂中的重要意义[J].中国输血杂志,2013,26(6):544-545.
[3]韩晓旭,欧阳金鸣,孙宏,等.三、四代酶联免疫吸附试验应用于HIV-1早期感染者的比较[J].中华检验医学杂志,2012,35(6):538-543.
[4]Normand J,Montaner J,Fang CT,et al.HIV:seek,test,treat,and retain[J].J Food Drug Anal,2013,21(4):S4-S6.
[5]梁启忠,掌友湖,程玉根.第4代与第3代HIV 检测试剂质量比较[J].临床血液杂志,2010,6(3):356-358.
[6]邵世和.人类免疫缺陷病毒//张卓然.临床微生物学和微生物检验[M].3版,北京:人民卫生出版社,2003,395-406.
[7]Bi X,Ning H,Wang T,et al.Comparative performance of electrochemiluminescence immunoassay and EIA for HIV screening in a multiethnic region of China[J].PLoS One.2012,7(10):e48162.
[8]Hollingsworth TD,Anderson RM,Fraser C.HIV-1transmission,by stage of infection[J].J Infect Dis,2008,198(5):687-693.
[9]Tamhane M,Gautney B,Persaud D,et al.Analysis of the optimal cut-point for HIV-p24antigen testing to diagnose HIV infection in HIV-exposed children from resource constrained settings[J].J Clin Virol,2011,50(4):338-341.
[10]谢进荣,张兴明,王淑芳.第3代和第4代HIV 检测试剂对无偿献血人群筛查结果比较[J].中国输血杂志,2012,25(12):1326-1327.
