甘草饮片、药对以及四君子汤中药效组分的测定
2014-11-21李景松张贵君
李景松 张贵君
(北京中医药大学中药学院,北京,100102)
内蒙古甘草为传统道地的中药。中药甘草(Radix Glycyrrhizae)是豆科植物甘草 Glycyrrhiza uralensis Fisch.、胀果甘草 Glycyrrhiza inflata Bat.或光果甘草Glycyrrhiza glabra L.的干燥根及根茎。甘草具有补脾益气、止咳祛痰、清热解毒、缓急定痛、调和诸药的功能。
目前内蒙古炙甘草补脾益气的临床应用,本研究在中药药效组分理论的指导下[1],依据其功能与主治,选用临床上常用的四君子汤中,炙甘草的单味药,2个药对,四君子汤中的含量测定,探讨内蒙古炙甘草的质量特征和评价方法。何三民[2]依据《中华人民共和国药典》使用HPLC法测定2010年版一部收载有甘草Lycyrrhiza uralensis Fisc.的甘草苷和甘草素、异甘草素的含量分别为3.64%、0.14%、0.125%。栾海云等[3]建立甘草中甘草苷含量测定的HPLC法,测定不同产地甘草中甘草苷的含量,以控制其质量。刘磊等[4]采用HPLC法测定了同一产地、批次的生甘草和炙甘草中甘草苷和甘草酸的含量,发现蜜炙甘草后的甘草苷和甘草酸的含量增加,验证蜜炙因素可显著增加甘草中二者的含量。张玲等[5]用HPLC法测定甘草酸和甘草苷含量在四君子汤复方中分别为1.41%和1.44%。刘红文[6]使用薄层色谱法定性鉴别六味地黄丸中的甘草苷,使用液相色谱法测量甘草苷的含量,为该味成药的生产提供相应的质量控制标准。以控制其主要活性成分为甘草苷、异甘草苷、甘草素和异甘草素等甘草黄酮类具有抑菌、以及保肝作用等活性[7-10],和甘草皂苷类成分质量。四君子汤作为治疗脾胃气虚证,在中医内科脾胃气虚证的治疗中得到了广泛的运用[11]。甘草苷和异甘草苷具有抗溃疡、抗菌、抗炎[12],而其衍生物既能促进胰岛素的吸收,还具有抗心律失常、镇痛、抗过敏、抗缺氧等作用[13]。
1 材料与方法
1.1 材料 仪器,Agilent 1100高效液相色谱仪(HP真空脱气泵,HP四元泵,HP自动进样,HP柱温箱,HPDAD检测器);Agela Venusil HPLC Clumns(4.6 mm×250 mm,5 μm)色谱柱;BP110S电子分析天平;BT25S型电子分析天平。
标准品,甘草苷(批号:111208),异甘草苷(批号120112),甘草素(批号 120302),甘草酸(批号111201)。甲醇为色谱纯(购自fisher公司),水为娃哈哈纯净水。
内蒙古野生炙甘草饮片,均购于河北安国祁新饮片公司,经北京中医药大学张贵君教授鉴定。
药对又称“对药”“对子药”“姊妹药”是指临床常用的、相对固定的两味药物的配伍形式,是中药配伍中的最小单位[14]。《神农本草经·序例》指出:“药有单行者,有相须者,有相使者,有相畏者,有相恶者,有相反者,有相杀者,凡此七情,合和视之。药对炙甘草-人参,配伍比例:炙甘草-人参3∶5;出处:四君子汤,《太平惠民和剂局方》。药对炙甘草-白术,配伍比例:炙甘草-白术1∶1;出处:四君子汤,《太平惠民和剂局方》。复方四君子汤,组成:人参去芦(10 g),白术茯苓去皮、甘草炙(6 g)各等分;出处:四君子汤《太平惠民和剂局方》。
1.2 方法
1.2.1 色谱条件 色谱柱:Agela Venusil HPLC Clumns(4.6 mm ×250 mm,5 μm);流动相:甲醇-0.05%磷酸- 水(0—8 min,19∶81;8—11 min,23∶77;11—21 min,24—76;21—44 min,50∶50;44—45 min,100∶0;45—50 min,19—81);流速:1.0 mL·min-1;进样量:10 μL;柱温:室温(30℃);检测波长:237 nm、360 nm。
1.2.2 对照品溶液的制备 精密称取适量对照品甘草苷、异甘草苷、甘草素、甘草酸[15],分别置于 10 mL量瓶中,加甲醇溶解并定容至刻度,摇匀,分别得到浓度为 86 μg·mL-1、10 μg·mL-1、20 μg·mL-1、250 μg·mL-1的对照品溶液。
1.2.3 供试品溶液的制备 按照各配伍比例称取甘草及其他中药,加10倍量水浸泡30 min后煎煮两次,第一次30 min,第二次20 min,合并煎液,趁热过滤,滤液浓缩至每1 mL相当于原药材0.1 g的浓缩液,取浓缩液1 mL至10 mL容量瓶中,用甲醇稀释至刻度,静置20 min,分出上清液,相对中药浓度为 0.01 g·mL-1,即为供试液。进样前用0.45 μm滤膜过滤。
2 结果
2.1 线性关系考察 甘草苷标准品溶液分别进样0.3、3、6、9、12、18 μL,异甘草苷标准品溶液分别进样1、4、8、12、16、20 μL,甘草素标准品溶液分别进样1、3、6、9、12、18 μL,甘草酸标准品溶液分别进样 0.5、4、8、12、16、20 μL。以标准品浓度为横坐标,峰面积为纵坐标进行线性回归,得甘草苷回归方程Y=146.5X+20.51,R2=0.9993,表明甘草苷在25.800~154.800ng线性关系良好。异甘草苷的回归方程Y=28.25X–1.177,R2=0.9996,表明异甘草苷在10.000~200.000 ng线性关系良好。甘草素的回归方程Y=45.61X–0.022,R2=0.9996,表明甘草素在 20.000 ~360.000 ng线性关系良好。甘草酸的回归方程Y=75.32X–0.398,R2=0.9998,表明甘草酸 125.000 ~5000.000 ng在线性关系良好。
2.2 精密度试验 分别精密吸取甘草苷、异甘草苷、甘草素、甘草酸标准品溶液,连续进样6次,安各成分的色谱条件测定峰面积。RSD分别为1.04%、1.51%、1.69%、1.19%,表明仪器精密度良好。
2.3 稳定性试验 称取内蒙古野生炙甘草供试品6 g,按供试品按供试品的溶液的制备项下方法制备供试品溶液,室温放置,分别在 0,2,4,6,8,10,12 h 按2.1.1项下进行峰面积测定,甘草苷、异甘草苷、甘草素、甘草酸RSD依次分别为1.93%,1.69%,1.46%,2.73%,表明供试品溶液在12h内稳定。
2.4 重复性试液 精密吸取同一批供试品溶液,进样10 μL,依照标准曲线测定方法连续测定6次,根据峰面积计算RSD值,得到4种组分重现性RSD值分别为1.84%,1.77%,1.64%,2.24%,表明本方法重现性良好。
2.5 加样回收率试验 精密称取取内蒙古野生炙甘草饮片6份,按供试品溶液制备项下方法制备,分别精密加入4种基本等量标准品溶液,注入液相色谱仪进行含量测定,见表1。
2.6 药效组分测定 分别制备3批供试品,每个供试品连续进样3次,进样量10 μL,高效液相色谱测定峰面积,根据外标法计算各组分的含量,见图1-图8,表2。
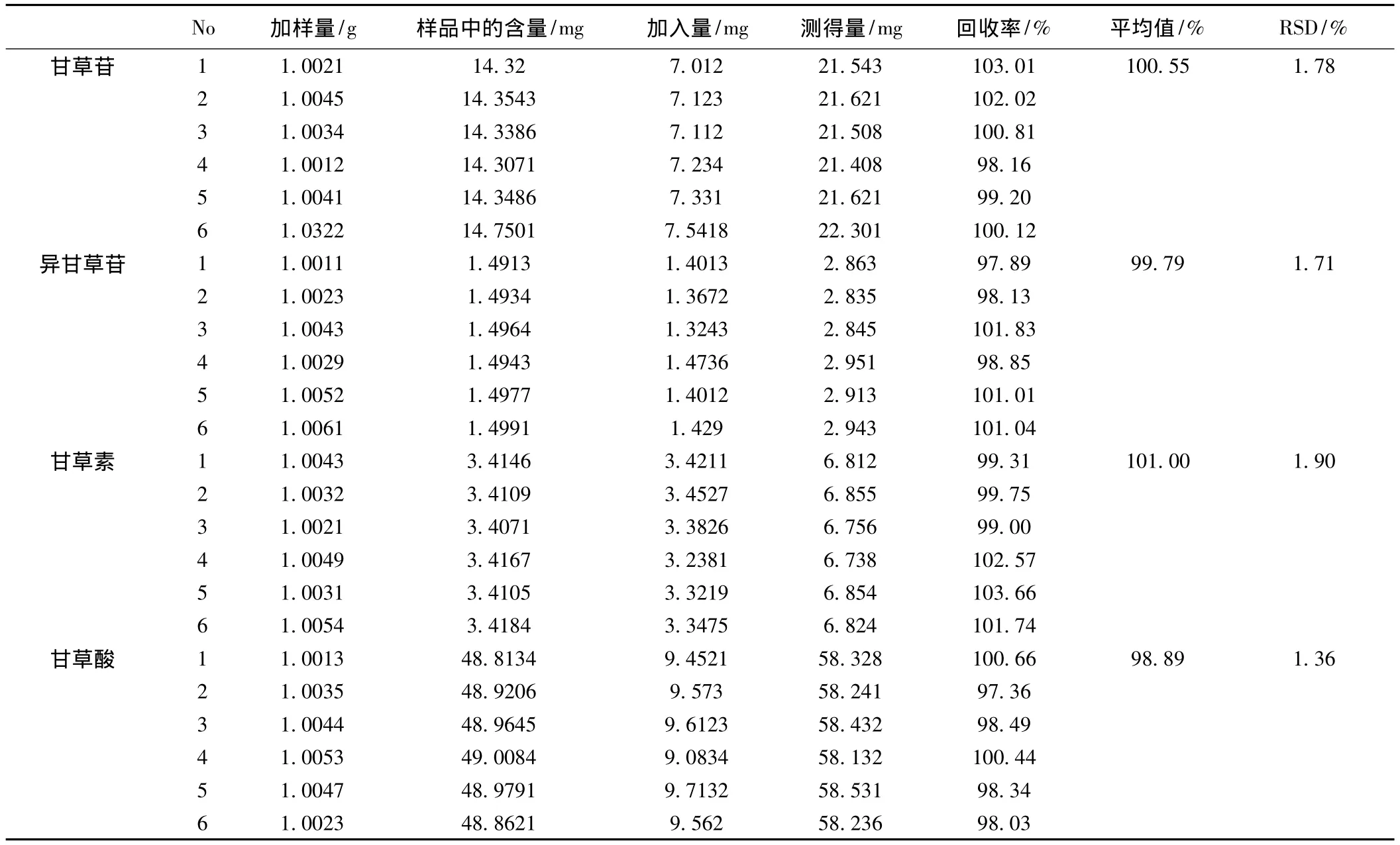
表1 内蒙古野生炙甘草药效组分加样回收率测定
2.6.1 标准品图谱 见图1-图4。
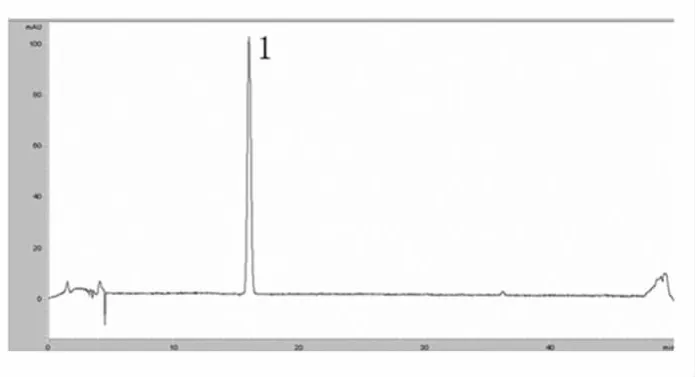
图1 甘草苷标品HPLC图谱
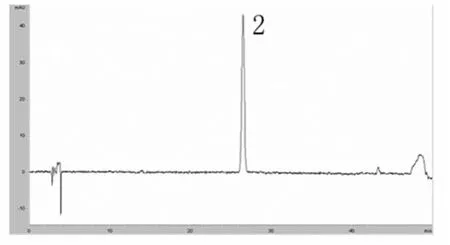
图2 异甘草苷标品HPLC图谱
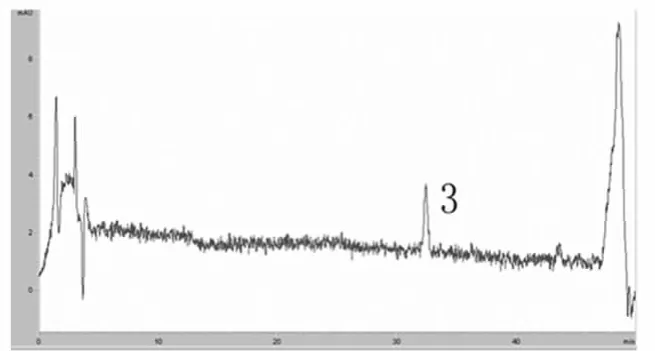
图3 甘草素标品HPLC图谱
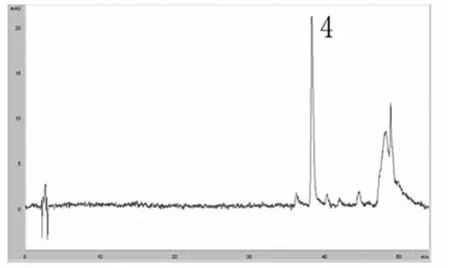
图4 甘草酸标品HPLC图谱
2.6.2 单味药图谱 见图5。

图5 内蒙古野生炙甘草HPLC图谱
2.6.3 药对图谱 见图6-图7。
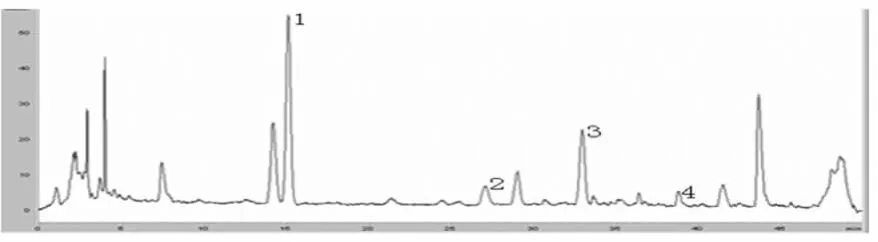
图6 炙甘草-人参药对HPLC图谱
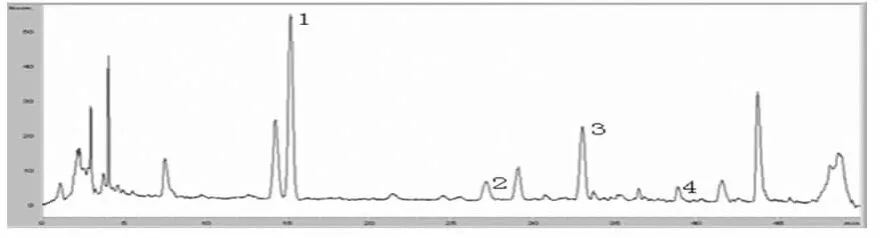
图7 炙甘草-白术药对HPLC图谱
2.6.4 复方图谱 见图8。

图8 四君子汤HPLC图谱
2.7 四种药效组分在单味药、药对、复方中的含量见表2。
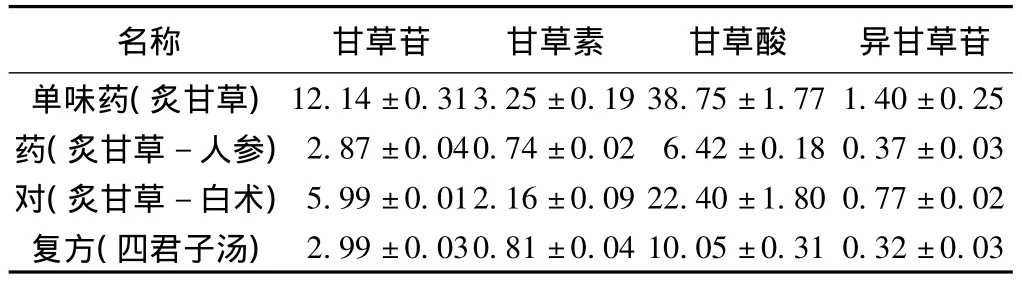
表2 药效组分含量(mg/mL)
3 讨论
课题实验结果显示,经过药对与复方配伍以后,四种药效组分含量均有下降,且下降幅度较大。其中,单味药与复方相比下降尤为明显(甘草苷下降75%,甘草素下降75%,甘草酸下降74%,异甘草苷下降77%)。可以看出,由于配伍的变化影响着甘草药效组分的溶出效率,而由于复方才是作为发挥作用疗效的关键,并非一种或某几种成分,而是多种成分的相互作用,所以,单纯地把某一单体或几个单体含量作为质量检测标准有欠妥当,而应该把疗效与质量标准联系起来,将药效组分作为质量控制的多指标。
就药对间实验结果来看,药对(炙甘草-白术)四种药效组分含量均高于药对(炙甘草-人参),药对(炙甘草-白术)与复方进行比较(甘草苷下降60%,甘草素下降62%,甘草酸下降55%,异甘草苷下降58%),而药对(炙甘草-人参)与复方四君子汤中各项含量差别较小。由于许多方剂组成复杂而为质量控制带来不便,可从方剂中选择合适的药对或者其中几味药的药效组分进行质量控制指标,药对代替复方的前提是务必选择合适的,如本课题中药对(炙甘草-人参),倘若选择欠佳,如课题中药对(炙甘草-白术)代替四君子汤则不利于质量控制。但在复方组成并不太复杂的情况下,为了质量控制的严谨性,应尽量选择整个复方作为控制载体。
本课题以内蒙古野生甘草单味药、药对以及复方作为研究载体,以探索甘草中药效组分变化规律,实验结果为药效组分甘草苷-甘草素-甘草酸-异甘草苷在单味药(内蒙古野生炙甘草)中含量为(12.14±0.31),(3.25 ±0.19),(38.75 ±1.77),(1.4 ±0.25);在药对(炙甘草-人参)中含量为(2.87±0.04),(0.74±0.02),(6.42±0.18),(0.37±0.03);在药对(炙甘草-白术)中含量为(5.99±0.01),(2.16±0.09),(22.4±1.8),(0.77±0.02):在复方(四君子汤)中含量为(2.99±0.03),(0.81±0.04),(10.05±0.31),(0.32±0.03)。其可以为甘草中药材完善严谨的质量标准提供一定的科学依据。
[1]张贵君,罗容,王奕洁.中药药效组分理论与中药组分学[J].中药材,2007,30(2):125.
[2]何三民.HPLC法测定甘草中甘草素、异甘草素、甘草苷的含量[J].中草药,2003,34(7):618-619.
[3]栾海云.HPLC法测定不同产地甘草中甘草苷的含量[J].安徽农业科学刊,2011,39(25):12121-12122.
[4]刘磊.炮制因素对甘草中有效成分甘草苷和甘草酸的影响[J],徐州医学院学报2009,29(10):637-640.
[5]张玲.四君子汤和理中丸中甘草酸及甘草苷含量测定[J],实验方剂学,2007,13(6):4-6.
[6]刘洪文.六味甘草丸中甘草苷的鉴别和含量测定[J],陕西中医,2010,31(3):353-354.
[7]靳茂礼,赵艳普,王润彪,等.高效液相色谱法测定胃痛舒片中甘草苷含量[J].中国药业,2012,21(24):66-67.
[8]杨玲娟.HPLC法测定芍药甘草汤总有效部位中4个活性成分的含量[J].中华中医药学刊,2007,3(25):521-523.
[9]TAMIRSS,EIZENBERGM,SOMJEND,et al.Estrogen- like activity of glabren and other constituents isolated from licorice root[J],J Steroid Biochem,2001,78(3):291-298.
[10]FUHRMAN B,VOLKOVAN,KAPLAN M,et al.Antiatherosclerotic effects of licorice extract supplementation on hypercholesterolemic patients:increased resistance of LDL to atherogenic m,Mifications,reduced plasma lipid levels,and decreased systolic blood pressure[J].Nutrition,2002,18(3):268-273.
[11]高永珍,武瑞珍,陈永利.四君子汤在中医内科疾病脾胃气虚证中的运用[J].中国民族民间医药,2013,22(3):52.
[12]张明发,沈雅琴.甘草及其活性成分抗炎与抗炎机制的研究进展[J].现代药物与临床,2011,26(4):261-2680.
[13]Li Songpei,Li Wei,Yinghua W,et al.Prenylflavonoids from Glycyrrhiza uralensis and their protein tyrosine phosphatase-1B inhibitory activities[J].Bioorganic & Medicinal Chemistry Letters,2010,20(18):5398-5401.
[14]刘萍,王平,刘松林,等.基于药对探讨中药复方配伍规律的思考[J].中华中医药学刊,2010,28(9):1833-1835.
[15]李伟,王跃飞,文红梅,等.HPLC-DAD同时分析甘草中7种有效成分[J].中国药学杂志,2008,43(24):1914-1918.
