弓形虫棒状体分泌毒性因子-假激酶的研究进展
2014-11-20赵桂华郝万东
赵桂华,郝万东,尹 昆
2.山东省金乡第一中学,金乡 272299
弓形虫为专性胞内寄生致病原虫,属顶复门,呈世界分布,中间宿主广泛,可感染包括人类在内的所有有核细胞。全世界约有三分之一的人感染,多数呈隐性感染,但对于免疫功能低下及受损人群危害重大,可引起死亡。因其复杂的生活史及致病机制,目前尚无高效的药物能够彻底清除隐性感染者及病人体内的虫体及包囊,也无安全有效地疫苗可用。弓形虫棒状体蛋白(ROPs)是虫体分泌于宿主细胞的效应因子,在虫体的入侵、纳虫泡形成、增殖、出胞和逃避宿主细胞效应分子的攻击中发挥重要作用。ROPs属蛋白激酶家族,被称为棒状体蛋白激酶(ROPKs),决定弓形虫毒力,是研制弓形虫药物潜在靶点和疫苗的理想对象。随着对弓形虫ROPKs研究的深入,发现决定虫体毒力的许多基因编码一种无催化活性的蛋白激酶,称为假激酶(Pseudokinase)。这种酶虽无激酶活性,但它们可通过非磷酸化的方式发挥作用,成为弓形虫不可或缺的毒性因子。假激酶与ROPKs其它成员一样具有调控宿主细胞信号通路,协助虫体逃避宿主免疫系统的攻击的功能,成为弓形虫病免疫诊断、疫苗研制和抗弓形虫药物筛选的潜在靶点[1]。假激酶的研究是目前研究的热点,对弓形虫病防治意义重大。本综述就近年来弓形虫棒状体分泌的假激酶的研究进展做一概述,认识它们的结构特点,揭示它们的作用机制,完善弓形虫的致病机理。
1 弓形虫棒状体假激酶的结构特点及命名
假激酶于2002年由Gerard Manning等在研究人类基因组草图中编码蛋白激酶的基因时发现并正式命名。人类蛋白激酶大约有10%属于假激酶,它们至少缺失一种激酶催化活性所必需的3个关键氨基酸(赖氨酸、天冬氨酸、天冬氨酸),导致丧失激酶活性[2]。随后的研究证明假激酶在生物界普遍存在,几乎遍布所有蛋白激酶家族,其中弓形虫的含量最高,占总蛋白激酶的30%(160余个)[3]。目前关于假激酶的来源有两种不同的观点,一是认为假激酶是由活性激酶基因突变而成[4];另一种观点则认为活性激酶来自假激酶,最初这些假激酶主要行使其非催化功能,随着基因的复制、突变,其中某些基因逐渐具备催化活性,形成真正的激酶[5]。从假激酶来源可看出与激酶联系紧密。弓形虫假激酶的研究主要集中于棒状体分泌的假激酶,其结构由N端结构域(NTE)和核心结构域组成。N端结构域保守性低、柔性强,由数个富含碱性氨基酸的α螺旋构成,称为N端延伸序列(NTE)。在某些假激酶(如ROP2)的晶体结构中,NTE缠绕在激酶折叠结构域的表面,充当假激酶行使非磷酸化功能的作用亚基[6]。激酶的核心结构域由12个亚结构域(分别命名为Ⅰ,Ⅱ,Ⅲ,Ⅳ,Ⅴ,Ⅵa,Ⅵb,Ⅶ,Ⅷ,Ⅸ,Ⅹ,Ⅺ )组成,包括ATP结合结构域、γ磷酸基转移结构域、Mg2+离子结合结构域等。假激酶与激酶的核心结构域序列比对分析(图1)揭示弓形虫棒状体假激酶成员在某些关键位点发生了不同程度的突变,如ROP2缺少结合ATPαβ磷酸基的富G环,Ⅱ亚结构域内赖氨酸(K72)突变为组氨酸(H),Ⅶ亚结构域中参与结合Mg2+的3个催化残基DFG中的天冬氨酸(D184)突变为甘氨酸(G),这些关键位点的突变,使ROP2不能与ATP结合(如图2),丧失了蛋白激酶活性。同样属于假激酶的ROP4,ROP5,ROP7和ROP8的关键催化位点的突变情况与之相似,其亚结构域(富G环、Ⅱ、Ⅶ)内缺少一个或多个关键氨基酸残基[7-9],导致不能或错误的与 ATP结合(如图2),不具备激酶活性。这种结构改变本质上是一种趋利进化方式,利于充分发挥假激酶的功能[10-11]。这些核心结构域内氨基酸序列结构特点及不能使底物磷酸化的功能特性是目前区分及定义假激酶的唯一标准。
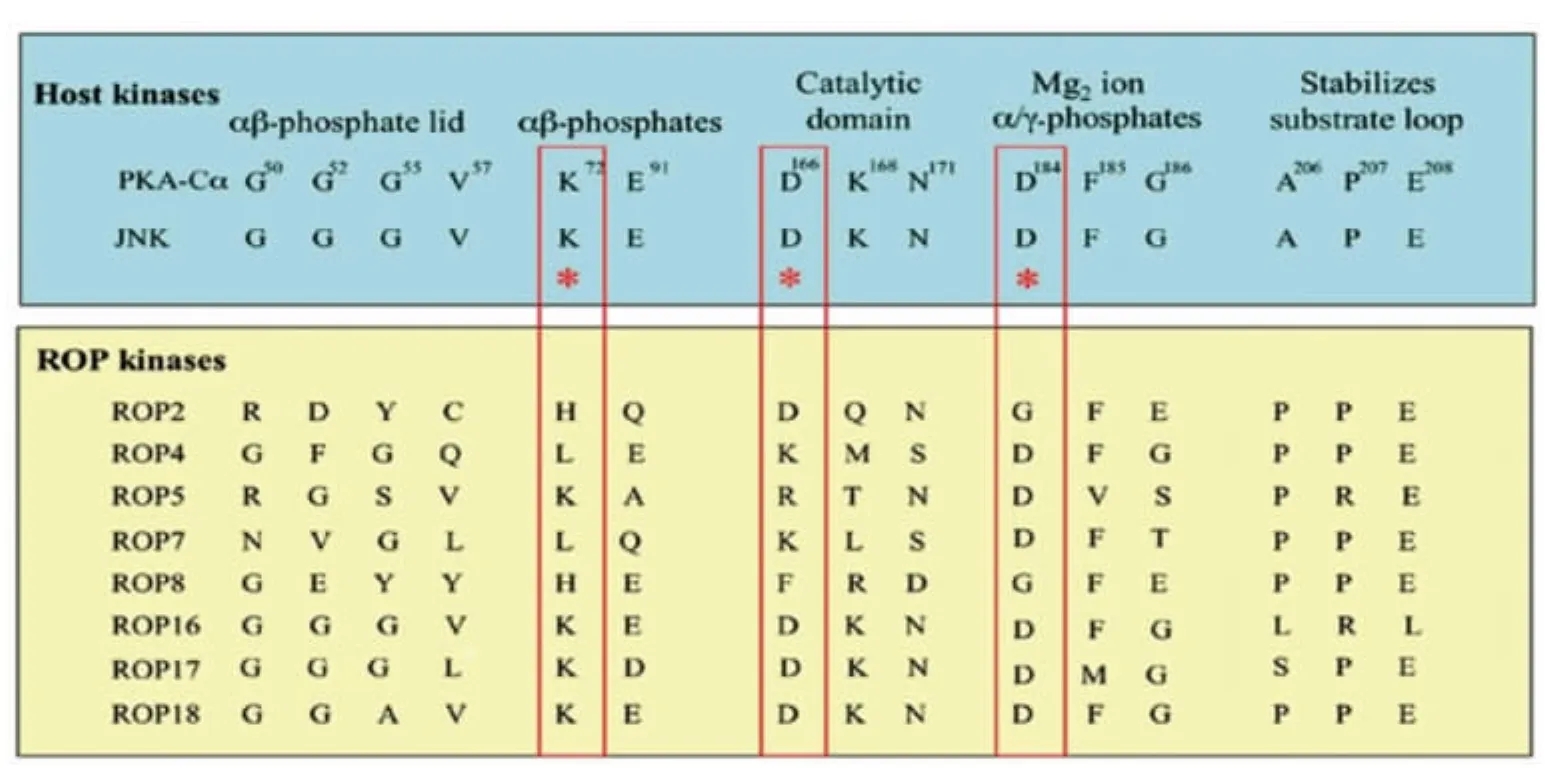
图1 假激酶与活性激酶核心结构域关键氨基酸残基的比较分析Fig.1 Comparison of key amino acid residues of kinases and pseudokinases core domain
2 假激酶的作用机制
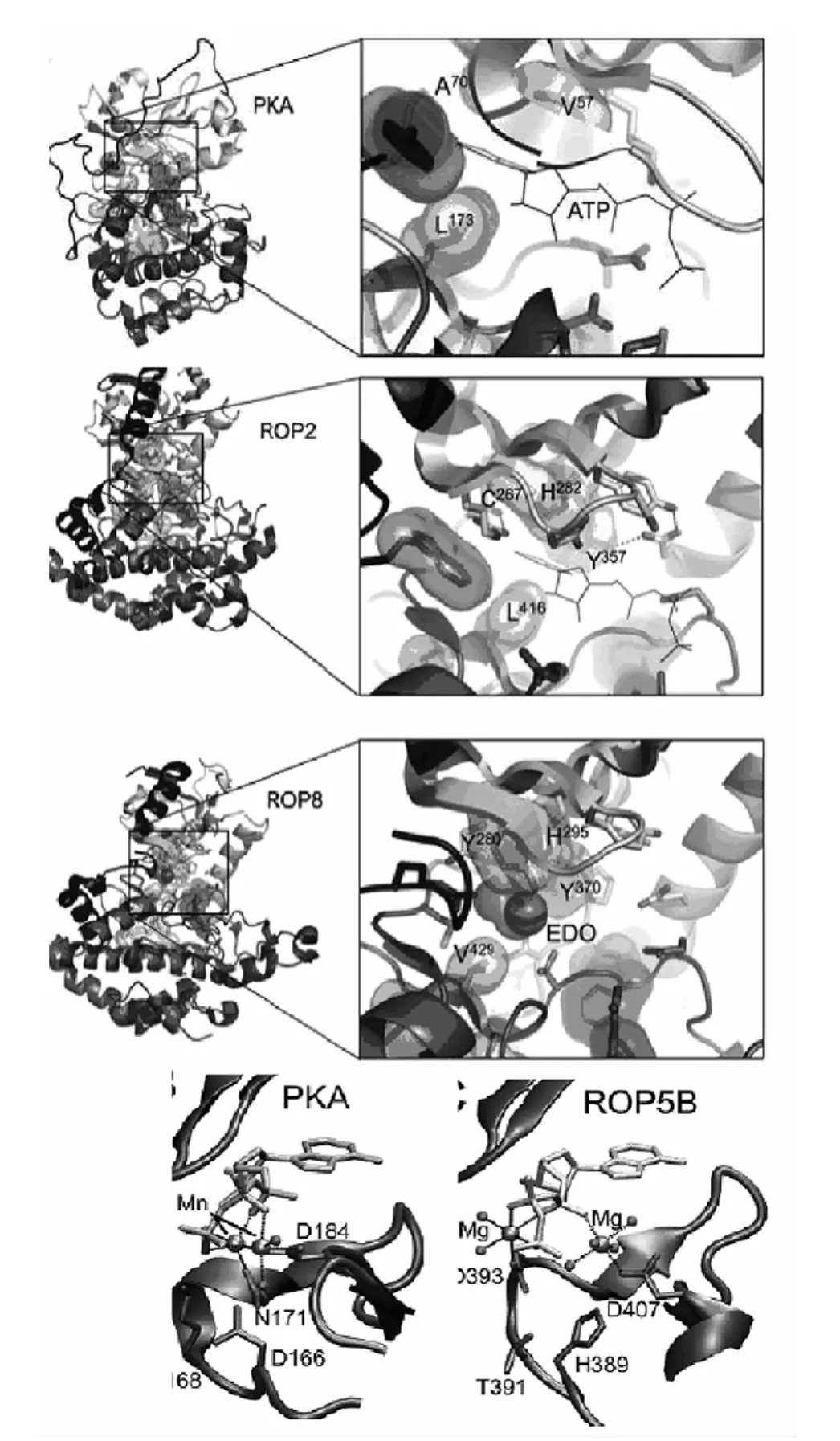
图2 假激酶与PKA激酶结合ATP结构示意图(Kornev AP,Tavlor SS.Structure,2009)Fig.2 Binding ATP structure of pseudokinases and PKA kinase(Kornev AP,Tavlor SS.Structure,2009)
假激酶虽无激酶活性,但在生物进化中,其基因一直保持编码活性,且序列高度保守,说明其编码产物-假激酶具备重要的生理功能。目前已知假激酶的作用方式有3种:(1)通过构象变化调控激酶活性;(2)作为支架蛋白为其它蛋白间的互相作用提供平台;(3)与受体共同发挥作用,促进细胞间的交流,或起到“保镖”的作用,帮助其它蛋白准确到达作用位点等。为揭示假激酶的作用机制,Elton Zeqiraj[12]等 研 究 了 三 元 复 合 物 LKB1-STRADMO25的晶体结构,其中LKB1是调控腺苷酸激酶(AMPK)活性的肿瘤抑制蛋白激酶,STRADα是假激酶,MO25α为支架蛋白。STRADα采用一种类似于典型的蛋白激酶构象(假的活性位点)结合LKB1为假底物,改变LKB1的构象,促进其活性构象形成,同时MO25α通过与LKB1催化活性环的互作稳定其活性构象,使LKB1一直处于活性状态。该研究揭示了假激酶STRADα通过自身构象变化调控激酶LKB1活性的作用机制。Freeman[13]等研究表明假激酶iRhom可作为一种调控蛋白发挥作用,其成员iRhom2与内质网中的TACE结合,使其离开内质网到达细胞膜,促进抗炎因子TNFα的释放,参与调控抗病原体的免疫保护反应。Ras激酶抑制剂(KSR)是一种假激酶,其成员包括KRS1和KRS2,是 MAP激酶信号通路中Ras诱导RAFMEK-ERK组件活性的必需成员。Raf,MEK,ERK蛋白形成一个重要的信号传导通路,该通路与癌症发生有关,在癌症患者体内被异常激活,KSR作为一种分子支架将RAF、MEK和ERK三成员绑定在一起。在芽殖酵母内采用替换的方式研究了KSR1的作用机制。KSR1的假激酶结构域结合MEK和RAF形成信号复合物,ERK通过一个保守结构域的N端与假激酶结构域结合形成三元信号转导复合物。KSR2在MAP激酶信号通路中的支架功能与KSR1相似,并且被Ca2+水平影响的去磷酸化作用调控[14-15]。假激酶无论哪种作用机制均与活性激酶的催化功能存在密切的联系,为活性激酶的功能伴侣。
3 弓形虫棒状体假激酶的功能
ROPKs家族中大量假激酶的存在,预示它们具有重要的功能,但目前多数假激酶的功能未知。ROP5由于缺少一个关键的催化残基(天冬氨酸)导致其错误的绑定ATP,不具备催化活性,属于假激酶[16]。目前有关它的研究比较深入,具多态性,决定弓形虫不同基因型的致病力[17]。ROP5被分泌后通过膜结合结构域(RAH)定位于PVM。在小鼠体内,ROP5通过阻止免疫相关GTP酶(IRGs)在PVM的积累维持PVM的完整性,逃避宿主细胞经干扰素γ(IFNγ)调控的虫体清除机制。目前关于ROP5的作用机制有2种观点,一是ROP5直接与IRGs互作,使IRGs的构象发生变化,易于ROP18对其进行磷酸化,导致IRGs失活,不能形成二聚体,影响它们在PVM上的积累。Boothroyd等的研究揭示,在小鼠体内,ROP5能够绑定IRGs家族的3个成员(IRGa6,IRGb6,IRGb10)。ROP5与IRGa6的互作占据掩盖了IRGa6的活性位点,使IRGa6处于GDP-lock构象状态,该构象不适于IRGa6在PVM聚集;且IRGa6核苷酸转换环loopⅠ内的两个关键苏氨酸(T102,T108)暴露在易被ROP18磷酸化的位置,有利于ROP18对ROP5-IRGa6复合物磷酸化,磷酸化的IRGa6永久失活,不能与PVM结合,从而丧失了对宿主细胞的保护作用[18]。二是ROP5通过改变ROP18构象调控它的激酶活性,为ROP18的变构增活因子。弓形虫强毒Ⅰ型遗传图谱显示ROP5与ROP18可相互作用控制弓形虫的毒性。Behnke等的研究表明ROP5通过构象变化调控ROP18的激酶活性,但不影响ROP18的表达及PVM定位。为了验证这一功能,用体外重组ROP18及从野生型虫株(RHDku80)和ROP5缺失株(RHDku80Drop5)中获得ROP18,分别对人工合成的dMBP和宿主细胞内的IRGb6进行磷酸化。结果表明,在缺失ROP5的情况下,重组及内原的ROP18对dMBP及IRGb6进行磷酸化的能力显著降低;在ROP5存在情况下,重组ROP18的活性增加12倍,内源ROP18的活性增加35倍,并且能够使dMBP和IRGb6磷酸化。这一研究否定了这些蛋白(ROP5,ROP18,IRGb6)形成稳定复合物、ROP5与IRGb6、ROP18与IRGb6是增强ROP18活性的原因;同时证明ROP18的催化活性受假激酶ROP5的调控[19-20]。上述 ROP5的功能均借助于ROP18的激酶活性。最近的研究表明,ROP5的作用底物除了IRGs和ROP18外,还有其它效应因子,其毒性作用亦可独立完成,因为缺失ROP5的Ⅰ型株的毒性减弱程度大于ROP18缺失的Ⅰ型株。至于ROP5其它的互作效应因子及毒性作用机制有待进一步的探讨[19]。
ROP2与ROP5一样定位于PVM,是弓形虫ROPKs家族中最早被发现的典型代表,早期研究表明ROP2是一种跨膜蛋白,参与PVM的形成,通过N端的信号序列招募宿主细胞的线粒体及高尔基体到PVM的周围,在宿主细胞线粒体与纳虫泡膜之间形成分子连接,参与营养物质的运输、代谢产物的排泄及虫体与宿主细胞的相互作用[21-22];但最近随着对它跨膜的拓补学结构及晶体结构特点研究的深入,认识到它的上述作用是次要的,在虫体入侵及胞内复制中可能通过其它方式担当重要角色[25],至于具体什么作用目前仍是未知。此外,Hooi Yee研究表明ROP2重组蛋白具有较强的免疫原性,可作为弓形虫病免疫诊断的标志物[6]。ROP2的功能是否与ROP5一样能够调控其它蛋白激酶的活性、是否具有其它重要的作用底物等都有待进一步的研究。
研究表明ROP8与ROP2关系密切。ROP8基因与ROP2基因串联存在,它们核苷酸及编码氨基酸的同源性分别为85%、75%。在功能方面,ROP8与ROP2一起参与PV的构建及PVM与宿主细胞线粒体的连接[23]。2014年,Alaganan A 等揭示ROP8,ROP2,ROP18,GRA7在PVM 上形成一个大的蛋白复合物;但通过基因敲除技术证明,ROP8,ROP2并不参与调控ROP18的功能[24]。与ROP2一样,ROP8的功能有待深入研究。
[1]Martin V,Arcavi M,Santillan G,et al.Detection of humanToxoplasma-specific immunoglobulins A,M,and G with a recombinantToxoplasmagondiiRop2protein[J].Clin Diaqn Lab Immunol,1998,5(5):627-631.
[2]Manning G,Plowman GD,Hunter T,et al.Evolution of protein kinase signaling from yeast to man[J].Trends Biochem Sci,2002,7(10):514-520.
[3]Peixoto L,Chen F,Harb OS,et al.Integrative genomics approaches highlight a family of parasite-specific kinases that regulate host responses[J].Cell Host Microbe,2010,8:208-218.DOI:10.1016/j.chom.2010.07.004
[4]Leslie M.‘Dead’enzymes show signs of life[J].Science,2013,340(6128):25-27.DOI:10.1126/science.340.6128.25
[5]Bartlett GJ,Porter CT,Borkakoti N,et al.Analysis of catalytic residues in enzyme active sites[J].J Mol Biol,2002,324(1):105-121.
[6]Chang PY,Fong MY,Nissapatorn V,et al.Evaluation of Pichia pastoris-expressed recombinant rhoptry protein 2ofToxoplasma gondiifor its application in diagnosis of toxoplasmosis[J].Am J Trop Med Hyg,2011,85(3):485-489.DOI:10.4269/ajtmh.2011.11-0351
[7]Qiu W,Wernimont A,Tang K,et al.Novel structural and regulatory features of rhoptry secretory kinases inToxoplasmagondii[J].EMBO J,2009,28:969-979.DOI:10.1038/emboj.2009.24
[8]Hanks SK,Hunter T.The eukaryotic protein kinase superfamily:kinase(catalytic)domain structure and classification[J].FASEB J,1995,9:576-596.
[9]Zheng B,Lu S,Tong Q,et al.The virulence-related rhoptry protein 5(ROP5)ofToxoplasmagondiiis a novel vaccine candidate against toxoplasmosis in mice[J].Vaccine,2013,31(41):4578-4584.DOI:10.1016/j.vaccine.2013.07.058
[10]Kornev AP,Tavlor SS.Pseudokinases:functional insights gleaned from structure[J].Structure,2009,17(1):5-7.DOI:10.1016/j.str.2008.12.005
[11]Reese ML,Boothroyd JC.A conserved non-canonical motif in the pseudoactive site of the ROP5pseudokinase domain mediates its effect onToxoplasmavirulence[J].J Biol Chem,2011,286(33):29366-29375.DOI:10.1074/jbc.M111.253435
[12]Zaqiraj E,Filippi BM,Deak M,et al.Structure of the LKB1-STRAD-MO25complex reveals an allosteric mechanism of kinase activation[J].Science,2009,326(5960):1707-1711.DOI:10.1126/science.1178377
[13]Christova Y,Adrain C,Bambrough P,et al.Mammalian iRhoms have distinct physiological functions including an essential role in TACE regulation[J].EMBO Rep,2013,14(10):884-890.DOI:10.1038/embor.2013.128
[14]Fisher KW,Das B,Kortum RL,et al.Kinase suppressor of Ras 1(KSR1)regulates PGC1αan estrogen-related receptorαto promote Oncogenic Ras-dependent anchorage-independent growth[J].Mol Cell Biol,2011,31(12):2453-2461.DOI:10.1128/MCB.05255-11
[15]Fernandez MR,Henry MD,Lewis RE.Kinase suppressor of Ras 2(KSR2)regulates tumor cell transformation via AMPK[J].Mol Cell Biol,2012,32(18):3718-3731.DOI:10.1128/MCB.06754-11
[16]Behnke MS,Khan A,Wootton JC,et al.Virulence differences inToxoplasmamediated by amplification of a family of polymorphic pseudokinases[J].Proc Natl Acad Sci U S A,2011,108(23):9631-9636.DOI:10.1073/pnas.1015338108
[17]Fleckenstein MC,Reese ML,Konen-Waisman S,et al.AToxoplasmagondiipseudokinase inhibits host IRG resistance proteins[J].PLoS Biol,2012,10(7):e1001358.DOI:10.1371/journal.pbio.1001358
[18]Behnke MS,Fentress SJ,Mashayekhi M,et al.The polymorphic pseudokinase ROP5controls virulence inToxoplasmagondiiby regulating the active kinase ROP18[J].PLoS Pathog,2012,8(11):e1002992.DOI:10.1371/journal.ppat.1002992
[19]Niedelman W,Gold DA,Rosowski EE,et al.The rhoptry proteins ROP18and ROP5MediateToxoplasmagondiievasion of the murine,but not the human,interferon-gamma response[J].PLoS Pathog,2012,8(6):e1002784.DOI:10.1371/journal.ppat.1002784
[20]Talevich E,Kannan N.Structural and evolutionary adaptation of rhoptry kinases and pseudokinases,a family of coccidian virulence factors[J].BMC Evol Biol,2013,13:117.DOI:10.1186/1471-2148-13-117
[21]Nakaar V,Ngo HM,Agronson EP,et al.Pleiotropic effect due to targeted depletion of secretory rhoptry protein R0P2inToxoplasmagondii[J].J Cell Sci,2003,116 (pt11):2311-2320.
[22]Labesse G,Gelin M,Bessin Y,et al.ROP2fromToxoplasma gondii:A virulence factor with a protein-kinase fold and no enzymatic activity[J].Structure,2009,17(1):139-146.DOI:10.1016/j.str.2008.11.005
[23]Pernas L,Boothroyd JC.Association of host mitochondria with the parasitophorous vacuole duringToxoplasmainfection is not dependent on rhoptry proteins ROP2/8[J].Int J Parasitol,2010,40(12):1367-1371.DOI:10.1016/j.ijpara.2010.07.002
[24]Alaganan A,Fentress SJ,Tang K,et al.Toxoplasma GRA7effector increases turnover of immunity-related GTPases and contributes to acute virulence in the mouse[J].Proc Natl Acad Sci U S A,2014,111(3):1126-1131.DOI:10.1073/pnas.1313501111
