慢性迁延性中心性浆液性脉络膜视网膜病变的两种自发荧光特征△
2014-11-13王志立李晓华李士清董应丽李萍
王志立 李晓华 李士清 董应丽 李萍
中心性浆液性脉络膜视网膜病变(central serous chorioretinopathy,CSC)是各种原因导致黄斑区或其附近的视网膜神经上皮和色素上皮之间的局限性浆液性脱离,进而导致视网膜色素上皮损害[1]。自发荧光(autofluorescence,AF)包括脂褐素相关的自发荧光(lipofuscin-related fundus autofluorescence,FAF)和黑色素相关的近红外自发荧光(melanin-related near-infrard fundus autofluorescence,NIA),是一种无创性检测视网膜色素上皮(retinal pigment epithelium,RPE)细胞损害的重要方法[2]。FAF已应用到老年性黄斑变性、特发性脉络膜新生血管及CSC等眼底病中[3-5],但NIA在慢性迁延性 CSC中应用的报道尚少。为此,我们回顾性分析了在我院就诊的一组慢性迁延性CSC患者两种自发荧光的临床资料,现将结果报告如下。
1 资料与方法
1.1 一般资料 选取2010年1月至2013年5月经我院眼科确诊为慢性迁延性CSC的患者57例63眼为研究对象。其中,男41例45眼,女16例18眼,年龄 24~42岁,病史 3个月~1 a,视力 0.1~0.6。排除伴有葡萄膜炎、青光眼、眼外伤及其他黄斑病变者。
1.2 方法 所有患者检查前应用复方托吡卡胺滴眼液散瞳,行眼底彩色照相、直接检眼镜检查。采用德国海德堡共焦激光扫描眼底血管造影仪(Spectralis HRA)行荧光素眼底血管造影(fundus fluorescence angiography,FFA)检查。在荧光素注射前,分别行FAF和NIA检查,使用HRA自带软件处理后得到FAF和NIA图像。然后将100 g·L-1的荧光素钠针(international Medication Systerms,Limited,USA)5 mL经过敏预试验后5 s内肘静脉快速注入,FFA检查持续时间为15 min,典型图像经计算机图像处理后分析备用。
2 结果
2.1 慢性迁延性CSC渗漏点FFA、AF像 典型图像见图1-图3。63眼在FFA造影早期呈不典型渗漏点或多发渗漏点等特征(图1A、图2A、图3A)。在FAF上呈异常荧光表现者47眼(占74.6%),分别表现为弱荧光39眼(占83.0%,图1B)、强荧光3眼(占 6.4%,图2B)、不典型荧光 5 眼(占 10.6%,图3B)。NIA上呈异常荧光表现者59眼(占93.7%),分别表现为弱荧光48眼(占81.4%,图1C)、斑驳状荧光5眼(占 8.5%,图2C)、不典型荧光 6眼(占10.2% ,图 3C)。

Figure 1 Leakage pinpoint of FFA and AF images in a 35-year old male patient with chronic CSC.A:FFA showed multiple fluorescein leakage pinpoints on temporal to macula of right eye(white arrowheads);B:Hypoautofluorescence of FAF corresponding to leakage pinpoints(black arrowheads);C:Hypoautofluorescence of NIA corresponding to leakage pinpoints(black arrowheads)35岁慢性迁延性CSC男性患者渗漏点FFA、AF像。A:右眼FFA示黄斑区颞侧可见多个斑点状荧光渗漏(白箭头);B:FAF示渗漏点呈弱荧光(黑箭头);C:NIA示渗漏点呈弱荧光(黑箭头)

Figure 2 Leakage pinpoint of FFA and AF image in a 30-year old male patient with chronic CSC.A:FFA showed a fluorescein leakage pinpoint on macula of right eye(white arrowhead);B:Hyperautofluorescence of FAF corresponding to leakage pinpoint(white arrowhead);C:Mottled autofluorescence of NIA corresponding to leakage pinpoint(white arrowhead),the abnormal autofluorescence of NIA corresponding to normal retina on FFA and FAF image(yellow arrowhead)30岁慢性迁延性CSC男性患者渗漏点FFA、AF像。A:右眼FFA示黄斑区针点状荧光渗漏(白箭头);B:FAF示对应渗漏点呈强荧光(白箭头);C:NIA示渗漏点呈斑驳状荧光(白箭头),NIA异常荧光区与FFA和FAF正常视网膜区域相对应(黄箭头)
2.2 慢性迁延性 CSC眼视网膜神经上皮脱离区FFA、AF像 典型图像见图4-图5。63眼FFA造影晚期呈斑片状或类圆形强荧光(图4A、图5A)。FAF上呈异常荧光者50眼(占79.4%),表现为弱荧光15 眼(占30.0%,图4B)、强荧光 35 眼(占 70.0%,图5B)。NIA上呈异常荧光者57眼(90.5%),表现为颗粒样混杂荧光51眼(占89.5%,图4C)、弱荧光6眼(占10.5%,图5C)。另外,在 FAF和 NIA上显示视网膜神经上皮脱离区范围大于FFA者分别有23 眼和 33 眼,占 36.5%和 52.4%(图5B-图5C)。
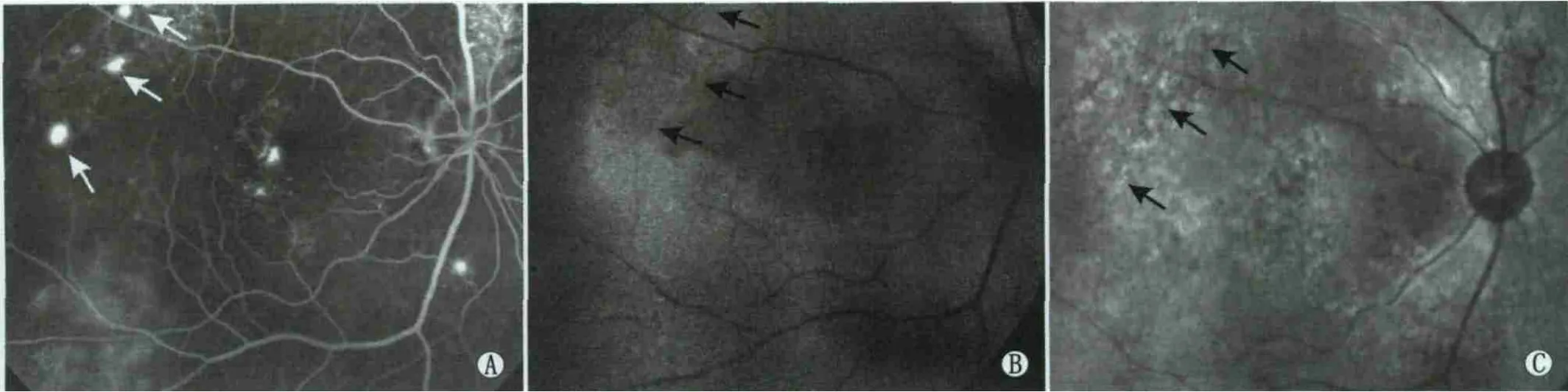
Figure 3 Leakage pinpoint of FFA and AF image in a 39-year old male patient with chronic CSC.A:FFA showed multiple fluorescein leakage pinpoints on posterior pole of right eye(white arrowheads);B:Atypical autofluorescence of FAF corresponding to leakage pinpoint(black arrowheads);C:Atypical autofluorescence of NIA corresponding to leakage pinpoint(black arrowheads)39岁慢性迁延性CSC男性患者渗漏点FFA、AF像。A:右眼FFA示视网膜后极部多个斑点状荧光渗漏(白箭头);B:FAF示渗漏点呈不典型荧光(黑箭头);C:NIA示渗漏点呈不典型荧光(黑箭头)

Figure 4 Neurosensory retinal detachment of FFA and AF image in a 34-year old male patient with chronic CSC.A:FFA showed two shallow neurosensory retinal detachment areas formatted by two fluorescein leakage pinpoints on temporal and nasal to macula of right eye(white arrowheads);B:Central hypoautofluorescence and surrounding hyperautofluorescence of FAF corresponding to two shallow neurosensory retinal detachment areas(black arrowheads);C:Multiple particles like hybrid autofluorescence of NIA corresponding to two shallow neurosensory retinal detachment areas(black arrowheads)34岁慢性迁延性CSC男性患者神经上皮脱离区FFA、AF像。A:右眼FFA示黄斑中心凹颞侧及鼻上两个斑点状渗漏形成的浅脱离区(白箭头);B:FAF示脱离区内呈弱荧光,边缘为强荧光(黑箭头);C:NIA示脱离区可见多个颗粒状荧光(黑箭头)

Figure 5 Neurosensory retinal detachment leakage of FFA and AF image in a 29-year old female patient with chronic CSC.A:FFA showed shallow neurosensory retinal detachment areas on macula of left eye(white arrowhead);B:Hyperautofluorescence areas of FAF corresponding to the neurosensory retinal detachment areas(white arrowhead),and the area of hyperautofluorescence was larger than that of FFA(black arrowhead);C:Hypoautofluorescence areas of NIA corresponding to neurosensory retinal detachment areas(white arrowhead),and the areas of hypoautofluorescence was larger than that of FFA(black arrowhead)29岁慢性迁延性CSC女性患者神经上皮脱离区FFA、AF像。A:左眼FFA示黄斑中心凹周围及下方荧光脱离区(白箭头);B:FAF示对应脱离区为强荧光(白箭头),荧光波及范围大于FFA(黑箭头);C:NIA示脱离区为弱荧光(白箭头),荧光波及范围大于FFA(黑箭头)
2.3 慢性迁延性CSC眼正常视网膜区域FFA、AF像 在63眼中,FFA和FAF显示正常的区域,而在NIA上表现异常者 3眼(图2A-图2C,黄箭头),占4.8%。
3 讨论
Kellner等[6]研究表明,慢性迁延性 CSC患者视力及视功能损害往往比急性CSC严重,主要原因是渗漏点反复发作或多点渗漏导致视细胞与RPE细胞代谢紊乱,从而引起不可逆的视力障碍。FAF产生的主要荧光物质是RPE细胞内的脂褐质成分,其主要来源于未被RPE细胞吞噬消化的感光细胞外节盘膜。NIA是二极管激光产生的787 nm的近红外激光,主要反映黑色素分布的光学图像[7]。临床上利用FAF检测RPE细胞内脂褐质成分的高低,利用NIA检测黑色素的分布,进而反映RPE细胞的功能状态、代谢状况及其损害情况[8-9]。
本研究中,慢性迁延性CSC患者渗漏点在FAF上表现为异常荧光者占74.6%,高于曹绪胜等[10]的64.3%,异常荧光偏高的原因可能与例数或患者的病程等因素有关。本研究结果显示,渗漏点在FAF上呈弱荧光者占 83.0%,在 NIA上呈弱荧光者占81.4%,此研究结果与 Framme等[11]的研究结果相似。我们发现FAF弱荧光区与NIA弱荧光区相对应。有研究表明,慢性迁延性CSC中FAF减弱可能为感光细胞缺失或广泛死亡所致,FAF增强提示患者渗漏点位置RPE细胞降解代谢产物的能力下降,尚未出现显著细胞坏死[12]。本研究中多数患者存在FAF和NIA弱荧光,进一步证实慢性迁延性CSC患者存在色素上皮损害和功能下降,应给予积极治疗。
本研究中,慢性迁延性CSC患者神经上皮脱离区FAF有多种异常表现,其中,FAF呈弱荧光者占30.0%,其余为强荧光。弱荧光斑与神经上皮下积液遮挡相关,而强荧光主要显示RPE损害[13]。慢性迁延性CSC患者神经上皮脱离区在NIA上表现以混杂荧光为主,提示RPE存在不同程度的损害[14]。本研究也发现,慢性迁延性CSC患者NIA和FAF检测到RPE损害区范围较FFA显示的病变区范围大。我们推测与多次反复发作致使RPE损害范围逐渐变大相关。FAF和NIA在检测RPE细胞损害范围方面均有一定优势[15]。因此,我们认为FAF和NIA适用于对慢性迁延性CSC中RPE损害范围的评估。
本研究中,少数CSC在FFA显示正常的区域,同样也可检测到异常NIA,但未检测到 FAF异常。我们的发现与以往报道的NIA较FAF能更早地检测到 RPE的异常损害相一致[16]。周芸芸等[17]研究表明,在某些眼底未发现异常的疾病早期,FAF可能已经发生了改变。因此,FAF和NIA不仅适合观察慢性迁延性CSC病变区域RPE的变化,也适合于正常眼底范围内RPE变化的研究。
FAF和NIA不足之处在于不能替代FFA对渗漏点渗漏程度的评估,也不能替代光学相干断层扫描(OCT)对视网膜神经上皮脱离的评估。因此,如能将FAF、NIA、FFA和 OCT结合起来,将能对慢性迁延性CSC提供更全面的评估。
总之,NIA联合FAF可以用于观察和评估慢性迁延性CSC视网膜渗漏点和神经上皮脱离区RPE损伤情况,也适用于观察病变范围外正常区域RPE的变化,有助于临床上对慢性迁延性CSC治疗前后RPE情况的评估。
1 Imamura Y,Fujiwara T,Spaide RF.Fundus autofluorescence and visual acuity in central serous chorioretinopathy[J].Ophthalmology,2011,118(4):700-705.
2 Kellner U,Kellner S,Weinitz S.Chloroquine retinopathy:lipofuscinand melanin-related fundus autofluorescence,optical coherence tomography and multifocal electroretinography[J].Doc Ophthalmol,2008,116(2):119-127.
3 Schachar IH,Zahid S,Comer GM,Stem M ,Schachar AG,Saxe SJ,et al.Quantification of fundus autofluorescence to detect disease severity in none exudative age-related macular degeration[J].Jama Ophthalmol,2013,131(8):1009-1015.
4 Peng X,Zhang W.Lipofuscin-and melanin-related fundus autofluorescence in patients with submacular idiopathic choroidal neovascularization[J].Eye Sci,2012,27(3):138-142.
5 Eandi CM,Ober M,Iranmanesh R,Peiretti E,Yannuzzi LA.Acute central serous chorioretinopathy and fundus autofluorescence[J].Retina,2005,25(8):989-993.
6 Kellner U,Kellner S,Weber BH,Fiebig B,Weinitz S,Ruether K.Lipofuscin-and melanin-related fundus autofluorescence visualize different retinal pigment epithelial alterations in patients with retinitis pigmentosa[J].Eye(Lond),2009,23(6):1349-1359.
7 Kim SK,Kim SW,Oh J,Huh K.Near-infrared and short-wavelength autofluorescence in resolved central serous chorioretinopathy:association with outer retinal layer abnormalities[J].Am J Ophthalmol,2013,156(1):157-164.
8 Keilhauer CN,Delori FC.Near-infrared autofluorescence imaging of the fundus:visualization of ocular melanin[J].Invest Ophthalmol Vis Sci,2006,47(8):3556-3564.
9 Kellner U,Kellner S,Weinitz S.Fundus autofluorescence(488 nm)and near-infrared autofluorescence(787 nm)visualize different retinal pigment epithelium alterations in patients with age-related macular degeneration[J].Retina,2010,30(1):6-15.
10 曹绪胜,彭晓燕,周辉,周海英.中心性浆液性脉络膜视网膜病变荧光素渗漏点的自身荧光改变[J].中华眼底病杂志,2011,27(4):314-317.
11 Framme C,Walter A,Gabler B,Roider J,Sachs HG,Gabel VP.Fundus autofluorescence in acute and chronic-recurrent central serous chorioretinopathy[J].Acta Ophthalmol Scand,2005,83(2):161-167.
12 von Rückmann A,Fitzke FW,Fan J,Halfyard A,Bird AC.Abnormalities of fundus autofluorescence in central serous retinopathy[J].Am J Ophthalmol,2002,133(6):780-786.
13 Ayata A,Tatlipinar S,Kar T,Unal M,Ersanli D,Bilge AH.Near-infrared and short-wavelength autofluorescence imaging in central serous chorioretinopathy[J].Br J Ophthalmol,2009,93(1):79-82.
14 苏兰萍,彭锡嘉,王雅东.中心性浆液性脉络膜视网膜病变FFA和FAF 图像的对比分析[J].眼科新进展,2011,31(3):235-238.
15 彭锡嘉.中心性浆液性脉络膜视网膜病变的两种眼底自发荧光特征观察[J].中华实验眼科杂志,2012,30(7):646-649.
16 Pilotto E,Vujosevic S,Melis R,Convento E,Sportiello P,Alemany-Rubio E,et al.Short wavelength fundus autofluorescence versus nearinfrared fundus autofluorescence,with microperimetric correspondence,in patients with geographic atrophy due to age-related macular degeneration[J].Br J Ophthalmol,2011,95(8):1140-1149.
17 周芸芸,陈长征,文峰.眼底自发荧光在视网膜疾病中应用新进展[J].中国实用眼科杂志,2007,25(12):1272-1274.
