维通静脉注射乳剂制备工艺研究*
2014-11-08王成蹊侯连兵
王成蹊 ,秦 飞 ,周 静 ,周 毅 ,李 磊 ,毛 萍 ,侯连兵
(1.广东药学院药科学院,广东 广州 510006;2.南方医科大学南方医院药学部,广东 广州 510515;3.内蒙古医科大学,内蒙古 呼和浩特 010110;4.广州医科大学,广东 广州 510182)
维通注射液是南方医科大学药学部在验方常通口服液的基础上开发的用于防治盆腹腔术后粘连的复方中药注射剂,主要由丹参、大黄等中药组方,具有益气养血、理气化瘀的的功效。试验证明,维通注射液可防治大鼠手术后腹腔粘连,显著降低大鼠术后盲肠组织内羟脯氨酸含量[1],亦可降低手术后兔体内羟脯氨酸与纤维蛋白原含量,病理切片表明其可抗炎、改善纤维化、修复创伤组织[2]。前期试验测得维通注射液的半数致死量为8.4 mg/kg,注射此剂小鼠会出现一系列中毒现象[3]。为进一步降低毒性并解决药物中部分脂溶性成分难溶的情况,本试验采用二步乳化法制备了维通静脉注射乳剂(WIE),并采用溶血试验研究其安全性。
1 仪器、试药与动物
Platisil ODS色谱柱(美国Dikma公司);CTO-20A型高效液相色谱仪(日本岛津公司);Nano ZS90型马尔文激光粒度仪(英国马尔文仪器有限公司);FA25型高剪切分散乳化机(德国FLUKO公司);M-110EH型高压均质机(美国Microfluidics公司)。注射用大豆油(广州汉方现代中药研究开发有限公司);中链甘油三酯、注射用蛋黄卵磷脂、注射用油酸均购自德国Lipoid公司;注射用甘油(汕头古汉紫光氨基酸有限公司);甲醇、乙腈(美国Fisher Scientific公司),其余试剂均为分析纯。新西兰家兔(南方医科大学实验动物中心)。
2 方法与结果
2.1 乳剂制备
经过预试验初步得到静脉注射乳剂制备方法,将脂溶性组分分散于混合油相(含MCT10g、大豆油10g)中,加入油酸、维生素E,60℃磁力搅拌溶解,制得油相。称取水溶性组分、蛋黄卵磷脂、甘油,分散于60 mL水相(注射用水)中,60℃搅拌溶解,制得水相。于60℃高速(9 500 r/min)剪切搅拌,将油相缓慢滴加入水相中,共剪切约10 min,用注射用水稀释定容至100 mL,制得初乳。25℃下转移至高压均质机中均质。装瓶,充氮,密封,105℃水浴灭菌30 min,冰水浴迅速降温,即得WIE。
2.2 组方优化
由于维通注射液由脂溶性和水溶性2种药物构成,2种药物会分别溶解于静脉乳的油相和水相,因此有必要对不同油相、不同乳化剂、不同稳定剂进行正交试验,观察在不同条件下乳剂的稳定性,寻找有利于2种药物稳定溶解的最佳处方。在初步固定工艺的基础上将油相、卵磷脂、油酸的用量这3个因素作为考察对象,每个因素选3个水平,采用 L9(34)正交试验,制备不同批次乳剂,以乳剂在80℃的稳定时间 K作为处方稳定性评价指标,研究处方的最佳配比。结果最佳处方组成为油相20%,卵磷脂 1.0%,油酸 0.06% 。
2.3 制备工艺优化
2.3.1 灭菌条件考察
在确定静脉注射乳剂处方基础上,取同一批静脉注射乳剂分成3组,每组分装3只西林瓶,充氮气,按不同条件消毒,研究WIE在不同高压灭菌方法下的耐热性。试验使用的3种条件分别为105℃高压灭菌30 min,115℃高压灭菌25 min,121℃高压灭菌20 min。灭菌后观察静脉注射乳剂性状,结果见表3。可见,其中115℃高压灭菌25 min和121℃高压灭菌20 min均发生破乳分层现象,105℃高压灭菌30 min未见破乳,灭菌效果最好。因此,灭菌条件选择为105℃高压灭菌30 min。
2.3.2 热压灭菌对pH的影响
由于磷脂遇热易水解产生脂肪酸而降低静脉注射乳剂的pH,影响其稳定性及包封率,故需考察热压灭菌对制剂pH的影响。按照试验优选后的处方配置静脉注射乳剂,任取1个样品,测定其粒径为200.2 nm,分别装到5个西林瓶内,用氢氧化钠和盐酸溶液分别调节制剂的 pH 至 6.0,7.0,8.0,9.0,10.0,并 105 ℃灭菌30 min,考察灭菌前后乳剂的pH、外观变化。结果见表1。由于pH经高压灭菌后会降低,因此在制得脂肪乳后应先将其pH调整至9.0,再灭菌。pH为6.2的乳剂灭菌后发生破乳现象,故无法测量。结果见表1。

表1 热压灭菌对乳剂pH的影响
2.3.3 不同均质压力和次数对乳剂的影响
按处方(0.002%DA,0.02%DB,20% 油相,0.06% 油酸,0.5%维生素E,2.5%甘油)制备初乳后,将初乳分成3批,各600 mL,3批分别在5 000 psi,10 000 psi和20 000 psi压力下用高压均质机均质乳化,并在均质乳化第 1,2,3,4,6,8,12,16 次留样,测定样品粒径并观察样品性状。结果样品性状均为白色乳状液体,无油花,粒径见表2。可见,随着均质次数的增加,静脉注射乳剂的粒径逐渐减小,最后趋向于一个恒定值,一般情况下均质3~4次后粒径大小和该值相差不大。但当使用不同压力时,该恒定值也存在较大差异,故需在正交试验中寻找最佳成乳压力。
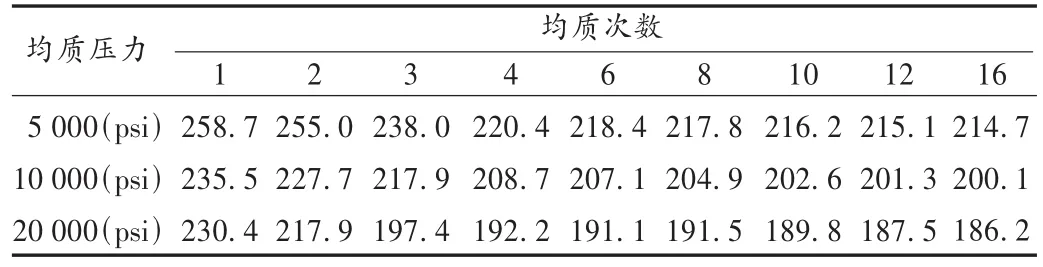
表2 不同均质压力和次数对乳剂粒径的影响(nm)
2.3.4 制备工艺条件优化
脂肪乳剂质量的好坏主要与乳化技术工艺有关。根据文献[5]对脂肪乳注射液生产的经验,列出制备工艺中对脂肪乳质量可能影响较大的各个因素和水平,选择混合温度、混合时间、均质压力作为影响因素,进行正交试验,以乳剂在80℃的稳定时间K作为处方稳定性评价指标,计算结果。得最佳工艺组成为混合温度为60℃,混合时间为10 min,均质压力为20 000 psi。
2.4 理化性质考察
2.4.1 亚微乳的粒径、ζ-电位、黏度测定
精密量取3批维通静脉注射乳剂样品各0.5 mL,以注射用水稀释定容至20 mL,使用粒度分布分析仪分别测定粒径和ζ-电位,结果平均粒径为(191.03±2.81)nm,平均 ζ-电位为(-38.83±2.40)mV,另精密量取3批维通静脉注射乳剂样品,使用黏度计测得平均黏度为(1.85 ±0.02)mPa·s。
2.4.2 维通静脉注射乳剂中有效成分含量测定
由于WIE成分较多,本试验选择丹参中具有代表性的药物丹参酮ⅡA作为含量测定指标。
色谱条件与方法学考察结果:色谱柱为C18柱;流动相为甲醇-水(85∶15);流速为1.0 mL/min;柱温为30℃;进样量为20 μL;检测波长为270 nm。线性回归方程为 Y=0.000 012 73X+0.012 698,R2=0.999 944 8,精密度的 RSD 为 0.13% 。
含量测定:取 500 μL(含 DA 10 μg)WIE 于试管中,加入0.1 mol/L NaOH 200 μL,并加入氯仿 1 000 μL,涡旋振荡 5 min,40℃避光超声20 min,继续涡旋混合5 min,15 000 r/min离心10 min,液体分3层,上层为上清液,中间层为磷脂层,下层为氯仿层(呈淡红色),取下层氯仿液,置减压干燥箱40℃干燥,残渣加入1 mL甲醇溶解,定容,用0.45 μm滤膜过滤,于270 nm波长处检测样品含量。色谱图见图1。结果吸收峰面积 A=770 408,代入标准曲线计算得丹参酮ⅡA含量为98.2%,证明制剂质量良好。
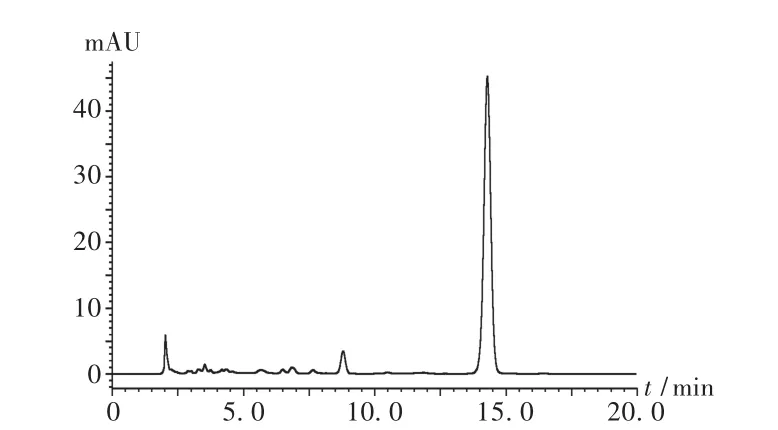
图1 维通静脉注射乳剂丹参酮ⅡA高效液相色谱图
2.5 体外溶血试验
取家兔血,5 mL置抗凝离心管中,放入装载小玻璃珠的洁净锥形瓶中振摇10 min,以除去纤维蛋白原,离心之后弃上清液,将红细胞层用0.9%氯化钠注射液冲洗4次,每次10 mL,每次冲洗后3 000 r/min离心20 min,除去上清液,直至上清液不呈红色为止,然后吸取一定量红细胞,用0.9%氯化钠注射液按体积比稀释制备2%红细胞混悬液,4℃冰箱中冷藏备用。
取7支试管,编号为1~7,溶血试验设计见表3,分别在各管内加入适量2%红细胞混悬液和0.9%氯化钠注射液(7号管内加蒸馏水做阳性对照),置37℃恒温水浴中30 min后又分别加入不同量的WIE(6号管做阴性空白对照),轻摇至均匀后放回37 ℃恒温水浴中,分别于 0.5,1,2,3,4 h 时观察试管内红细胞溶血情况。试验结束时,将各试管以2 500 r/min的速率离心10 min后,分别取上清液在550 nm波长处比色,以0.9%氯化钠注射液管上清液为空白,蒸馏水管上清液作为100%溶血,计算各试管的溶血率[4]。结果见表4。可见,在各时间点1~6管均未发生明显溶血现象,说明WIE组与阴性对照组无溶血现象;7号管在各个时间点均发生溶血现象。离心后比色得到溶血率在0.09%~1.22%之间,符合卫生部药品标准中溶血率不得超过5%的规定。因此,本试验制备的WIE渗透压在安全范围内,且不含溶血成分,作为注射剂可以安全使用。

表3 维通静脉注射乳剂溶血试验设计(mL)
3 讨论
脂肪乳注射液是以植物油(主要成分为脂肪酸三酰甘油)为油相,辅以磷脂为乳化剂、等渗剂和注射用水乳化制得的水包油(O/W)型乳剂,是一种以脂肪油为软基质而被磷脂膜包封的微粒体分散系[5]。本试验制备的静脉乳即为注射用脂肪乳,与其他微粒制剂相比较,载药脂肪乳注射液具有其独特的优点:将药物包裹于内相或界面层中,包封率高,提高药物稳定性并降低药物刺激性和毒性;能够耐受终端高压蒸汽灭菌,保证了制剂的安全性;载药量高,确保了药物的疗效[5]。

表4 维通静脉注射乳剂溶血试验结果
中药静脉注射乳剂已有数个相应产品上市。如鸦胆子油亚微乳注射剂[6]、薏苡仁油亚微乳注射剂、大蒜油亚微乳等[7-8]。本试验使用的药物维通静脉注射乳剂的主药来自于丹参、大黄等植物提取物,其中部分组分具有脂溶性强而水溶性弱的性质,无法直接溶解于水制备注射液,故采用先将脂溶性组分溶解于油相,再将水溶性组分溶解于水相后,制备静脉注射乳剂。通过正交试验等,分别对处方和工艺进行优化,获得生产乳剂的最佳条件。作者用超速离心法测定出药物在油相中的含量为98.2%,表明制剂符合试验设计要求。
采用紫外分光光度法测定溶血度准确、快速且重现性好,弥补了试管法判断误差较大之不足。试验表明,WIE与体积分数为2%的兔红细胞混悬液于37℃孵育4 h不发生溶血现象,说明制剂较为安全。
[1]赵 洁,曾煦欣,侯连兵.维通注射液对大鼠术后肠粘连的防治作用研究[J].中国药房,2009,20(21):1 611 -1 613.
[2]曾煦欣,赵 洁,黄嗣航,等.维通注射剂对兔腹腔术后粘连防治作用的研究[J].中药材,2008,31(4):580 -583.
[3]钟延松,曾煦欣,侯连兵.维通注射液的急性毒性实验研究[J].中药材,2008,31(11):1 720 -1 722.
[4]黎 玲,王东凯,李林穗,等.注射用WIE的制备[J].沈阳药科大学学报,2007,24(12):736 -739.
[5]赵明明,苏 敏,唐 星.载药脂肪乳注射液的研究进展[J].沈阳药科大学学报,2010,27(12):933-935.
[6]游荣辉,丛龙波,袁海龙.静脉亚微乳研究进展及其在现代中药研究中的应用[J].中草药,2007,38(6):946 -948.
[7]Guo T,Chu XQ,Yan M,et al.The effect of anti- eumycete and safe of garlic oil submicron emulsions[J].J Shenyang Pharm Univ,2005,22(6):458-462.
[8]Guo T,Chu XQ,He Jin,et al.Investigation on stabilities of garlicoil submicron emulsion[J].Pharm J Chin PLA,2005,21(2):81 - 84.
