自然水体生物膜形态对其生成H2O2与降解十二烷基苯磺酸钠的影响
2014-10-25董德明赵天宇孙家倩郭爱桐花修艺梁大鹏郭志勇
李 明,毛 丹,董德明,赵天宇,孙家倩,郭爱桐,花修艺,梁大鹏,郭志勇
(吉林大学 地下水资源与环境教育部重点实验室,水资源与水环境吉林省重点实验室,环境与资源学院,长春130012)
自然水体生物膜是一种典型的以微藻类(硅藻和绿藻为主)和细菌为生命组分、以无机矿物和金属氧化物(铁锰氧化物为主)及胞外聚合物(EPS)为非生命组分构成的复合生物群落[1-2].自然水体生物膜普遍存在于河流、湖泊、湿地、河口海岸带及人工景观的各种固相物质表面上,如表层沉积物、沙石和岩石等[1-2].在水环境中,生物膜与污染物间存在吸附、富集和降解转化等相互作用[1-2].由于水体流动和生物扰动等因素使生物膜分散、脱落到水相中,破坏了生物膜的微观生态结构,因此对生物膜中生命与非生命间以及固相与水相中的物质交换产生影响,从而改变生物膜的生态功能[3-4].文献[5-6]研究了昼夜变化对重金属类污染物浓度的影响;文献[7]研究了藻类等生物的新陈代谢.由于H2O2可转化为具有强氧化性的羟基自由基(·OH),即在光照和金属离子存在条件下通过类Fenton反应促进H2O2生成·OH,进而降解有机污染物[8-9].因此,本文以十二烷基苯磺酸钠(DBS)[10-11]作为可降解有机污染物,在光照和无光条件下,通过模拟实验考察有活性和无活性及不同形态生物膜体系中生成H2O2并降解DBS的规律,并分析光照和生物膜形态对H2O2生成规律和DBS降解的影响机理.
1 实 验
1.1 试剂与仪器
CaCl2,MgSO4,(NH4)2SO4,KNO3和 NaHCO3均为北京化工厂产品(分析纯);NaN3为天津市光复精细化工厂产品(分析纯);DBS为国药集团化学试剂有限公司产品(分析纯).TC501恒温水浴控制装置(金坛市华城开元实验仪器厂);UNICO 7200型分光光度计(尤尼柯上海仪器有限公司).
1.2 方 法

1.2.2 降解实验 在转子扰动条件下,将2.8LMMS置于烧杯(3L)中,溶液初始pH≈7.5±0.1,溶解氧(DO)质量浓度约为(10±0.2)mg/L,DBS初始质量浓度为2.0mg/L,每个体系含有4片生物膜.由于温度影响生物膜的新陈代谢和降解,因此采用恒温水浴控制装置将实验体系温度控制为(22±2)℃.在光照实验(L)中,采用温室稀土补光灯作为实验模拟光源,波长为300~1 000nm,光照强度为(40 000±3 000)lx.在无光实验(D)中,将烧杯外壁用锡纸包裹,顶部用不透光盖遮挡(非完全封闭体系).
将生物膜分为聚集态(J,附着在载玻片上的生物膜)和分散态(X,从载玻片上分离的生物膜).分散态生物膜制备方法:从培养缸中取出载玻片,将载玻片上的生物膜从载玻片上分离至含有50mL MMS溶液的烧杯中,若生物膜分离后的载玻片与未培养过生物膜的载玻片对照无差异,则表明生物膜已从载玻片上基本分离.在收集分散态生物膜的烧杯中使用20mL MMS溶液冲洗载玻片3次.实验时将分散态生物膜转移至含有2.6L的MMS体系中,转移后使用30mL MMS溶液冲洗制备分散态生物膜的烧杯3次.在分散态生物膜实验体系中,测定H2O2和DBS前先将水样过0.45μm的微孔滤膜.
将生物膜分为活性生物膜(BF)和无活性生物膜(NaN3).无活性生物膜在实验前12h使用NaN3灭活[12].
1.2.3 样品测定 采用标准方法测定DBS的质量浓度,水样经亚甲基蓝染色和三氯甲烷萃取后,使用分光光度计在652nm处测定其吸光值[12].H2O2浓度使用钛盐比色法测定[14-15].pH值和DO值使用美国哈希公司生产的HQ40d型电极测定.
2 结果与讨论
2.1 光照条件下生物膜形态对DBS降解的影响
光照条件下有活性和无活性以及聚集态和分散态的生物膜降解实验结果如图1所示,由图1(A)和(B)可见:在L-BF(J)-NaN3和L-BF(X)-NaN3体系中的 DBS质量浓度未发生变化,也未检测到H2O2,表明无活性的生物膜未降解DBS,也未生成H2O2,生物膜对DBS的吸附作用较小,与文献[12]研究结果相符;在L-BF(J)和L-BF(X)体系中的DBS质量浓度降低、H2O2浓度升高,生物膜体系中的生物降解作用对DBS影响较小[12],表明有活性生物膜体系中生成的H2O2促进了DBS降解.由图1(C)和(D)可见:在L-BF(J)-NaN3和L-BF(X)-NaN3体系中的DO和pH 值变化较小,在L-BF(X)和L-BF(J)体系中的DO和pH值均呈明显下降趋势,其中DO的质量浓度分别减少约1.23mg/L和1.11mg/L,pH值分别减少约1.15和1.5.DBS在降解过程中会生成小分子酸(甲酸、乙酸和丁二酸等)、直链烷基链、磺化苯基羧酸(SPC)和其他有机酸,DBS完全降解可生成硫酸氢盐和碳酸氢盐,进而导致pH 值降低[16-17].
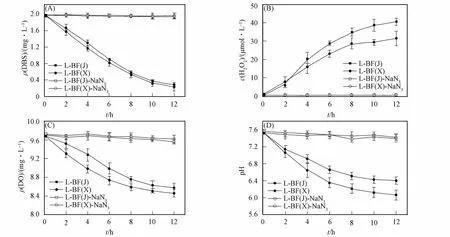
图1 L-BF(J)和L-BF(X)及L-BF(J)-NaN3 和L-BF(X)-NaN3 体系中的DBS质量浓度(A)、H2O2浓度(B)、DO质量浓度(C)和pH变化(D)Fig.1 Mass concentration of DBS(A),concentration of H2O2 (B),mass concentration of DO(C)and pH (D)in systems L-BF(J),L-BF(X),L-BF(J)-NaN3and L-BF(X)-NaN3
由于聚集态生物膜转变为分散态生物膜过程中破坏了部分生物细胞壁,且细胞液中富含铁等金属离子可促进H2O2分解生成·OH[18],因此在L-BF(X)体系中的H2O2浓度相对较低,进而导致DO质量浓度也较低.L-BF(X)体系的pH值略高于L-BF(J)体系的pH值,这可能是由于DBS降解中间产物的质量浓度存在差异所致.
2.2 无光条件下生物膜形态对DBS降解的影响
无光条件下有活性和无活性及聚集态和分散态的生物膜降解实验结果如图2所示.由图2(A)和(B)可见:在 D-BF(J)-NaN3和 D-BF(X)-NaN3体系中的 DBS质量浓度未发生变化,也未检测到H2O2;在D-BF(X)和D-BF(J)体系中的DBS质量浓度逐渐降低,并生成H2O2,表明无光条件下的生物膜也可生成H2O2并降解DBS.由图2(C)和(D)可见,在D-BF(X)和D-BF(J)体系中的pH 值和DO均呈下降趋势,其中pH值分别减少约1.2和1.0,DO质量浓度分别减少约0.95mg/L和1.32mg/L.由于DBS降解量越大,其消耗的DO越多,pH值下降越大,因此DO和pH值相对较低.

图2 D-BF(J)和 D-BF(X)及D-BF(J)-NaN3 和 D-BF(X)-NaN3 体系中的DBS质量浓度(A)、H2O2浓度(B)、DO质量浓度(C)和pH变化(D)Fig.2 Mass concentration of DBS(A),concentration of H2O2 (B),mass concentration of DO(C)and pH (D)in systems D-BF(J),D-BF(X),D-BF(J)-NaN3and D-BF(X)-NaN3
活性生物膜在光照条件下H2O2生成量约为无光条件下H2O2生成量的2~3倍,表明光照是生物膜生成H2O2的重要因素.光照条件下DBS降解量约为无光条件下DBS降解量的3~4倍,这可能是因为光照促进生成H2O2和其他活性氧化剂(如·OH).光照不能直接降解DBS,但吸光后处于激发态的有机物比处于基态的有机物更易被光催化氧化[19].因此,光照对DBS降解的中间产物有降解作用.
综上所述,在光照和无光条件下,具有活性的自然水体生物膜均可生成一定量的H2O2并降解DBS;光照是生物膜生成H2O2并降解DBS的重要因素;分散态比聚集态生物膜的H2O2生成量少,但其DBS降解量高于聚集态生物膜.
[1]董德明,张菁菁,李鱼,等.自然水体生物膜吸附 Mn2+过程中吸附液pH值的变化 [J].吉林大学学报:理学版,2003,41(2):234-237.(DONG Deming,ZHANG Jingjing,LI Yu,et al.Changes of Solution pH during Mn2+Adsorption to the Natural Surface Coatings[J].Journal of Jilin University:Science Edition,2003,41(2):234-237.)
[2]董德明,李鱼,花修艺,等.淡水中生物膜主要化学组分选择性萃取分离的比较 [J].吉林大学学报:理学版,2002,40(2):209-211.(DONG Deming,LI Yu,HUA Xiuyi,et al.Comparison of Separation Results of Components of Fresh-Water Surface Coatings by Selective Extraction [J].Journal of Jilin University:Science Edition,2002,40(2):209-211.)
[3]Villeneuve A,Montuelle B,Bouchez A.Influence of Slight Differences in Environmental Conditions(Light,Hydrodynamics)on the Structure and Function of Periphyton[J].Aquatic Sciences,2010,72(1):33-44.
[4]Fuhrman J A.Microbial Community Structure and Its Functional Implications[J].Nature,2009,459:193-199.
[5]Beck A J,Janssen F,Polerecky L,et al.Phototrophic Biofilm Activity and Dynamics of Diurnal Cd Cycling in a Freshwater Stream [J].Environ Sci Technol,2009,43(19):7245-7251.
[6]Nimick D A,Gammons C H,Parker S R.Diel Biogeochemical Processes and Their Effect on the Aqueous Chemistry of Streams:A Review [J].Chem Geol,2011,283(1/2):3-17.
[7]Rose A L,Salmon T P,Lukondeh T,et al.Use of Superoxide as an Electron Shuttle for Iron Acquisition by the Marine Cyanobacterium Lyngbya Majuscula[J].Environ Sci Technol,2005,39(10):3708-3715.
[8]CHENG Mingming,MA Wanhong,LI Jing,et al.Visible-Light-Assisted Degradation of Dye Pollutants over Fe(Ⅲ)-Loaded Resin in the Presence of H2O2at Neutral pH Values[J].Environ Sci Technol,2004,38(5):1569-1575.
[9]Vermilyea A W,Voelker B M.Photo-Fenton Reaction at near Neutral pH [J].Environ Sci Technol,2009,43(18):6927-6933.
[10]Wolf W,de,Feijtel T.Terrestrial Risk Assessment for Linear Alkyl Benzene Sulfonate (LAS)in Sludge-Amended Soils[J].Chemosphere,1998,36(6):1319-1343.
[11]雷鸣,廖柏寒.表面活性剂的生态毒理学及其应用研究进展 [J].安全与环境学报,2004,4(增刊1):27-30.(LEI Ming,LIAO Baihan.Progress of Application and Ecotoxicty of Surfacts [J].Journal of Safety and Environment,2004,4(Suppl 1):27-30.)
[12]HUA Xiuyi,LI Ming,SU Yulong,et al.The Degradation of Linear Alkylbenzene Sulfonate(LAS)in the Presence of Light and Natural Biofilms:The Important Role of Photosynthesis[J].J Hazard Mater,2012,229/230:450-454.
[13]郑娜,花修艺,董德明,等.重金属在自然水体生物膜上的竞争吸附 [J].吉林大学学报:理学版,2005,43(3):388-393.(ZHENG Na,HUA Xiuyi,DONG Deming,et al.Competitive Adsorption of Metal Cations onto Natural Surface Coatings[J].Journal of Jilin University:Science Edition,2005,43(3):388-393.)
[14]Eisenberg G.Colorimetric Determination of Hydrogen Peroxide [J].Ind Eng Chem Anal Ed,1943,15(5):327-328.
[15]Manousaki E,Psillakis E,Kalogerakis N,et al.Degradation of Sodium Dodecylbenzene Sulfonate in Water by Ultrasonic Irradiation[J].Water Res,2004,38(17):3751-3759.
[16]Hidaka H,Oyama T,Horiuchi T,et al.Photo-Induced Oxidative Synergistic Degradation of Mixed Anionic/Cationic Surfactant Systems in Aqueous Dispersions.A Detailed Study of the DBS/HTAB System [J].Appl Catal B:Environment,2010,99(3/4):485-489.
[17]郭伟,李培军.阴离子表面活性剂(LAS)环境行为与环境效应 [J].安全与环境学报,2004,4(6):37-42.(GUO Wei,LI Peijun.Environmental Behavior and Effect of Anionic Surfactant(LAS)[J].Journal of Safety and Environment,2004,4(6):37-42.)
[18]Freinbichler W,Colivicchi M A,Stefanini C,et al.Highly Reactive Oxygen Species:Detection,Formation,and Possible Functions[J].Cell Mol Life Sci,2011,68(12):2067-2079.
[19]赵杨,魏宏斌,徐迪民.光催化氧化法处理表面活性剂废水 [J].中国给水排水杂志,2004,20(10):26-30.(ZHAO Yang,WEI Hongbin,XU Dimin.Photocatalytic Oxidation Process for Surfactant Waste Water Treatment[J].China Water & Wastewater,2004,20(10):26-30.)
