基于抑制葡萄糖氧化酶活性快速检测重金属离子的研究
2014-10-11迟德富关桦楠
孙 璐,迟德富*,宇 佳,关桦楠
(1.东北林业大学生命科学院,中国哈尔滨 150040;2.哈尔滨商业大学食品工程学院,中国 哈尔滨 150076)
近年来重金属中毒的事件频繁发生,重金属离子检测显得越来越重要.检测重金属离子的方法主要有原子吸收光谱法[1]、原子荧光光谱法[2]、阳极溶出伏安法[3]等,但传统的重金属检测方法存在着待检测样品前处理复杂、仪器费用高等缺陷,在实际应用中不能广泛普及.因此,寻求一种操作简单、灵敏度高的重金属离子快速检测技术具有重大的意义[4].基于酶抑制作用并利用分光光度法检测食品及环境中重金属残留已逐渐兴起,此方法简单方便、快速灵敏,并且检测样品及使用药品的用量少,对各种重金属元素的检测具有相对较好的普遍性.
葡萄糖氧化酶(glucose oxidase,GOD)具有较好的催化特性,已经在许多领域广泛应用,如食品、医药、化学等[5].重金属离子作用于葡萄糖氧化酶的活性中心,对其活性中心具有极强的亲和力,较多含量的重金属离子会使葡萄糖氧化酶迅速失去活性,导致酶活力下降.同时,重金属对酶具有抑制效应,当重金属在生物体内沉积后,对生物体具有毒性,利用酶抑制法还能对受污染环境中的重金属离子的生物毒性进行风险评估[6].相关文献中提到在反应底物中添加指示剂如2,4-二氯苯酚[7]、靛蓝胭脂红等,当底物与重金属发生反应时,会使底物中指示剂的颜色、吸光度等发生变化,通过检测其被转换的信号或用肉眼即可区分酶活性的变化.本研究基于重金属离子对酶的抑制作用,在其他研究的基础上,考察葡萄糖氧化酶对重金属Pb2+、Cu2+、Ag+离子的检测性能,优化反应体系,尝试拟合出一种快速检测这3种重金属离子的数学检测模型[8].为今后的实际应用提供理论依据.
1 材料与方法
1.1 主要仪器与试剂
主要仪器:TU-1900双光束紫外可见分光光度计(北京普析通用仪器);DZKW-122电热恒温水浴锅(北京市永光明医疗仪器厂);PHS-3C型pH计(上海精密科学仪器设备有限公司);电子天平、微量移液器等.
试剂:0.2 mol/L葡萄糖(沈阳东兴试剂厂);靛蓝胭脂红(天津科密欧)[9];0.2 mol/L乙酸-乙酸钠缓冲液(pH=5.2);乙酸缓冲液(pH=2.55)[10];葡萄糖氧化酶(EC 1.1.3.4,来源于 Bomei公司);3 种重金属标准液:Pb2+标准液:10 μmol/L,根据乙酸铅的分子量用乙酸缓冲液配制(pH=2.55);Cu2+标准液:10 μmol/L,根据硫酸铜的分子量用乙酸缓冲液配制(pH=2.55);Ag+标准液:10 μmol/L,根据硝酸银的分子量用乙酸缓冲液配制(pH=2.55);去离子水;其他试剂均为分析纯或生物纯等.
1.2 实验方法
酶液和葡萄糖溶液置于37℃水浴,将等量的酶液和重金属离子标准液混匀,调整pH后分别置于不同温度条件下(4℃、室温21℃、30℃、35℃、40℃、45℃和50℃)15 min.另取2 mL温热的葡萄糖溶液(0.2 mol·L-1)和2 mL在不同温度条件下的反应液37℃反应10 min后,迅速冰浴,同时另取离心管分别加入3 mL乙酸-乙酸钠缓冲溶液、1.3 mL的靛蓝胭脂红溶液(1.0×10-3mol/L)、1 mL的冰浴反应液,稀释至25 mL,沸水浴13 min后,流水冲洗冷却5 min.打开双光束紫外可见分光光度计,设定参数,在615 nm处,去离子水作参比,分别记录测定的吸光度值.对照组以2 mL乙酸缓冲液(pH=2.55)代替,以上步骤重复3次.
按温度、pH、反应时间的顺序,在确定最适温度后分别进行不同 pH(1~7)、反应时间(5、10、15、20、25、30 min)条件的优化,最后以最适反应条件,考察葡萄糖氧化酶检测3种重金属离子的性能[11].以吸光度变化值为纵坐标,以重金属离子浓度为横坐标,绘制标准曲线.确定抑制方程、检出限等技术指标,并利用方差分析确定各指标的显著性.
2 结果与讨论
2.1 实验原理
由于葡萄糖氧化酶是一种含有两个黄素腺嘌呤二核苷酸分子的蛋白,能将葡萄糖转化为葡萄糖酸并产生H2O2.H2O2具有氧化性,在一定条件下,能够使添加的指示剂靛蓝胭脂红发生褪色反应,在一定范围内,可利用分光光度计测定的吸光度来确定产生H2O2的量[12].而重金属离子又会结合在葡萄糖氧化酶的活性中心,对其活性中心具有极强的亲和力,使葡萄糖氧化酶迅速失去活性,从而导致酶活力下降.从吸光度的变化即可判断酶活性受抑制的程度[13].测得吸光度的变化值ΔA(实验组吸光度值A1与对照组吸光度值A0的差值).以变化值ΔA为纵坐标,反应温度、pH、反应时间分别为横坐标,绘制曲线.
2.2 最适反应温度的选择
采用在pH为3、反应时间为10 min的条件下,设定不同温度梯度进行实验,结果如图1所示.由图1可见,通过与对照(CK线)进行比较,Pb2+在4℃ ~40℃,随着温度的升高,吸光度差值变化不明显,只有很小的波动;40℃~45℃,随温度的升高,吸光度差值突然明显增加,抑制程度升高,切线的斜率最大;45℃时,差值最大,说明此时反应重金属离子抑制葡萄糖氧化酶的程度最大,使靛蓝胭脂红褪色的程度最低;之后随着温度的继续升高,吸光度差值又迅速降低.因此,在所选择的的温度梯度范围内,选择45℃为Pb2+对葡萄糖氧化酶抑制反应的最适保温温度.同理,Cu2+、Ag+的最适温度分别选择室温21℃和40℃.
通过对温度条件的对比,可以看到Cu2+与葡萄糖氧化酶作用,随着保温温度的升高,吸光度差值变化的更为显著,其他两种重金属离子Ag+和Pb2+与葡萄糖氧化酶作用时,随着温度的升高,吸光度差值在0~0.015的小范围内波动,抑制程度相比之下,没有Cu2+的现象明显.
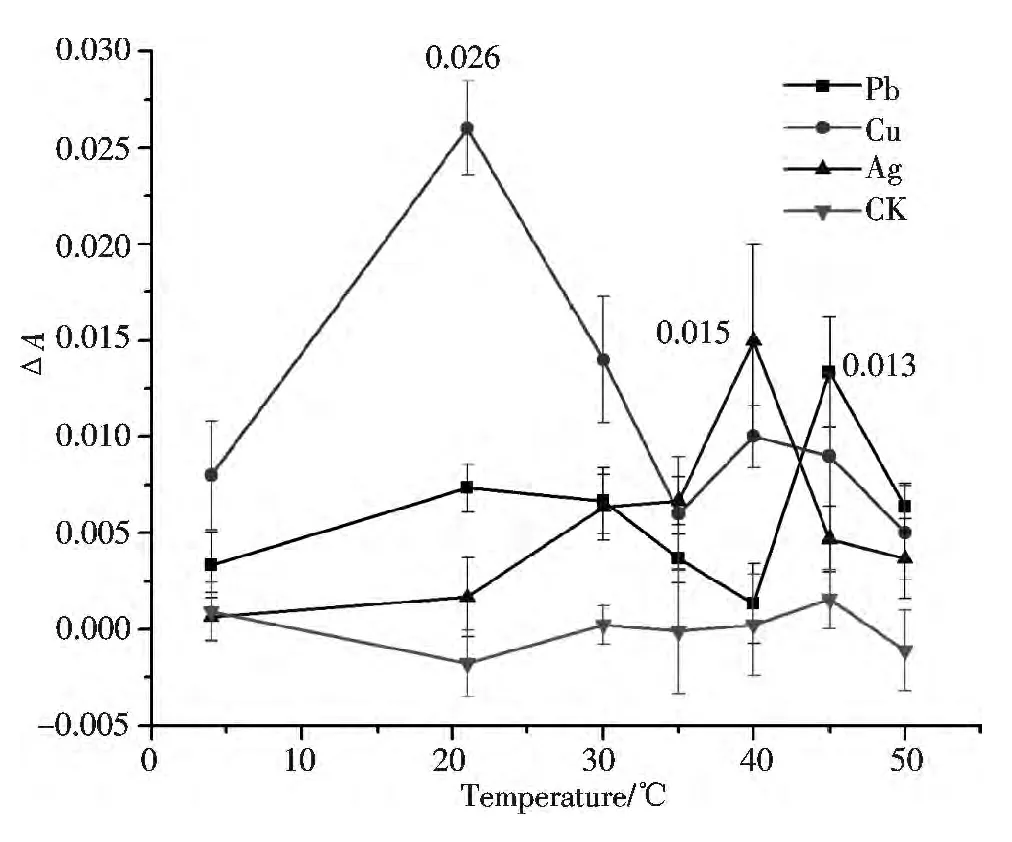
图1 抑制GOD活性法检测重金属离子的最适温度Fig.1 Optimal temperature to detect heavy metal ions by GOD activity inhibiting method
2.3 最适反应pH的选择
反应溶液的pH环境不但会影响酶分子的稳定性,还会影响酶与底物的作用,组成酶活性中心的氨基酸残基侧链存在不同的基团,pH环境的变化会影响到这些基团的解离状态,从而影响酶促反应的速度.按照实验方法在pH 1.0~7.0范围内,在最适温度下,考察pH对Pb2+、Cu2+、Ag+抑制葡萄糖氧化酶作用的影响.由图2可知,最适宜反应的pH分别为:pH为5(Pb2+)、pH为3(Cu2+)、pH为6(Ag+).由实验组所得吸光度数据进行方差分析,结果表明,Pb2+、Cu2+的实验组吸光度得到的P值小于0.01,所以pH对Pb2+、Cu2+抑制葡萄糖氧化酶的程度有极为显著的影响;Ag+的P值小于0.05,所以pH对Ag+的影响较为显著.
通过pH的变化对比可见:Pb2+抑制葡萄糖氧化酶的吸光度差值变化在0.002~0.015范围内,Cu2+在0.007~0.036范围内波动,Ag+在0.014~0.038范围内波动,Cu2+的吸光度波动范围最大,同样证明 Cu2+对pH的变化在3种重金属中最为敏感.虽然酶在一定pH值范围内有较高的活性,pH太高或太低都会影响酶的活性,实验结果表明Cu2+在pH为3这样相对较低的环境下对葡萄糖氧化酶产生了明显的抑制作用,但经对照比较可以证明发生的褪色反应确实是由于重金属离子产生了较大的抑制作用造成的.同时,在汤琳等的研究中提到,酶电极的pH值适应范围最低可达2.55.结合本实验结果说明,在较低的pH条件下,电子的传递速率增大,可能对重金属离子与酶活性中心的结合有一定的促进作用.
2.4 最适反应时间的选择
将重金属离子溶液和葡萄糖氧化酶混合液在最适反应温度条件下放置不同反应时间t,调节为最适pH,考察反应时间对重金属离子抑制葡萄糖氧化酶的影响.由不同反应时间对酶抑制程度的影响(图3)可知,在一定范围内,不同重金属离子对酶的抑制程度都会随反应时间的增加而增加,增大到一定程度后又会受到抑制,所以,经过实验,选择Pb2+、Cu2+、Ag+对葡萄糖氧化酶抑制反应的最适反应时间分别为15、25、20 min,此时,每种重金属离子对葡萄糖氧化酶的抑制作用最大.
通过比较分析,在5~15 min范围内,3种重金属离子抑制葡萄糖氧化酶的吸光度差值变化都不大,均在0.015上下波动,直至达到Ag+的最适反应时间20 min时3种重金属的抑制程度呈现相对较大的差异;20 min时,抑制程度Pb2+<Cu2+<Ag+;随着时间的继续延长,达到Cu2+的最适反应时间25 min.通过方差分析,结果表明,反应时间对铅离子抑制葡萄糖氧化酶程度的影响不显著,而Cu2+离子、Ag+离子的P值小于0.05,说明反应时间对Cu2+离子、Ag+离子抑制葡萄糖氧化酶的程度相对显著.尽管方差分析表明,反应时间对Pb2+抑制葡萄糖氧化酶活性的差异不显著,但是在第15 min时,Pb2+处理组的反应体系的吸光度最高,达到0.018.因此,检测Pb2+的最适反应时间t定为15 min.
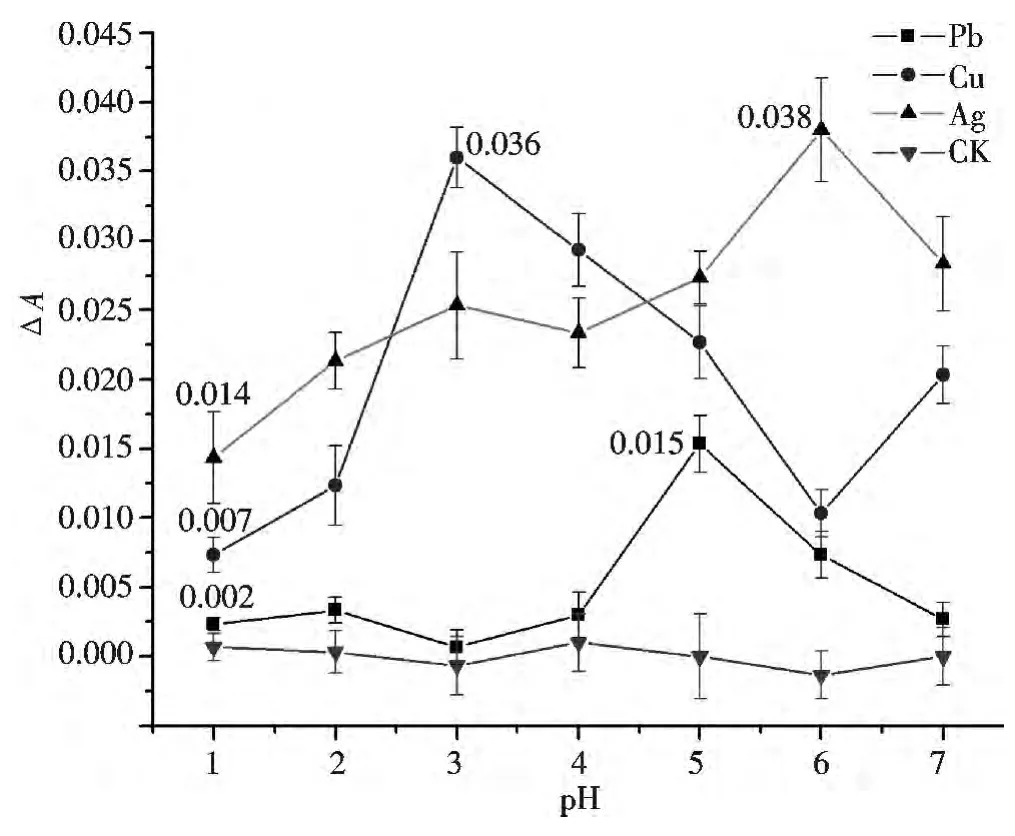
图2 抑制GOD活性法检测重金属离子的最适pHFig.2 Optimal pH to detect heavy metal ions by GOD activity inhibiting method
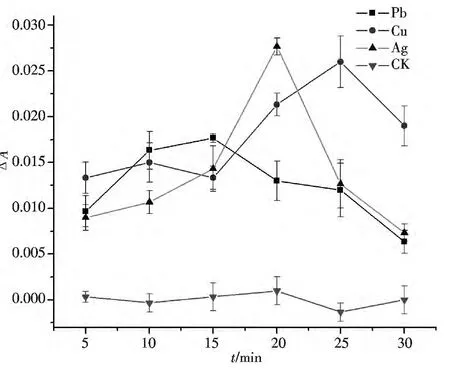
图3 抑制GOD活性法检测重金属离子的最适反应时间Fig.3 Optimal reaction time to detect heavy metal ions by GOD activity inhibiting method
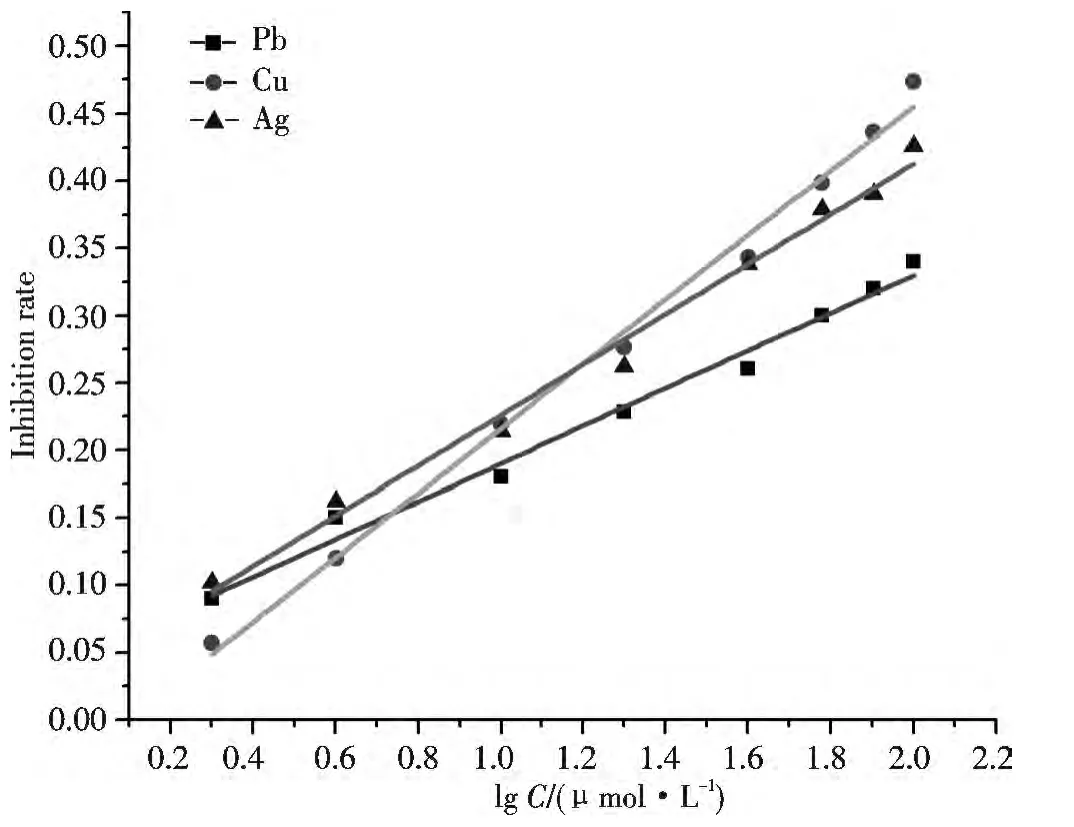
图4 GOD受重金属离子Pb2+、Cu2+、Ag+抑制的标准曲线Fig.4 Standard curves of GOD activity inhibited by the heavy metal ions
2.5 标准曲线的绘制
在最适反应体系下,选择不同的浓度重金属离子溶液继续进行检测.以抑制率为纵坐标,重金属离子浓度的对数为横坐标作图,将所得数据利用Origin 8软件进行拟合曲线,确定抑制方程,所得结果如表1 所示,Pb2+、Cu2+、Ag+分别在10 ~100 μmol/L、4 ~80 μmol/L、10 ~100 μmol/L 范围内存在线性关系,其相关系数均在0.99以上,说明利用该方法对重金属离子进行检测具有一定的可靠性.通过实验获得3种重金属离子的空白样品相对标准偏差(RSD%)分别为 2.47%、1.71%、1.96%.相比之下,RSD 值较小,误差较低[14].且可求出 Pb2+、Cu2+、Ag+的检出限分别为 0.53、0.21 和 0.18 μmol/L.对图4中3种重金属标准曲线的比较可见,Pb2+、Cu2+和Ag+对酶活性具有明显的抑制作用,获得的曲线在一定范围具有良好的线性关系,Cu2+的斜率最大,表明受抑制效果相对明显,Pb2+、Ag+虽然没有Cu2+的抑制效果明显,但是这两种重金属具有相对较宽的检测范围.

表1 抑制酶活性法检测重金属离子的标准曲线方程及线性响应范围Tab.1 Standard curve equation and linear response range to detect heavy metal ions by enzymatic activity inhibiting method
2.6 分析与讨论
实验建立葡萄糖氧化酶检测Pb2+、Cu2+和Ag+的反应体系,并对检测每种重金属离子的最适反应温度、pH值和反应时间等条件进行了优化.选择靛蓝胭脂红为指示剂,根据周建芹等的相关研究确定靛蓝胭脂红用量为1.3 mL[15].研究中葡萄糖氧化酶用量及显色剂用量使用合理,反应时间适宜,研究结果就较为合理.基于重金属离子对葡萄糖氧化酶活性的抑制作用,得到的最佳工艺条件如表2所示.在最佳工艺条件下,选择不同浓度重金属离子溶液进行试验,获得标准曲线,在一定范围内,3种重金属离子对葡萄糖氧化酶活性的抑制具有良好的线性关系,即酶抑制法对重金属离子的快速检测具有较高的灵敏性;利用该方法得到的检出限比翟彤宁[16]、刘京萍[17]等人利用其他方法得到的铜离子和铅离子的最低检出浓度更低.连兰[18]等人利用生物传感器的方法测得铜离子抑制酶电极活性得到的线性范围是0~1.5 μmol/L,李彤[19]等人应用二氧化硅溶胶-凝胶固定化酶技术制备葡萄糖氧化酶电极检测重金属离子的方法测得的线性范围0~1.5 μmol/L和0~60 μmol/L,以及利用其他传统的检测技术能够检测的线性范围较窄[20],相比之下,本实验方法具有的差异性较为显著.
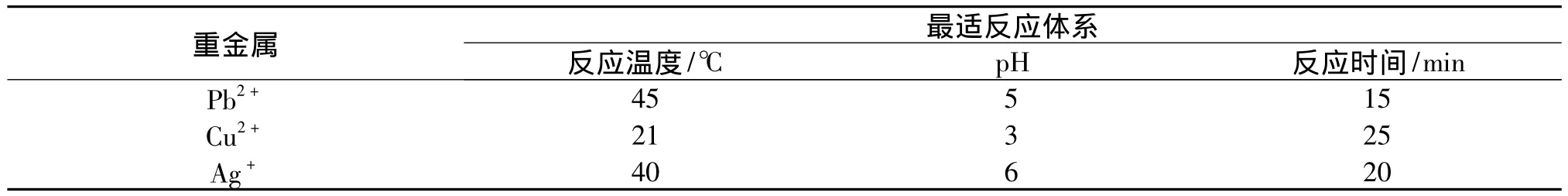
表2 抑制GOD活性检测重金属离子的最佳反应体系Tab.2 Optimal reaction system to detect heavy metal ions by GOD activity inhibiting method
3 结论
利用靛蓝胭脂红褪色的原理并结合分光光度法对重金属离子抑制葡萄糖氧化酶活性的检测方法能够获得的线性范围更宽,具有显著的差异[21-22].通过标准曲线建立数学模型确定的抑制方程置信度均在99%以上,说明该方法具有充分的理论依据及可行性.
本研究中只进行了单一重金属离子的检测,在实际应用中,需要检测的未知液大多为重金属的混合液,若存在离子之间的相互干扰问题,只需加入合适的掩蔽剂就可以排除各种干扰,因而该研究为环境中多元素的同时分析提供了参考.另外,此方法还可以设计成相关的试剂盒,用于重金属离子更为快速、便捷的检测.
[1]朱 睿.原子吸收光谱法在测定水中重金属的应用[J].污染防治技术,2013,26(4):66-70.
[2]王 琰,孙珞新,张 帆.原子吸收光谱法、原子荧光光谱法连续测定化探样品中的Cu、Zn、As、Sb、Bi和Hg[J].光谱实验室,2013,30(2):0737-0741.
[3]黄灿灿,简锦明,曾立波,等.阳极溶出伏安法测定水样中痕量铜离子的研究[J].现代科学仪器,2013,149(3):104-106.
[4]翟慧泉,金星龙,岳俊杰,等.重金属快速检测方法的研究进展[J].湖北农业科学,2010,49(8):1995-1998.
[5]曹 健,师俊玲.食品酶学[M].郑州:郑州大学出版社,2011:293-298.
[6]吕彩云.重金属检测方法研究综述[J].资源开发与市场,2008,24(10):887-890.
[7]范孝用,翟彤宁,王 洁,等.2,4-二氯苯酚测定葡萄糖氧化酶活性的探讨[J].河北省科学院学报,1991(4):67-71.
[8]MARIA R G,COSIMINO M,ELISABETTA M,et al.Inhibitive determination of metal ions by an amperometric glucose oxidase biosensor:Study of the effect of hydrogen peroxide decomposition[J].Sens Actuat B:Chem,2008,131(2):394-402.
[9]庄会荣,胡顺香,陈鸿琪.靛红褪色光度法测定过氧化氢[J].理化检验-化学分册,2000,36(1):36-38.
[10]汤 琳,曾光明,沈国励,等.基于抑制作用的新型葡萄糖氧化酶传感器测定环境污染物汞离子的研究[J].分析科学学报,2005,21(2):123-126.
[11]袁勤生.酶与酶工程[M].上海:华东理工大学出版社,2012:38-49.
[12]陆贻通,沈国清,华银锋.污染环境重金属酶抑制法快速检测技术研究进展[J].安全与环境学报,2005,5(2):68-71.
[13]华银锋,陆贻通.脲酶抑制法检测环境样品中重金属离子研究[J].上海环境科学,2003,22(12):939-942.
[14]国大旺.几种重金属离子的检测及应用的新方法研究[D].长春:吉林大学,2011:76-85.
[15]周建芹,陈韶华,王剑文.测定葡萄糖氧化酶活力的一种简便方法[J].实验技术与管理,2008,25(12):58-60.
[16]翟彤宁,胡常英,王 洁,等.金属离子对葡萄糖氧化酶活性测定的影响[J].河北省科学院学报,1997(4):11-14.
[17]刘京萍,李 金,葛 兴.葡萄糖氧化酶抑制法检测食品中镉、锡、铅的残留[J].北京农学院学报,2007,22(4):59-62.
[18]连 兰,伍 林,易德莲,等.葡萄糖生物传感器检测重金属离子的研究[J].传感器世界,2006(4):6-8.
[19]李 彤,伊丽丽,魏福祥,等.重金属离子对葡萄糖氧化酶电极抑制作用的研究[J].河北科技大学学报,2009,30(2):166-170.
[20]寇冬梅.快速检测重金属离子的酶膜生物传感器及应用研究[D].重庆:西南大学,2008:32-33.
[21]CIUCUA A,LUPU A,PIRVUTOIU S,et al.Biosensors for heavy metals determination based on enzyme inhibition [J].Chem Mater Sci,2001,63(4):33-44.
[22]周焕英,邹 峰,高志贤,等.水中铜的酶抑制快速定量检测方法研究[J].冶金分析,2007,27(9):22-24.
