番禺区南村医院阻断乙型肝炎病毒宫内传播的随机对照研究
2014-09-21吴雪媚
吴雪媚
乙型病毒性肝炎,简称乙肝,是一种由乙型肝炎病毒(HBV)感染机体后所引起的疾病。乙型肝炎病毒是一种嗜肝病毒,主要存在于肝细胞内并损害肝细胞,引起肝细胞炎症、坏死、纤维化。我国目前乙肝病毒携带率为7.18%,母婴传播是最重要的传播途径,母亲是家庭聚集的主体,我国约有30%~50%的乙肝患者是母婴传播所致,成人肝硬化、肝癌90%以上是婴幼儿时期感染上乙肝病毒的。接种乙肝疫苗可以有效地阻断母婴传播途径,但仍有大约10%~20%的婴儿会免疫失败,而导致形成慢性HBV感染[1]。研究显示免疫之前已经发生的宫内感染是导致免疫失败的一个主要原因[2],因此及时有效的切断乙肝病毒的宫内传播就显得尤为重要[3],为此我们进行了一系列的研究,以找到能够有效阻断乙型肝炎病毒在宫内传播的临床方法,现报道如下。
1 资料与方法
1.1 一般资料 资料来自于番禺区南村医院2010年5月~2012年5月携带乙肝病毒的150例孕妇,年龄在22~35岁,平均年龄(24.6±0.6)岁,以上孕妇均无症状表现。将150例孕妇随机分成2组,实验组和对照组,每组75例,2组患者的一般资料比较差异无统计学意义,具有可比性。对150例孕妇及产下的健康新生儿152例(女72例,男80例)进行12个月的随访。
1.2 方法 仅给予对照组孕妇常规检查,实验组孕妇在常规观察的基础上给予免疫球蛋白(HBIG)注射,在妊娠28w开始进行免疫球蛋白(上海生物制品研究所生产)的肌内注射,每4w注射1次,直到孕妇临产,每次200IU,如果孕妇是HBsAg及HBeAg双阳性者每次注射400IU,2组孕妇所生婴儿出生时和出生2w后再分别肌内注射免疫球蛋白100IU;于婴儿1、2、7个月时再次接种乙肝基因重组疫苗(由上海生物制品研究所提供),并于出生时和1、2、7、12个月龄时随访采外周静脉血,采用聚合酶链反应(PCR)检测新生儿外周血乙肝病毒基因(HBVDNA),HBV-DNA是反应宫内感染强弱的直接指标,具有快速、高效以及敏感性强等特点。并检测乙肝表面抗原(HBsAg)及乙型肝炎E抗原(HBeAg),并监测丙氨酸转氨酶(ALT)[4]。
1.3 判断标准 (1)患儿ALT>40IU/L且持续6个月以上者定为慢性乙型肝炎[4]。
(2)新生儿出生时外周血检验HBsAg呈阳性(或HBeAg阳性),至1岁时HBsAg仍阳性者同时抗HBs阴性者认为是宫内感染免疫失败。出生时及1月龄外周血HBsAg呈阳性,出生1年之内HBsAg转阴,并持续阴性且抗HBs阳性者,则可以判断是宫内感染免疫成功[1]。
1.4 统计学方法 采用SPSS11.0软件包进行数据分析,正态计量资料采用“±s”表示;2组正态计量数据的组间比较采用t检验。计数资料用例数(n)表示,计数资料组间率(%)的比较采用χ2检验;P<0.05为差异有统计学意义。
2 结果
2.1 发生宫内感染HBV的例数及比例 在实验组75例新生儿共中有18例随访测出HBsAg(+)和/或HBeAg(+)的婴儿,占新生儿总数的24.00%;对照组77例新生儿中有54例随访测出HBsAg(+)和/或HBeAg(+)的婴儿,占新生儿总数的70.13%。新生儿宫内感染率比较,实验组为6.67%,对照组为15.58%,实验组显著低于对照组(P<0.05);慢性肝炎(ALT持续>40IU/L)的发生率比较,实验组为2.63%,对照组为7.79%,实验组显著低于对照组(P<0.05,见表1)。

表1 2组孕妇所生婴儿发生宫内HBV感染的例数及比例(n)
2.2 2组宫内感染患儿的HBV-DNA检测阳性率比较实验组宫内感染儿的HBV-DNA检测阳性率为40%,对照组为50%,2组比较差异无统计学意义(见表2)。
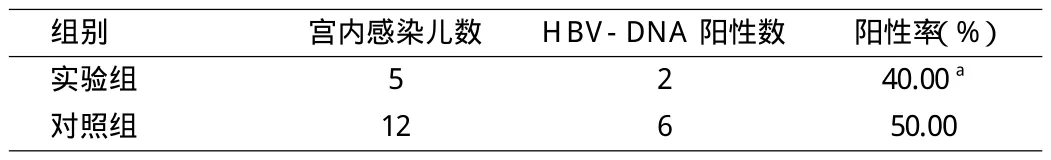
表2 宫内感染婴儿的HBV-DNA检测阳性率
2.3 不良反应观察 进行2年随访,2组婴儿并没有出现明显的不良反应。
3 讨论
目前HBV感染的宫内诊断仍然具有较大的困难,通过经母腹脐血穿刺检出HBsAg阳性也不能证明HBV宫内感染,主要是由于脐血容易被母血感染[5]。研究显示被HBV感染的单核细胞可能通过胎盘感染胎儿,主要是由于HBV感染的肝脏与患者的免疫系统密切相关,而单核细胞在机体免疫应答中发挥着重要作用,HBV感染的单核细胞在病毒致病和传播方面均有作用,HBV感染的单核细胞很可能成为HBV宫内感染的重要载体,因此在外周血中检出HBV-DNA可作为宫内感染的标志[6]。而采用PCR检测新生儿的外周血HBV-DNA可有效提高HBV的检出率,HBV可在宫内感染胎儿的淋巴细胞,因此从外周血淋巴细胞中检出HBV-DNA对于早期诊断HBV宫内感染具有一定的意义。
目前,乙型肝炎疫苗已广泛应用于预防HBV感染,并已取得了突破性的进展,但现在普遍推广的乙肝疫苗的免疫对阻断HBV母婴传播仍存在近20%免疫后失败,而宫内感染正是导致生后免疫失败的主要原因[5]。本研究发现,在实验组75例新生儿共中有18例随访测出HBsAg(+)和/或HBeAg(+)的婴儿,占新生儿总数的24%;对照组77例新生儿中有54例随访测出HBsAg(+)和/或HBeAg(+)的婴儿,占新生儿总数的70.13%。实验组新生儿生下检测外周血HBsAg,测到阳性者5例。我们同时发现发生宫内感染的婴儿其HBV-DNA阳性检出率非常高,本研究的结果显示对照组婴儿的HBV-DNA阳性率为50%,实验组阳性率为40%,2组比较无显著差异。新生儿宫内感染率比较,实验组为6.67%,对照组为15.58%,实验组显著低于对照组(P<0.05)。分析其原因可能是因为,孕妇在孕后期,胎儿在逐渐成熟,胎盘子宫壁也非常容易形成撕裂,因此母体的血液就会进入胎儿的体循环,从而导致胎儿的感染[7-8]。慢性肝炎(ALT持续>40IU/L)的发生率比较,实验组为2.67%,对照组为7.79%,实验组显著低于对照组(P<0.05)。实验组宫内感染儿的HBVDNA检测阳性率为40.00%,对照组为50.00%,2组比较无统计学差异。以上结果说明产前给予孕妇多次肌内注射免疫球蛋白可以有效地阻断乙型肝炎病毒的宫内感染。对2组婴儿进行随访发现,进行产前免疫阻断的孕妇及新生儿均未发现不良反应,说明其具有很好地安全性。综上所述,做好产前乙肝预防工作具有重要的临床意义。
[1]彭美莲,刘玮,吕雯,等.替比夫定与乙型肝炎疫苗及免疫球蛋白联合阻断乙型肝炎病毒母婴垂直传播的研究[J].中华医院感染学杂志,2014(1):8.
[2]王得玲.乙型肝炎病毒母婴传播阻断的临床研究现状[J].当代医学,2010,16(14):39-40.
[3]Shi Z,Yang Y,Ma L,et al.Lamivudine in late pregnancy to interrupt in utero transmission of hepatitis B virus:a systematic review and metaanalysis[J].Obstetrics & Gynecology,2010,116(1):147-159.
[4]周煜,金辉,刘沛.乙肝免疫球蛋白宫内注射阻断乙肝母婴传播的系统评价[J].中国循证医学杂志,2012,12(7):791-798.
[5]姚喜芳.拉米夫定阻断乙型肝炎病毒母婴传播临床研究[J].白求恩军医学院学报,2013,11(5):403-404.
[6]栾峰.阻断乙型肝炎病毒宫内传播的随机对照研究[J].中国实用医药,2012,7(35):79-80.
[7]王清图,修霞.乙肝病毒宫内感染及阻断母婴垂直传播的研究进展[J].临床肝胆病杂志,2009,16(3):142-143.
[8]张福奎,范昕,于耕红,等.阻断围产期乙型肝炎病毒母婴传播的研究进展[J].中华预防医学杂志,2012,3(7):1.