百日咳疫苗及其免疫接种的问题分析
2014-09-18郑俐敏
郑俐敏
百日咳是临床常见儿科传染性疾病,严重威胁患儿生活质量及生命安全,积极有效的预防措施是降低百日咳发生率及保障儿童健康成长的关键因素[1]。本文将于2013年1月1日-2013年12月31日期间,对前来本中心进行百日咳疫苗免疫接种的1386例儿童给予临床研究,分析百日咳疫苗及其免疫接种问题并探讨应对措施,为提高接种率及安全性提供可靠依据,现总结如下。
1 资料与方法
1.1 一般资料 1386例儿童均于2013年1-12月间前来接受百白破疫苗接种,其中男701例,女685例,年龄3~9个月,平均(5.79±0.34)个月。按照接种疫苗不同将其分为无细胞组(719例)及全细胞组(667例),两组儿童的性别、年龄等一般资料比较差异均无统计学意义(P>0.05),具有可比性。
1.2 方法
1.2.1 纳入与排除标准 (1)于本时期自愿前来接种百日咳疫苗;(2)接种前无感染性疾病;(3)排除先天性疾病患儿[2];(4)无心、肝、肾等机体重要器官严重器质性病变;(5)无百日咳疫苗相关禁忌证[3];(6)患儿家属对本次研究具有知情权。
1.2.2 研究方法 对1386例儿童临床资料进行回顾性分析,指定具有专业知识及丰富经验的临床医护人员完成其百日咳疫苗接种工作。记录疫苗接种后不良反应发生情况并探讨防治措施,分析方法为查阅相关病历资料、询问家属、询问当事医护人员等。将所得资料给予统计学分析并得出结论。
1.2.3 疫苗接种 无细胞组儿童接种无细胞百白破疫苗(DTaP),由成都生物制品研究所提供;全细胞组儿童接种全细胞百白破疫苗(DTwP)由上海生物制品研究所提供,疫苗使用时均处于规定有效期内,两组接种方法相同。疫苗接种部位位于上臂外侧三角肌处(左右均可),给药方式为肌肉注射,基础免疫应连续注射3针,0.5 mL/针,3针间隔时间均为28~31 d,根据被接种儿童实际情况可选择是否实施加强免疫(0.5 mL/针)。不良反应:严重不良反应包括脑病、接种部位脓肿、急性过敏反应等,其余如发热、接种局部红肿等均为一般反应。
1.3 统计学处理 将所得数据利用SPSS 17.0软件包完成统计学分析,计量资料采用(±s)表示,比较采用t检验,计数资料采用 字2检验,用(%)表示,以P<0.05为差异具有统计学意义。
2 结果
2.1 不良反应 1386例儿童接种第1剂不良反应发生率最低(0.01%),接种第2剂不良反应发生率上升至0.72%,接种第3剂不良反应发生率最高(1.23%),比较差异具有统计学意义(P<0.05),具体情况见表1。
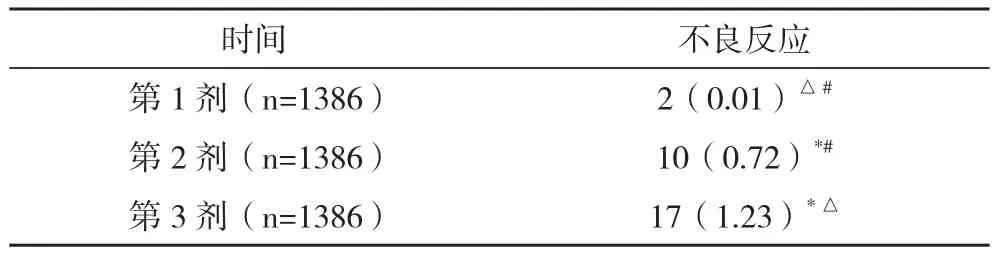
表1 1386例儿童接种百白破疫苗不良反应发生情况分析 例(%)
2.2 组间比较 全细胞组儿童接种百白破疫苗后不良反应发生率均显著高于无细胞组,两组比较差异具有统计学意义(P<0.05),具体情况见表2。
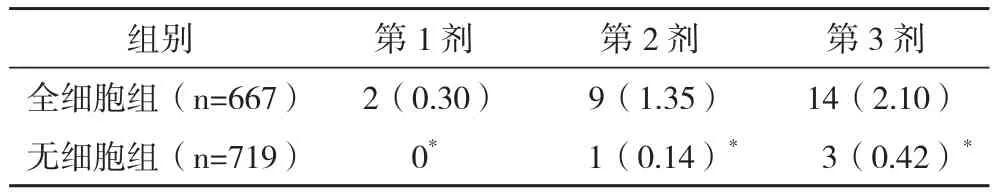
表2 两组儿童接种百白破疫苗不良反应发生情况分析 例(%)
3 讨论
研究表明,随着临床医学水平不断进步,我国已逐渐将百白破三联疫苗取代百日咳疫苗进行百日咳、白喉及破伤风联合免疫接种工作[4]。近年来,由于人们自我保护意识逐渐增强,儿童百白破疫苗接种率逐年增高,计划免疫效果较为理想,但由于接种儿童间具有个体差异,部分儿童经百白破疫苗接种后将出现局部红肿、发热、脑病等不良反应,需引起相关医务工作者高度重视[5-6]。
本文研究可知,全细胞组儿童接种全细胞百白破疫苗后不良反应发生率显著高于无细胞组,接种DTwP可能会导致一些罕见疾病的出现,如脑病、婴儿痉挛或猝死、学习障碍等许多其他综合征,甚至会导致死亡的发生[7]。现阶段未能证实DTwP与注射产生的不良反应有关,但是受相关反应病例数的限制,并不能真正确定两者不存在因果关系。据有关研究表明,严重急性神经系统疾病的出现和接种DTwP没有特别大的关联,接种DTwP后可能促使急性脑病的发生,注射DTwP之后产生的不良反应并不能完全确定,这要求笔者在药剂注射过程中要注意一些细节问题;随着儿童接种量增加,疫苗在体内聚积量升高,其不良反应发生率也随之上升[8]。提示无细胞百白破疫苗可显著降低儿童不良反应发生率;第2剂、第3剂疫苗接种儿童属于不良反应高危人群,临床医护人员应加强其生命体征监测工作[9]。
不良反应防治措施:(1)接种前详细询问病史、药物治疗史等基本情况;(2)接种过程中及接种后进行严密的生命体征监测[10];(3)若接种后局部皮肤发生红肿硬结等不良反应则给予针对性的处理措施;(4)接种完成后无论是否发生局部皮肤红肿均应于穿刺部位给予温开水湿热敷;(5)若接种2 d后局部皮肤红肿仍未好转可给予50%硫酸镁湿热敷[11];(6)若发生局部脓肿、急性过敏反应等严重不良反应需及时告知医生并配合其进行处理。
百日咳疫苗的应用有效降低了百日咳总发病率,但是对于总发病率的抑制还有一定的上升空间[12]。常规的疫苗接种不能完全消除百日咳杆菌的扩散和传播,且不具备预防百日咳的发生和减轻病情的严重性[13]。所以,笔者要在新技术的辅助下,开发出新的疫苗,新疫苗的主要要求是扩大现有的抗原免疫应答,即黏膜抗体、体液抗体以及CMI应答,腺苷酸环化酶也可以用于新型百日咳疫苗中,它是一种毒力因子,产生的中和抗体可以促进白细胞对百日咳杆菌的吞噬作用,减少百日咳杆菌的数量,可以有效地减轻病情。所以,现阶段的主要任务是研究出新的疫苗,减少百日咳疫苗注射后的不良反应。
综上所述,提高百日咳疫苗接种率可显著降低百日咳疾病发生率,接种过程中应提供针对性的干预措施防治相关不良反应,保障接种儿童生活质量及生命安全,值得今后实际工作中推广应用。
[1]王丽婵,张路民,侯启明,等.我国无细胞百白破联合疫苗中百日咳疫苗的批签发及效力试验的回顾性分析[J].中国生物制品学杂志,2012,25(8):1072-1074.
[2]徐颖华,张华捷,侯启明.百日咳杆菌分子分型方法研究进展[J].国际检验医学杂志,2012,33(21):2621-2623.
[3]叶秀萍.护理干预对儿童免疫接种百白破疫苗不良反应的影响分析[J].齐齐哈尔医学院学报,2014,25(13):1995-1996.
[4]胡慧琼,潘海龙,顾洁,等.2-苯氧乙醇对无细胞百日咳原液及无细胞百白破联合疫苗安全性及免疫原性的影响[J].中国生物制品学杂志,2011,24(10):1165-1167.
[5]姜崴,竭晶,杨红育,等.我国百日咳疫苗生产用菌株主要抗原片段基因序列分析[J].中国生物制品学杂志,2012,25(12):1573-1577.
[6]李淑林,刘万清,杨荣.接种吸附无细胞百日咳-白喉-破伤风联合疫苗致血小板减少性紫癜1例报告[J].中国保健营养(中旬刊),2013,24(9):937.
[7]骆鹏,沈立濛,孙琦,等.第6代百日咳疫苗效力国家标准品的建立[J].中国生物制品学杂志,2011,24(11):1303-1305,1312.
[8]王丽婵,马霄,孟丽,等.百日咳疫苗免疫接种策略及相关研究进展[J].中华预防医学杂志,2013,47(1):70-73.
[9]王丽婵,张路民,侯启明,等.我国无细胞百白破联合疫苗中百日咳疫苗的批签发及效力试验的回顾性分析[J].中国生物制品学杂志,2012,25(8):1072-1074.
[10]吴腾捷,张斌,张青,等.无细胞百日咳疫苗纯化新工艺的建立[J].中国生物制品学杂志,2013,26(1):5-8.
[11]徐颖华,骆鹏,王丽婵,等.低抗原含量百日咳疫苗效力评价研究[J].国际检验医学杂志,2012,33(21):2561-2562,2564.
[12]张巧风.接种过期2天百日咳-白喉-破伤风联合疫苗引起臀部无菌性脓肿1例报告[J].中国社区医师(医学专业),2011,13(25):8.
[13]田阳,史秋明,隋礼丽.百日咳毒素、丝状血凝素和黏附素的纯化[J].中国生物制品学杂志,2013,26(8):1186-1189.
