胸腺法新联合吉西他滨治疗晚期胰腺癌疗效观察*
2014-09-18叶建明王春丽黄莉王祥财
叶建明 王春丽 黄莉 王祥财
胰腺癌为临床常见的恶性肿瘤之一,约占恶性肿瘤发病率的1%~2%。吉西他滨单药是晚期胰腺癌的标准一线化疗[1]。肿瘤患者往往免疫功能低下,细胞免疫也出现异常;化疗杀伤肿瘤的同时会影响患者的免疫功能,严重影响到患者的生活质量和生存期。胸腺法新能增强淋巴细胞功能,促进体内细胞因子分泌,增加T细胞表面淋巴因子受体水平;并通过激活CD4细胞,增强自体和异体的混合淋巴细胞反应[2]。本研究采用胸腺法新联合吉西他滨与单药吉西他滨治疗晚期胰腺癌,对比两种治疗方法的疗效及副反应。现报道如下。
1 资料与方法
1.1 一般资料 收集2013年1月~2014年6月本院收治的胰腺癌患者50例,将患者按随机数字表法分为治疗组和对照组,每组25例。纳入标准:(1)预计生存期>3个月;(2)体力状况评分(Karnofsky)≥60分;(3)经病理组织学检查或影像学结合临床表现证实为胰腺癌;(4)排除严重肝肾功能障碍、血常规异常及化疗禁忌;(5)Ⅲ~Ⅳ期不能手术或术后复发、转移;(6)完成吉西他滨化疗2个疗程;(7)具有可测量或可评价病灶;(8)曾应用非吉西他滨类药物化疗失败,并持续停用4周以上;(9)随访≥3个月者;(10)非靶病灶放疗结束1个月以上,或者靶病灶未接受放疗,或放疗结束3个月以上且病灶进展者。治疗组男15例,女10例,年龄36~73岁,平均52.40岁,Ⅲ期12例,Ⅳ期13例;对照组男14例,女11例,年龄38~69岁,平均50.80岁,Ⅲ期12例,Ⅳ期13例。两组患者的年龄、性别、肿瘤组织学类型、临床分期等方面比较差异均无统计学意义(P>0.05),具有可比性。
1.2 方法 对照组患者均采用吉西他滨单药化疗方案,吉西他滨(法国礼来公司生产,批号201203901)1000 mg/m2,第1、8、15天,静脉滴注30 min,28 d为1个周期,化疗2个周期;治疗组在对照组基础上予以加用胸腺法新(美国赛生制药有限公司生产,1.6 mg/支),以1 mL注射用水溶解后立即皮下注射,1.6 mg/次,2次/周,两次间隔3~4 d。连续给药3个月,并给予对症、支持治疗。
1.3 观察指标 (1)体力状况评价:分别于化疗第1天和第90天,按Karnofsky评分标准进行评估。有效:治疗后增加>10分;稳定:增加或减少<10分;无效:减少>10分;总有效=有效+稳定。(2)不良反应及免疫指标观察:第一程化疗前和两程化疗结束后1个月,观察白细胞、血小板下降及血红蛋白变化情况。流式细胞仪检测T淋巴细胞群及自然杀伤细胞(NK)。(3)两程化疗后1个月进行影像学检查,观察评估可见病灶大小的变化情况。并根据WHO的疗效评价标准,分为完全缓解(CR)、部分缓解(PR)、疾病稳定(SD)及疾病进展(PD)。客观缓解=CR+PR;稳定=CR+PR+SD。
1.4 统计学处理 采用SPSS 13.0统计学软件分析数据,计量资料以(±s)表示,比较采用t检验,计数资料采用 字2检验,以P<0.05为差异有统计学意义。
2 结果
2.1 两组体力状况评分的比较 治疗组体力状况改善有效率明显高于对照组,差异有统计学意义(P<0.05),见表1。
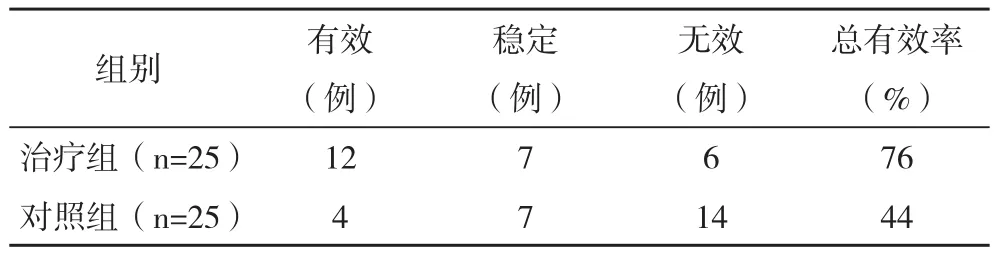
表1 两组体力状况评分的比较
2.2 两组治疗前后T和NK细胞的比较 对照组治疗前后T淋巴细胞群和NK细胞无明显变化(P>0.05);治疗后,治疗组的CD3+、CD4+增高,CD4+/CD8+比值下降,CD8+上升,差异均有统计学意义(P<0.05),见表2。
表2 两组治疗前后T和NK细胞的比较(-±s) %
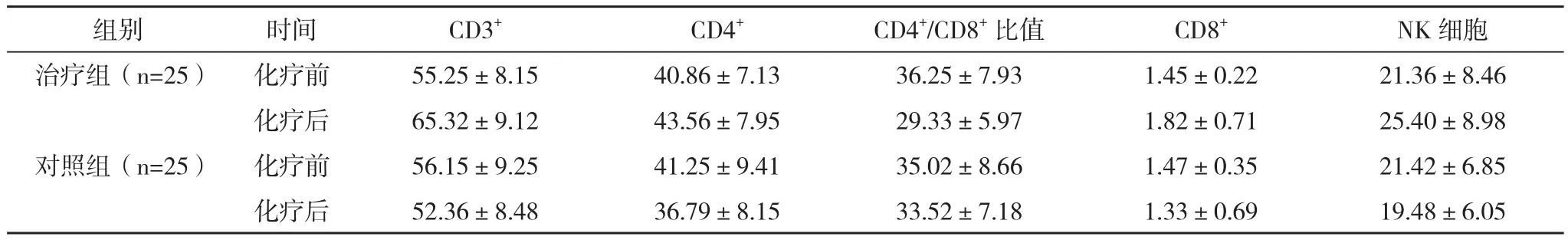
表2 两组治疗前后T和NK细胞的比较(-±s) %
组别 时间 CD3+ CD4+ CD4+/CD8+比值 CD8+ NK细胞治疗组(n=25) 化疗前 55.25±8.15 40.86±7.13 36.25±7.93 1.45±0.22 21.36±8.46化疗后 65.32±9.12 43.56±7.95 29.33±5.97 1.82±0.71 25.40±8.98对照组(n=25) 化疗前 56.15±9.25 41.25±9.41 35.02±8.66 1.47±0.35 21.42±6.85化疗后 52.36±8.48 36.79±8.15 33.52±7.18 1.33±0.69 19.48±6.05
2.3 两组不良反应的比较 治疗组治疗后的不良反应例数与对照组比较差异无统计学意义(P>0.05),见表3。
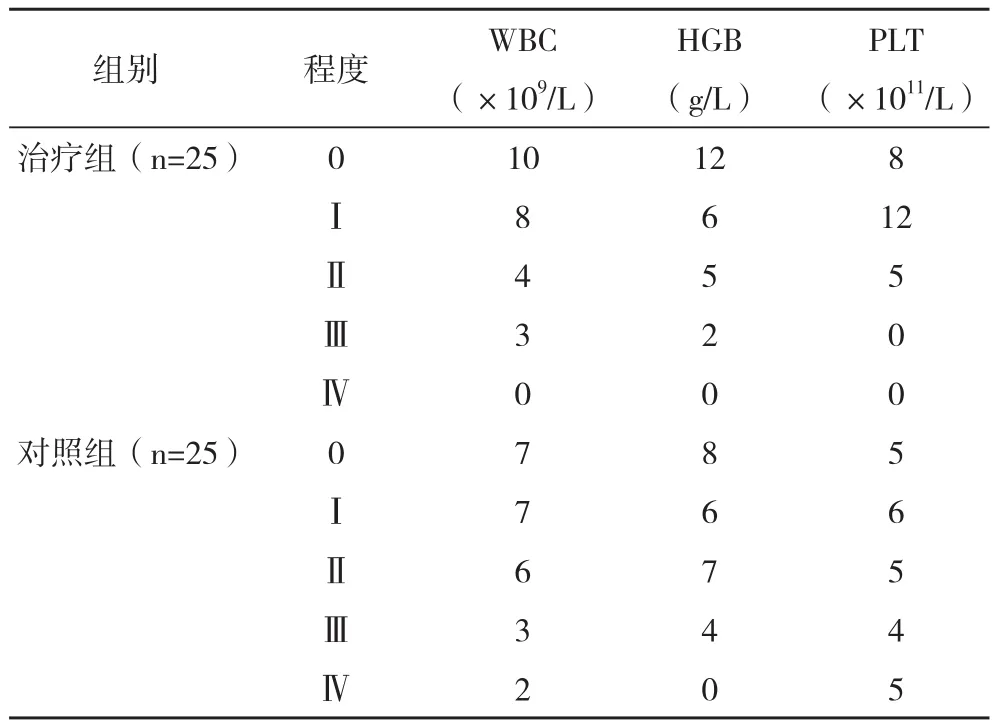
表3 两组不良反应的比较 例
2.4 两组治疗效果的比较 治疗组的客观缓解率及稳定率均明显高于对照组,差异均有统计学意义(P<0.05),见表 4。
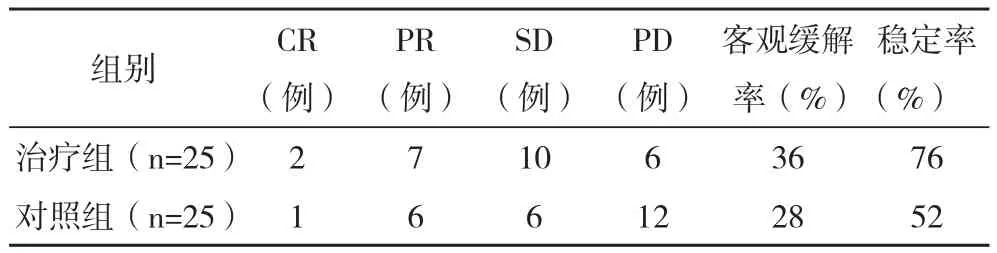
表4 两组治疗后的疗效比较
3 讨论
目前,晚期胰腺癌为临床治疗的难点,减轻患者痛苦、控制疾病进展成为目前进展期胰腺癌治疗的主要目的。有研究发现,与氟尿嘧啶方案比较,吉西他滨可显著改善患者的生存质量,已成为胰腺癌治疗的标准方案[1]。尽管吉西他滨联合化疗较单药可延长一定的总生存时间,但差异无统计学意义[3-5]。NK细胞和T淋巴细胞功能与肿瘤的发生与发展直接相关。激活的CD4+、CD8+、巨噬细胞、T与NK细胞共同参与杀瘤作用。研究表明,胰腺癌患者外周血中CD4+/CD8+比值低于对照组,化疗药物可降低机体的细胞免疫功能活性。因此,多数胰腺癌患者化疗后,其免疫功能进一步受到抑制[6]。
胸腺肽α1能增强淋巴细胞功能,促进体内细胞因子的分泌,促进胸腺内干细胞向T淋巴细胞转化[7]。近年来胸腺肽α1应用于消化系统肿瘤的治疗中取得较好的效果[8]。本研究中,化疗后连续使用胸腺肽α1,发现CD3+、CD4+百分率NK细胞比值较化疗前有所上升,可能与胸腺肽α1能上调CD4以及由TNF-α诱导的标志分子的表达有关[9]。
综上所述,吉西他滨联合胸腺法新可显著提高患者T细胞亚群活性及机体免疫力,保护骨髓功能,降低化疗毒副作用,有利于改善胰腺癌患者预后,提高患者生存质量,值得临床推广。
[1]金伟.吉西他滨联合奥沙利铂双周方案治疗中晚期胰腺癌临床观察[J].中国临床医学,2006,13(8):21-23.
[2]傅德良,倪泉兴,虞先浚,等.胸腺肽α1对围手术期胰腺癌患者血中T和NK细胞的影响[J].上海免疫学杂志,2001,21(6):362-363.
[3] Philip P A,Zalupski M M,Vaitkevicius V K,et al.Phase Ⅱstudy of gemcitabine and cisplatin in the treatment of patients with advanced pancreatic carcinoma[J].Cancer,2001,92(3):569-577.
[4]贾林,袁世珍.胰腺癌化疗新指标-临床受益疗效极其应用[J].医学综述,2002,9(5):30.
[5]马冬,彭杰文,邓卫萍.吉西他滨联合奥沙利铂治疗晚期胰腺癌疗效观察[J].中华肿瘤防治杂志,2005,12(12):936-937.
[6] Wu Y,Denhardt D T,Rittling S R.Osteopontin is required for full expression of the transformed phenotype by the ras oncogene[J].Br J Cancer,2000,83(2):156-163.
[7] Hirama M,Takahashi F,Takahashi K,et al.Osteopontin overproduced by tumor cells acts as a potent angiogenic factor contributing to tumor growth[J].Cancer Lett,2003,198(1):107-117.
[8] Zhang J,Takahashi K,Takahashi F,et al.Differential osteopontin expression in lung cancer[J].Cancer Lett,2001,17(2):215-222.
[9] Shijubo N,Uede T,Kon S,et al.Vascular endothelial growth factor and osteopontin in stage 1 lung adenocarcinoma[J].Am J Respir Crit Care Med,1999,160(4):1269-1273.
