β-环糊精交联聚合物对两种重金属处理研究
2014-09-14刘志彬
刘 志 彬
(1. 哈尔滨商业大学 化学中心,哈尔滨 150076;2. 哈尔滨工业大学 应用化学系,哈尔滨 150076)
环糊精(Cyclodextrin, CD)是直链淀粉在芽孢杆菌产生的环糊精葡萄糖转移酶作用下生成的一系列环状低聚糖的总称,是一类来源广泛的天然化合物,具有成本低、产量大、安全环保等特点.已被广泛应用于食品、药品、化工等行业中[1-3].环糊精分子表面有丰富的伯仲羟基,易对其进行化学交联并修饰新的官能团,对环糊精的结构修饰能够提高其溶解度,并且改变其空间结构,能够产生一些和环糊精本体不同的化学性质.文献报道经修饰的环糊精在一定条件下对几种常见重金属离子的去除效果良好[4-6],使排出的工业废水重金属离子含量达到国家标准.
1 材料和方法
1.1 药品与试剂
β-环糊精(分析纯,天津市科密欧化学试剂有限公司);氢氧化钠(分析纯,天津市天新精细化工开发中心);环氧氯丙烷(分析纯,天津市博迪化工有限公司);乙酸(分析纯,南京化学试剂有限公司);丙酮(分析纯,天津市东丽区天大化工有限公司);硫酸亚铁(分析纯,天津市博迪化工有限公司);硫酸锌(分析纯,天津市巴斯夫化工有限公司);硫酸铜(分析纯,天津市双船化学试剂厂).
1.2 仪器及设备
分析天平(北京赛多利斯仪器系统有限公司),循环水式真空泵(SHZ-D)(巩义市子华仪器有限责任公司),电热恒温水槽(DK-8D)(上海一恒科学仪器有限公司),电热恒温水浴锅(DK-9K-1)(天津市泰斯特仪器有限公司),电热恒温鼓风干燥烘箱(DHG-9123A)(上海一恒科学仪器有限公司),玻璃仪器烘干器(KQ-C)(巩义市莫峪予华仪器厂),磁力搅拌器(EMS-9A)(天津市欧若仪器仪表有限公司),火焰原子吸收分光光度计(TS-990)(北京普析通用仪器有限公司),电冰箱(海尔集团).
1.3 实验方法
1.3.1β-环糊精交联聚合物的制备
称取10 g NaOH固体溶于50 mL蒸馏水中配成20%的NaOH 溶液,然后称取20 g重结晶的β-环糊精(β-CD).将β-CD不断加入到NaOH 溶液中,并用磁力搅拌器进行搅拌,搅拌1 h后,20 g的β-CD全部溶于NaOH 溶液中,此时溶液变成透明.
然后量取25 mL环氧氯丙烷,在65 ℃水浴条件下用分液漏斗逐滴加入到溶于NaOH的β-CD中,滴加时不断用玻璃棒进行搅拌,使其充分反应.滴加0.5 h后溶液变成黄色凝胶状胶体,将其搅碎,最终呈现黄白色胶块.然后加入丙酮浸泡过夜.将浸泡过夜的胶块用大量丙酮冲洗,再用自来水冲洗数次,使之为中性,最后用蒸馏水冲洗数次,反应产物用真空泵过滤抽干.
将抽滤后胶块烘干12 h,温度80 ℃.得到白色(掺有些许黄色)的固体颗粒,将其进行充分研磨,过60目筛.实验成功制得β-CD的交联聚合物产物27.60 g.
1.3.2 金属离子模拟废水水样的制备
通过公式:X=0.25g×M2÷M1
其中:X为称取金属离子化合物的质量,g;M1为金属离子的相对原子质量,g∕mol;M2为金属离子化合物的相对分子质量,g∕mol.具体数据如表1所示.
表1金属主要参数

金属离子相对原子质量对应化合物相对分子质量X/gFe2+56FeSO4·7H2O278.021.241Cu2+64CuSO4·5H2O249.690.975
将称得的金属化合物溶于蒸馏水中,搅拌使其充分溶解,然后定容到250 mL容量瓶中,配成浓度为1 g/L的Fe2+、 Cu2+模拟废水水样.
1.3.3β-环糊精交联聚合物处理Fe2+的实验
1) 不同浓度β-环糊精交联聚合物对Fe2+处理实验
取2.5 mL1 g/L的Fe2+溶液定容于250 mL容量瓶中配成10 mg/L的模拟废水水样,然后分别称取0.5、1.0、1.5、2.0、3.0、4.0 g的β-环糊精交联聚合物分别加入到六组水样中,加入蒸馏水作为空白实验组.3 h后取上清液用火焰原子吸收分光光度计测其吸光度值,见表2、3.
表2吸光度与浓度关系

质量分数/10-60.0000.5001.0002.0003.000吸光度0.0000.1080.1210.3160.434
表3吸光度与β-环糊精交联聚合物量关系

β-环糊精交联聚合物量/g0.00.51.02.03.04.0吸光度1.9801.8501.6910.0900.2550.726
2) 反应时间因素对实验的影响
取2.5 mL 1 g/L的Fe2+溶液定容于250 mL容量瓶中配成10 mg/L的模拟废水水样,然后加入2 g的β-环糊精交联聚合物,反应0.5、1.0、2.0、3.0、4.0、6.0 h后分别取上清液测定其吸光度,分别为1.797、0.247、0.150、0.090、-0.034、0.081.
1.3.4β-环糊精交联聚合物处理Cu2+的实验
1) 不同质量浓度β-环糊精交联聚合物对Cu2+处理实验
取2.5 mL 1g/L的Cu2+溶液定容于250 mL容量瓶中配成10 mg/L的模拟废水水样,然后分别称取0.5、1.0、0.5、2.0、3.0、4.0 g的β-环糊精交联聚合物分别加入到六组水样中,加入蒸馏水作为空白实验组测得吸光度值分别为0.000、0.105、0.209、0.300、0.393、0.478.2 h后取上清液用原子火焰分光光度计测其吸光度值分别为2.009、1.990、1.497 、1.490、1.768、1.892.
2) 反应温度因素对实验的影响
取2.5 mL 1g/L的 Cu2+溶液定容于250 mL容量瓶中配成10 mg/L的模拟废水水样,然后加入2 g的β-环糊精交联聚合物,反应在温度为0、20、40、60、80 ℃下反应2 h后分别取上清液测定其吸光度,数据见表4、5.
表4吸光度与温度关系

温度/℃020406080吸光度1.5801.4901.5201.6301.630
表5吸光度与β-环糊精交联聚合物量的关系
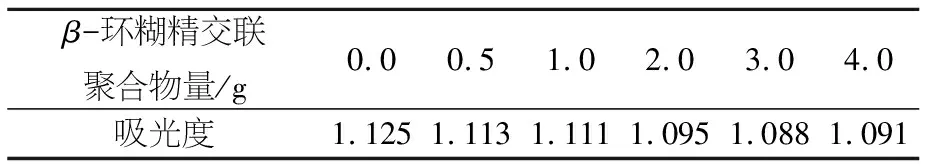
β-环糊精交联聚合物量/g0.00.51.02.03.04.0吸光度1.1251.1131.1111.0951.0881.091
2 结果与讨论
2.1 β-环糊精交联聚合物处理Fe2+的结果
2.1.1 Fe2+的标准曲线
以Fe2+的质量分数为横坐标,吸光度为纵坐标,绘制标准曲线,结果见图1.
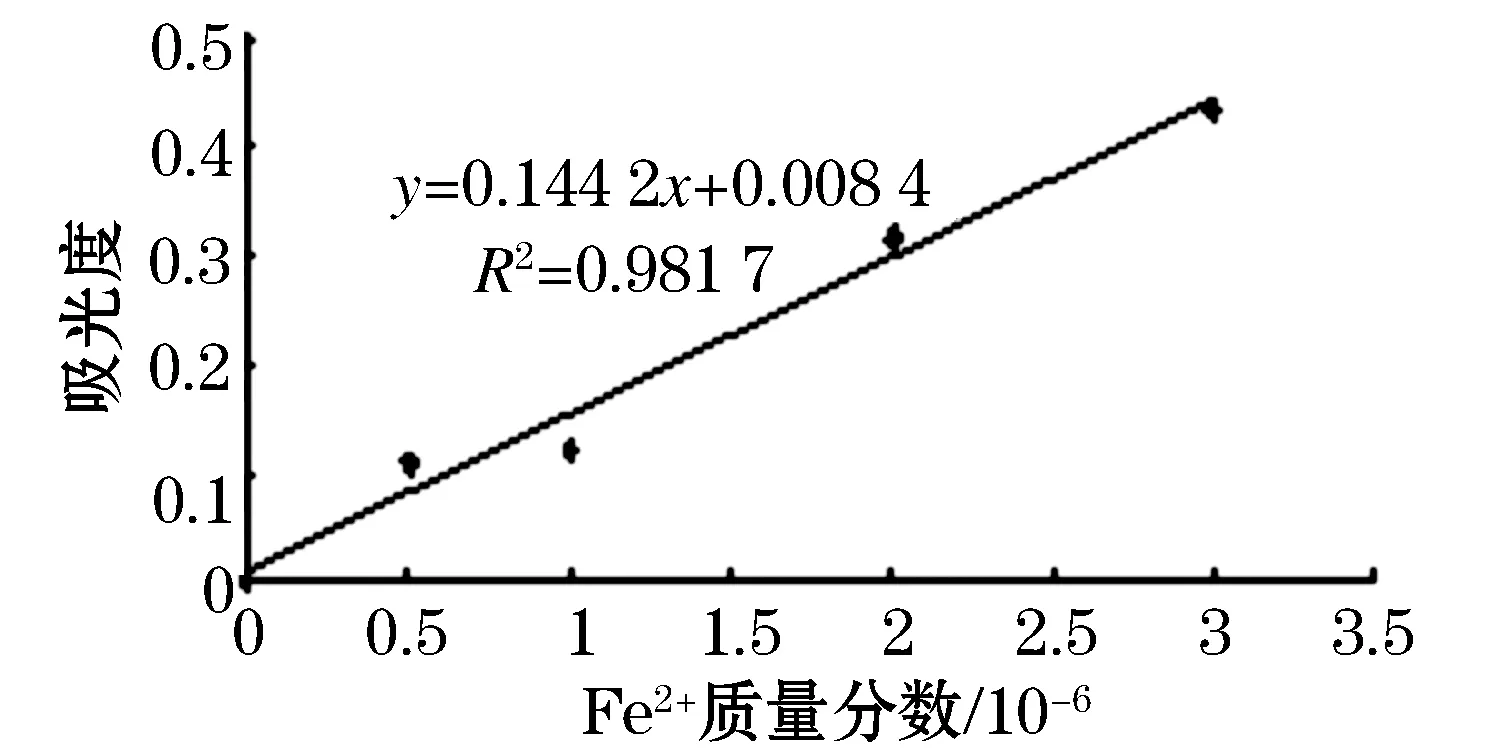
图1 Fe2+的标准曲线
2.1.2 不同质量β-环糊精交联聚合物处理Fe2+的结果
根据表4的数据,绘制随加入β-环糊精交联聚合物量变化Fe2+的处理效果,结果见图2.
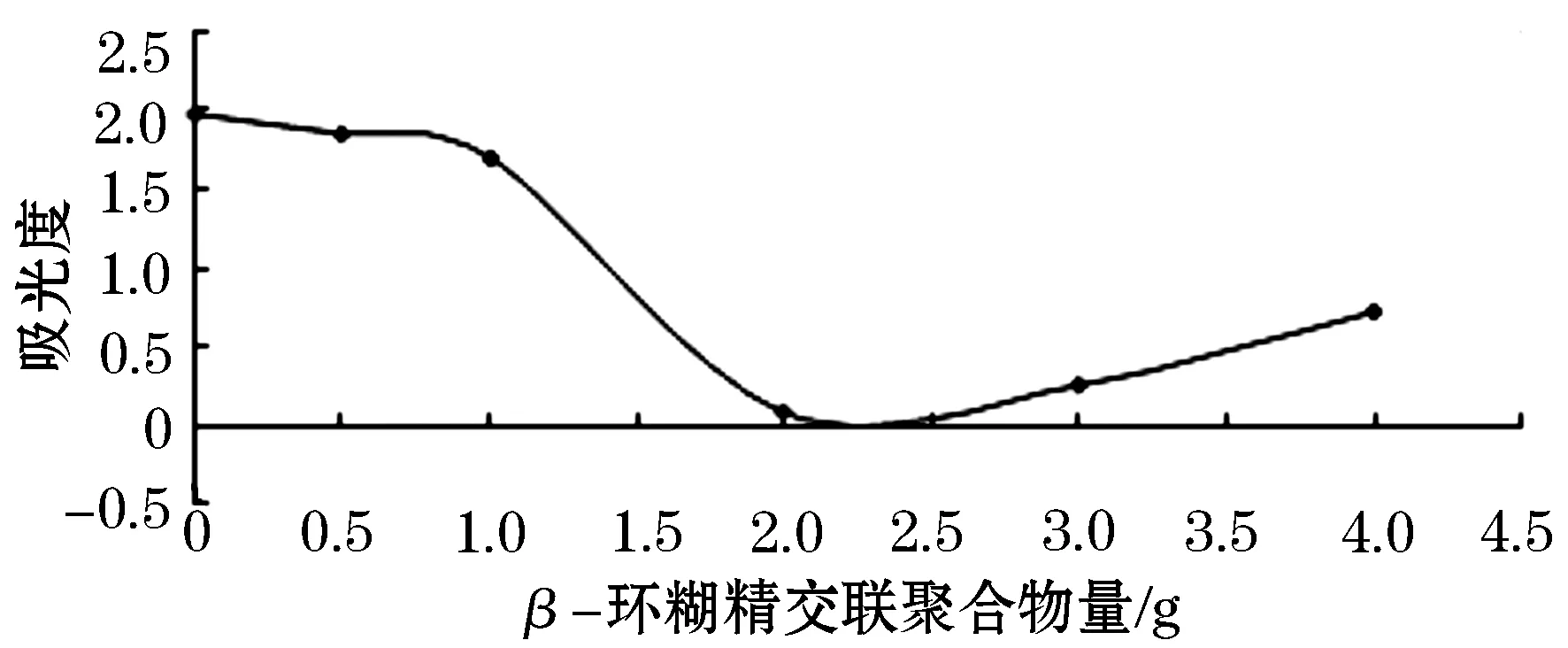
图2 β-环糊精交联聚合物量对Fe2+处理效果影响曲线
由图2可知,加入2 gβ-环糊精交联聚合物Fe2+的去除率为95.8%,加入3 gβ-环糊精交联聚合物Fe2+的去除率为87.5%,加入4 gβ-环糊精交联聚合物Fe(Ⅱ)的去除率为95.8%.综合经济因素考虑,加入2 g是最佳加入量.
2.1.3 反应时间因素对实验结果影响
根据Fe2+的标准曲线方程,计算得出不同时间下β-环糊精交联聚合物对Fe2+的去除率,结果见图4.

图3 Fe2+质量分数变化曲线
由图3可知反应时间在3~5 h时间段Fe2+得去除效果最好,可以达到95%以上.所以反应时间选择4 h最佳.
2.2 β-环糊精交联聚合物处理Cu2+的结果
2.2.1 Cu2+的标准曲线
以Cu2+的质量分数/10-6为纵坐标,吸光度为横坐标,绘制标准曲线,结果见图4.

图4 Cu2+的标准曲线
2.2.2 不同质量β-环糊精交联聚合物处理Cu2+的结果
根据数据,绘制随加入β-环糊精交联聚合物量/g变化Cu2+的处理效果,结果见图5.

图5 β-环糊精交联聚合物量对Cu2+处理效果影响曲线
由图5可知,β-环糊精交联聚合物对于Cu2+的去除效果一般,加入1 gβ-环糊精交联聚合物Cu2+的去除率为25.6%,加入2 gβ-环糊精交联聚合物Cu2+的去除率为25.9%,而且再随着β-环糊精交联聚合物加入量继续增多,Cu2+的去除效果反而下降,说明本实验β-环糊精交联聚合物对于Cu2+的去除率最好,为25.9%.
2.2.3 反应温度因素对实验结果影响
根据Cu2+的标准曲线方程,计算得出不同温度下β-环糊精交联聚合物对Cu2+的去除率,结果见图6.

图6 Cu2+质量分数变化曲线
由图6可知,相对而言,在20~30 ℃范围内Cu2+的去除率较好,随着温度的上升,Cu2+的质量分数明显的上升,说明高温条件不适宜对Cu2+的去除作用.
3 讨论与结论
环糊精外侧有大量的羟基,对高价金属离子具有螯合作用,经过改性后形成的交联聚合物引入了大量的C-O-C醚键,醚键中的O原子具有孤对电子,易与金属离子形成配位键,可以与无机离子形成包合物.研究表明环糊精交联聚合物与重金属离子的络合是一个极其复杂的过程,其络合物形成的稳定性受到众多因素的影响,如中心离子的电荷、半径和电子构型等.
本文在试验中研究制取了以β-环糊精和环氧氯丙烷为原料的β-环糊精的衍生物——β-环糊精交联聚合物,并用此衍生物处理了含Fe2+、Cu2+两种金属离子的模拟废水,并分析了反应物质量分数、反应时间、pH值对去除效果的影响,研究结果表明:
1)β-环糊精交联聚合物对Fe2+的去除率可达到95.8%,去除效果良好,反应最佳时间为4 h.
2)β-环糊精交联聚合物对Cu2+的去除率为25.9%,去除效果较好.
此实验方法操作简单、造价低,对Fe2+的去除作用效果良好,这为减少废水中重金属离子的污染、高浓度金属离子生活饮用水的处理和生活生产废水的处理提供了一种新思路,具有一定的研究价值和应用前景.
参考文献:
[1] 童林荟.环糊精化学—基础与应用[M]. 北京:科学出版社,2001.
[2] 金征宇,徐学明,陈寒青.环糊精化学—制备与应用[M]. 北京:化学工业出版社,2009.
[3] 何仲贵.环糊精包合物技术[M]. 北京:人民卫生出版社,2008.
[4] CHATAIN V, HANNA K, DE BRAUER C,etal. Enhance solubilization of arsenic and 2,3,4,6 tetrachlorophenol from soils by a cyclodextrin derivatrive [J].Chemosphere, 2004, 57(3): 197-206.
[5] BADR T, HANNA K, DE BRAUER C. Enhance solubilization and removal of naphthalene and phenanthrene by cyclodextrins from two contaminated soils [J].Journal of Hazardous Materials, 2004, 112(3): 215-223.
[6] SKOLD M E, THYNE G D, DREXLER J W,etal. Enhanced Solubilization of a Metal—Organic Contaminant Mixture (Pb,Sr,Zn,and Perchloroethylene) by Cyclodextrin [J].Environmental Science Technology, 2008, 42(23): 8930-8934.
