胸外科围术期并发感染的病原菌分布特征及耐药性分析
2014-09-12王光锁吴劲松饶展鹏林少霖
王光锁 吴劲松 杨 林 王 健 饶展鹏 林少霖 王 正
(暨南大学第二临床医学院 深圳市人民医院胸外科,广东 深圳 518020)
普胸外科患者围术期多种因素如术中气道分泌物增多、单肺通气导致肺泡萎陷、肺不张;术前微生物定植;合并重要器官基础疾病如糖尿病、慢性阻塞性肺病等;有吸烟史等,极易并发围术期感染,导致患者住院时间延长、住院费用增加,甚至病死率的增加〔1~4〕。本文通过回顾分析胸外科确诊围术期感染患者的病原学特征,为指导围术期合理有效使用抗生素进行感染预防和治疗提供病原学依据。
1 资料和方法
1.1临床资料 选择2002 年1月至2012年6月深圳市人民医院胸外科确诊围术期感染307例患者,男198例,女109例,年龄19~88〔平均(66.5±20.9)〕岁,按照常规方法留取各种标本(痰液、血液、胸水、伤口分泌物、术中标本分泌物等)并送检。其中肺外科165例,食管68例,胸壁及胸腔51例,胸部创伤18例,纵隔5例。除外结核和非结核分枝杆菌,累计425株病原微生物。同一患者同一部位连续检出同一细菌以一株计算。合格痰液标本要求:痰液直接涂片光镜下检查,每低倍镜视野鳞状上皮细胞<10个,白细胞>25个;或鳞状上皮细胞∶白细胞<1∶2.5。
1.2方法 所有送检的标本均按照标准化操作程序进行培养,细菌菌种鉴定采用Vitek-two(法国bioMe′rieux公司)微生物鉴定分析系统进行,药敏试验采用K-B法,药敏质控菌株为大肠埃希菌ATCC25922、铜绿假单胞菌ATCC27853、金黄色葡萄球菌ATCC29213,药敏试验结果的解释参照CLSI 2012抗菌药物体外敏感性试验标准;厌氧菌的鉴定采用API 20A试剂条(法国bioMe′rieux公司),念珠菌的鉴定采用API 20C(法国bioMe′rieux公司)。统计各类标本中病原菌的分离情况,并分析其对抗菌药物的体外敏感性。
1.3统计学分析 采用WHONET5.4 软件进行处理。
2 结 果
2.1病原菌分布 307例患者共分离到病原菌425 株,其中呼吸道标本最多,检出率占44.5%(189/425),其次是胸水标本,检出率占29.9%(127/425),血液标本9.7%(41/425),分泌物标本40%(40/425),其中包括术中分泌物标本22例,检出率占5.2%(22/425)。425 株病原菌中,革兰阴性杆菌249株(58.6%),革兰阳性球菌130株(30.6%),真菌46株(10.8%)。最常见病原菌依次为鲍曼不动杆菌55株(13.0%)、铜绿假单胞菌41株(9.6%)、肺炎克雷伯菌34株(8.0%)、白色念珠菌33株(7.8%)、表皮葡萄球菌32株(7.5%)、金黄色葡萄球菌28株(6.6%),其余为大肠杆菌21株(4.9%),溶血性葡萄球菌20株(4.7%),嗜麦芽窄食单孢菌17株(4.0%),阴沟肠杆菌16株(4.2%),粪肠球菌14株(3.7%),非白色念珠菌属13株(3.1%),屎肠球菌8株(1.9%),人葡萄球菌6株(1.4%),缓症链球菌6株(1.4%),鹑鸡肠球菌5株(1.2%),流感嗜血菌5株(1.2%),草绿色链球菌5株(1.2%),瓦氏葡萄球菌4株(0.9%),星座链球菌4株(0.9%),洋葱伯霍尔德杆菌3株(0.7%),粘质沙雷菌3株(0.7%),其他52株(12.2%)。
其中呼吸道标本中革兰阴性杆菌128株,占67.7%(128/189),以非发酵菌(38.7%)和肠杆菌属(19.0%)为主,鲍曼不动杆菌40株(21.2%),铜绿假单孢菌24株(12.7%),肺炎克雷伯菌24株(12.7%),大肠杆菌20株(6.3%),嗜麦芽窄食单孢菌9株(4.8%),其他11株(5.8%);革兰阳性球菌38株,占20.1%(38/189),金黄色葡萄球菌12株(6.3%),溶血性葡萄球菌6株(3.2%),表皮葡萄球菌4株(2.1%),其他16株(8.5%);真菌23株,占12.2%(23/189),以白色念珠菌为主,占10.6%(20/189),其他3株(1.6%)。
胸水标本最常见病原菌依次为鲍曼不动杆菌12.6%(16/127)、表皮葡萄球菌11.0%(14/127)、铜绿假单胞菌10.2%(10/127)、粪肠球菌7.1%(9/127)、溶血性葡萄球菌5.5%(7/127)、金黄色葡萄球菌4.7%(6/127)等。嗜麦芽窄食单孢菌6株(4.7%),缓症链球菌6株(4.7%),白色念珠菌5株(3.9%),阴沟肠杆菌5株(3.9%),肺炎克雷伯菌5株(3.9%),大肠杆菌2株(1.6%),热带念珠菌2株(1.6%),其他34株(26.8%)。
2.2主要细菌病原体的体外药物敏感性 根据药敏监测结果,非发酵菌(包括鲍曼不动杆菌、铜绿假单胞菌等)对头孢克洛耐药(100%),而克雷伯菌、大肠埃希菌对头孢西丁尚具有较低的耐药率,头孢克洛对克雷伯菌、大肠埃希菌的耐药率较高。 头孢曲松对革兰阴性杆菌均具有较高的耐药率。常见革兰阴性杆菌对β-内酰胺酶抑制剂复合制剂如头孢哌酮/舒巴坦耐药率总体较低。见表1。
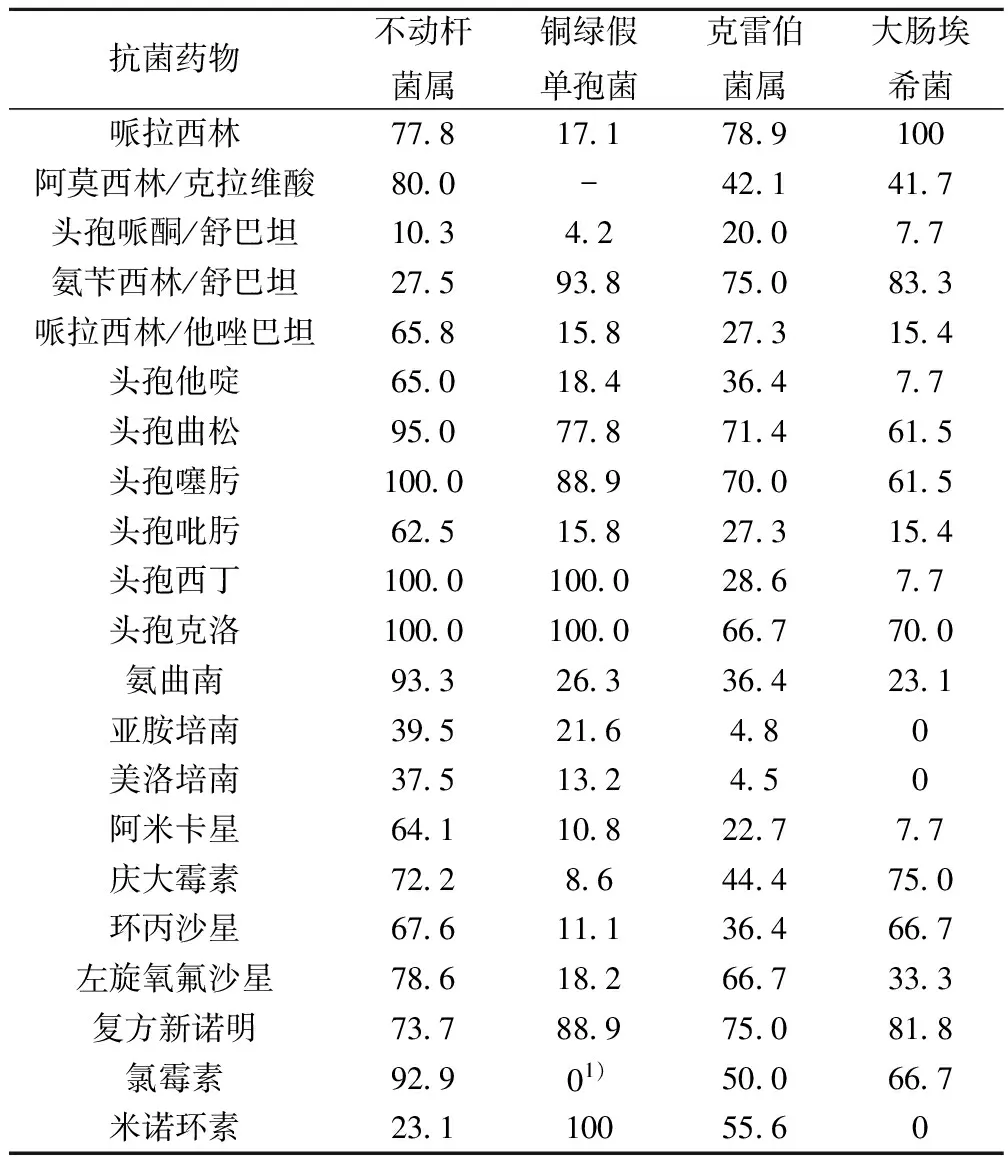
表1 革兰阴性杆菌对抗菌药物的耐药率(%)
1)多粘菌素B
3 讨 论
普胸外科主要包含肺外科、食管外科和纵隔、胸壁外科,前两者为清洁-污染伤口。围术期使用抗生素的目的,除治疗已经存在的感染,如肺脓肿、支气管扩张、肺真菌病等,更多的是预防手术部位感染,包括手术切口感染、手术部位的深部腔隙或器官感染。Classen等〔5〕早在1992年确认了术前预防性使用抗生素降低伤口感染发生率的确切价值。《卫生部关于抗菌药物临床应用管理有关问题》也指出胸外科手术(食管、肺)围手术应用抗生素建议使用第一、二代头孢菌素,如头孢曲松。然而,上述建议方案是否足够预防胸外科围术期感染的发生,特别是围术期发生感染高危人群的胸腔或肺部感染尚无定论〔6〕。
本文在长期的临床实践中,把胸外科围术期患者抗生素使用细分为四类,①限制使用,如简单胸壁肿瘤、纵隔肿瘤切除、手汗症交感神经切除等;②预防性使用,大部分常规肺部、胸壁、纵隔及胸腔手术均属于此类;③目标性治疗,有明确的感染及微生物学证据的患者;④初始经验治疗,分为两种情况:第1种,感染的早期进行治疗性的经验用药,这与非外科相关性感染的初始经验治疗原则一致;第2种,称为围术期感染高危人群的预防性经验用药,换句话说,如果围术期未能给予充分有效的覆盖可能的致病菌的抗感染药物,感染的概率将会大幅度增加。问题的核心在于,如何识别这部分围手术期胸腔和肺部感染的高危人群。通常在这种情况下,需要针对胸外科围术期感染高危因素、结合胸外科围术期感染病原学特征给予充分覆盖。这些高危因素包括:①肺癌、食管癌患者,高龄,合并内科疾病如糖尿病,慢性阻塞性肺病等居多,免疫功能低,多有吸烟史;②食管癌、慢性阻塞性肺病患者营养状态差;③支气管扩张、慢性肺结核空洞、毁损肺、曲霉菌空洞等多以混合感染的形式存在;④麻醉过程反复插管、胸外科手术时间长,肺水肿、肺不张可能性大等。
如何选择恰当的抗生素覆盖可能的致病菌是另一个核心问题。本研究发现,胸外科围术期感染425 株病原菌中,革兰氏阴性杆菌感染比率最高,其次为革兰阳性球菌和真菌,与以往文献报道基本一致〔3,4,6〕。这些革兰阴性杆菌通常与院内获得性肺炎致病菌谱一致,其主要原因可能与咽喉部和气管支气管树的定植菌密切相关,且这些病原菌通常对一、二代头孢耐药〔6,7〕。从标本来源看,以呼吸道和胸水标本为主,伤口分泌物和血液标本较少,提示肺部感染和胸腔感染依然是围术期预防和治疗的主要感染并发症。肺部感染病原菌以非发酵菌和肠杆菌属为主,胸腔感染则要同时考虑非发酵菌和革兰阳性球菌〔3,4,6〕。从本组主要细菌病原体的体外药物敏感性来看,常见革兰阴性杆菌对二代头孢、三代头孢中的头孢曲松、头孢噻肟耐药率较高。一方面,提示临床上在标本送检后尚未获得病原学诊断依据时的经验性治疗中,应考虑使用对革兰阴性杆菌作用强的抗菌药物,且抗菌谱能够覆盖非发酵菌属和肠杆菌属〔4〕。另一方面,特别突出强调的是,在胸外科(食管、肺外科)围术期感染高危人群的预防性经验性用药过程中,现有针对伤口感染的抗菌药物无法覆盖上述细菌,对胸腔和肺部感染的预防和治疗存在用药不足的问题〔6〕。
鉴于念珠菌属常常在上呼吸道定植,痰液标本经常受上呼吸道分泌物污染,在用药之前需要区分定植和感染。另外,非呼吸道标本如血液、胸水更多可见非白色念珠菌感染,因此也需要经验性或根据药敏试验调整抗真菌药物。
本研究中革兰阳性球菌主要是金黄色葡萄球菌、凝固酶阴性葡萄球菌和肠球菌属。金黄色葡萄球菌对苯唑西林的耐药率高,而对替考拉宁、万古霉素、利奈唑胺、米诺环素敏感率极高。重症患者对耐苯唑西林的葡萄球菌引起的感染应首选糖肽类抗菌药物,同时也应避免滥用,需要进行保护性使用〔4〕。米诺环素尽管体外敏感性高,体内疗效多偏差。
本研究的缺陷:①研究纳入10年跨度单中心单一外科微生物学数据,总体分离菌株数量不多,如要评估耐药的纵向变迁,分阶段菌株更少,代表意义不大。②如果能够对纳入研究的胸外科患者进一步细分,可能对临床的指导价值针对性更强。③本研究仅涉及病原学数据,未进一步结合临床数据进行分析。亟需通过前瞻性多中心的临床试验监测胸外科围术期病原菌的分布、耐药性的变化以及评估新的、更加合理、有效、经济、适当的预防方案,避免用药过度以及用药不足产生的问题〔8,9〕。
4 参考文献
1黎沾良,崔德健.重视外科病人围手术期呼吸道并发症的防治〔J〕.中国实用外科杂志,2004;24(3):134-5.
2雷国荣,谭黎杰.80例胸外科术后患者医院感染原因分析与预防〔J〕.中华医院感染学杂志,2012;22(11):2315-6.
3何 超,郭培玲,康 梅,等.肺癌术后患者并发感染的病原菌特征分析〔J〕.中国胸心血管外科临床杂志,2012;19(2):145-7.
4王春梅,支修益,白书媛,等.开胸手术后下呼吸道感染病原菌及其耐药分析〔J〕.中国胸心血管外科临床杂志,2011;18(2):126-9.
5Classen DC,Evans RS,Pestotnik SL,etal.The timing of prophylactic administration of antibiotics and the risk of surgical-wound infection〔J〕.N Engl J Med,1992;326(5):281-6.
6Radu DM,Jauréguy F,Seguin A,etal.Postoperative pneumonia after major pulmonary resections:an unsolved problem in thoracic surgery〔J〕.Ann Thorac Surg,2007;84(5):1669-73.
7Mizgerd JP.Acute lower respiratory tract infection〔J〕.N Engl J Med,2008;358(7):716-27.
8Edwards FH,Engelman RM,Houck P,etal.The society of thoracic surgeons practice guideline series:antibiotic prophylaxis in cardiac surgery,part I:duration〔J〕.Ann Thorac Surg,2006;81(1):397-404.
9黄阿莉,刘娇娇.老年患者下呼吸道感染主要病原菌分布及耐药性分析〔J〕.中国老年学杂志,2011;31(22):4463-4.
