导电聚苯胺纳米纤维的快速制备及其导电性研究
2014-08-28柯志坚潘泽森吉学盛毛兴宇
柯志坚,潘泽森 ,吉学盛,毛兴宇
(集美大学理学院,福建 厦门 361021)
导电聚苯胺纳米纤维的快速制备及其导电性研究
柯志坚,潘泽森 ,吉学盛,毛兴宇
(集美大学理学院,福建 厦门 361021)
以盐酸为掺杂剂,在苯胺单体氧化合成导电聚苯胺的聚合反应过程中,通过加入N-苯基对苯二胺,可以显著加快聚苯胺的合成反应速度,并提高聚苯胺的产率.经电子显微镜观察发现,生成的聚苯胺呈现出明显的纳米纤维形貌特征,直径约50 nm,长度可达微米.实验表明:聚苯胺的产率和电导率都是随着HCl浓度的增加呈先增大后减小的趋势,浓度1 mol/L的盐酸掺杂下合成的聚苯胺的电导率最大;在苯胺和酸浓度固定时,改变氧化剂过硫酸铵的量也会影响聚苯胺纳米纤维的产率和电导率,n(苯胺)∶n(过硫酸铵)=1∶1时,生成物聚苯胺的电导率最大.
导电聚苯胺;纳米纤维;合成方法;电导率
0 引言
有机聚合物过去一直被当作绝缘体,直到20世纪70年代末,MacDiarmid、Shirakawa和Heeger等人首次发现经过卤素掺杂后的聚乙炔,其导电率增加了十个数量级以上,接近于金属导体.这引发了对高分子聚合物的导电性的大量研究[1],并逐步地把注意力从聚乙炔转移到化学稳定性较好的聚吡咯、聚噻吩、聚苯胺等共轭聚合物上.相对于其他共轭高分子而言,聚苯胺原料易得、合成方法简单、具有较高的导电性和良好的环境友好性,聚苯胺一直是导电高分子研究的热点和最受关注的导电聚合物之一[2-3].
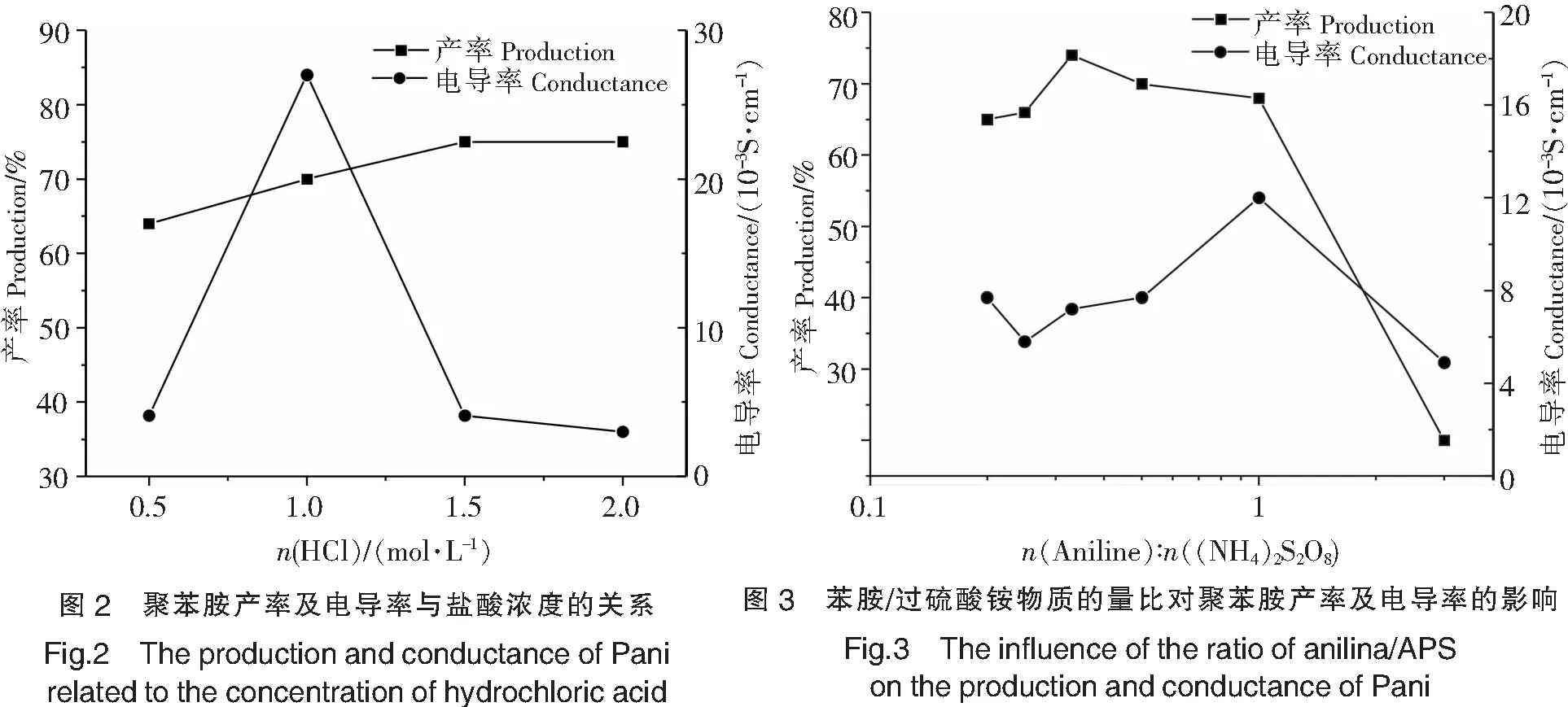
聚苯胺的导电性取决于它的氧化还原状态,作为一种共轭结构的高分子材料,聚苯胺具有苯式(还原单元)-醌式(氧化单元)结构共存的特点[1].随着两种结构单元的含量不同,聚苯胺处于不同程度的氧化还原状态,并且可以相互转化,它的氧化还原状态也决定了它的电导性.y=1时的完全还原态和y=0时的完全氧化态都是不导电的绝缘体,通过质子酸掺杂,使其处于0 化学氧化合成是制备聚苯胺的主要方法[4-5],通过在酸性溶液中加入氧化剂(催化剂)使苯胺单体氧化得以聚合.由此合成的聚苯胺性质主要受反应介质酸的种类及浓度、氧化剂的种类及浓度、单体浓度和反应温度、反应时间等因素的影响.然而这种直接从苯胺单体聚合的方法时间长,产率低,而且由此制备的聚苯胺呈粉体,要想获得有一定纳米结构的聚苯胺,如纳米纤维,还要辅助以种子聚合法或软硬模板法[6-8].本文采用化学氧化聚合方式,通过在聚合反应中引入低聚物N-苯基对苯二胺,提高聚苯胺的产率和降低聚合反应时间,快速合成出具有纳米纤维结构的导电聚苯胺纤维,并分析在不同的掺杂剂浓度以及不同的氧化剂比例情况下合成的聚苯胺的产率及电导率. 1.1 主要药品与仪器 苯胺单体、过硫酸铵((NH4)2S2O8)、甲醇、N-苯基对苯二胺、盐酸(HCl)等均为分析纯. DKS-24电热恒温水浴加热器(杭州蓝天化验仪器厂)用于控制反应温度,RTS-8型四探针电阻测试仪(广州矽美科技有限公司)测量电阻率, JEM-1200透射电镜(JEOL),S-3400N扫描电镜(日立)对样品进行形貌观察. 1.2 聚苯胺的合成与电导率的测量 分别配制苯胺单体的盐酸溶液和氧化剂过硫酸铵的盐酸溶液,另将25 mg的N-苯基对苯二胺用微量(0.5 mL)的甲醇溶解后,加入到苯胺单体的盐酸溶液里,最后将氧化剂过硫酸铵的盐酸溶液缓慢滴入并搅拌,即刻可以看到墨绿色聚苯胺的生成,说明氧化聚合反应在快速进行.反应结束后经过滤、水洗、干燥之后就能得到所需的聚苯胺产物.作为对照,直接用苯胺单体氧化聚合制备聚苯胺,方法与上述相同,只是反应物中不加入N-苯基对苯二胺.两种方式所得的聚苯胺都通过RTS-8型四探针电阻测试仪来测量其电导率大小. 对于利用低聚物N-苯基对苯二胺快速制备的聚苯胺,其电导率依赖于聚合反应条件.掺杂剂的浓度是聚合聚苯胺的重要参数,分别使用0.5 mol/L、1 mol/L、1.5 mol/L和2 mol/L不同浓度的盐酸作为掺杂剂,制备了一系列的导电聚苯胺纳米纤维,测量并分析了它们的产率及导电性.反应过程中氧化剂的比例是另一个影响聚苯胺性质的参数,按照n(苯胺)∶n(过硫酸铵)分别为3∶1,1∶1,1∶2,1∶3,1∶4和1∶5,制备一系列导电聚苯胺纳米纤维,测量并分析了它们的产率及导电性. 在有N-苯基对苯二胺参与的聚合反应中,可以观察到合成聚苯胺更快,而且12 h后反应就基本完成,产率达到了70%以上.而在没有N-苯基对苯二胺的对照组中,聚合反应就慢很多,12 h后的产率不到40%.它们的电导率也有所不同,实验结果见表1. 表1 聚合反应时有低聚物和无低聚物聚苯胺的产率及其电导率 通过对N-苯基对苯二胺的分子结构的分析可以看出,该分子结构跟聚苯胺的结构类似,也是属于1,4偶联[1],本身就是聚苯胺长链分子的一部分,因此N-苯基对苯二胺也可看成合成聚苯胺的反应物之一.所以,N-苯基对苯二胺可以有效地引发聚苯胺的聚合[3],并显著地提高了聚合反应速率,而且从实验数据中也看到它能提高聚苯胺的合成率. 利用扫描电镜和透射电镜(80 kV)对制备的聚苯胺进行了形貌观察,如图1所示.对照组中生成的聚苯胺的形貌不是规则的(图1a),而通过低聚物N-苯基对苯二胺生成的聚苯胺呈现明显的纤维状,长度可达1微米,纤维直径约为50 nm(图1b,图1c).这一纳米纤维形貌的形成无需经过种子聚合或模板聚合,这对获得纳米纤维结构是很有意义的.有研究者在通过界面反应制备聚苯胺纳米纤维时,曾注意到,在直接用苯胺氧化来聚合苯胺时,反应最初期有纳米纤维状的聚苯胺产生,只是随着反应的继续进行,大量的二次横向生长使最终的聚苯胺呈无定形的颗粒[9].在本实验里,低聚物N-苯基对苯二胺的存在起到了抑制聚合反应中的二次生长,而生成纵向的纳米纤维. 实验中也注意到,N-苯基对苯二胺的用量只要很少一点,聚合的速率就明显加快,并生成墨绿色的聚苯胺纳米纤维.当选用不同浓度的掺杂剂(盐酸),都可以利用N-苯基对苯二胺快速合成聚苯胺纳米纤维,其形貌没有观察到明显变化. 实验观察到掺杂剂(盐酸)的浓度对聚苯胺的产率有细微的影响,而对电导率的影响是明显的,如图2所示.在盐酸浓度很低时,聚苯胺的产率不高,并随盐酸浓度的增加而缓慢增加.低浓度掺杂制得的聚苯胺的导电率也很低,随着盐酸浓度的升高,聚合物的电导率随之升高,但继续提高酸浓度(当酸浓度超过临界点——本实验中约为1 mol/L),其电导率不再增加,而是减小.这一现象可以解释为,质子酸在反应中起到两个作用:一是以掺杂剂的形式进入聚苯胺的骨架,二是提供反应需要的酸性环境.当酸的浓度较低时,酸性较弱,苯胺聚合效率低,进入主链的质子也少,相应聚合物的导电能力较低.而当酸的浓度过高时,会使主链上质子和阴离子的最佳比例偏离,而且酸性过强时会造成苯胺局部的深度氧化,破坏其共轭结构,也会导致产物的导电能力下降. 图3反映的是在其他反应物及反应条件固定的情况下,氧化剂过硫酸铵的用量对聚苯胺的产率及电导性的影响.产率最初随苯胺与过硫酸铵的比例的增加而增加,当苯胺与过硫酸铵的物质的量比为1∶3时,聚苯胺产率可达74.6%.之后,再增加过硫酸铵用量时,聚苯胺产率反而下降.聚苯胺的电导率也是随着过硫酸铵用量而变化的,当苯胺与过硫酸铵的物质的量比为1∶1时,电导率最大,而当苯胺与过硫酸铵物质的量之比大于或小于1∶1时,产物的电导率都将下降.这种现象可以解释为,过硫酸铵用量过低时,在反应液中的浓度会快速下降,氧化不足,聚合反应变慢,产率下降,电导率将维持在某一水平.过硫酸铵浓度过大时,反应在溶液中各处同时快速进行,出现大量的饱和氧化态,聚苯胺的活性被降低,不利于进一步聚合.同时,过剩的氧化剂会使生成的聚苯胺被过度氧化,醌式结构远远多于苯式结构,从而导致产物的电导率下降,这点与其他一些观察者的实验结果[10]相一致. 化学氧化聚合生成聚苯胺的反应过程中,加入N-苯基对苯二胺将加快反应速度,也能提高聚苯胺的产率及其电导率.N-苯基对苯二胺的存在有助于生成具有纳米纤维形貌特征的聚苯胺,长度可达微米以上,直径在50 nm左右.掺杂剂HCl浓度会明显影响聚苯胺的电导率,实验结果表明,1 mol/L的盐酸掺杂下合成的聚苯胺的电导率最大,盐酸浓度过低,掺杂量不够,浓度过高,会使长链分子局部过度氧化,破坏共轭结构.聚苯胺的导电性取决于长链分子中苯式结构与醌式结构的比例,氧化剂过硫酸铵相对于苯胺的量也会影响聚苯胺纳米纤维的产率和电导率.根据实验结果,n(苯胺)∶n(过硫酸铵)=1∶1时,产物聚苯胺的电导率最大. [1]MACDIARMID A G,CHIANG J C,RICHTER A F,et a1.Polyaniline:a new concept in conducting polymers[J].Synth Met,1987,18(1/3):285-290. [2]景遐斌,王利祥,王献红,等.导电聚苯胺的合成、结构、性能和应用[J].高分子学报,2005,10(5):655-663.[3]徐浩,延卫,冯江涛.聚苯胺的合成与聚合机理研究进展[J].化工进展,2008,27(10):1561-1568. [4]曹丰,李东旭,管自生.导电高分子聚苯胺研究进展 [J].材料导报,2007,21(8):48-51. [5]GENIE E M,PENNEAU J F,LAPKOWSKI M,et al.Electropolymerisation reaction mechanism of para-aminodiphenylamine [J].Journal of Electroanalytical Chemistry and Interfacial Electrochemistry,1989,269(1):63-75. [6]WEI Z X,ZHANG Z M,WAN M X.Formation mechanism of self-assembled polyaniline micro/nanotubes [J].Langmuir,2002,18(3):917-921. [7]ZHANG X Y,GOUX W J ,MANOHAR S K.Synthesis of polyaniline nanofibers by“nanofiber seeding”[J].J Am Chem Soc,2004,126(14):4502- 4503. [8]张艳,孙培培,蒋晓青.纳米结构聚苯胺的合成及性质[J].南京师范大学学报:工程技术版,2009,9(2):41- 47.[9]HUANG J X,KANER R B.A general chemical route to polyaniline nanofibers[J].J Am Chem Soc,2004,126(3):851-855. [10]任斌,余成.导电聚苯胺的合成及其性能研究[J].光谱实验室,2005,22(1):148-151. (责任编辑 马建华 英文审校 黄振坤) The Fast Synthesis of Polyaniline Nanofiber and the Research on Its Conductivity KE Zhi-jian,PAN Ze-sen,JI Xue-sheng,MAO Xing-yu (School of Science,Jimei University,Xiamen 361021,China) With the hydrochloric acid as the doping agent,the synthesis process of polyaniline(Pani) can be remarkably accelerated and the yield of Pani can be increased by introducing N-phenyl para-phenylene diamine into the polymerizaiton.Electron scanning microscopy reveals the Pani appears as nanofibers,with a length of 1 μm and a diameter of 50 nm.The experiment also shows the conductivity of the Pani rises first and then drops with the increase of HCl concentration,and reaches its top when concentration of HCl is 1 mol/L.The experiment shows that the amount of the oxidant also affects conductivity of Pani,when the molar ratio of aniline and the oxidant reach 1∶1,the product exhibits the best conductivity. polyaniline;nano-fiber;synthesis method;conductivity 2013-06-19 2013-12-05 福建省自然科学基金资助项目(2011J01014) 柯志坚(1968—),男,讲师,从事材料物理研究. 1007-7405(2014)02-0148-04 O 631.2+3 A1 实验过程
2 实验结果与讨论


3 结论
