盐酸头孢吡肟在小鼠肺内的药代动力学研究
2014-08-20侯文洁李梓源丁红梓周秋云南京市胸科医院药学部南京009南京医科大学药学院南京66
侯文洁,张 亮,李梓源,丁红梓,周秋云*(.南京市胸科医院药学部,南京 009;.南京医科大学药学院,南京 66)
头孢吡肟 (cefepime) 为第四代广谱头孢菌素,具有较强的抗革兰阳性菌和革兰阴性菌作用[1-2]。目前,头孢吡肟在敏感菌所致的下呼吸道感染治疗中应用广泛[3-4]。因此,探索头孢吡肟在肺组织中的药动学特性,对指导临床合理使用有一定的意义。本实验结合已有的文献报道,摸索并建立了简单的方法来测定头孢吡肟在肺组织中的浓度。研究小鼠进行单次尾静脉注射后肺内头孢吡肟的药动学特性,为临床上其治疗下呼吸道感染提供实验基础,为进一步开展头孢吡肟的药动学和生物利用度研究提供依据。
1 仪器与材料
1.1仪器 岛津 LC-20AB高效液相色谱仪(检测器为SPD-M20A,日本岛津公司);组织匀浆机(Bioprap-24.杭州奥盛);高速离心机(TG1650-ws,上海卢湘仪);全自动涡旋仪(MX-S,大龙兴利)。
1.2试药 头孢吡肟对照品(中国药品生物制品检定所,批号:130524-200502,质量分数大于83.0%);茶碱对照品 (中国药品生物制品检定所,批号:100121-201104,质量分数大于98.0% );盐酸头孢吡肟(中美上海施贵宝制药有限公司,批号:3H00316,规格:1.0 g);甲醇、乙腈、三氯乙酸(色谱纯,美国TEDIA公司);其他试剂为分析纯(南京化学试剂有限公司)。
1.3动物 ICR小鼠,18~22 g(SPF级,雌雄各半,动物生产许可证号:SCXK(沪)2008-0016,上海西普尔-必凯实验动物有限公司)。
2 方法与结果
2.1色谱条件 色谱柱:Waters Xselect-HSS T3(250 mm×4.6 mm,5 μm);流动相:乙腈-20 mmol·L-1醋酸铵溶液(冰醋酸调pH至5)=9∶11;流速:1 mL·min-1;柱温:40 ℃;检测波长:254 nm;进样量:20 μL。
2.2溶液的配制
2.2.1对照品溶液的配制 精密称取头孢吡肟对照品,置于10 mL量瓶中,用超纯水溶解定容后配成1.0 mg·mL-1的对照品储备液,4 ℃冰箱保存备用。
2.2.2内标溶液的配制 精密称取茶碱对照品,用甲醇溶解后稀释成0.1 mg·mL-1的溶液,备用。
2.3给药方案与样品采集 ICR小鼠,78只,随机分为13 组,每组禁食 12 h后,静脉注射给药1 000 mg·kg-1。分别于给药后 0.08,0.16,0.30,0.45,0.60,0.85,1.17,1.5,2,3,4,6和8 h取肺组织,-20 ℃冰箱保存。
2.4样品处理 取空白小鼠肺脏,吸水纸吸干后用剪刀剪碎,分析天平称质量,加3倍量的生理盐水并用匀浆器制成均质的肺组织匀浆液。取300 μL加入1.5 mL离心管中,再加入质量浓度为0.1 mg·mL-1的内标茶碱溶液20 μL,加入0.1 mg·mL-1的三氯乙酸溶液150 μL,涡旋2 min,以16 000 r · min-1离心5 min,取上清液经0.45 μm滤膜过滤。
2.5方法学考察
2.5.1方法专属性 取6只ICR小鼠( 雌雄各半) 的空白肺组织匀浆液各2份,每份300 μL,1份置于2.5 mL离心管中,不加内标,按2.4项下方法操作,进样20 μL获得空白色谱图(图1A);另1份空白肺组织中加入一定质量浓度的头孢吡肟标准溶液及内标茶碱溶液,同法操作后获得相应的色谱图(图1B),头孢吡肟对照品及内标的保留时间分别为6.4和8.7 min; 取给药后的小鼠10 min时间段的肺组织样品,同法操作后获得相应的色谱图(图1C) 。结果表明,本实验条件下的头孢吡肟和内标物分离良好,肺组织中内源性杂质对样品测定不产生干扰。
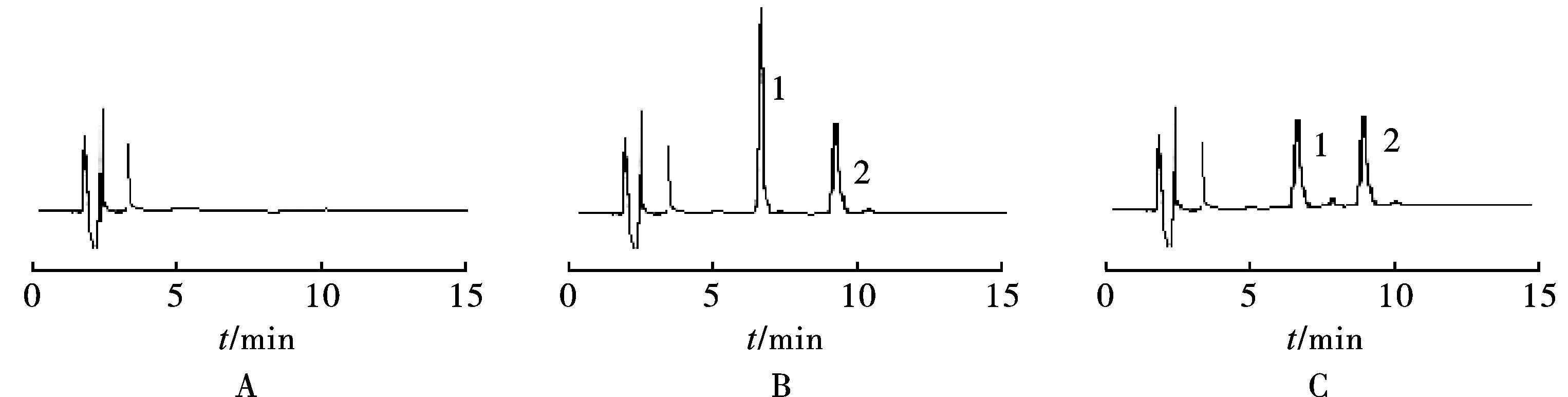
图1 盐酸头孢吡肟肺组织样品HPLC图
2.5.2线性范围和定量限 精密量取300 μL空白肺组织匀浆液,加入一定量的对照品储备液及质量浓度为0.1 mg·mL-1的内标茶碱溶液20 μL,涡旋混匀后,配制成头孢吡肟肺组织匀浆液,标准模拟肺组织匀浆液工作曲线,质量浓度分别为0.1,0.2,1,2,10和20 μg· mL-1。按2.4项下进行处理,进样20 μL,HPLC分析。以肺组织中头孢吡肟质量浓度为横坐标、头孢吡肟及内标峰面积比值为纵坐标,用最小二乘法回归运算,得到直线回归方程:
Y=0.175 9X+0.021 6(r=0.999 2)
结果表明,在 0.1~20 μg·mL-1范围内,线性关系良好。
取肺组织终质量浓度为0.1 μg·mL-1的质控样品5份,按2.4项下进行测定,结果平均值为0.085 μg·mL-1,标准差为0.004,RSD为4.167%,定量下限为0.1 μg·mL-1,满足方法学样品的测定要求。
2.5.3精密度 精密量取300 μL空白肺组织匀浆液,加入一定量的对照品储备液,加入质量浓度为0.1 mg·mL-1内标茶碱溶液20 μL,涡旋混匀后,配制成低、中、高质量浓度质控样本,头孢吡肟肺组织质量浓度分别为0.2,2和20 μg·mL-1。按2.4项下进行处理,进样量20 μL。每个质量浓度分别测5份样品,连续测3 d,考察日内及日间精密度,其RSD为2.05%~13.18%。
2.5.4回收率 精密量取300 μL空白肺组织匀浆液,加入一定量的对照品储备液,加入质量浓度为0.1 mg·mL-1内标茶碱溶液20 μL,涡旋混匀后,配制成低、中、高质量浓度质控样本,头孢吡肟肺组织质量浓度分别为0.2,2和20 μg·mL-1,按2.4项下进行处理,每个质量浓度测5次,进样量20 μL。求出头孢吡肟与内标的峰面积比,代入标准曲线,计算头孢吡肟的质量浓度以及方法回收率。该方法回收率分别为95.22%,98.74%和100.32%,RSD分别为5.76%,5.32%,4.28%。以标准肺组织样品中提取后测得的峰面积与对应质量浓度对照品溶液所测得的峰面积之比计算提取回收率,其值分别为80.29%,83.97%和86.21%,RSD分别为8.76%,5.48%,2.94%。
2.5.5稳定性 配制头孢吡肟在肺组织匀浆液中高、中、低质量浓度质控样品,质量浓度分别为0.2,2和20 μg·mL-1。考察其在室温放置24 h后的稳定性。其值稳定,RSD为3.73%~11.87%;样品在-20 ℃冰箱中保存3 d稳定,RSD为1.18%~11.45%;样品反复冻融解冻2次后稳定,RSD为1.68%~13.14%。
2.5.6小鼠肺内药动学 按2.3项下处理并测定各个时间点小鼠肺组织中的药物浓度(表1),得盐酸头孢吡肟在肺组织中药时曲线图(图2)。用DAS3.1药代动力学软件对肺组织药物浓度-时间数据进行处理,盐酸头孢吡肟的肺内药动学符合一室模型,以统计矩方法求得相应的药动学参数(表2)。

表1 各个时间点小鼠肺组织中的药物浓度

图2 盐酸头孢吡肟肺组织中药物浓度-时间曲线
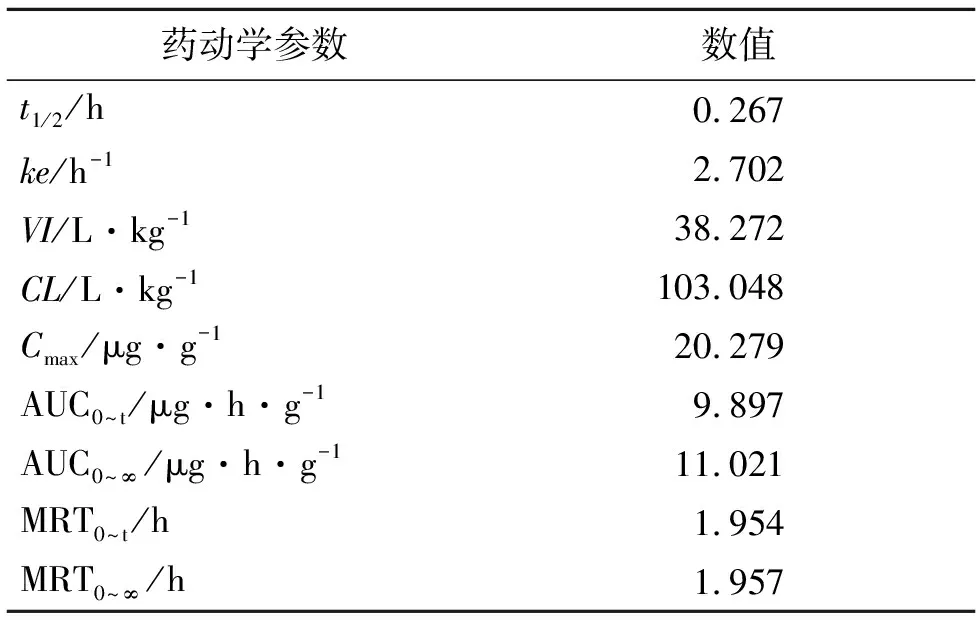
表2 盐酸头孢吡肟在肺中的药动学参数
3 讨论
本实验在建立色谱条件时,参考了已有文献[5-6],对流动相磷酸盐和醋酸铵进行了系统适用性比较,两者的色谱行为相差不大,最终选择了对色谱柱损害相对较小的醋酸铵。本实验在选择沉淀剂时,比较了体积分数30%,20%和10%三氯乙酸,通过色谱图发现体积分数30%和20%三氯乙酸的杂质峰多于体积分数10%三氯乙酸,推测可能是体积分数较高的三氯乙酸本身有可能会引入杂质。体积分数10%的三氯乙酸已经可以沉淀完全。准确进行生物样品含量测定时,选择合适的内标最为关键。在类似研究中,有文献报道以茶碱、对乙酰氨基酚、头孢他啶、阿司匹林等作为生物样品检测的内标[5-7],其中茶碱的色谱行为与头孢吡肟最为相近且不干扰其测定,因此本实验选用茶碱作为内标。
研究表明,在常规给药剂量范围内,头孢吡肟在人体内的代谢符合线性动力学的过程,未见药物在体内有明显蓄积的现象[8]。本实验结果表明,头孢吡肟在小鼠肺内的药动学符合一室模型,药物能够快速进入肺组织,肺内半衰期较短,临床上可以通过增加给药频次或持续外周静脉给药以期达到更好的疗效。
参考文献:
[1] 吕冬梅,李玥琦,王来成,等. 头孢吡肟的临床应用与评价[J]. 抗感染药学, 2013,10(1): 51-55.
[2] 聂书卉. 头孢吡肟抗感染临床疗效观察[J]. 药物与临床,2008,5(17): 76-77.
[3] 党宏万,杨小英,繆月琴. 医院细菌耐药性分析[J]. 西北药学杂志,2003, 18(6): 277-278.
[4] 任光进,杨秀莲,牛俊霞, 等. 铜绿假单胞菌对抗生素的耐药分析[J]. 西北药学杂志,2003,18(5): 230-231.
[5] 段威,夏东亚,郭涛. HPLC法测定人血浆中头孢吡肟的浓度[J]. 中国药房, 2008,19(29): 2262-2264.
[6] 胡婕慧,谢林,肖大为,等. 高效液相色谱法测定人血浆中头孢吡肟浓度及其药动学[J]. 中国现代应用药学,2007,24(1): 53-56.
[7] 陈华英,林阳,董平,等. 头孢吡肟血药浓度HPLC测定方法建立及临床应用[J]. 中国药学杂志,2009,44(2): 144-146.
[8] Barbhaiya R H, Forgue S T, Gleason C R, et al. Pharmacokinetics of cefepime after single and multiple intravenous administrations in healthy subjects[J]. Antimicrob Agents Chem,1992,36(3): 552-557.
