BODIPY在表面活性剂溶液中的荧光性质研究
2014-08-18吕永军
吕永军
(四川理工学院材料与化学工程学院, 四川自贡643000)
BODIPY在表面活性剂溶液中的荧光性质研究
吕永军
(四川理工学院材料与化学工程学院, 四川自贡643000)
合成了氟硼二吡咯亚甲基(BODIPY)黄绿色荧光染料,使用ESI-MS、1H NMR和13C NMR进行了结构表征,并测试了其在不同类型表面活性剂溶液中的荧光光谱性质。实验结果表明,十四烷基三甲基溴化铵(MTAB)对染料有显著的荧光增敏效应,这主要归因于BODIPY分子进入MTAB胶束中。BODIPY荧光强度和MTAB浓度在0-2.1×10-3mol/L范围内呈良好的线性关系,检测限为1.56×10-6mol/L。
BODIPY;表面活性剂;荧光性质;增敏效应
引言
分子荧光传感器以其灵敏度高、选择性好、开-关间可转换性以及使用方便等优点而备受关注[1-5]。荧光传感器一般由接受单元和信号报告单元两部分组成。BODIPY作为一类光物理与光化学性能优异的荧光信号报告单元,已被广泛应用于阴离子、金属离子、自由基和中性小分子等荧光分析检测领域[6-9]。BODIPY具有:高摩尔吸光系数(ε≈7×104-7×105L·mol-1·cm-1)、高荧光量子产率(φ>0.5)、最大激发波长达500-700 nm、光化学稳定性好等优点。但是,此类染料水溶性较差,当前基于BODIPY类的传感器的识别过程多是在乙腈或二甲基亚砜等有机体系中进行。通过在BODIPY骨架上引入水溶性基团如磺酸基、乙二醇链等可改善BODIPY类染料在水中的溶解性[10-13]。因此,为避免大量的合成工作,针对BODIPY类染料开发新的识别溶液体系是十分必要的。
表面活性剂在溶液中达到一定浓度后可缔合形成胶束结构,改变本体溶液的微观环境。荧光分析中,适当的表面活性剂可以改善体系的荧光发射环境以提高检测的灵敏度,消除干扰,增强探针分子荧光强度。近年来,表面活性剂与荧光分子复配体系已被用于环境分析与检测研究[14-16]。
本文通过研究BODIPY荧光分子在阴离子、阳离子和非离子表面活性剂溶液中的荧光光谱变化,期望发现适宜的表面活性剂体系,提高BODIPY水溶性并实现荧光增敏效应。实验结果表明,十四烷基三甲基溴化铵使其荧光强度显著增强;十二烷基苯磺酸钠增敏现象相对较弱;十二烷基硫酸钠和曲拉通X-100对其荧光性质基本无影响。
1 实验部分
1.1仪器和试剂
LS-55荧光分光光度计(Perkin Elmer公司);Varian INOVA-400核磁共振仪(Varian公司);超纯水器(成都超纯科技公司)。
十四烷基三甲基溴化铵(MTAB)、十二烷基苯磺酸钠(SBDS)、十二烷基硫酸钠(SDS)和曲拉通X-100均为市售产品,实验室用水为超纯水。
BODIPY的合成[17]:
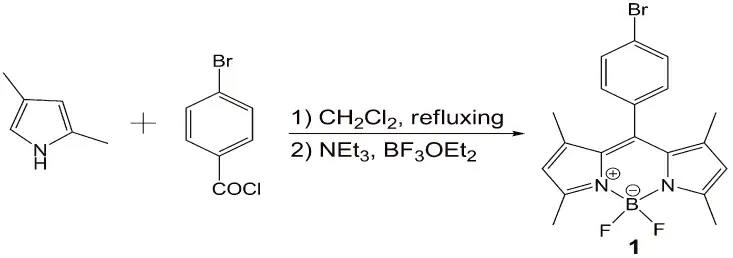
取5.8 g对溴苯甲酰氯和5.0 g 2,4-二甲基吡咯于250 mL CH2Cl2中,N2气保护,加热回流,TLC检测2,4-二甲基吡咯反应完全。冰水浴下,滴加15 mL三乙胺,搅拌反应20 min后,滴加15 mL三氟化硼乙醚,室温反应3 h。水洗多次,收集有机相用无水MgSO4干燥,旋蒸除去溶剂。柱层析,洗脱液为CH2Cl2和正己烷(1∶1,体积比),收集黄绿色溶液,得3.0 g红色固体1,产率30%,熔点:176-177 ℃.ESI-MS:403.1[M+H]+.1H NMR(400 MHz,CDCl3):δ=1.392(s,6 H,2 CH3),2.530(s,6 H,2 CH3),5.970(s,2 H,2 CH),7.158(d,J=6.4 Hz,2 H,ArH),7.624(d,J=6.4 Hz,2H,ArH).13C NMR(100 MHz,CDCl3):δ=14.63,121.42,123.23,129.79,131.14,132.42,133.92,139.98,142.89,155.87.
1.2实验方法
于一系列10 mL比色管中,分别加入2.0 mL的3.1×10-6mol/L的BODIPY的乙腈溶液,N2吹干乙腈溶剂,用不同浓度及类型的表面活性剂水溶液分别定容至5.0 mL,震荡摇均,然后测定荧光光谱。荧光仪激发波长为490 nm,激发和发射狭缝分别为15 nm和10 nm。
2 结果与讨论
2.1 BODIPY荧光光谱
BODIPY(3.1×10-6mol/L)在乙腈溶液中呈现亮黄绿色荧光,其激发和发射光谱如图1所示,最大激发和发射波长分别为499 nm和510 nm,斯托克斯位移为11 nm。两峰为窄峰,半峰宽均为25 nm。

图1 乙腈中BODIPY光谱
注:(1)激发光谱,(2)发射光谱
2.2 BODIPY在表面活性剂溶液中的荧光光谱
图2为BODIPY在MTAB、SDBS、SDS和曲拉通X-100四种表面活性剂溶液中的荧光光谱,其中,MTAB属于阳离子表面活性剂,SDBS和SDS属于阴离子表面活性剂,X-100属于非离子表面活性剂。在四种溶液中,主体1的荧光最大发射峰均出现3-6 nm红移。这主要是由于表面活性剂分子使得水溶液极性增大,发射波长向长波方向移动[18]。MTAB使荧光强度增强了11倍。SDBS使主体荧光强度增强幅度略低,仅为3倍。而SDS对主体的荧光干扰最大,显示的荧光增强归因于SDS溶液被激发后的散射效应。非离子表面活性剂曲拉通X-100对主体的荧光强度基本没有影响。
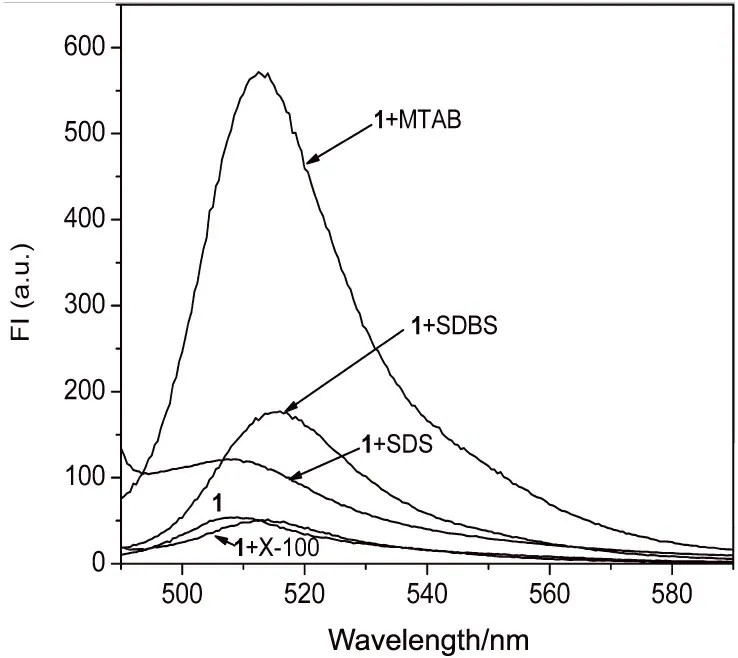
图2 BODIPY(1.24×10-6mol/L)在不同表面活性剂溶液(2.1×10-3mol/L)中的荧光光谱

图3 BODIPY(1.24×10-6mol/L)在不同MTAB浓度下的荧光光谱
注:自下而上MTAB浓度依次为:0, 4.19×10-4mol/L, 6.29×10-4mol/L,8.38×10-4mol/L, 1.05×10-3mol/L, 1.26×10-3mol/L, 1.67×10-3mol/L, 2.1×10-3mol/L, 2.5×10-3mol/L
图3考察了不同MTAB浓度下BODIPY的荧光性质变化。由荧光滴定实验可知,随着MTAB浓度的逐渐增加,BODIPY的荧光发射波长先发生由510 nm红移到513 nm,荧光强度逐渐增强,浓度达到2.1×10-3mol/L时,荧光强度值最大,进一步增大MTAB浓度,荧光强度基本恒定。这说明MTAB在水溶液中逐渐达到临界胶束浓度(cmc)形成胶束,BODIPY分子逐渐被疏水烷基链包围,激发态的荧光分子碰撞猝灭几率减小,使得荧光量子效率增大,强度增强[19]。根据513 nm处的荧光强度变化,发现MTAB浓度在0-2.1×10-3mol/L范围内与ΔF呈良好的线性关系,线性回归方程:ΔF=7.31+269.22×10-4C(mol/L),线性相关系数:R=0.9985。依据荧光仪器的3倍信噪比,测得检测限为1.56×10-6mol/L。采用荧光滴定法同样考察BODIPY在不同浓度SDBS,SDS及X-100溶液中的荧光性能,如图4所示。相同浓度下,随着SDBS浓度的增高主体荧光发射波长红移6 nm,荧光强度增强了120 a.u.,浓度为2.1×10-3mol/L时基本恒定,基本接近其cmc值。对比MTAB和SDBS发现,浓度升高主体荧光强度分别增强了11倍与3倍,推测是MTAB胶束比SDBS胶束尺寸大且疏松,主体分子更易进入,导致荧光显著增强。SDS和X-100均使荧光峰红移,荧光强度基本不变,这可能归因于BODIPY芳香环结构与两者胶束内部环境的相溶性低,使得BODIPY不能够有效进入胶核。
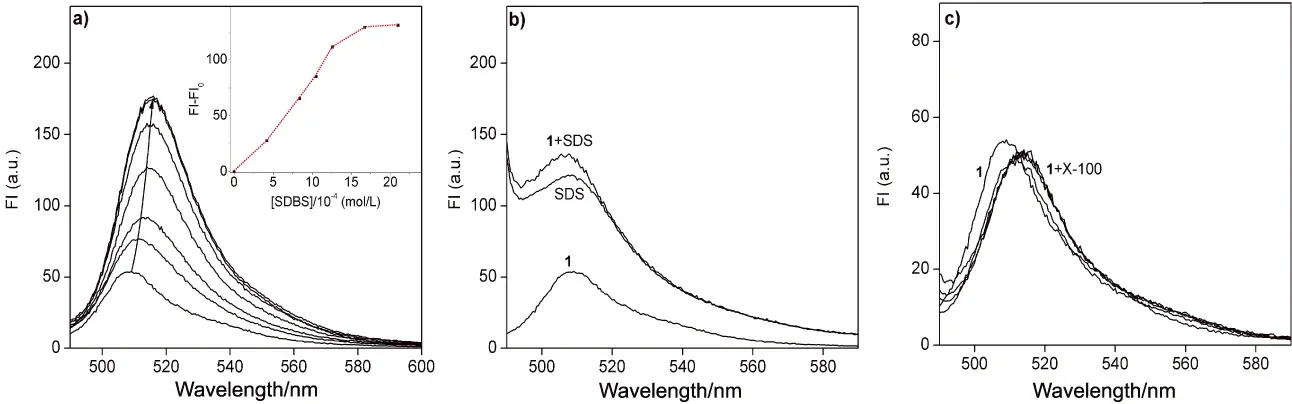
图4 BODIPY(1.24×10-6mol/L)在不同SDBS、SDS及X-100浓度(0-2.1×10-3mol/L)下的荧光光谱
注:(a)SDBS, (b)SDS, (c)X-100
2.3影响因素考察
2.3.1 温度的影响
以MTAB-BODIPY溶液体系为例,MTAB浓度为2.1×10-3mol/L,BODIPY浓度为1.24×10-6mol/L,考察了不同温度下溶液体系的荧光性质,如图5(a)所示。随着温度的逐渐升高,荧光强度逐渐降低。温度在15-40 ℃之间,体系的荧光强度没有显著变化;当温度超过50 ℃时,荧光强度明显降低。主要是由于高温使非辐射跃迁引起的分子荧光部分猝灭[20]。因此,实验控制在室温范围内。

图5 温度、平衡时间及光照时间对MTAB中BODIPY荧光强度的影响
2.3.2 平衡时间的影响
在室温条件下,BODIPY主体与MTAB的混合溶液0.5 h时荧光强度最大,延长平衡时间,强度略降低,4 h后基本恒定,如见图5(b)所示。表明形成BODIPY-MTAB稳定体系需平衡4 h以上,这可能取决于BODIPY分子进入MTAB胶束的动力学影响因素。
2.3.3 光照的影响
BODIPY-MTAB体系避光平衡4 h后,分别测定其在不同的光照时间下荧光强度变化,如图5(c)所示。光辐射条件下体系荧光强度逐渐降低,2 h后基本不变,进一步延长光照时间荧光强度仅降低了约60 a.u。说明该体系无明显的光漂白现象,光学稳定性较好。
3 结束语
设计合成了BODIPY荧光染料,并考察了其在不同类型表面活性剂溶液中的荧光性质。研究表明,MTAB对主体有显著的荧光增敏效应,浓度在0-2.1×10-3mol/L范围内呈现较好的线性关系,相关系数:R=0.9985。通过考察温度、平衡时间及光照等影响因素,发现BODIPY-MTAB溶液体系在室温条件下荧光强度稳定、体系在4 h后达到平衡、光学稳定性好。
[1] Carter K P,Young A M,Palmer A E.Fluorescent sensors for measuring metal ions in living systems[J].Chem.Rev.,2014,114(8):4564-4601.
[2 韩庆鑫,石兆华,唐晓亮,等.荧光化学传感器的研究与应用[J].兰州大学学报:自然科学版,2013,49(3):416-428.
[3] Valeur B.Molecular fluorescence:Principles and applications[M].London:Wiley-VCH,2001.
[4] Silva A P,Gunaratne H Q,Gunnlaugsson T,et al.Signaling recognition events with fluorescent sensors and switches[J].Chem.Rev.,1997,97(5):1515-1566.
[5] 李 照,马会民.试卤灵类光学探针的研究进展[J].影像科学与光化学,2014,32(1):60-68.
[6] Loudet A,Burgess K.BODIPY dyes and their derivatives:synthesis and spectroscopic properties[J].Chem.Rev.,2007,107(11):4891-4932.
[7] 王红萍,崔爱军,田茂忠,等.氟硼荧(BODIPY)染料的研究进展[J].当代化工,2007,36(2):198-201.
[8] Ulrich G,Ziessel R,Harriman A.The chemistry of fluorescent bodipy dyes:versatility unsurpassed[J].Angew.Chem.Int.Ed.,2008,47(7):1184-1201.
[9] Kumar N,Bhalla V,Kumar M.Recent developments of fluorescent probes for the detection of gasotransmitters (NO,CO,and H2S)[J].Coord.Chem.Rev.,2013,257(15):2335-2347.
[10] Yoshii R,Yamane H,Nagai A,et al.π-conjugated polymers composed of BODIPY or aza-BODIPY derivatives exhibiting high electron mobility and low threshold voltage in electron-only devices[J].Macromolecules.,2014,47(7):2316-2323.
[11] Vegesna G K,Sripathi S R,Zhang J T,et al.Highly water-soluble BODIPY-based fluorescence probe for sensitive and selective detection of metric oxide in living cells[J].ACS Appl.Mater.Interfaces.,2013,5(10):4107-4112.
[12] Bura T,Ziessel R.Water-soluble phosphonate-substituted BODIPY derivatives with tunable emission channels[J].Org.Lett.,2011,13(12):3072-3075.
[13] Niu S L,Ulrich G,Ziessel R,et al.Water-soluble BODIPY derivatives[J].Org.Lett.,2009,11(10):2049-2052.
[14] 冯永兰,邝代治,许金生,等,1-吡啶-3-[4-(苯基偶氮)苯基]-三氮烯与阳离子表面活性剂显色反应[J].化学研究与应用,2004,16(5):708-710.
[15] 秦宗会,胡武洪.刚果红-溴化十六烷基吡啶光度法测定阴离子表面活性剂[J].化学研究与应用,2008,20(7):879-882.
[16] 占海红,仉 华,李全民,等.表面活性剂增敏硝普钠分光光度法测定甲硝唑[J].化学研究与应用,2011,23(6):784-787.
[17] Qin W W,Baruah M,Auweaer M V,et al.Photoophysical properties of borondipyrromethene analogues in solution[J].J.Phs.Chem.A.,2005,109(33):7371-7384.
[18] Guo B C,Peng X J,Cui A J,et al.Synthesis and spectral properties of new boron dipyrrometnene[J].Dyes and Pigments.,2007,37(2):206-210.
[19] Pallavicini P,Diaz F Y,Pasotti L.Micelles as nanosized containers for the self-assenbly of multicomponent fluorescent sensors[J].Coor.Chem.Rev.,2009,253(17):2226-2240.
[20] 刘淑芳,陈致国.荧光猝灭效应的温度特性研究[J].黑龙江商学院学报:自然科学版,1997,13(1):46-49.
Fluorescence Characters of BODIPY in the Surfactant Solution
LVYongjun
(School of Material and Chemical Engineering, Sichuan University of Science & Engineering, Zigong 643000, China)
A novel yellow-green fluorochrome BODIPY was synthesized and the structur was characterized by ESI-MS,1H NMR and13C NMR. It’s fluorescence spectral properties were tested in different types of surfactant solutions. The experimental results showed that the MTAB solution had an obvious fluorescence sensitizing effect on dye, which can be attributed to the entrance of BODIPY into MTAB micelle. Moreover, there was a good linear relationship between the fluorescence intensity of BODIPY and MTAB concentration in the range of 0~2.1×10-3mol/L, with the detection limit of 1.56×10-6mol/L.
BODIPY; surfactant; fluorescence property; sensitizing effect
2014-07-18
四川理工学院人才引进项目(2012RC02);四川理工学院大学生创新基金项目(CX20130301)
吕永军(1984-),男,四川自贡人,讲师,博士,主要从事光化学分子识别方面的研究,(E-mail)yongjunlv@qq.com
1673-1549(2014)06-0001-04
10.11863/j.suse.2014.06.01
O657.39
A
