RP-HPLC法测定患者血浆中异烟肼及乙酰异烟肼的浓度
2014-08-15侯文洁钱智磊周秋云丁红梓
张 亮,侯文洁,钱智磊,周秋云,丁红梓,王 洁
0 引言
结核病(Tuberculosis,TB)每年会导致数百万人死亡[1]。异烟肼(INH)是结核病初始治疗方案中最重要的组成部分[2]。但有部分患者由于自身代谢能力的差异导致血药浓度太低而最终治疗失败。乙酰异烟肼(AcINH)是INH最主要的代谢产物,也是肝毒性最大的物质,是INH在肝脏内经乙酰化而成,该过程分为快乙酰化和慢乙酰化两种类型,其治疗效果和毒副作用有所不同。肝损害多见于快乙酰化型,这可能是因为INH在体内被迅速代谢为AcINH而造成的。因此,可以通过监测相同给药间隔后AcINH的浓度来判断患者乙酰化的类型[3],调整INH的给药剂量以提高治疗效率,减少毒副作用的发生。此外,肺结核的治疗通常为联合治疗,而药物联用也会对INH的血药浓度产生影响。因此,对结核患者进行血药浓度监测是有必要的。
目前,已有高效液相色谱(HPLC)法分析抗结核药物含量的报道[4-5],但这些方法都不能用来分析成分极为复杂的血浆中的药物浓度。也有报道使用HPLC同时测定血浆中的多组分抗结核药,但使用了离子对试剂,后者成本过高且重现性较差[6]。液相—联用(LC-MS)拥有超高的选择性和灵敏度,可同时分析血浆中的多种药物[7],但其成本过高而且仪器在医院尚未普及。因此,使用HPLC对多种抗结核药及其代谢物进行血药浓度监测依然是最常用和最经济的方法。本文对HPLC同时测定血浆中INH和AcINH进行了方法学研究,并且使用本方法对30例患者血浆中的药物浓度进行了监测。
1 仪器与试药
1.1 仪器 LC-20AB高效液相色谱系统(检测器为SPD-M20A,岛津,日本);涡旋仪(WH-2,上海沪西分析仪器厂有限公司);电子分析天平(EB224,上海舜宇恒平科学仪器有限公司);高速离心机(TG1650-WS,上海卢湘仪);微量移液器(Eppendorf,德国)。
1.2 试药 异烟肼对照品(批号:100578-200401,中国药品生物制品检定所),乙酰异烟肼对照品(批号:3-JES-102-4,Toronto Research Chemicals Inc.),茶碱对照品(批号:100121-199903,中国药品生物制品检定所)。
1.3 试剂 甲醇(Merck,德国)为色谱纯,磷酸二氢钾(国药集团,中国)、三乙胺(国药集团,中国)均为分析纯。水为自制双蒸水(MILLIPORE,美国)。
2 方法与结果
2.1 色谱条件 色谱柱为Inertsil ODS-SP(4.6 mm×150 mm,5 μm),流动相:甲醇(A)-0.05 mol/L磷酸二氢钾(B,三乙胺调pH=5.6)(梯度:1~10 min梯度A∶B为4∶98,10~11 min梯度A∶B为80∶20,11 min梯度A∶B为80∶20,淋洗时间共20 min),柱温:40 ℃,流速:1 mL/min,进样体积20 μL,检测波长:261 nm。
2.2 血浆样品处理 取血浆样品300 μL放入2 mL离心管中,精密加入2.4 μg/mL茶碱甲醇溶液10 μL作为内标物质,涡旋混匀1 min,加甲醇700 μL,涡旋混合5 min,16 000 r/min离心15 min,取上清液经0.45 μm滤膜过滤后转移至自动进样器小瓶。
2.3 方法专属性试验 按照本方法,INH和AcINH有较好分离,互不干扰测定,血浆中的杂质峰对样品的测定也没有影响。色谱图见图1。

图1 INH和AcINH的色谱图
2.4 线性关系考察 精密称取对照品置于10 mL容量瓶中,加入甲醇超声溶解并稀释至刻度,配成浓度分别为INH 1 000 μg/mL、AcINH 1 000 μg/mL的标准储备液。取数支2 mL的离心管,每支加入不同量的INH和AcINH标准储备液及300 μL空白血浆,使血浆中药物浓度为0.15、0.3、0.6、1.2、2.4、4.8、9.6、19.2、38.4 μg/mL。按“2.2”项下操作,记录色谱图,以浓度(C)为横坐标、样品与内标峰面积比值(Y)为纵坐标进行线性回归。见表1。
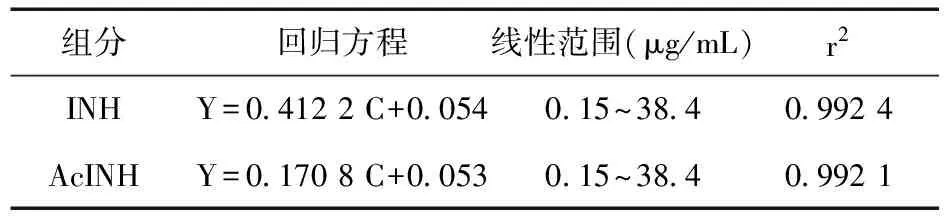
表1 回归方程和线性范围
2.5 精密度和准确度试验 分别于300 μL的空白血浆中加入标准储备液,精确配置成含低、中、高3种不同浓度INH(0.5、5、25 μg/mL)、AcINH(0.5、5、25 μg/mL)的血浆样品,按“2.2”项下操作,测定日内(5次)和日间(5 d)精密度,RSD均<10%。见表2。
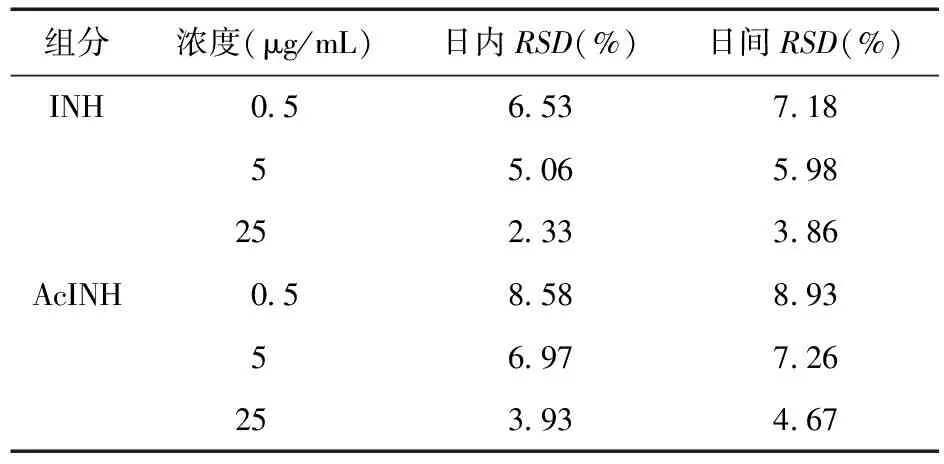
表2 日间、日内精密度试验(n=5)
2.6 稳定性考察 在300 μL的空白血浆中加入标准储备液,精确配置成含INH(0.5、5、25 μg/mL)、AcINH(0.5、5、25 μg/mL)浓度的血浆样品,分别室温放置0、2、4、8、12 h后按“2.2”项下操作,测定峰面积和内标峰面积的比值。结果表明,测定基本保持稳定。见表3。
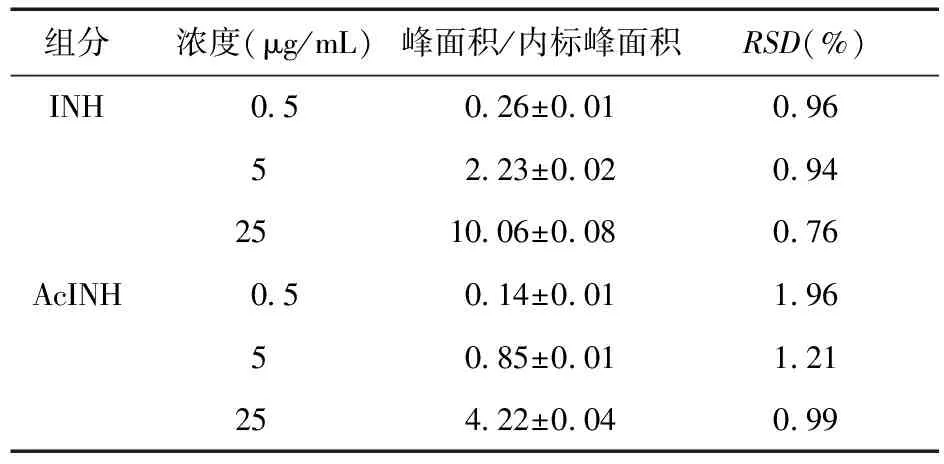
表3 稳定性试验结果(n=5)
2.7 回收率试验 分别于300 μL的空白血浆中加入标准储备液,精确配置成含低、中、高3种不同浓度INH(0.5、5、25 μg/mL)、AcINH(0.5、5、25 μg/mL)的血浆样品,按“2.2”项下操作,每个浓度测5遍,计算平均回收率和RSD。见表4。
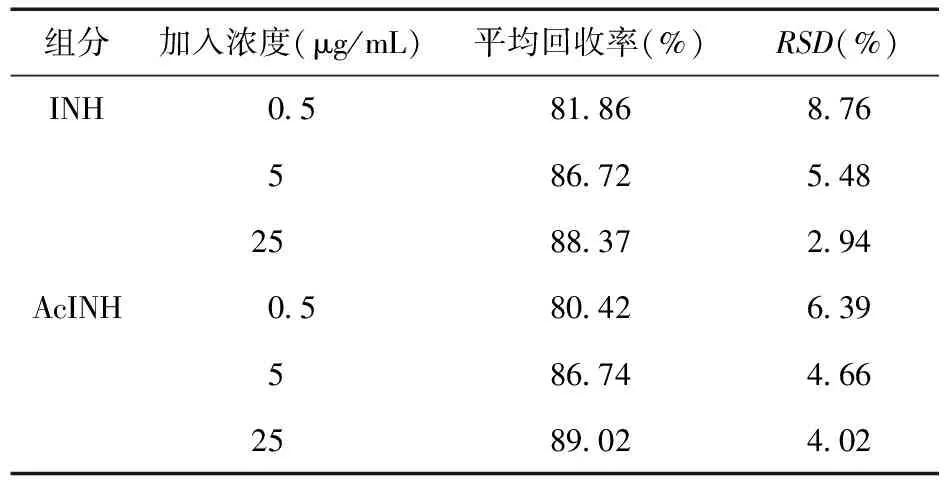
表4 回收率测定结果
3 血药浓度检测的应用
本方法成功用于30例服用INH患者的血药浓度检测。服药方法为INH 0.3 g,1次/d,早饭后0.5 h顿服。早饭后2.5 h采集血样,并于3 h内分析完毕,不能及时测试的保存在-40 ℃冰箱内。测试结果表明,患者的血浆药物浓度差异较大。INH血药浓度为0.34~5.9 μg/mL,平均(1.9±0.61)μg/mL;AcINH血药浓度为0.36~3.3 μg/mL,平均(1.75±0.59)μg/mL。
4 讨论
由于INH和AcINH极性较强,导致其在色谱柱上保留时间过短,且易受血浆杂质的影响。为了获得良好的分离度和峰形,本试验曾尝试使用苯基柱和氰基柱[8-9],其虽可延长保留时间,但峰形不满意。经过反复比较和试验,笔者认为使用C18柱以pH 5.6的磷酸二氢钾为缓冲对,在高极性流动相的洗脱下可以得到很好的分离。
在血浆样品处理方法中,本试验尝试了液液萃取法,结果发现,由于这三种组分的极性过大,用乙酸乙酯无法全部萃取,严重影响分析的准确性。此外,本试验尝试将沉淀蛋白后的上清液吹干后再用流动相复溶,结果显示,除了增加操作步骤、给方法学的考察增加了难度外,还需加入抗氧化剂,影响了多组分药物的稳定性。通过试验和对比,选择使用甲醇沉淀蛋白后直接取上清液进样,该方法可以在不影响可靠性的前提下简化操作步骤,方便临床大批量样本的检测。
本试验方法简单、准确、成本较低,灵敏度不低于LC-MS,即使样本中药物的含量较低也能测定;保留时间较为合适,如果使用250 mm的C18柱还可以延长保留时间,增加分离度;方法回收率高于80%,日间和日内RSD<10%,完全符合生物样品分析要求;可以用于临床药物检测及药物动力学研究,可作为同行进行抗结核药物测定的参考。
参考文献:
[1] World Health Organization.10 Facts about Tuberculosis(March 2009)[EB/OL].http://www.who.int/fearutes/factifiles/tuberculosis/en/.
[2] World Health Organization.“Treatment of Tuberculosis:Guideline for National Programmers”,3rd ed.,2003,Geneva.
[3] 郎美琦,蒋利,黄佳盛.抗结核病药物治疗综述[J].临床肺科杂志,2010,15(8):1153-1154.
[4] Calleri E,Lorenzi DE,Furlanetto S,et al.Validation of a RP-LC method for the simultaneous determination of isoniazid,pyrazinamide and rifampicin in a pharmaceutical formulation[J].Pharm Biomed Anal,2002,29(6):1089-1096.
[5] Khuhawar MY,Rind FMA.Liquid chromatographic determination of isoniazid,pyrazinamide and rifampicin from pharmaceutical preparations and blood[J].Chromatogr B,2002,766(2):357-363.
[6] Zhou ZF,Chen LY,Liu P,et al.Stimulatneous deteination of isoniazid,pyrazinamide,rifampicin and acetylisoniazid in human plasma by high-perfomance liquid chromatography [J].Anal Sci,2010,26(11):1133-1138.
[7] Gong Z,Basir Y,Chu D,et al.A rapid and robust liquid chromatography/tandem mass spectrometry method for simultaneous analysis of anti-tuberculosis drugs-ethambutol and pyrazinamide in human plasma[J].Chromatogr B,2009,877(16):1698-1703.
[8] 谭志荣,陈尧,郭栋,等.HPLC-MS/MS法测定人血浆中西洛他唑浓度[J].中南药学,2009,7(11):827-830.
[9] 刘艳文,张文渊,颜苗,等.UPLC-MS/MS法测定小鼠血浆及脑组织中马钱子碱浓度[J].中南药学,2010,8(5):321-325.
