血流储备分数指导经皮冠状动脉介入治疗术中非罪犯中度狭窄血管治疗策略的研究
2014-08-10朱贵家刘洋洋曹阳陈琳孙兑荣董国甘润韬杨树森
朱贵家 刘洋洋 曹阳 陈琳 孙兑荣 董国 甘润韬 杨树森
血流储备分数与冠状动脉造影对多支血管病变评价比较(fractional fl ow reserve versus angiography for multivessel evaluation,FAME)研究[1]显示,多支血管病变(MVD)中,血流储备分数(FFR)指导的经皮冠状动脉介入治疗(PCI)可有效降低不良事件发生率。对MVD 患者在明确罪犯血管之外,造影还能发现很多其他中度病变血管[2-4]。研究表明,在治疗MVD 患者罪犯病变期间,也对其他病变进行血运重建,可降低不良事件的发生率[5]。临床实践中,大多数手术仍是通过冠状动脉造影(CAG)决定是否进行血运重建,但最近这种方法在用于MVD 时表现出一定的局限性[6]。通过冠状动脉压力导丝测得的FFR 被视为对血管造影检出的中度或不确定冠状动脉狭窄进行血运重建的金标准[7]。本研究根据CAG、临床相关检查(如心电图等)判断罪犯血管,对已明确的罪犯血管行PCI 治疗后,对非罪犯中度狭窄血管行FFR 检测,根据FFR 值决定是否同时行PCI 治疗,并判断临床转归。
对象与方法
1.研究对象:选择2012 年11 月至2013 年11 月哈尔滨医科大学附属第一医院心内科患者。纳入标准:(1)明确诊断不稳定型心绞痛患者,诊断标准参考2011 年欧洲心脏病学会(ESC)《非ST 段抬高急性冠状动脉综合征治疗指南》[8],年龄30 ~70 岁,门诊收入本科;(2)心绞痛分级Ⅳ级[加拿大心血管病学会(CCS)分级)];(3)所有置入的支架均为西罗莫司药物洗脱支架;(4)除罪犯血管(罪犯血管定义为CAG、心电图及心脏彩超共同明确判定的血管)外,CAG 还可检出至少一支非罪犯中度狭窄病变血管,且该病变部位参考直径>2 mm。排除标准:(1)除罪犯血管外,其余血管含有重度狭窄病变者,重度狭窄>75%狭窄;(2)心源性休克或血流动力学不稳定;(3)慢性肾病≥Ⅲ期的患者;(4)结合CAG 排除:高度迂曲或钙化的动脉;造影结果结合临床综合判断首选冠状动脉旁路移植术(CABG)患者;左主干病变,需要血运重建者;慢性闭塞病变患者;(5)预期生存寿命<1 年;(6)不能耐受双联抗血小板、血管紧张素转化酶抑制剂(ACEI)/血管紧张素受体阻滞剂(ARB)、β阻滞剂、他汀类药物治疗或存在禁忌证者;(7)伴随非冠状动脉手术(如瓣膜置换或修复、既往CABG 术后);(8)严重左心室肥厚;(9)左心室射血分数(LVEF)<30%;(10)腺苷应用禁忌证者。
2.试验设计:根据CAG 及临床相关检查(如心电图、心脏彩超等)明确罪犯血管,对已明确的罪犯血管行PCI 治疗后,针对非罪犯中度狭窄血管按照单双号分为对照组(非支架组)和观察组(FFR 指导下行PCI 组)。其中,FFR <0.8 的患者对非罪犯中度狭窄血管行PCI 治疗,然后对该中度狭窄血管行FFR 检测,确保FFR≥0.95[9]。入选患者均给予最优化药物治疗。
3.CAG 和PCI:行PCI 时手术入路途径首选桡动脉路径,必要时可行尺动脉、肱动脉、股动脉等入路途径。CAG、罪犯血管的判定、非罪犯中度狭窄血管的选择、支架置入以及FFR 检测过程均由三位经验丰富的介入心脏病医师(施行过1000 例以上的冠状动脉介入术)共同实施。冠状动脉中度狭窄判断采用国际通用的目测直径法,计算公式:血管狭窄程度=(狭窄血管近心端正常血管直径-狭窄处直径)/狭窄段近心端血管直径×100%,血管狭窄程度50%~75%为中度狭窄。PCI 造影成功标准:在支架使用前,单纯球囊扩张后管腔狭窄<50%、TIMI 血流Ⅲ级;使用支架后,管腔狭窄<20%。术后所有患者均给予血小板糖蛋白Ⅱb/Ⅲa 抑制剂0.15μg/(kg·min)持续24 h。
4.FFR 检测:在决定对病变血管进行一项功能研究后,通过导引导管给予200 ~300μg 硝酸甘油。使用该导管重复采集能对病变进行最佳显像的投照图。此项功能评价使用一根0.014 in(1 in=2.54 cm)冠状动脉压力导丝(Pressure-Wire,圣犹达旗下Radi Medical Systems 公司,瑞典乌普萨拉或Volcano Primewire ™,Volcano 股份有限公司,美国加利福尼亚州Rancho Cordova)进行。FFR 检测通过肘正中静脉给予腺苷180 μg/(kg·min)静脉点滴,FFR 数值降至最低,不再下降时停止静脉点滴腺苷,FFR 至少测定三次,第一次FFR 测完后等待血压稳定再行第二次检测,根据最低的FFR 值做出治疗决策。
5.药物治疗:所有患者均服用阿司匹林 (100 mg/次、每日一次,首次负荷剂量为300 mg)和氯吡格雷(75 mg/次、每日一次,首次负荷剂量为600 mg),美托洛尔(每天25 ~200 mg 或任一种β阻滞剂,维持静息心率55 ~65 次/min),培哚普利(≥2 mg/d 或其他的ACEI,不能耐受ACEI 的给予ARB),阿托伐他汀[20 ~40 mg/d,或其他相似的他汀类药物,使低密度脂蛋白(LDL)≤1.8 mmol/L]。术后氯吡格雷口服12 个月,其余药物长期口服。对患者的口服药物进行每周追踪,吸烟的患者停止吸烟,合并糖尿病的患者依照糖尿病专科医师意见给予最优化药物治疗。
6.资料收集和随访:记录所有研究对象入院后的临床资料,包括一般资料、心电图、心脏彩超、冠心病危险因素(高血压、糖尿病、吸烟史、高脂血症等)、肾功能及既往PCI、心肌梗死、脑卒中等。术后随访1 个月、3 个月、6 个月、9 个月和12 个月,记录随访期间的临床表现以及患者CCS 心绞痛分级;观察主要终点事件[包括全因死亡、非致死性心肌梗死、再次血运重建(TLR)发生率]和次要终点事件[包括心绞痛临床表现(CCS 分级)]发生情况。再次血运重建定义为因急性心肌梗死或严重心绞痛需PCI 者。靶血管定义为非罪犯中度狭窄血管。靶血管不良事件定义为因非罪犯中度狭窄血管所产生的一切不良事件,包括再次血运重建、非致死性心肌梗死和死亡。
7.统计学分析:所有数据均用统计软件SPSS 17.0 进行分析。计量资料采用方差分析,计数资料采用卡方检验。对随访期间每次事件的生存率估计采用Kaplan-Meier法,生存率的组间比较采用Log-rank test检验方法。以P<0.05 为差异有统计学意义。
结 果
1.两组患者基线资料比较:共纳入71 例患者,对照组35 例,观察组36 例。观察组中FFR≥0.8的 患 者 共23 例(63.9%),FFR <0.8 共13 例(36.1%)。两组患者的性别、年龄,高血压、糖尿病、高脂血症、吸烟、肾功能不全,既往PCI 史、心肌梗死和脑卒中等比较,差异均无统计学意义(P>0.05,表1)。
2.主要终点事件发生情况分析:(1)入选的71 例患者中共22 例(31.0%)发生主要终点事件,观察组6 例(16.7%)[包括全因死亡2 例(5.6%),再次血运重建5 例(13.9%),非致死性心肌梗死4 例(11.1%)],对照组16 例(45.7%)[包括全因死亡5 例(14.3%),再次血运重建14例(40.0%),非致死性心肌梗死11 例(31.4%)]。对照组主要终点事件以及组成因素的发生率较观察组显著升高(图1)。(2)靶血管不良事件发生:观察组患者再次血运重建2 例(5.6%),非致死性心肌梗死2 例(5.6%);对照组患者再次血运重建11 例(31.4%),非致死性心肌梗死10 例(28.6%);两组再次血运重建及非致死性心肌梗死分别比较,差异均有统计学意义(P<0.05)。(3)Kaplan-Meier生存率分析显示,两组患者无主要终点事件和再次血运重建生存率分别比较,差异均有统计学意义(P<0.05);无全因死亡与非致死性心肌梗死生存率分别比较,差异均无统计学意义(P>0.05)(表2)。

表1 两组患者基线资料比较
3.次要终点事件发生情况分析:随访术后12个月期间患者心绞痛临床表现,对于无心绞痛表现的患者心绞痛设为0 级,统计分析显示,观察组心绞痛情况较对照组显著改善(表3)。

表2 两组Kaplan-Meier生存率分析
讨 论
FFR 在1993 年由Pijls 等[10]首次提出以来,广泛应用于临界病变、多支病变、分叉病变等。随着DEFER、COURAGE、FAME、FAME Ⅱ等大型临床研究结果的公布,将FFR 推向顶峰,现已广泛应用于临床,指导PCI 治疗策略的选择。Pim等[11]回顾分析FAME 研究人群,FFR 指导PCI 患者中,1329 处(94%)病变成功行FFR 检测,其中640 处(48.2%)病变处于50%~70%狭窄,且这48.2% 的患者中,有218 处(34.1%)FFR<0.8。FAME 研究[12]中入选不稳定型心绞痛或非ST 段抬高心肌梗死(NSTEMI)患者共328 例,但对罪犯血管行PCI 后,在给予最优化药物治疗时,不良事件是否发生变化,以及对于非罪犯中度狭窄血管是行PCI 治疗,还是暂且最优化药物治疗,未进行研究。本研究入选不稳定型心绞痛多支血管病变患者,对已明确的罪犯血管行PCI 治疗,对中度狭窄血管行FFR 检测,根据FFR 值决定是否行PCI 治疗。
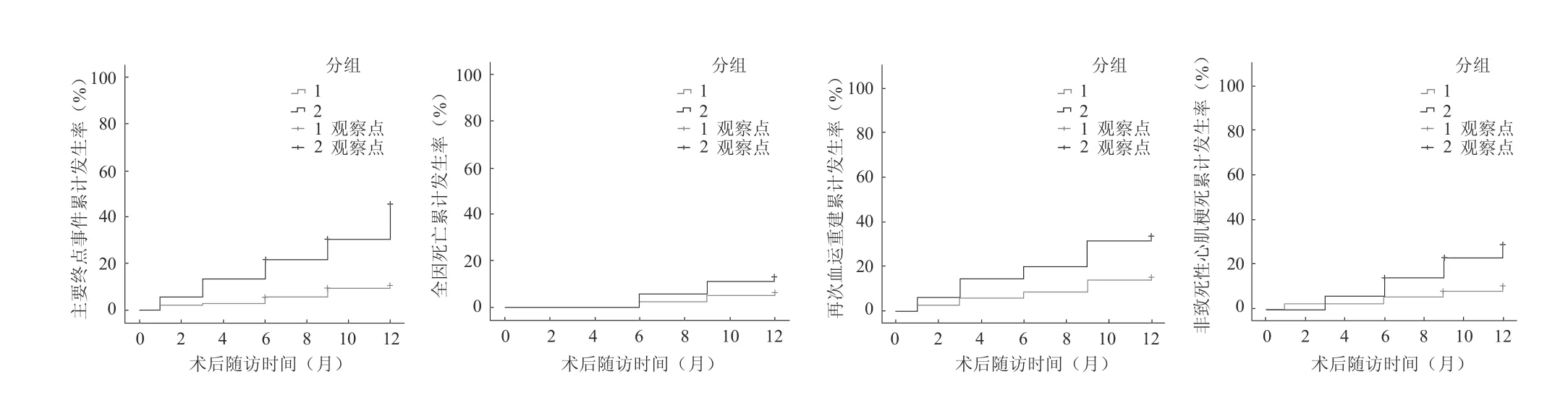
图1 两组患者不良事件累计发生率分析

表3 两组患者术后随访不同时间心绞痛分级比较[例(%)]
本研究中不稳定型心绞痛多支血管病变患者,对于非罪犯中度狭窄血管常规使用FFR 指导PCI治疗,随访12 个月,主要终点事件发生率和再次血运重建发生率较单纯CAG 指导PCI 治疗显著降低。观察组行FFR 检测,发现36.1%中度狭窄血管FFR 值<0.8,与FAME 研究[1]基本一致。
本研究结果和既往试验研究结果的不同可能有以下几点原因:(1)对于很多临床试验,不稳定型心绞痛患者给予最优化药物治疗或者PCI 治疗,但是并未在FFR 指导下行PCI 或者药物治疗,对于该处冠状动脉狭窄是否能在功能学上导致患者心绞痛发作,目前还未得到证实,如FRISC-Ⅱ、ICTUS、RIAT-3 等研究并未采取FFR 指导PCI 治疗[13]。临床实践中,采取FFR 指导PCI 的比例小于三分之一[14]。本研究中,观察组研究对象均采取FFR 检测,PCI 术后亦行FFR 检测,使病变部位血管达到功能学重建。(2)PCI 所有置入的支架均为西罗莫司药物洗脱支架,这可能是减少血运重建比例的原因之一[15]。局部抗缺血药物的使用与COURAGE 研究[16]类似,且比既往一般试验研究[17]使用浓度更高。(3)本研究主要终点事件不仅包括全因死亡、非致死性心肌梗死,而且将再次血运重建纳入范围内,这在既往试验研究中比较少见。已经证明,急性冠状动脉综合征高危人群经血运重建可以改善生存率和降低心肌梗死的发生率[18]。(4)观察组心绞痛临床表现较对照组显著改善,可能与观察组完全功能学重建相关。
结合本研究结果及临床分析,并非每次施行介入手术都需要测定FFR,若患者表现出典型性胸痛,心电图及心脏彩超等辅助无创检查结果呈阳性,并且CAG 结果也同样显示胸痛因该罪犯血管所致,可直接进行支架置入术治疗。但这类简单病例较少,对于中度狭窄的血管,为更好地指导治疗,建议行FFR 检测,根据FFR 决定是否行PCI 治疗,并且使用FFR 决定是否对中度狭窄血管行支架置入治疗,可以节省医疗费用并且改善患者的临床预后。
本研究局限性:(1)入选标准严格,研究样本量少,术后随访时间相对较短,对心血管事件的预测存在一定局限性,仍需大样本的临床研究进一步证实。(2)随访期间虽然基于严格控制相关指标,但是不能改善所有患者生活习惯等问题,可能对研究结果造成一定影响。(3)随访期间出现的不良事件,对行PCI 的患者未再行FFR 检测,不能排除PCI 后未达到完全血运重建的可能。(4)入选人群中可能合并微循环重度病变的患者,重度微循环疾病导致FFR 测量出现误差,FFR 测量值将高于预期值并会低估心外膜血管狭窄的严重程度,为更好地排除此项,可行心肌灌注显像或行微循环阻力指数检测,明确微循环病变状况。(5)此研究入选的人群只是冠状动脉多支血管病变不稳定型心绞痛患者,对于稳定型心绞痛、急性心肌梗死等患者已排除,以上论证不能扩展至该类人群。
总之,在多支不稳定型心绞痛患者中,使用压力导丝测出的FFR 值来决定是否对非罪犯中度病变进行血运重建是安全的。随访12 个月后,FFR 结合CAG 指导PCI 治疗较单纯CAG 指导PCI 的不良事件发生率显著减少,尤其在再次血运重建方面,并且心绞痛临床表现显著缓解。治疗中,对于非罪犯中度狭窄血管在FFR 指导下行PCI 治疗,具有临床借鉴意义。
[1] Tonino PA, De Bruyne B, Pijls NH, et al. Fractional flow reserve versus angiography for guiding percutaneous coronary intervention.N Engl J Med, 2009, 360:213-224.
[2] Wright RS, Anderson JL, Adams CD, et al. 2011 ACCF/AHA focused update incorporated into the ACC/AHA 2007 guidelines for the management of patients with unstable angina/non-STelevation myocardial infarction:A report of the American College of Cardiology Foundation/American Heart Association task force on practice guidelines. J Am Coll Cardiol, 2011, 57:e215-367.
[3] 朱贵家,杨树森.血流储备分数在冠状动脉介入诊疗中的应用.中国介入心脏病学杂志,2013,21:326-329.
[4] 黄峻.心力衰竭合并冠心病处理的现代概念.中国介入心脏病学杂志,2014,22:201-204.
[5] Sels JW, Tonino PA, Siebert U, et al. Fractional flow reserve in unstable angina andnon-STsegment elevation myocardial infarction:experience fromthe FAME (Fractional Flow Reserve Versus Angiography for Multivessel Evaluation) study. JACC Cardiovasc Interv, 2011, 4:1183-1189.
[6] Pijls NH, Fearon WF, Tonino PA, et al. Fractional flow reserve versus angiography for guiding percutaneous coronary intervention in patients with multivessel coronary artery disease 2-year followup of the FAME (Fractional Flow ReserveVersus Angiography for Multivessel Evaluation) Study. J Am Coll Cardiol, 2010, 56:177-184.
[7] Wijns W, Kolh P, Danchin N, et al. Guidelines on myocardial revascularization: The Task Force onMyocardial Revascularization of the European Society of Cardiology(ESC) and the European Association for Cardio-Thoracic Surgery(EACTS). Eur Heart J,2010, 31:2501-2555.
[8] Hamm CW, Bassand JP, Agewall S, et al. ESC Guidelines for the management of acute coronary syndromes in patients presenting without persistent ST-segment elevation: the task force for the management of acute coronary syndromes (ACS) in patients presenting without persistent ST-segment elevation of the European Society of Cardiology (ESC). Eur Heart J, 2011, 32:2999-3054.
[9] Dupouy P, Gilard M, Morelle JF,et al. Usefulness and clinical impact of a fractional fl ow reserve and angiographic targeted strategy for coronary artery stenting: FROST III, a multicenter prospective registry. Euro Intervention, 2005, 1:85-92.
[10] Pijls NHJ, van Son JA, Kirkeeide RL, et al. Experimental basis of determining maximum coronary, myocardial, and collateral blood flow by pressure measurements for assessing functional stenosis severity before and after percutaneous trans luminal coronary angioplasty. Circulation, 1993, 87:1354-1367.
[11] Pim AL Tonino, William F Fearon, Bernard De Bruyne, et al.Angiographic versus functional severity of coronary artery stenoses in the FAME study. Fractional fl ow reserve versus angiography in multivessel evaluation. JACC, 2010, 22:2816 -2821.
[12] Sels JW, Tonino PA, Siebert U, et al. Fractional flow reserve in unstable angina and non-ST-segment elevation myocardial infarction experience from the FAME (Fractional flow reserve versus Angiography for Multivessel evaluation) study. JACC Cardiovasc Interv, 2011, 4:1183-1189.
[13] Damman P, Clayton T, Wallentin L,et al. Effects of age on longterm outcomes after a routine invasive or selective invasive strategy in patients presenting with non-ST segment elevation acute coronary syndromes: a collaborative analysis of individual data from the FRISC II - ICTUS - RITA-3 (FIR) trials. Heart, 2012, 98:207-213.
[14] Lin GA, Dudley RA, Lucas FL, et al. Frequency of stress testing to document ischemiaprior to elective percutaneous coronary intervention. JAMA, 2008, 300:1765-1773.
[15] Windecker S, Serruys PW, Wandel S, et al. Biolimus-eluting stent with biode-gradablepolymer versus sirolimus-eluting stent with durable polymer for coronary revascularisation (LEADERS): a randomised non-inferiority trial. Lancet, 2008, 372:1163-1173.
[16] Maron DJ, Boden WE, O’Rourke RA, et al. Intensive multifactorial intervention for stable coronary artery disease: opti-mal medical therapy in the COURAGE (clinical outcomes utilizing revascularization and aggressive drug evaluation) trial. J Am Coll Cardiol,2010, 55:1348-1358.
[17] Naderi SH, Bestwick JP, Wald DS. Ad-herence to drugs that prevent cardiovascular disease: meta-analysis on 376 162 patients. Am J Med, 2012.(Epub ahead of print).
[18] Damman P, Hirsch A, Windhausen F, et al. 5-year clinical outcomes in the ICTUS (Invasive versus Conservative Treatment in Unstable coronary Syndromes) trial: a randomized comparison of an early invasive versus selective invasive management in patients with non-ST-segment elevation acute coronary syndrome. J Am Coll Cardiol,2010, 55:858-864.
