SCN5A基因A1180V突变致扩张型心肌病(DCM)伴房室传导阻滞(AVB)的家系随访分析
2014-08-07程徐磊杨志寅苏春玺孙爱军
申 程徐 磊杨志寅苏春玺孙爱军△
(1山东大学医学院 济南 250012;2复旦大学附属中山医院心内科 上海 200032;3上海市心血管病研究所 上海 200032;4复旦大学生物医学研究院 上海 200032;5山东省济宁医学院行为医学研究所 济宁 272067;6山东省济宁市金乡县人民医院急诊科 济宁 272200)
SCN5A基因A1180V突变致扩张型心肌病(DCM)伴房室传导阻滞(AVB)的家系随访分析
申 程1,2,3徐 磊2,3,4杨志寅5苏春玺6孙爱军2,3,4△
(1山东大学医学院 济南 250012;2复旦大学附属中山医院心内科 上海 200032;3上海市心血管病研究所 上海 200032;4复旦大学生物医学研究院 上海 200032;5山东省济宁医学院行为医学研究所 济宁 272067;6山东省济宁市金乡县人民医院急诊科 济宁 272200)
目的通过对已发现的心脏钠通道基因SCN5A点突变A1180V相关的扩张型心肌病(dilated cardiomyopathy,DCM)伴房室传导阻滞(atrioventricular block,AVB)的家系进行随访,探究A1180V突变致DCM的临床特征及病情演变特点。方法参考前期2007年的资料,于2012年对家系中健在的8名A1180V突变携带者及8名非携带者再次予以询问病史及12导联心电图、超声心动图检查,回顾性分析该家系中10名突变携带者(含2名已故的携带者),8名非携带者及1名已故的基因型不详成员的临床资料。结果随访期间,3名A1180V突变携带者首次诊断为一度AVB或二度Ⅰ型AVB;1名A1180V突变携带者由一度AVB进展为DCM伴三度AVB;1名A1180V突变携带者DCM表现进一步加重,心衰症状明显。该家系中A1180V突变携带者发病首发症状常为一度AVB,平均诊断年龄为(34±3.0)岁,并在约5年内逐渐进展为DCM伴三度AVB。结论本随访分析进一步证实了A1180V突变对DCM的致病作用及特点。对该家系定期随访观察,有助于发现A1180V突变携带者的早期病变。
心脏钠通道基因SCN5A; A1180V突变; 扩张型心肌病
扩张型心肌病(dilated cardiomyopathy,DCM)是以心室扩大和心肌收缩功能障碍为特征的心肌疾病,导致不可逆性心功能衰退,人群患病率约40/10万,5年病死率达50%,是心力衰竭的第3位原因,心脏移植的第1位原因[1-2]。DCM发病原因多样,其中由遗传因素导致的DCM约占20%~50%[3],如心肌肌球蛋白(tropomyosin)基因、核纤层蛋白(lamin A/C)基因等均与 DCM 的发生有明确关系[4-5]。
既往研究发现,心脏钠通道基因SCN 5A突变可导致多种心律失常,包括长QT综合征3型(1ong QT syndrome 3,LQT3),Brugada综合征,病态窦房结综合征(sick sinus syndrome,SSS)等[6-8]。2004年 Mc Nair等[9]首次提出SCN 5A突变与DCM有关以来,针对SCN5A突变致DCM的机制研就得到了广泛关注。传统观点认为SCN5A突变可能通过导致心律失常,进而引起血流动力学紊乱和心脏扩大。而我们课题组曾通过对一DCM伴房室传导阻滞(atrioventricular block,AVB)的家系进行候选基因测序分析,发现了一个新的SCN 5A突变A1180V,并利用膜片钳技术,观察到A1180V突变可影响心肌细胞内钙稳态,由此提出SCN 5A基因突变可通过直接损伤心肌导致DCM的观点[10]。随后,D1595 H、R222Q、E446K等数个致DCM 的SCN5A突变的相继发现也支持了我们的观点[11-13]。
本研究为进一步探究SCN 5A基因A1180V突变在该DCM伴AVB家系中的致病规律及特点,进行了5年的随访分析,现将随访结果报道如下。
资料和方法
研究对象参考2007年来自于山东省金乡县的DCM伴AVB的家系成员的临床资料及测序结果[10],经复旦大学附属中山医院伦理委员会审核批准,取得所有健在对象的同意并签署知情同意书。于2012年对该家系中健在的8名A1180V突变携带者和8名非携带者再次随访,予以询问病史和体格检查,并进行12导联心电图及超声心动图检查。回顾性分析该家系中10名突变携带者(包括2名已故的突变携带者),8名非携带者及1名已故的基因型不详成员的临床资料,以了解A1180V突变所致DCM的病情进展特点。
家系调查随访该家系共3代,主要包括先证者及其一、二级亲属:其父亲及子女3人,同父母的2个胞弟和2个胞妹及各自的子女共10人。
诊断标准DCM的诊断参考2007年中国制定的《心肌病诊断与治疗建议》[14],主要以超声心动图为诊断依据,主要包括:(1)左室舒张末期内径(left ventricular end-diastolic diameter,LVEDD)>50 mm(女性)和>55 mm(男性);(2)左室射血分数(left ventricular ejection fraction,LVEF)<45%和(或)左心室缩短速率(left ventricular fractional shortening,LVFS)<25%;(3)排除其他心脏病。
AVB的诊断参考第7版《内科学》的诊断标准[15],主要以心电图为诊断依据,其中一度AVB的诊断标准:每一个P波后均有QRS波,PR间期>0.20 s;二度Ⅰ型AVB的诊断标准:(1)PR间期进行性延长,直至一个P波下传受阻;(2)相邻RR间期进行性缩短直至心室波脱漏;(3)包含受阻P波在内的RR间期小于正常窦性PP间期的两倍,三度AVB的诊断标准:(1)心房心室活动各自独立;(2)心房率快于心室率;(3)心室起搏点多位于阻滞部位稍下方。
统计学方法数据用SPSS 16.0软件处理,结果用±s表示。
结 果
先证者及已去世家庭成员临床资料先证者(图1,Ⅱ-1)为A1180V携带者:37岁因心悸不适首诊为一度AVB,心超结果无异常;4年后心超提示心脏扩大,伴发三度AVB和房颤;47岁时安装起搏器,但心功能仍继续恶化,最终因严重心力衰竭去世。先证者父亲(Ⅰ-2),已去世,基因型不详:35岁左右出现心悸、气短等不适,体力活动受限,47岁心电图提示三度AVB,51岁时因“心脏病”(具体不详)去世。先证者弟弟(Ⅱ-3),A1180V 携带者:37岁首诊为一度AVB,40岁进展为三度AVB,约5年后发展为DCM伴发三度AVB,53岁时因心衰去世。
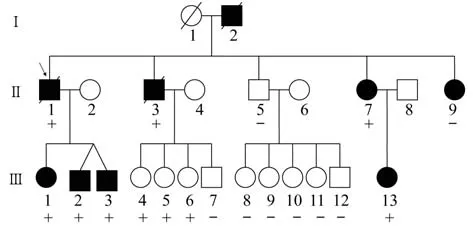
图1 扩张型心肌病伴房室传导阻滞家系图Fig1 Pedigree of the family displaying DCM and AVBFamily members are identified by generations and numbers,and male and female members are represented by squares and circles,respectively.Individuals diagnosed with various cardiopathies are marked by darkened symbols.The deceased are denoted by a slash through the symbol.The arrow represents the proband.“+”indicates individuals who were identified as carriers of the heterozygous A1180V mutation,and“-”indicates non-carriers.
A1180V突变携带者随访资料A1180V突变携带者Ⅱ-7、Ⅲ-1、Ⅲ-2、Ⅲ-3及Ⅲ-13在随访5年期间,疾病表型逐渐出现并加重。先证者妹妹(Ⅱ-7):37岁初诊为一度AVB,41岁进展为三度AVB,常伴有一过性黑朦,53岁发现心脏扩大,5年后随访发现病症进一步加重;自诉常感胸闷乏力,体力活动明显受限,体格检查发现心脏扩大,心电图示三度AVB,心超提示全心扩大,二、三尖瓣中重度反流,中度肺动脉高压,LVEF仅为36%。先证者女儿(Ⅲ-1):31岁时表现为一度AVB,35岁时未发现心脏扩大,42岁随访自诉偶感不适,体力活动轻度受限,心电图示三度AVB,心超提示左心扩大,多瓣膜轻度返流。先证者的双胞胎儿子(Ⅲ-2、Ⅲ-3):5年前病史询问和体检均无明显异常,33岁随访时两者均自诉偶感心悸不适,重体力劳动受限,心电图提示一度AVB,心超见三尖瓣微量反流。Ⅲ-13:25岁时心电图提示PR间期处于临界值,30岁随访进展为二度Ⅰ型AVB,心超无异常发现。Ⅲ-4、Ⅲ-5及Ⅲ-6在2012年5月的随访检查中未发现异常。所有突变携带者均排除其他心脏异常。
A1180V突变非携带者随访资料A1180V突变非携带者Ⅱ-5、Ⅲ-7、Ⅲ-9、Ⅲ-8、Ⅲ-10、Ⅲ-11及Ⅲ-12在询问病史、体检及相关检查中均未发现明显异常。
回顾性分析该家系所有A1180V突变携带者(包括已去世的Ⅱ-1和Ⅱ-3)的临床特点发现(表1),A1180V突变携带者常因心悸、运动耐受力下降就诊,心电图表现为一度AVB,平均诊断年龄为(34±3.0)岁,病情逐渐加重,大约在5年内逐渐进展为心脏扩大伴三度AVB。
讨 论
扩张型心肌病患病率较高,可导致进行性心力衰竭、心律失常、血栓栓塞和猝死。我们通过随访观察A1180V突变致DCM伴房室传导阻滞的家系成员特点,进一步证实了A1180V突变在该家系中的致病作用,为研究该SCN 5A突变致DCM的具体机制提供了依据。
随访发现,随着年龄的增长,A1180V突变携带者疾病症状逐渐出现并加重,多在34岁左右诊断为一度AVB,约在5年内进展为DCM伴三度AVB。此次随访中A1180V突变携带者Ⅱ-7、Ⅲ-1、Ⅲ-2、Ⅲ-3及Ⅲ-13的病情变化均基本符合该规律。先证者父亲(Ⅰ-2)的大部分临床资料已丢失,但仍有明确诊断为三度AVB的病史,并在诊断为三度AVB 4年后去世,大致符合该家系特征。Ⅲ-4及Ⅲ-5两姐妹是A1180V突变携带者,年龄已达该家系发病的平均年龄,但是12导联心电图及超声心动图检查未见明显AVB及心脏扩大表现。然而Ⅲ-4自诉日常生活中,偶感心悸不适,易疲劳,有可能存在间歇性心电图异常但未被发现,因此定期行心电图和心超等检查有助于发现早期病变,并可以早期予以相应干预。此次随访还进一步追踪到另一家系成员Ⅱ-9,经测序分析发现其并未携带A1180V突变,但也有一些心功能不好的表现。虽然不能完全排除A1180V与其他因素发挥共致病作用,但是综合该家系所有成员的特点,仍认为该突变是该家系发病的主要原因。通过细胞膜片钳技术发现,A1180V导致钠通道失活后恢复期延长,引发速率依赖性钠电流减少和晚期钠电流增加;通过运动心电图检测发现,该家系中当时尚未发病的A1180V突变携带者表现出心率依赖性的心电图参数异常(运动后QRS和QTc时限延长)[10],提示心率增加可能会促进突变携带者疾病表型的出现。在该家系成员中,A1180V突变携带者Ⅲ-13常参与体育比赛项目,其心电图出现异常的年龄要明显早于其他携带者。因此,A1180V突变携带者尽量避免从事重体力劳动或剧烈运动,可能有助于延缓疾病发生及进展。

表1 扩张型心肌病伴房室传导阻滞家系中A1180V突变携带者的临床资料Tah 1 Clinical characteristics of A1180V mutation carriers in the family displaying DCM and AVB
虽然SCN5A突变的致DCM作用已明确,但具体机制目前仍处在探索阶段。Chopra等[16]运用反义引物抑制斑马鱼的SCN5A基因,观察到胚胎心脏发育障碍。Royer等[17]通过制备SCN5A+/-小鼠模型,观察到年龄相关的进行性心房、心室传导障碍,发现老年SCN5A+/-小鼠出现广泛的左室心肌纤维化,且连接蛋白43和心肌肥厚标志物β-MHC、α骨架蛋白表达异常,提供了SCN5A异常与心脏结构的直接关联证据,但目前仍缺乏研究SCN5A突变致DCM的准确动物模型。A1180V突变致DCM的具体作用机制也需要在突变敲入的动物模型中进一步分析与验证。
综上所述,我们通过对该家系的随访进一步证实了A1180V突变的致DCM作用。定期行心电图和超声心动图检查有助于发现A1180V突变携带者的早期病变,避免重体力劳动及剧烈运动的生活方式可能有助于减缓甚至预防疾病发展。
[1] van de Meerakker JB,Christiaans I,Barnett P,et al.A novel alpha-tropomyosin mutation associates with dilated and non-compaction cardiomyopathy and diminishes actin binding[J].Biochim Biophys Acta,2013,1833(4):833-839.
[2] 张茜,孙爱军,范铮,等.一个扩张型心肌病伴房室传导阻滞家系SCN5A基因的突变研究[J].中国分子心脏病学杂志,2009,9(2):65-69.
[3] Mcnally EM,Golbus JR,Puckelwartz MJ.Genetic mutations and mechanisms in dilated cardiomyopathy[J].J Clin Invest,2013,123(1):19-26.
[4] Karam CN,Warren CM,Rajan S,et al.Expression of tropomyosin-kappa induces dilated cardiomyopathy and depresses cardiac myofilament tension by mechanisms involving cross-bridge dependent activation and altered tropomyosin phosphorylation[J].J Muscle Res Cell Motil,2011,31(5-6):315-322.
[5] Arimura T,Onoue K,Takahashi-Tanaka Y,et al.Nuclear accumulation of androgen receptor in gender difference of dilated cardiomyopathy due to lamin A/C mutations[J].Cardiovasc Res,2013,99(3):382-394.
[6] Tester DJ,Benton AJ,Train L,et al.Prevalence and spectrum of large deletions or duplications in the major long QT syndrome-susceptibility genes and implications for long QT syndrome genetic testing[J].Am J Cardiol,2010,106(8):1124-1128.
[7] Calloe K,Refaat MM,Grubb S,et al.Characterization and mechanisms of action of novel Na V1.5 channel mutations associated with Brugada syndrome[J].Circ Arrhythm Electrophysiol,2013,6(1):177-184.
[8] Butters TD,Aslanidi OV,Inada S,et al.Mechanistic links between Na+channel(SCN5 A)mutations and impaired cardiac pacemaking in sick sinus syndrome[J].Circ Res,2010,107(1):126-137.
[9] Mc Nair WP,Ku L,Taylor MR,et al.SCN5A mutation associated with dilated cardiomyopathy,conduction disorder,and arrhythmia[J].Circulation,2004,110(15):2163-2167.
[10] Ge J,Sun A,Paajanen V,et al.Molecular and clinical characterization of a novel SCN5A mutation associated with atrioventricular block and dilated cardiomyopathy[J].Circ Arrhythm Electrophysiol,2008,1(2):83-92.
[11] Nguyen TP,Wang DW,Rhodes TH,et al.Divergent biophysical defects caused by mutant sodium channels in dilated cardiomyopathy with arrhythmia[J].Circ Res,2008,102(3):364-371.
[12] Mann SA,Castro ML,Ohanian M,et al.R222Q SCN5A mutation is associated with reversible ventricular ectopy and dilated cardiomyopathy[J].J Am Coll Cardiol,2012,60(16):1566-1573.
[13] Mcnair WP,Sinagra G,Taylor MR,et al.SCN5A mutations associate with arrhythmic dilated cardiomyopathy and commonly localize to the voltagesensing mechanism[J].J Am Coll Cardiol,2011,57(21):2160-2168.
[14] 中华医学会心血管病学分会,中华心血管病杂志编辑委员会,中国心肌病诊断与治疗建议工作组.心肌病诊断与治疗建议现代心脏病学[J].中华心血管病杂志,2007,35(1):5-16.
[15] 陆再英,钟南山.内科学[M].7版.北京:人民卫生出版社,2010:212-213.
[16] Chopra SS,Stroud DM,Watanabe H,et al.Voltage-gated sodium channels are required for heart development in zebrafish[J].Circ Res,2010,106(8):1342-1350.
[17] Royer A,van Veen TA,Le Bouter S,et al.Mouse model of SCN5A-linked hereditary Lenegre's disease:age-related conduction slowing and myocardial fibrosis[J].Circulation,2005,111(14):1738-1746.
A follow-up analysis of a family displaying dilated cardiomyopathy(DCM)and atrioventricular hlock(AVB)caused hy A1180V mutation ofSCN5Agene
SHEN Cheng1,2,3,XU Lei2,3,4,YANG Zhi-ying5,SU Chun-xi6,SUN Ai-jun2,3,4△
(1School of Medicine,Shandong University,Jinan250012,Shandong Province,China;2Department of Cardiology,Zhongshan Hospital,Fudan University,Shanghai200032,China;3Shanghai Institute of Cardiovascular Diseases Shanghai200032,China;4Institutes of Biomedical Sciences,Fudan University,Shanghai200032,China;5Institute of Behavioral Medicine,Jining Medical College,Jining272067,Shandong Province,China;6Department of Emergency,Jinxiang People′s Hospital,Jining272200,Shandong Province,China)
cardiac sodium channel gene SCN5A; A1180V mutation; dilated cardiomyopathy
R 542.2
A
10.3969/j.issn.1672-8467.2014.02.006
2013-04-24;编辑:张秀峰)
国家自然科学基金(81170202);新世纪优秀人才支持计划(NVET-12-0125)
△Corresponding author E-mail:angelasunsh@163.com
【Ahstract】 OhJectiveTo explore the clinical characteristics and disease progression resulting from A1180V mutation of cardiac sodium channel geneSCN5Ain a family displaying dilated cardiomyopathy(DCM)and atrioventricular block (AVB).MethodsAccording to the data of 2007,8 carriers of A1180V muntation and 8 non-carriers were followed up by inquiring medical history,physical examination,12-lead electrocardiogram (ECG)examination and echocardiography in 2012.Clinical datafrom all of the 10 carriers(including 2 dead patients),8 non-carriers and a dead man with unknown genotype were analyzed retrospectively.ResultsDuring this follow-up period,3 carriers were first diagnosed with first-degree AVB or second-degree AVB of typeⅠ;one carrier's condition progressed to cardiac dilation and third-degree AVB;another carrier's disease developed even worse with severe heart failure and the patient has been diagnosed with DCM before.In addition,the first-degree AVB were mostly the primary performance among carriers with a mean diagnosed age of(34±3.0)years.And their disease would progress to DCM with proceeding third-degree AVB in about 5 years.ConclusionsThe results further confirm the pathogenic role of A1180V mutation in DCM.Regular follow-up of the family may provide more opportunity to detect early abnormalities in carriers of A1180V mutation.
*This work was supported hy the National Natural Science Foundation of China(81170202)and the New Century Excellent Talents ProJect(NCET-12-0125).
