恩替卡韦治疗失代偿期乙肝肝硬化病人的长期疗效观察
2014-08-06马雪梅于德磊王洪波刘振文
任 辉,马雪梅,于德磊,赵 林,王洪波,刘振文*
(1.解放军第三零二医院肝胆外科二中心,北京 100039;2.解放军第三零二医院肝硬化诊疗中心,北京100039)
乙肝肝硬化(hepatitis B cirrhosis,HBC)是慢性乙肝发展的结果,乙肝病毒(HBV)持续高水平存在和不断复制是肝硬化不断进展极其重要的因素。感染HBV病人中近25%将最终发展为肝硬化,未经治疗的代偿性肝硬化病人及未经治疗的失代偿性肝硬化病人的 5年病死率分别为14%和84%[1]。研究表明, HBC病人均存在不同程度的HBV复制, 抑制病毒复制是控制病情进展的关键。恩替卡韦作为兼具强效和高基因屏障、低耐药发生率的抗病毒药物,能快速抑制HBV复制,促进肝功能恢复和改善肝组织病理学变化,安全性较好[2,3]。目前已进行的恩替卡韦临床研究主要针对慢性乙肝病人,而治疗失代偿期肝硬化病人的资料还较少。现将解放军第三零二医院应用恩替卡韦治疗失代偿期HBC病人的长期疗效观察结果报道如下。
1 资料和方法
1.1 病例选择 选择2005年1月—2011年2月于解放军第三零二医院住院诊治的病人112例,根据临床表现、实验室检查、影像学检查诊断为失代偿期HBC,诊断符合2000年《病毒性肝炎防治方案》的诊断标准。入选标准:(1)HBV DNA>100 IU/ml;(2)既往无核苷(酸)类似物用药史;(3)病例具有完整的3年随访资料。排除标准:(1)诊断符合2000 年《病毒性肝炎防治方案》的慢性重型肝炎的诊断标准;(2)重叠其他病毒性肝炎如甲型、丙型、丁型、戊型肝炎病毒感染;(3)其他肝病引起的肝硬化,如酒精性或非酒精性脂肪性肝病、药物性肝炎、自身免疫性肝病、胆汁瘀积性肝病、肝脏肿瘤等;(4)妊娠期或哺乳期妇女;(5)伴有其他严重疾病,如恶性肿瘤,严重的心、肺、肾等脏器疾病,精神疾病,甲状腺功能亢进或减退,糖尿病等。
1.2 治疗方法 所有病人在常规保肝对症治疗基础上,长期坚持口服恩替卡韦片[规格0.5 mg×7片/盒,中美(上海)施贵宝制药有限公司]抗病毒治疗,0.5 mg/d。
1.3 观察指标 由一组医师观察恩替卡韦抗病毒治疗前(即基线水平)、治疗后1年、2年、3年血清病毒学指标,肝功能指标:包括白蛋白(ALB)、总胆红素(TBIL)、丙氨酸氨基转移酶(ALT)、胆碱酯酶(CHE),以及凝血酶原时间(PT)的变化情况,Child-Pugh评分及终末期肝病模型(model for end-stage liver disease,MELD)评分的变化情况,合并症的改善情况,以及肝癌、药物不良反应(ADRs)的发生情况。HBeAg/HBeAb转换率指治疗后HBeAg从阳性转变为阴性的病人中,HBeAb转变为阳性的病人的百分率。
1.4 检测方法 采用分光光度法检测肝功能(贝克曼试剂),透射比浊法(贝克曼试剂)检测PT,化学发光法(罗氏试剂)检测血清HBV标志物,实时荧光定量PCR法(上海复星公司试剂)检测HBV DNA 定量,检测下限为100 IU/ml。
1.5 统计学处理 采用SPSS 13.0 软件进行统计分析,治疗后结果以治疗前为对照,计量资料采用单因素方差分析(one-way ANOVA)和SNK-q检验,计数资料采用χ2检验,P<0.05表示差异有统计学意义。
2 结 果
2.1 入选病例的基线情况 共入选失代偿期HBC病人112例,男性89例,女性23例,年龄(45.5±10.8)岁,已知HBV感染时间(12.1±6.1)年,HBV DNA(4.24×104±1.12×102) IU/ml,其中HBVe抗原(HBeAg)阳性61例,HBeAg阴性51例,合并腹水102例,合并腹膜炎20例,合并上消化道出血6例,合并肝性脑病5例,合并慢性肝功能衰竭9例。
2.2 治疗前后血清病毒学指标变化 在全部112例观察病例中,恩替卡韦抗病毒治疗后1年、2年、3年时HBV DNA的转阴率见表1。其中有1例病人在治疗后2年时出现病毒学反弹,DNA序列检测未见耐药位点,联用阿德福韦酯后HBV DNA阴转。在HBeAg阳性的61例观察病例中,恩替卡韦抗病毒治疗后1年、2年、3年时HBeAg阴转率及HBeAg/HBeAb血清学转换率见表1。
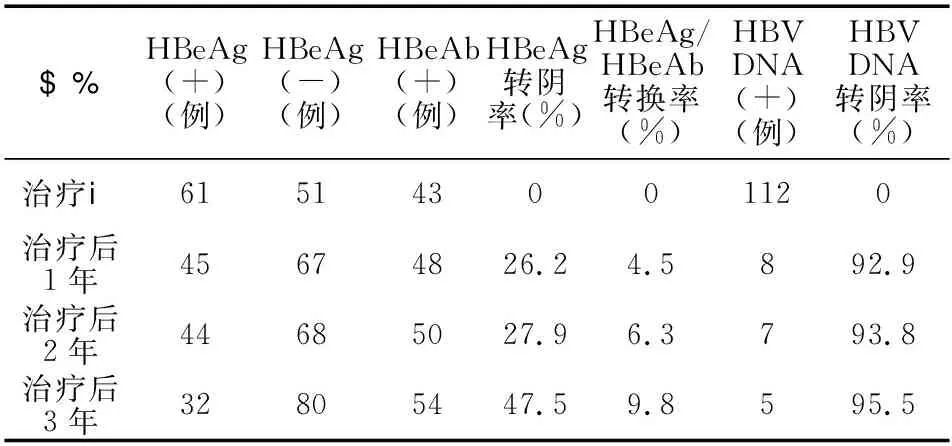
表1 恩替卡韦治疗前后血清病毒学指标的变化
2.3 治疗前后肝功能和PT的变化 应用恩替卡韦抗病毒治疗后ALB、ALT、CHE、PT等各项指标较治疗前明显改善,差异有统计学意义(P<0.05)。与治疗前相比,恩替卡韦抗病毒治疗1年后TBIL差异无统计学意义,但治疗2年、3年后TBIL差异有统计学意义(P<0.05),具体见表2和表3。
2.4 Child-Pugh评分及MELD评分变化 恩替卡韦抗病毒治疗后,Child-Pugh评分较治疗前显著降低, 差异有统计学意义 (P<0.05)。 MELD评分较治疗前无明显变化,差异无统计学意义(P>0.05),具体见表4。
表2 恩替卡韦治疗前后肝功能与凝血酶原时间的变化
Table 2 Changes in liver function and prothrombin time before and after entecavir treatment

表2 恩替卡韦治疗前后肝功能与凝血酶原时间的变化
*P<0.05,与治疗前比较;ALB:白蛋白;TBIL:总胆红素; ALT:丙氨酸氨基转移酶; CHE:胆碱酯酶; PT:凝血酶原时间
时间ALB(ρB/g·L-1)TBIL(cB/μmol·L-1)ALT(zB/U·L-1)CHE(zB/U·L-1)PT(t/s)治疗前33±6 30.0±18.4 94±54 2876±1462 15.9±2.0治疗后1年37±6*26.6±13.9 32±17*4603±1954*13.8±1.8*治疗后2年37±7*22.2±11.9*31±14*5124±2133*13.3±1.7*治疗后3年37±8*21.7±10.7*34±15*5426±2152*12.9±1.5*
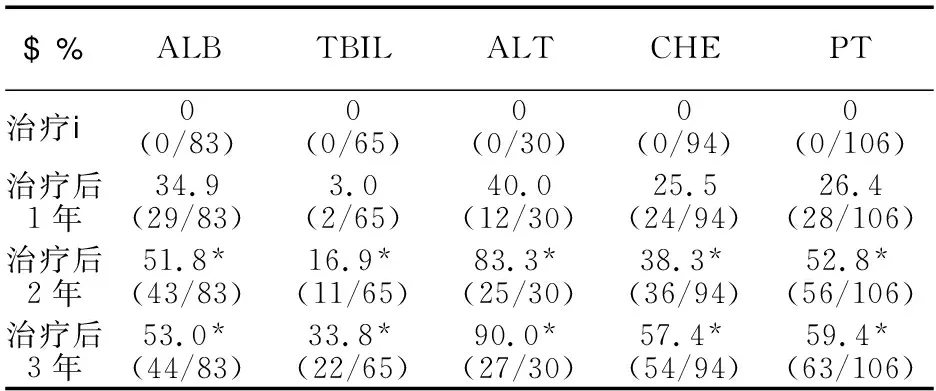
表3 恩替卡韦治疗前后肝功能和凝血酶原时间复常率
表4 恩替卡韦治疗前后Child-Pugh评分及MELD评分变化
Table 4 Changes in Child-Pugh scores and MELD scoresbefore and after entecavir treatment

表4 恩替卡韦治疗前后Child-Pugh评分及MELD评分变化
*P<0.05,与治疗前比较;MELD:终末期肝病模型
时间Child-Pugh评分MELD评分治疗前8.2±1.8 10.96±3.27治疗后1年6.8±1.4*10.65±2.98治疗后2年6.7±1.4*10.32±3.14治疗后3年6.5±1.4*10.01±3.03
2.5 并发症的改善情况 由于合并上消化道出血、肝性脑病、慢性肝功能衰竭的基线病例数较少,无法进行统计比较,故仅比较了失代偿期 HBC 病人经恩替卡韦治疗后腹水及腹膜炎并发症发生率。与治疗前比较,该两项指标得到了显著改善,差异有统计学意义(P<0.05)。具体见表5。

表5 恩替卡韦治疗前后各种并发症的例数及其比例
2.6 肝癌的发生情况 在本组病例治疗过程中,共有8人(7.1%)先后明确诊断为原发性肝癌,其中发生在抗病毒治疗后1年、 2年、 3年时各6例、 1例和1例。
2.7 安全性评价 本研究中的112例病人未发生明确的中枢神经系统、消化系统、肌肉骨骼系统等ADRs。1例病人在治疗前后血肌酐始终轻度异常,明确诊断为糖尿病肾病;1例病人在治疗前血肌酐轻度异常,未明确病因,治疗后3年肾功能恢复正常;4例病人在治疗后1年出现血肌酐轻度异常,明确与腹腔感染相关,经抗感染治疗后恢复正常;1例病人在治疗后2年出现血肌酐轻度异常,明确与肺部感染相关,经抗感染治疗后恢复正常。本研究中未发生与研究药物相关的不良事件。
3 讨 论
HBV复制是导致肝组织长期处于炎症反应状态以及不断纤维化的根本原因[4],肝硬化是慢性乙肝发展的结果,导致发生肝癌的风险显著升高,疾病由代偿期进入失代偿期后,肝功能迅速恶化,会出现各种并发症,导致病死率大幅上升。在慢性乙肝病人中,肝硬化失代偿的年发生率约3%,5年累计发生率约16%。失代偿期肝硬化病人的5年病死率为86%,显著高于代偿期肝硬化(16%)。肝硬化病人中肝癌的年发生率为3%~6%[5,6]。HBV所致的肝脏炎症坏死及其所继发的肝纤维化进程是肝病进展的主要病理学基础,如果能持久抑制病毒复制,有效控制肝组织炎症,就有可能减少肝细胞破坏和延缓肝纤维化的发展,从而减缓肝硬化的进展,降低肝癌的发生风险。
2010年我国《慢性乙型肝炎防治指南》中指出,对于失代偿期肝硬化病人,只要能检出HBV DNA,不论ALT或天冬氨酸氨基转移酶(AST)是否升高,建议在知情同意的基础上,及时应用核苷(酸)类药物抗病毒治疗,以改善肝功能并延缓或减少肝移植的需求。因需要长期治疗,最好选用耐药发生率低的核苷(酸)类药物治疗,不能随意停药,一旦发生耐药变异,应及时加用其他已批准的能治疗耐药变异的核苷(酸)类药物。恩替卡韦是鸟嘌呤核苷类似物,对HBV多聚酶具有较强抑制作用,且不易发生耐药[7],已广泛用于慢性乙肝的抗病毒治疗,是目前公认的核苷(酸)类似物中强效、低耐药的抗HBV药物。多项恩替卡韦的全球性临床研究均报道,恩替卡韦治疗可延缓病人肝脏纤维化,持续抑制病毒复制,可缓解或逆转肝纤维化/肝硬化。目前应用恩替卡韦治疗失代偿期HBC的临床资料不足,对其疗效及安全性尚缺乏循证医学证据。
本研究结果表明, 恩替卡韦治疗失代偿期HBC的过程中未见明显的ADRs, 未见耐药发生, 用药安全性好。 恩替卡韦对于失代偿期HBC病人的病毒复制有很强的抑制作用, 通过抑制HBV复制, 减轻肝细胞炎症, 同时改善了肝功能及凝血功能等各项指标, 与文献[3]相符, 而与之不符的是TBIL的改善情况, 考虑与本研究TBIL的基础水平较低[(30.0±18.4) μmol/L]有关。在本研究中恩替卡韦可以减少腹水、腹膜炎等并发症,由于本研究中合并肝性脑病、上消化道出血及慢性肝功能衰竭的基线病例少,无法进行统计学比较,尚待扩大样本量进一步研究。在恩替卡韦抗病毒治疗过程中,112例病人中共有8例明确诊断为原发性肝癌,1年、2年、3年肝癌发生率分别为5.4%、0.9%和0.9%,1年肝癌发生率与文献报道的肝硬化病人中肝癌的年发生率为3%~6%基本相符,而2年、3年的肝癌发生率低于文献报道的数据。可见随着恩替卡韦抗病毒治疗时间的延长,肝癌的发生率逐渐降低,因此考虑恩替卡韦抗病毒治疗有可能降低肝癌的发生率。考虑到本研究为回顾性分析,未设立对照组,研究人群仅限于需要治疗的住院病人,且为具有完整3年随访资料的病例,因此对肝癌发生率的评价不够全面,故上述结论还需要大量的循证医学证据进一步支持。
【参考文献】
[1]de Jongh F E,Janssen H L,de Man R A,etal.Survival and prognostic indicators in hepatitis B surface antigen-positive cirrhosis of the liver[J].Gastroenterology,1992,103(5):1630-1635.
[2]罗红彬,胡中伟,郭家伟.恩替卡韦治疗失代偿期乙型肝炎肝硬化48周疗效观察[J].实用肝脏病杂志,2009,12(2):121-123.
Luo HongBin,Hu ZhongWei,Guo JiaWei.Study on 48-week treatment of entecavir in patients with decompensated hepatitis B-induced cirrhosis[J].J Clin Hepatol,2009,12(2):121-123.In Chinese with English abstract.
[3]Schiff E,Simsek H,Lee W M,etal.Efficacy and safety of entecavir in patients with chronic hepatitis B and advanced hepatic fibrosis or cirrhosis[J].Am J Gastroenterol,2008,103(11):2776-2783.
[4]王慧芬, 苏海滨. 肝衰竭治疗进展[J].传染病信息, 2010, 23(2):65-67.
Wang HuiFen,Su HaiBin.Progress in the treatment of liver failure[J].Infect Dis Inf,2010,23(2):65-67.In Chinese with English abstract.
[5]Chu C M,Liaw Y F.Hepatitis B virus-related cirrhosis:natural history and treatment[J].Semin Liver Dis,2006,26(2):142-152.
[6]Chen YiCheng,Chu C M,Yeh C T,etal. Natural course following the onset of cirrhosis in patients with chronic hepatitis B: a long-term follow-up study[J].Hepatol Int,2007,1(1):267-273.
[7]Chae H B,Kim M J,Seo E G,etal. High efficacy of adefovir and entecavir combination therapy in patients with nucleoside-refractory hepatitis B[J].Korean J Hepatol,2012,18(1):75-83.
