青霉属生物中分离出的抗真菌四肽的固相合成
2014-08-06杨璐晶李文娟李仁武王晓燕胡宏岗第二军医大学研究生管理大队药学院上海00433
杨璐晶,王 露,李文娟,李仁武,王晓燕,胡宏岗 (第二军医大学,.研究生管理大队,.药学院,上海 00433)
随着人类社会的发展与进步,人口不断增加,环境污染日益严重,可供给人类生存所必需的农耕田逐年减少。因此,农作物的产率就极大的引起了人们的关注,而真菌感染正是影响农作物产率的一个重要因素。抗菌肽通常序列短,由微生物集体合成,是机体天然防御的一部分。抗菌肽可以抵御真菌入侵,对各种植物疾病有良好的作用[1]。因此,抗菌肽有可能成为一种新型农药用于现代农业[2]。
近期研究表明,从变灰青霉中分离得到的直链四肽D-Phe-Val-D-Val-Tyr-OH有显著的抗菌活性,该化合物对Fusariumvirguliforme(为大豆猝死综合征病原菌)的MIC达9.5×10-3μmol/L,其抗真菌能力优于市场上广泛使用的抗菌药物[3],其化学合成方法尚未见报道。固相多肽合成是近年来迅速发展的一种快捷高效的获得多肽的方法。所以,本研究首次采用固相多肽合成,以2-氯三苯基氯树脂为固相载体,首先将C端的酪氨酸与树脂相连,再将其余3个氨基酸逐一与酪氨酸进行连接,合成完毕后将四肽从树脂上剪切下来,并脱去侧链上的保护,获得目标多肽。
1 仪器与试剂
1.1仪器 恒温磁力搅拌器(上海志威电器有限公司)、旋转蒸发仪(LOOYE ZX98-1), 水浴锅(LOOYE ZX98-1) , 2ZX-4型旋片真空泵(上海豫康科教仪器设备有限公司) , 低温冷却循环泵(上海豫康科教仪器设备有限公司), 循环水式多用真空泵SHB-IIIA(上海豫康科教仪器设备有限公司), ZF7B三用紫外分析仪(上海康化生化仪器制造厂),Selecta固相合成仪。
1.2试剂 Fmoc-氨基酸(吉尔生化)、2-氯三苯基氯树脂(CTC)、N,N′-二环己基碳二亚胺(DCC)、1-羟基苯并三氮唑( HOBt )、三氟乙酸( TFA)、N,N-二异丙基乙基胺( DIPEA )、三氟乙醇(TFE) 均购自上海吉尔生化有限公司;茚三酮、哌啶、甲醇、N,N-二甲基甲酰胺(DMF)、二氯甲烷( DCM)、N-甲基吡咯烷酮( NMP )均为市售分析纯试剂;乙腈(色谱纯,J&K)。
2 合成实验
2.1合成路线
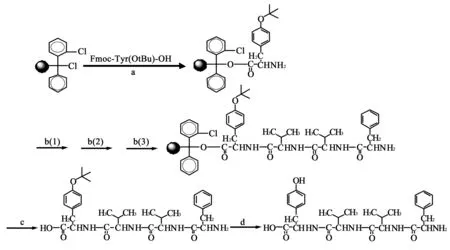
图1 D-Phe-Val-D-Val-Tyr-OH合成路线
a:DCM/DIPEA, 3 h; b(1) :HOBt/DMF/DCC/DCM, Fmoc-D-Val-OH, 30 min, b(2):HOBt/DMF/DCC/DCM, Fmoc-Val-OH, 30 min;
b(3):HOBt/DMF/DCC/DCM, Fmoc-D-Phe-OH, 30 min; c:TFE/AcOH/DCM(1:1:8),1 h; d:TFA/DCM(1:3),30 min
2.2Fmoc-酪氨酸与树脂相连[4]取CTC树脂1.0 g(取代度为1.08 mmol/g)加入到固相合成反应管中,用DCM 30 ml浸泡30 min使CTC树脂充分溶胀,活化待用。随后加入Fmoc-Tyr(OtBu)-OH (749 mg,1.5 mmol)、二氯甲烷15 ml、DIPEA 0.42 ml,震荡反应3 h。反应结束后,将液体滤去,依次用甲醇、二氯甲烷洗涤树脂各3次,抽干待用。
2.3氨基酸的逐步连接 在上步反应树脂中加入20%哌啶-DMF溶液15 ml,震荡反应30 min。将称量好的Fmoc-氨基酸(2 eq)与HOBt(3 eq)混溶于5 ml DMF溶液中,再加入DCC(3 eq)、二氯甲烷 15 ml,震荡反应30 min。并用20%哌啶-DMF溶液15 ml脱去Fmoc,然后将下一个Fmoc-氨基酸活化,将活化液过滤至固相反应管中,震荡反应2 h,反应完毕后用DMF、二氯甲烷各洗涤3次。根据多肽序列如此重复脱保护→缩合→脱保护,直到所有氨基酸连接完毕。
2.4四肽的游离和脱侧链保护 本研究采用稀酸体系将多肽从树脂上进行游离。具体操作如下:在上步反应树脂中加入乙酸:三氟乙醇:二氯甲烷=1:1:8(V/V/V)30 ml,振荡反应1 h,过滤,树脂再用二氯甲烷洗涤3次,浓缩滤液(期间加入甲苯除去残留乙酸)得带保护的多肽粗品409 mg。并且在粗品中加入TFA:DCM=1:3(V/V)20 ml,搅拌反应30 min,浓缩得目标多肽粗品,再用制备型高效液相进行纯化得纯品267.5 mg,收率47.0%,纯度大于95%。1H-NMR (DMSO-d6, 600 MHz): δ 9.22~9.20 (m, 1H, NH), 8.46 (d, 1H,J=9.2 Hz, NH), 8.32 (d, 1H,J=8.4 Hz, NH), 8.13 (d, 1H,J=9.2 Hz, NH), 7.32~7.20 (m, 5H, Ar-H), 7.00(d, 2H,J=8.4 Hz,Ar-H), 6.63 (d, 2H,J=8.4 Hz, Ar-H), 4.56~4.53 (m, 1H, α-H), 4.39~4.34 (m, 1H, α-H), 4.34~4.31 (m, 1H, α-H), 4.56~4.53 (m, 1H, α-H), 4.26 (t, 1H,J=7.5 Hz), 3.06~3.02 (m, 1H), 2.96~2.90 (m, 2H), 2.70~2.65 (m, 1H), 1.86~1.74 (m, 2H), 0.68~0.62 (m, 9H, CH3), 0.54 (d, 3H,J=6.8 Hz, CH3),m/zC28H39N4O6[M+ H]+: 527.36。
3 结果与讨论
本研究通过4步反应合成得到了目标化合物D-Phe-Val-D-Val-Tyr-OH,终产物的合成收率为 47.0%。其结构经核磁和质谱确证,合成方法简便易行,反应条件温和,收率高,合成得到的目标化合物可用于抗真菌活性研究。
在用二氯甲烷洗涤树脂过程中,遇到过抽滤速度瞬间减慢的情况,经过分析可能原因是固相合成管在震荡时发生堵塞。在浓缩滤液得粗品的过程中,蒸发得不带固体粗品,经过分析可能的原因为粗品溶解在稀酸体系中,所以加入甲苯降低其溶解度,并且得到了多肽粗品。
抗菌肽的发现促进农业发展,使农作物产量有了进一步提高的可能。但是,在抗菌肽广泛应用于农业生产前,还需要验证和考虑很多问题。如需要进一步实验验证抗菌肽的安全性,需要考虑真菌等微生物对抗菌肽的耐药性等。所以,要想在农业生产上真正使用抗菌肽还需要进行很多研究。
【参考文献】
[1] Montesinos E, Bardaji E. Synthetic antimicrobial peptides as agricultural pesticides for plant disease control[J]. Chem Biodiver,2008, 5(7): 1225-1237.
[2] Chernysh S, Kim SI, Bekker G,etal. Antiviral and antitumor peptides from insects[J]. Proc Natl Acad Sci, 2002, 99(20):12628-12632.
[3] Bertinetti BV, Pea NI, Cabrera GM. An antifungal tetrapeptide from the culture ofpenicilliumcanescens[J]. Chem Biodiver,2009, 6(8): 1178- 1184.
[4] 胡春玲.鳖甲抗肝纤维化活性多肽的固相合成[J]. 医药导报, 2011, 30(5):561-562.
