EDTA法测定牛奶中钙含量及条件探讨*
2014-08-03李云
李 云
(包头师范学院 化学学院,内蒙古 包头 014030)
钙是人体内最重要的、含量最多的矿物元素,约占体重的2%。它广泛分布于全身各组织器官中,其中约99%分布于骨骼和牙齿中,构成骨盐并维持它们的正常生理功能。钙也与身体健康息息相关,钙除成骨以支撑身体外,还参与人体的代谢活动。约1%的钙分布在体液(即肌肉的软组织和细胞的外液)中,它是细胞的主要阳离子,还是人体最活跃的元素之一,其含量虽少,却对体内的生理和生化反应起着重要的调节作用。缺钙可导致儿童佝偻病、青少年发育迟缓、孕妇高血压、老年人骨质疏松症等。目前,我国居民摄入钙量严重不足,尤其是儿童、青少年和老年人缺钙比例比较高[1]。钙含量的测定通常采用火焰原子吸收光谱法[2],EDTA滴定法[3],高锰酸钾滴定法[4]。EDTA滴定法所用仪器普通易得、成本低廉、分析时间短、操作简单、条件要求不高[5],且EDTA与金属离子配位反应具有广泛性,生成的配合物稳定、颜色明显,易判断滴定终点,并且是1:1配位,没有分级现象[6]。下面将以EDTA滴定法测定牛奶中钙含量为例,结合实际检验过程中的一些问题,将该方法的原理、方法及注意事项等进行简单阐述。
1 测定牛奶中钙含量的不同条件
1.1 几种不同的测定条件
查阅文献得知,蒸发牛奶普遍使用酒精灯加热,过滤牛奶钙沉淀物普遍使用定量滤纸过滤[7],但酒精灯温度不可控,滤纸过滤法步骤繁琐且滤纸消耗量较大,可能并不合适,实验中将加以探讨。此外,查阅文献得知,马弗炉灰化温度为 550-600℃,灰化时间为1-2h[7],此条件是否为最佳条件实验中也将加以探讨。实验中针对牛奶钙沉淀物的过滤方法可选择定量滤纸过滤和离心机分离倒掉清液保留沉淀2种,实验中也将加以探讨。另外,本次实验还将进行指示剂加入量、三乙醇胺加入量、溶液PH值等其他测定条件的探讨。通过以上各项条件探讨,从而找出最优实验条件。
1.2 EDTA滴定法的选择依据
EDTA滴定法所用仪器普通易得、成本低廉、分析时间短、操作简单、条件要求不高[5],且EDTA与金属离子配位反应具有广泛性,生成的配合物稳定、颜色明显,易判断滴定终点,并且是1:1配位,没有分级现象[6]。故通过实验,确定EDTA滴定法测定小丽花牛奶中的钙含量的最佳测试条件。
2 实验部分
2.1 实验原理
EDTA与金属离子配位反应具有广泛性,生成的配合物稳定、颜色明显,易判断滴定终点,并且是1:1配位,没有分级现象[6-7]。
本实验中调节PH=9-10[9],滴定前向样品中加入指示剂铬蓝黑R,它先与Ca2+反应生成红色络合物,反应式为:
Ca2++In2-→CaIn(红色)
当在样品中滴入EDTA溶液时,EDTA首先与溶液中未络合的Ca2+反应生成无色络合物,其反应式为:
Ca2++Y2-→CaY(无色)。
因为Ca2+与指示剂形成的络合物不如与EDTA形成的络合物稳定,所以过量的EDTA滴定液便能夺取红色络合物CaIn中的Ca2+,从而使铬蓝黑R还原为原来的形态,于是溶液由红色又变为蓝色,即达到终点。其反应式为:
CaIn+Y2-→CaY+In2-
其中In2-代表指示剂,Y2-代表EDTA。
2.2 实验用品
分析天平、马弗炉、电热恒温鼓风干燥箱、PH仪、碱式滴定管、浓盐酸、浓氨水、三乙醇胺、锌粉、乙二胺四乙酸二钠、铬蓝黑R(钙试剂)、六亚甲基四胺、草酸铵、二甲酚橙、氢氧化钠
2.3 实验步骤
分析中,除另有说明,均限用分析纯试剂和蒸馏水,EDTA由EDTA二钠代替。先预热马弗炉至580℃。
2.3.1溶液的配制
(1)2mol/L HCL溶液:取41.67ml浓盐酸于250ml容量瓶中,润洗量筒3-4次,洗液转移到容量瓶中,之后定容,摇匀
(2)2mol/LNH3·H2O溶液:取33.33ml浓氨水于250ml容量瓶中,润洗量筒3-4次,洗液转移到容量瓶中,之后定容,摇匀
(3)1:1HCl溶液:5ml蒸馏水与5ml浓盐酸配制而成
(4)锌标准溶液:分析天平称取锌粉0.1668g于100ml烧杯中,加入10ml 1:1HCL溶液,迅速盖上表面皿。待锌粉完全溶解后,冲洗表面皿和烧杯2-3次,洗液转入250ml容量瓶中,之后定容至刻度线,摇匀
(5)20%六亚甲基四胺溶液:称取20g六亚甲基四胺固体粉末于100ml烧杯中,加入50ml水微热溶解,转入100ml容量瓶中,洗涤烧杯内壁2-3次,洗液也转移入容量瓶,之后定容至刻度线,摇匀
(6)0.2%二甲酚橙溶液:称取0.4998g二甲酚橙粉末于100ml烧杯中,加入50ml蒸馏水搅拌溶解,转移到棕色瓶中,再用50ml蒸馏水洗涤烧杯2-3次,洗液也转入棕色瓶中,加盖,摇匀
(7)铬蓝黑R(钙试剂)溶液(现配现用):称取0.1004g铬蓝黑R粉末于50ml烧杯中,加入5ml浓氨水,再加入10ml无水乙醇,搅拌后转入棕色瓶中,再用10ml无水乙醇洗涤烧杯,洗液也转入棕色瓶中,加盖,摇匀
(8)草酸铵溶液:称取5g草酸铵固体于100ml烧杯中,加入100ml蒸馏水微热溶解,转移到玻璃瓶中
(9)EDTA二钠溶液:称取3.7232gEDTA二钠固体粉末于100ml烧杯中,搅拌溶解,之后转移到500ml容量瓶中,洗涤烧杯2-3次,洗液也转移到容量瓶中,定容,摇匀
2.3.2牛奶的蒸发
此步比较耗费时间故应先进行此步,操作此步等待时可进行其他步骤。取2个干燥的250ml烧杯,编号后分别称重。将牛奶分别倒入100ml于烧杯中,再分别称重。将2个烧杯分别置于可调式电炉上蒸发至粘稠状,冷却后称重。将2个烧杯中部分样品取出分别包于8张滤纸中,放于坩埚中并编号,每次取样后称重烧杯(若使用玻璃棒取样,第一次取样前应再称量一次包含玻璃棒重量的烧杯重量)。将8个样品连同坩埚一起放于干燥箱中干燥0.5-1h。干燥后将8个样品连同坩埚放于可调式电炉上在通风橱中小火碳化至无烟。将8个样品连同坩埚转入马弗炉中550-600℃灰化2-3h,灼烧为固体粉末
2.3.3 EDTA的滴定
用EDTA二钠溶液润洗碱式滴定管2-3次,将EDTA二钠溶液加入滴定管中,记下读数。用锌标准溶液润洗移液管2-3次,平行移取25.00ml锌标准溶液3次于3个锥形瓶中,并分别加入1-2滴二甲酚橙溶液。分别向3个锥形瓶中滴加20%六亚甲基四胺溶液至稳定的紫红色后,再多滴加5ml(或调节PH=5-6)[8]。用EDTA二钠溶液滴定至溶液由紫红变为亮黄即为滴定终点,记下读数
2.3.4牛奶的滴定
将8份样品转移到8个烧杯中,用2mol/L HCL溶液和蒸馏水洗涤坩埚3-4次,洗液也转入烧杯中。向8个烧杯中加入2mol/L的盐酸溶液,使样品完全溶解,之后调节PH≈4。向8个烧杯中加入过量草酸铵溶液,约10ml,充分搅拌后过滤(此处为条件探讨,用离心机分离3份样品作为对比)。用2mol/L的盐酸溶液分别洗涤漏斗中的沉淀及滤纸4-6次(此处为条件探讨,与之前用离心机分离3份样品同步,用2mol/L HCL溶液和蒸馏水洗涤离心管4-6次),并将洗液分别转入8个250ml锥形瓶中,加入适量的水,分别滴加2mol/L氨水溶液,调节PH=9-10。分别向8个锥形瓶中滴加4-5滴铬蓝黑R溶液,分别用EDTA二钠溶液滴定至溶液由红色变为蓝色即为终点
3 实验数据记录、处理及计算公式
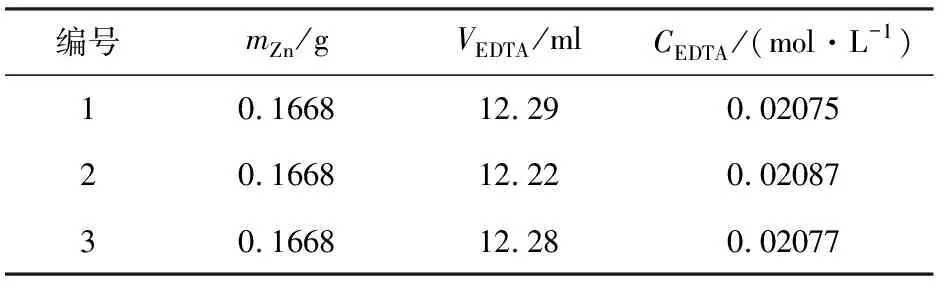
表1:EDTA浓度的标定
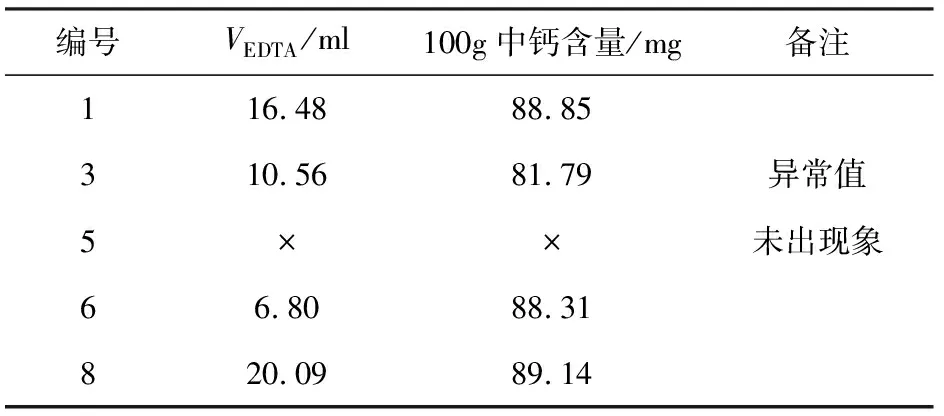
表2:小丽花牛奶中的钙含量(过滤的)
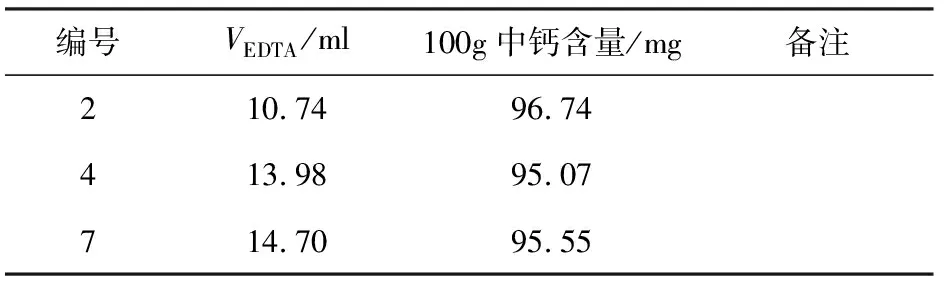
表3:小丽花牛奶中的钙含量(离心的)
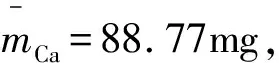
平均偏差:
4 实验条件探索及讨论
4.1 蒸发牛奶的加热方式
由实验过程可知,使用酒精灯蒸发牛奶全程耗费工业酒精较多,且牛奶蒸发到后期时易引起牛奶溅出导致实验失败甚至引起烫伤,原因是酒精灯温度不可控且搅拌不及时导致热量积聚过多。蒸发牛奶时不宜使用酒精灯,应使用可调式电炉,在牛奶蒸发后期时调低温度且应该使用较大的烧杯并不断搅拌,这样可以更快的散发牛奶中积聚的热量,防止牛奶溅出。
4.2 样品的灰化条件
由实验过程可知,灰化时间为1小时、灰化温度为550℃时,样品灰化不完全,有黑色结块产生,测定结果偏低;灰化时间为3小时、灰化温度为580℃时,样品灰化完全,无黑色结块产生,测定结果较好;灰化时间为3小时、灰化温度为780℃时,样品灰化完全,无黑色结块产生,测定结果严重偏低;灰化时间为3小时、灰化温度为980℃时,样品灰化完全,无黑色结块产生,几乎测不到钙含量。故灰化时间为3小时、灰化温度为580℃为最佳灰化条件,低于此条件会造成有机物灰化不完全形成黑色结块[9],影响过滤和测定结果;高于此条件含钙成分会丢失,造成测定值偏低甚至无法测出钙含量(过高的灰化温度会导致钙元素蒸发或升华)[10]。
4.3 牛奶钙沉淀物的过滤方式
由表2、表3可看出,使用离心机分离含钙沉淀比使用滤纸过滤含钙沉淀所得的钙含量要高,原因是滤纸过滤操作步骤较繁琐,每步均损失一定量的钙成分,导致最后总体钙含量较低。另外,过滤时滤纸的消耗量较大,并不节能环保。
4.4 溶液PH值的影响
由实验过程可知,在酸性环境下无法准确测定样品溶液中的钙含量,只有在PH=9左右的弱碱性环境下才可准确测定。经查阅文献得知,只有在PH=9~10的弱碱性环境下,指示剂铬蓝黑R才可变色[5-6]。
4.5 三乙醇胺加入量的影响
作为掩蔽剂的三乙醇胺在实验中起到掩蔽铁、铝离子,从而提高实验准确性的作用[4-5]。由实验过程可知,在三乙醇胺的加入量分别为1滴、3滴、5滴、7滴、10滴时对最后样品溶液中钙含量的测定结果有明显影响,但值得注意的是,三乙醇胺需要在调节PH值之前也就是酸性环境下加入,否则将无法起到掩蔽铁、铝离子的作用[5]。
4.6 指示剂加入量的影响
由实验过程可知,铬蓝黑R作为滴定牛奶钙沉淀物时的指示剂[7],在加入1滴时,样品溶液颜色过淡,变色时不易判断;在加入2-3滴时,样品溶液颜色较明显,变色时易判断;在加入4-6滴时,样品溶液颜色过深,变色时不易判断且变色临界点明显后移。故指示剂加入量应为2-3滴为宜。
5 实验结论
实验条件方面:蒸发牛奶时使用较大的烧杯在可调式电炉上蒸发并不断搅拌;马弗炉灰化条件为580℃时灰化3小时;分离牛奶钙沉淀物时使用离心机分离;样品溶液PH值应为9-10且应在调节样品溶液PH值之前加入三乙醇胺掩蔽铁、铝离子;指示剂铬蓝黑R只需加入2-3滴即可。以上实验条件即为本实验的优选实验条件。
实验结果方面:购买的五袋小丽花牛奶中钙平均含量为95.79mg/100g。
〔参考文献〕
[1]王喜明,等.滴定法测定保健食品中的钙[J].中国卫生检验杂志,2006(06):754-755.
[2]李敏,等.火焰原子吸收法测定补钙制品中的钙及其干扰抑制[J].中国公共卫生,2001,17(8):759-760.
[3]杨惠芬.食品卫生理化检验标准手册[M].北京:中国标准出版社,1997.
[4]I.M.科尔索夫,等.定量化学分析(中册)[M].北京:高等教育出版社,1987:1853-870.
[5]R·蒲希比.实用络合滴定法[M].广州:中山大学出版社,1987.
[6]李玉珍,吕宝华,荆志杰.EDTA络合滴定法测定不同品质牛奶中钙含量[J].山西大同大学学报(自然科学版),2011,27(1):42-44.
[7]赫春香.微型定量分析化学实验[M].大连:大连海事大学出版社,2000.
[8]杨润泉,杨学芬,曾波.EDTA容量法测定饲料级磷酸三钙中的钙含量[J].云南化工,2004,(01):30-31.
[9]殷华山.污水中钙离子含量测定方法的改进[J].宁夏石油化工,2004,(01):20-22.
[10]黄运显,孙维贞.常见元素化学分析方法[M].北京:化学工业出版社,2008:78-80.
